Introducción
El uso del láser fue reportado por primera vez en 1960 por Theodore Harold Maiman1) y hasta el día de hoy son numerosos los reportes que se han realizado en torno a su aplicación en diferentes áreas de la salud. Su uso en odontología se basa en el conocimiento de una serie de procesos físicos y biológicos que son parámetros fundamentales que condicionan la acción del láser y su mecanismo de acción como instrumento de trabajo. Asimismo, el reconocimiento del tipo de láser, su longitud de onda, los efectos biológicos que produce y las características ópticas de los tejidos orales son aspectos que necesariamente debe conocer el odontólogo.2,3,4,5)
En Colombia se viene comercializando el láser de Er, Cr: YSGG (2780 nm). Este es un láser de alta potencia, no ionizante, que emite en modo pulsado y su longitud de onda es 2780 nm, además, se sitúa en la zona de radiación infrarroja del espectro electromagnético. Su medio activo está conformado por el granatio (Garnet, G), Itrio (Yttrium, Y), Escandio (Scandium, S) y Galio (Gallium, G) contaminado con Erbio (Erbium, Er) y Cromo (Chromium, Cr). Este equipo viene provisto de un aerosol de agua y aire, que, al combinarse con el haz de luz láser, refrigera la zona de incidencia del haz, lo que minimiza los efectos térmicos colaterales y potencia su mecanismo de acción. Por su alta absorción en agua e hidroxiapatita ha demostrado excelentes resultados cuando es utilizado en procedimientos quirúrgicos sobre tejido óseo y tejidos blandos de la cavidad oral, remoción de caries en esmalte y dentina, remoción de restauraciones antiguas entre otras aplicaciones que corresponden a sus indicaciones más comunes.6,7
En cirugía de tejidos blandos se le han atribuido al láser de Er, Cr: YSGG (2780 nm) diferentes beneficios que lo aventajan frente a los instrumentos tradicionales, algunos son:8,9,10
Se elimina el uso de anestesia (solo uso de anestesia tópica);
Excelente hemostasia por el efecto fototérmico del instrumento, el cual logra el sellado de vasos sanguíneos y acelera el proceso de coagulación;
Disminución del dolor posoperatorio e inflamación, ya que, no existe trauma mecánico durante el corte. La luz irradiada a los tejidos durante el corte produce un drenaje linfático a nivel local que descongestiona las zonas donde existe inflamación y dolor; y
Reducción del potencial de contaminación bacteriana postoperatoria y rápida cicatrización en comparación con los métodos convencionales.
Los beneficios anteriormente mencionados para el láser de Er, Cr: YSGG (2780 nm) se sustentan en los principios físicos que rigen su mecanismo de acción y en el efecto biológico que genera el instrumento sobre el tejido para realizar la incisión. Por lo tanto, los cambios a nivel histológico y molecular que ocurren en el tejido intervenido pueden reflejar el efecto del instrumento y se relacionan con el proceso de reparación y cicatrización de la mucosa.11,12)
Estos hallazgos son importantes para proveer evidencia científica que respalde las ventajas atribuidas al láser de Er, Cr: YSGG (2780 nm) como instrumento de primera elección para cirugía de tejidos blandos. Por lo tanto, el objetivo de este artículo es describir los hallazgos histológicos asociados al corte con láser de Er, Cr: YSGG de 2780 nm en muestras de encía obtenidas mediante gingivectomía.
Reporte del caso
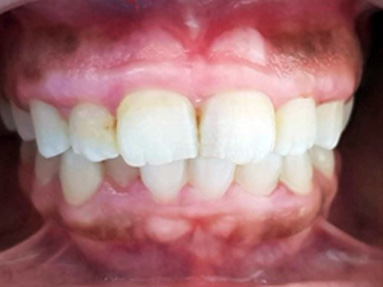
Paciente femenina, de 21 años, sistémicamente sana. Asistió a la consulta por presentar inconformidad estética, lo que argumentó diciendo que exponía gran cantidad de encía al sonreír. No presentó antecedentes médicos personales o familiares relevantes. Al realizar el examen estomatológico se observó una exposición de banda de encía queratinizada en el maxilar superior mayor a 4 mm, tejido gingival de color rosa y textura normal dentro de los parámetros periodontales, de consistencia firme y con ausencia de sangrado al sondaje (Fig. 1). Como plan de tratamiento se indicó enseñanza en salud oral, profilaxis, gingivectomía y gingivoplastia con láser de Er, Cr: YSGG de 2780 nm de longitud de onda en maxilar superior. Se le explicó a la paciente el procedimiento a realizar, luego aceptó voluntariamente la realización del procedimiento quirúrgico mediante la firma de un consentimiento informado.
Gingivectomía
Inicialmente se realizó sondaje periodontal con sonda Michigan para determinar altura y cantidad de tejido gingival a cortar y se aplicó anestesia tópica (Roxicaína® solución tópica - atomizador) en la zona a intervenir. Para el procedimiento se empleó un equipo Waterlase® (BIOLASE ®), configurado bajo un protocolo de 2,5 W, 75 Hz, modo H, aire 20, agua 40, Tip (GOLD) MT4. El corte gingival se inició en dientes 11 y 21, que fueron utilizados como guías para determinar la altura del zenit gingival, seguidamente se realizó corte a nivel de dientes 12, 13, 14, 22, 23 y 24.
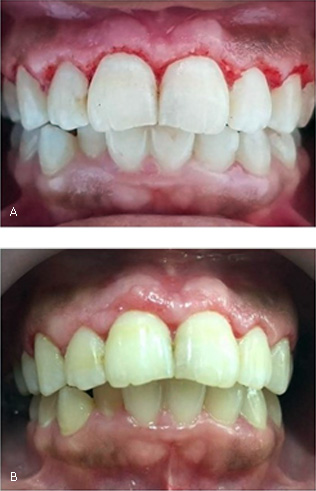
Durante el procedimiento se observó sangrado leve, buena hemostasia. La paciente refirió dolor intraoperatorio con puntuación 3 de acuerdo con la escala visual analógica del dolor (EVA), el que fue clasificado como un dolor leve de acuerdo a la escala. Al examinar las características macroscópicas de la zona intervenida, se observó margen de resección gingival regular con eritema y sangrado leve sin signos de carbonización del tejido. Muestras de tejido gingival fueron almacenadas y fijadas en tubos limpios con formaldehído al 10 % para realizar análisis histológicos (tinción con hematoxilina-eosina). Al finalizar el procedimiento se indicó a la paciente el consumo de alimentos blandos y fríos durante al menos 24 horas. Se realizó control a los 4 y 15 días posteriores a la cirugía. En los controles la paciente no reportó dolor ni sangrado gingival. Al cuarto día se observó reparación casi total del margen gingival, con zonas localizadas de eritema en las papilas interdentales (Fig. 2).
Reporte histológico
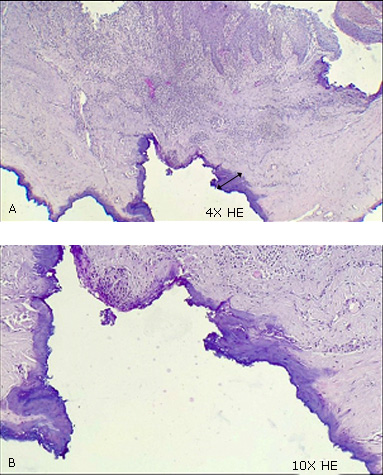
Mucosa cuyo epitelio escamoso reveló acantosis y espongiosis. La lámina propia presenta intenso infiltrado inflamatorio de predominio mononuclear (linfocitos y plasmocitos) con fibrosis del tejido conectivo. Los márgenes de resección profundos muestran cambios del colágeno por lesión térmica asociada al instrumento de corte, que se muestran como una banda delgada de colágeno con basofilia cerca al borde de resección, pero que permite observar la morfología de los fibroblastos rodeados por colágeno alterado (Fig. 3).
Discusión
El uso del láser de Er, Cr: YSGG (2780nm) en este caso tuvo dos evidentes beneficios: 1) la ausencia de inflamación y dolor posoperatorio y, 2) la reparación rápida del epitelio gingival. Tan solo cuatro días posterior a la intervención quirúrgica, se observó un proceso de cicatrización casi completa. El efecto térmico del instrumento fue mínimo, se limitó al borde, sin profundizar más allá del margen de resección. Se preservó la morfología de los fibroblastos y no hubo carbonización del tejido. Los hallazgos histológicos descritos ut supra son totalmente congruentes con las características clínicas observadas en el paciente, con la ausencia de dolor posoperatorio y con su proceso de cicatrización posterior al procedimiento.
Este resultado es respaldado por los reportes de Cercadillo y otros13, quienes desarrollaron un estudio in vitro en mucosa oral de cerdo para evaluar histológicamente el efecto térmico producido en tejidos blandos irradiados con láser de CO2, láser de Er,Cr:YSGG y láseres de diodo. Estos autores describieron que las muestras obtenidas con láser de Er, Cr: YSGG, con aerosol de agua/aire mostraron una pequeña área de carbonización en menos del 25 % del perímetro del margen de irradiación. En cuanto a características macroscópicas, las muestras irradiadas con este láser exhibieron carbonización insignificante en el área de corte del tejido blando.
España y otros14) expusieron en su revisión que la interacción de los láseres de alta potencia con los tejidos produce un efecto fototérmico y que, en dependencia de la temperatura que adquiera el tejido diana, se pueden producir diferentes efectos, los que pueden variar desde una hipertermia transitoria hasta la carbonización del tejido. En el caso del láser de Er, Cr: YSGG (2780nm), el efecto de carbonización se redujo al emplear el aerosol de agua, cuya función principal es refrigerar la zona de intervención durante el corte con el fin de proteger los tejidos adyacentes, minimizar el efecto térmico y favorecer su mecanismo de acción.
En las heridas por daño térmico existe una fase inflamatoria inicial en la que migran neutrófilos y monocitos al sitio de la lesión a través de la vasodilatación localizada y la extravasación de fluidos, lo que da inicio a una respuesta inmune. La fase inflamatoria sirve, no solo para prevenir la infección durante la curación, sino también para degradar el tejido necrótico y activar las señales necesarias para la reparación de la herida.15) Al no existir carbonización en el tejido y mantenerse la integridad celular, el epitelio inicia casi de manera inmediata el proceso de reparación, por otro lado, cuando sí existe carbonización, el epitelio promueve una serie de eventos celulares previos para inducir la necrosis y la eliminación del tejido quemado, esto se traduce en inflamación posoperatoria y extensión del tiempo de cicatrización.
El estudio de Ryu y otros16 comparó la cicatrización de heridas después de realizar incisiones con bisturí, láser de CO2 y láser Er, Cr: YSGG (2780 nm) en la mucosa oral de cobayos. En los resultados se explicó que el láser de Er, Cr: YSGG generó una respuesta inflamatoria baja, menos ulceración y generó un daño mínimo del tejido mucoperióstico. Por tales razones concluyeron que el láser tiene muchas ventajas para su uso en cirugía oral.
La aplicabilidad del láser de Er, Cr: YSGG (2780 nm) en el área odontológica es amplia y por su gran utilidad cada vez se realizan más estudios que demuestran científicamente las ventajas que se le atribuyen. Es importante que el odontólogo tenga conocimientos de los fundamentos del uso del láser para utilizarlo confiadamente.
En conclusión, el láser Er, Cr: YSGG (2780 nm) preservó la morfología de los fibroblastos después del corte, no hubo evidencia de carbonización, ni profundización de la lesión térmica en el tejido. Este instrumento fue una herramienta de gran utilidad para la ejecución del tratamiento en este caso. Tuvo ventajas importantes como la ausencia de dolor posoperatorio, buena hemostasia y la reparación epitelial casi completa en tan solo 4 días.