Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm vol.49 no.2 Ciudad de la Habana abr.-jun. 2015
ARTÍCULO DE REVISIÓN
Ciclótidos, proteínas circulares producidas por plantas con potencial farmacológico
Cyclotides, circular proteins produced by plants with pharmacological potential
Ing. Escarleth Contreras Puentes,I MSc. Antonio Díaz Caballero,I MSc. Arnulfo Taron DunoyerII
I Universidad de Cartagena. Facultad de Odontología, campus de Zaragocilla, Cartagena, Bolívar. Colombia.
II Facultad de Ingeniería, campus de piedra de Bolívar, Cartagena, Bolívar. Colombia.
RESUMEN
Los ciclótidos son proteínas circulares de alrededor de 28 a 37 residuos de aminoácidos, poseen una marcada importancia biológica gracias a su estructura cíclica que le proporciona estabilidad. En este estudio se realizó una búsqueda bibliográfica en las bases de datos EBSCOHOST, Science Direct, Pubmed y ACS publication. Los artículos seleccionados entre los años 2010 a 2014 contenían las palabras claves cyclotides, cyclic peptides, macrocyclic peptides y drugs, se seleccionaron teniendo en cuenta como criterios de inclusión artículos con texto completo en ingles, de investigaciones experimentales originales, relacionadas con el uso de ciclótidos para el diseño de fármacos. Mediante el análisis de los artículos se encontró que los ciclótidos tienen un amplio rango de bioactividades tales como insecticida, uterotónica, antimicrobiana, antiVIH, anticáncer, hemolítica, antagonista de la neurotensina e inhibidora de la tripsina por lo cual se pueden emplear como bases para la elaboración de nuevos fármacos que puedan ser aplicados al tratamiento de distintas enfermedades.
Palabras clave: ciclótidos, proteínas circulares, fármacos, estructura, actividad biológica.
ABSTRACT
The ciclotydes are circular proteins of 28 to 37 aminoacid that have a unique and strong cyclic structural motif which confers stability and relevant biological activities. In this study we searched in data bases EBSCOHOST, Science Direct, Pubmed and ACS publication to identify relevant studies considering inclusion criteria such as full-text articles in English, original experimental research related to the use of cyclotides in drug design. The biological activities of the cyclotides have been reported as insecticide, uterotonic, antimicrobial, antiHIV, anticancer, hemolytic, neurotensin antagonist and inhibitor of trypsin which can be used as basis for the development of new drugs that can be applied to the treatment of various diseases.
Keywords: ciclotydes, circular peptides, drugs, structure, biological activity.
INTRODUCCIÓN
Los ciclótidos son péptidos aislados a partir de plantas que presentan un esqueleto cíclico continuo de uniones peptídicas con seis residuos de cisteína que forman puentes disulfuro para estabilizar la molécula. Esta característica estructural conocida como el nudo cíclico de cisteína le proporciona a los ciclótidos alta estabilidad a la degradación térmica, enzimática y química. Esto permite su intervención en los mecanismos de defensa de las plantas contra el ataque de microorganismos e insectos. Los bucles del esqueleto del ciclótido corresponden a las regiones entre los residuos de cisteína que están constituidas por una diversidad de aminoácidos que podrían ser intercambiados por nuevos aminoácidos y así constituir nuevas estructuras con mejores actividades biológica.1
Los ciclótidos se han estudiado ampliamente en especies vegetales, como por ejemplo, las familias de plantas: Rubiácea y Violaceae, comportándose como moléculas de defensa contra los depredadores. De igual forma, también presentan importancia biológica por poseer actividad uterotónica, antiVIH, antitumoral y antimicrobiana, por lo que se consideran con potencial farmacológico promisorio.2
Debido a la combinación del nudo de cistina y el esqueleto circular que contienen los ciclótidos son susceptibles de síntesis química, lo cual los hacen más tolerantes a una amplia gama de sustituciones de los residuos de aminoácidos; por este motivo, son efectivos como moldes de péptidos para la introducción de un amplio rango de diferentes bioactividades.2 En definitiva, el estudio de los ciclótidos ha generado nuevas posibilidades para la ingeniería de péptidos bioactivos y el desarrollo de estrategias que permitan sintetizar productos químicos que contribuyan al diseño y obtención de novedosos fármacos o el diseño de nuevos ciclótidos mejorados con aplicaciones farmacéuticas.1 El estudio se realizó para lograr la respuesta a la pregunta ¿Cuál es el potencial farmacológico que presentan los ciclótidos en la actualidad, de acuerdo a la literatura disponible en las bases de datos?
MÉTODOS
Mediante las bases de datos EBSCOHOST, Science Direct, Pubmed, ACS publication, se realizo la búsqueda de artículos de alto rigor científico, desde los años 2010 a 2014, se emplea como palabras clave cyclotides, cyclic peptides, macrocyclic peptides y drugs. La búsqueda se realizó limitada a artículos en ingles con los siguientes requisitos de inclusión: artículos originales con texto completo en ingles, estudios experimentales con metodologías relacionadas al uso de ciclótidos con potencialidades orientadas al diseño de fármacos para el tratamiento de diferentes enfermedades.
RESULTADOS
En las bases de datos consultadas se hallaron en total 2 832 332 artículos, con las palabras claves escogidas y sus combinaciones (tabla). De los cuales se seleccionaron 20 referencias que cumplieron con los criterios de inclusión. De igual forma fue tenida en cuenta la relevancia del estudio y su marcada relación con el tema. Para desarrollar de forma acertada el análisis de los artículos concernientes al uso de la estructura rígida de los ciclótidos como plataformas para el mejoramiento de fármacos.
PROTEÍNAS CIRCULARES
Las proteínas son moléculas formadas por una cadena lineal de aminoácidos que se pliega en el espacio, adoptando una configuración tridimensional determinada que define su función biológica. Sin embargo, este carácter lineal de las proteínas convencionales resta estabilidad a las moléculas, pues sus extremos, muchas veces flexibles, sirven de diana para numerosas enzimas proteolíticas. Para evitar esta situación, algunas proteínas presentan modificaciones postraduccionales tales como acetilaciones, hidroxilaciones o glicosilaciones, que las hace resistentes a las exoproteasas.3
En los hongos y las bacterias se describe la producción de moléculas denominadas péptidas cíclicas (menos de 12 aminoácidos) de síntesis no ribosómica, que son sintetizados gracias a la existencia de enzimas con actividad péptido sintasa. Estos péptidos resultan menos sensibles a las proteasas ya que presentan aminoácidos modificados mediante metilaciones, cambios en la quiralidad y enlaces no peptídicos, además, algunos de ellos para aumentar su estabilidad, establecen conexiones intramoleculares mediante puentes disulfuro, que hacen que, al menos, parte de la molécula adopte una estructura cíclica.1
Hasta el momento no existen mecanismos que expliquen que los extremos de las proteínas no puedan estar unidos por enlaces peptídicos al igual que el resto de la cadena, por lo cual, se admite la existencia de proteínas circulares de síntesis ribosómica descritas en microorganismos, plantas y animales. Se trata de moléculas constituidas por ciclos continuos de uniones peptídicas, por tanto, carentes de extremos amino o carboxilo y con estructura tridimensional definida. Son moléculas bien diferenciadas de los péptidos cíclicos de síntesis no ribosómica descritos previamente.4 Actualmente las proteínas circulares se convierten en blanco de primera línea de investigación, debido a sus ya comprobadas ventajas e interés biotecnológico.
Existen diversidad de proteínas circulares de origen natural con una estructura tridimensional bien definida y motivos que se repiten regularmente en su estructura secundaria, sin diferencias notables con los que aparecen en las proteínas lineales; dentro de este vasto grupo de proteínas, se encuentran las producidas por plantas, denominadas también ciclótidos, las cuales constituyen el grupo más abundante de proteínas circulares. El descubrimiento de estas proteínas macrocíclicas bioactivas se produjo en la década de los años setenta con la búsqueda de nuevos compuestos para aplicación en medicina natural.4
CICLÓTIDOS: proteínas circulares producidas por plantas
Los ciclótidos conforman una familia de miniproteínas circulares, aislados de varias especies pertenecientes principalmente a tres familias de plantas Rubiaceae, Violaceae y Cucurbitaceae, con un amplio rango de bioactividades; son proteínas cíclicas con 28 a 37 residuos de aminoácidos, la diferencia fundamental con las proteínas tradicionales, es que están constituidas por un ciclo continuo con uniones peptídicas y además poseen tres puentes disulfuro que enlazan los seis residuos de cisteína formando de esta manera un nudo cíclico de cistina (NCC). Este nudo de cistina se forma cuando los dos puentes disulfuro enlazan extremos opuestos de segmentos peptídicos del anillo, los cuales a su vez están atravesados por un tercer puente disulfuro, de esta manera, la combinación del nudo de cistina y el esqueleto cíclico forman el nudo cíclico de cistina (NCC).5
El NCC, también denominado como motivo CCK (Cyclic-Cystine-Knot) es la responsable de la gran rigidez estructural y notable estabilidad térmica, química y enzimática, características que los diferencian de los péptidos lineales; puesto que la estructura lineal le resta estabilidad a la molécula y son más susceptibles a transformaciones enzimáticas o químicas. Razón por la cual, los ciclótidos se convierten en objeto de investigación e interés para las industrias farmacéutica y agrícola en general.6
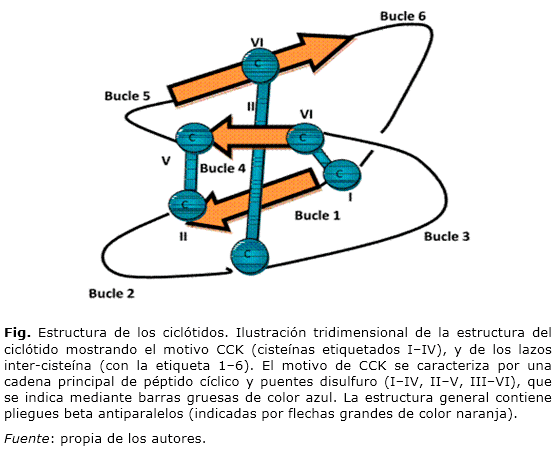
A pesar del pequeño número de aminoácidos existentes en la molécula y la presencia de residuos muy conservados, los ciclótidos muestran un grado de diversidad que permite su división en dos subfamilias (Mobius y Bracelet) de acuerdo con la similitud en la secuencia, tamaño de las asas, estructuras e incluso mecanismo de acción.4 Los ciclótidos en general se nombran con base a los seis residuos de cisteína enumerados con números romanos de uno a seis en el orden en el cual se encuentran en la línea precursora (Fig.). En los bucles (vueltas) del esqueleto del ciclótido están representadas las cadenas de aminoácidos responsables de las diversas actividades que presentan los mismos.5
ORÍGENES DE LOS CICLÓTIDOS
Su descubrimiento se enmarca entre 1960-1970, cuando mujeres en el Congo (África) utilizaban las infusiones de la planta Oldenlandia affinis (Rubiaceae) para acelerar el trabajo de parto, más tarde el agente activo fue aislado y se descubrió que el ciclótido estaba constituido con 30 residuos de aminoácidos y se le denomió Kalata B1.7,8 Originariamente, estos péptidos macrocíclicos fueron descubiertos en programas de tamizado al azar o mediante estudios etnofarmacológicos de especies nativas, como fue el caso del Kalata B1. Las circulinas, aisladas de Chassalia parvifolia Shumann (Rubiaceae) fueron descubiertas por un tamizado al azar pero con actividad antiVIH. Varios péptidos de distintas especies de Viola fueron descubiertos a partir de un tamizaje de actividad hemolítica.9
SUBFAMILIAS DE LOS CICLÓTIDOS
Los ciclótidos se dividen principalmente en dos subfamilias, Brazalete y Mobius, esta clasificación se basa en la presencia o la ausencia de un residuo de cisprolina en el bucle5. Las subfamilias también se diferencian por el tamaño y contenido de aminoácidos.10
Los miembros de la subfamilia Mobius se caracterizan por la presencia de un enlace peptídico en cis delante de una pro conservada del asa 5, que introduce un giro en la cadena peptídica. Estos ciclótidos poseen 29 o 30 aminoácidos mayoritariamente hidrófobos, de los cuales el 60 % están muy conservados, por lo que la diversidad en este grupo es limitada. A esta subfamilia pertenecen los ciclótidos Kalata B1 y Kalata B2.2
Se han descrito más de 60 miembros de la subfamilia Bracelet. Todos ellos carecen del enlace peptídico en cis, por lo que se representan como un brazalete. Estas moléculas presentan entre 28 y 31 residuos, que son sólo 10 de los 20 aminoácidos naturales. Ninguna de las asas de las moléculas esta conservada. Tan sólo 10 residuos están conservados (las 6 cis responsables del motivo CCK). Pertenecen a esta subfamilia la circulina A11 y la cicloviolacina O1.12
CICLÓTIDOS EN LAS FAMILIAS DE PLANTAS CURCUBITACEAE, RUBIACEAE Y VIOLACEAE
Más de 160 ciclótidos se han elucidado de estas tres familias hasta ahora, y es la familia Violaceae la que contribuye con un porcentaje mayor, dado que en ella se han encontrado ciclótidos en todos los géneros investigados hasta el momento.6 También están en la familia Fabaceae con uso en medicina tradicional al facilitar el trabajo de parto, de manera similar con el primer ciclótido aislado (Kalata B1).5 Los ciclótidos se encuentran en una amplia gama de tejidos incluyendo hojas, flores, tallos y raíces.5
Kalata B1, las circulinas, cyclopsychotride, varios péptidos de Viola arvensis Murray (Violacea) se descubrieron en programas de cribaje al azar o mediante estudios etnofarmacológicos de especies nativas.9 Estos péptidos tienen distintas actividades biológicas: kalata B1, cyclopsychotride A y circulinas A y B inhiben el crecimiento de microorganismos y la kalata B1 posee actividad insecticida.13
Pranting M y Cols12 determinaron la actividad antibacteriana del ciclótido Cycloviolacin de O2 (cyO2) aislado de Viola odorata contra Salmonella entéricas erovar Typhimurium LT2, Escherichia coli y Staphylococcus aureus; sus resultados demostraron que CyO2 inhibía eficazmente el crecimiento de Salmonella entéricas erovarty phimurium LT2 y Escherichia coli, mientras que contra Staphylococcus aureus no poseía elevada actividad. Dichas conclusiones concuerdan con los estudios de Tang y cols14 quienes indicaron que los ciclótidos aislados de las especies Viola labridorica (Violaceae) son inactivos frente a Staphylococcus aureus.
Las anteriores evidencias sugieren que los ciclótidos intervienen en los mecanismos de defensa contra microorganismos, debido a su presencia en todas las especies hasta ahora examinadas de la familia Violacea, entre las cuales se destaca la especie Psychotrial eptothyrsavar, Longicarpa (Rubiaceae).15 Sin embargo, la distribución de estos aun no ha sido dilucidada por completo en la familia de plantas Rubiaceae. Por tanto, se hace necesario más investigaciones que permitan caracterizar e identificar los ciclótidos presentes en las especies vegetales.
ACTIVIDAD BIOLÓGICA DE LOS CICLÓTIDOS
Los ciclótidos se consideran de gran importancia en el campo medicinal y farmacéutico, al tener gran potencial como moléculas líderes para el desarrollo de nuevas drogas y nuevos agentes agroquímicos.16
El descubrimiento inicial del primer ciclótido Kalata B1 fue motivado por la observación de las contracciones uterinas después de la ingestión de una infusión de las hojas de la planta Oldenlandia affinis.17 La actividad anti-VIH, se observó por primera vez y fue llevada a cabo por el Instituto Nacional del cáncer en EE. UU como resultado de un tamizaje de productos naturales a los cuales se les realizó análisis de RMN y se determinó la presencia de dos péptidos más resistentes que el péptido estándar; además, se ejecutaron métodos de secuenciación y se consideraron como péptidos con actividad anti-VIH.11 Sin embargo, la verdadera razón por la cual los ciclótidos son producidos por las plantas es para intervenir en los mecanismos de defensa contra plagas; es por esto que el papel principal de los ciclótidos es comportarse como agentes insecticidas en los cultivos, ya que causan un retraso marcado del crecimiento y desarrollo de los insectos.18
Los estudios de antimicrobianos demuestran que algunos ciclótidos actúan sobre diferentes clases de bacterias; por ejemplo, el Kalata B1 presentó actividad frente a la bacteria grampositiva Staphylococcus aureus; mientras que circulina A y cyclopsychotride A actuaron contra bacterias grampositivas y gramnegativas.12
Todas estas actividades tienen la característica común de estar asociadas con la desorganización de las membranas; además, de formar poros grandes en las bicapas lipídicas, aunque las membranas probablemente sean el sitio de acción de su función natural en las plantas como moléculas de defensa. En general, los ciclótidos parecen tener preferencia por la fosfatidietanolamina g, la cual le da mayor afinidad por las membranas en fase desordenada como sucede con el Kalata B1.18,19
DISCUSIÓN
La aplicabilidad de los péptidos lineales, como drogas, es potencialmente limitada por su susceptibilidad al clivaje proteolítico y por su escasa biodisponibilidad; estas limitaciones podrían ser superadas con el empleo de la estructura de los ciclótidos como andamiaje para el desarrollo de nuevas drogas con diferentes actividades.
El amplio rango de actividades biológicas atribuidas a los ciclótidos indica que la estabilidad provista por NCC los convierte en modelos promisorios para nuevos agentes en las industrias farmacéutica y agrícola. Por esto se explora en diseñar estas miniproteínas cíclicas, con el fin de desarrollar análogos sintéticos, metabólicamente estables, en los que se pueda disociar la acción farmacológica específica de la citotoxicidad para producir potenciales modelos terapéuticos.20 Sobre esta estructura podrían injertarse aminoácidos diferentes a los de la secuencia nativa para obtener nuevas funcionalidades y actividades.21
En los bucles están expuestas las cadenas de aminoácidos responsables de las diversas actividades de los ciclótidos, un análisis en su secuencia da idea de las variaciones estructurales que podrían ser posibles en el diseño de nuevos ciclótidos con aplicaciones farmacéuticas.
Actualmente la existencia de productos farmacéuticos por descubrir es una de las razones más importantes para el estudio de las plantas, de las cuales provienen unas moléculas de gran trascendencia como son los ciclótidos (miniproteínas cíclicas). Estas moléculas son promisorias en la producción industrial de fármacos al ser aislados directamente de plantas o mediante su obtención por síntesis, los inconvenientes de los péptidos lineales se superan con el empleo de la estructura de NCC de los ciclótidos, como base para el desarrollo de nuevos medicamentos.
AGRADECIMIENTOS
A la Universidad de Cartagena por su buena labor en el fomento de la investigación.
Escarleth Contreras Puentes agradece a la Universidad de Cartagena y a Colciencias por el programa de joven investigador.
REFERENCIAS BIBLIOGRÁFICAS
1. Park S, Stromstedt AA, Goransson U. Cyclotide structure-activity relationships: qualitative and quantitative approaches linking cytotoxic and anthelmintic activity to the clustering of physicochemical forces. PloS one. 2014;9(3):e91430.
2. Hashempour H, Koehbach J, Daly NL, Ghassempour A, Gruber CW. Characterizing circular peptides in mixtures: sequence fragment assembly of cyclotides from a violet plant by MALDI-TOF/TOF mass spectrometry. Amino acids. 2013;44(2):581-95.
3. Wang CK, Clark RJ, Harvey PJ, Rosengren KJ, Cemazar M, Craik DJ. The role of conserved Glu residue on cyclotide stability and activity: a structural and functional study of kalata B12, a naturally occurring Glu to Asp mutant. Biochemistry. 2011;50(19):4077-86.
4. Garcia AE, Camarero JA. Biological activities of natural and engineered cyclotides, a novel molecular scaffold for peptide-based therapeutics. Current molecular pharmacology. 2010;3(3):153-63.
5. Poth AG, Colgrave ML, Philip R, Kerenga B, Daly NL, Anderson MA, et al. Discovery of cyclotides in the fabaceae plant family provides new insights into the cyclization, evolution, and distribution of circular proteins. ACS chemical biology. 2011;6(4):345-55.
6. Craik DJ, Conibear AC. The chemistry of cyclotides. The Journal of organic chemistry. 2011;76(12):4805-17.
7. Ireland DC, Clark RJ, Daly NL, Craik DJ. Isolation, sequencing, and structure-activity relationships of cyclotides. Journal of natural products. 2010;73(9):1610-22.
8. Gran L. Oxytocic principles of Oldenlandia affinis. Lloydia. 1973;36(2):174-8. Epub 1973/06/01.
9. Goransson U, Burman R, Gunasekera S, Stromstedt AA, Rosengren KJ. Circular proteins from plants and fungi. The Journal of biological chemistry. 2012;287(32):27001-6.
10. Burman R, Gruber CW, Rizzardi K, Herrmann A, Craik DJ, Gupta MP, et al. Cyclotide proteins and precursors from the genus Gloeospermum: filling a blank spot in the cyclotide map of Violaceae. Phytochemistry. 2010;71(1):13-20.
11. Henriques ST, Huang YH, Rosengren KJ, Franquelim HG, Carvalho FA, Johnson A, et al. Decoding the membrane activity of the cyclotide kalata B1: the importance of phosphatidylethanolamine phospholipids and lipid organization on hemolytic and anti-HIV activities. The Journal of biological chemistry. 2011;286(27):24231-41.
12. Pranting M, Loov C, Burman R, Goransson U, Andersson DI. The cyclotide cycloviolacin O2 from Viola odorata has potent bactericidal activity against Gram-negative bacteria. The Journal of antimicrobial chemotherapy. 2010;65(9):1964-71.
13. Sando L, Henriques ST, Foley F, Simonsen SM, Daly NL, Hall KN, et al. A Synthetic mirror image of kalata B1 reveals that cyclotide activity is independent of a protein receptor. Chembiochem. 2011;12(16):2456-62.
14. Tang J, Wang CK, Pan X, Yan H, Zeng G, Xu W, et al. Isolation and characterization of cytotoxic cyclotides from Viola tricolor. Peptides. 2010;31(8):1434-40.
15. Gerlach SL, Burman R, Bohlin L, Mondal D, Goransson U. Isolation, characterization, and bioactivity of cyclotides from the Micronesian plant Psychotria leptothyrsa. Journal of natural products. 2010;73(7):1207-13.
16. Yeshak MY, Burman R, Asres K, Goransson U. Cyclotides from an extreme habitat: characterization of cyclic peptides from Viola abyssinica of the Ethiopian highlands. Journal of natural products. 2011;74(4):727-31.
17. Craik DJ, Mylne JS, Daly NL. Cyclotides: macrocyclic peptides with applications in drug design and agriculture. Cellular and molecular life sciences. CMLS. 2010;67(1):9-16.
18. Craik DJ. Host-defense activities of cyclotides. Toxins. 2012;4(2):139-56.
19. Nawae W, Hannongbua S, Ruengjitchatchawalya M. Defining the membrane disruption mechanism of kalata B1 via coarse-grained molecular dynamics simulations. Scientific reports. 2014;4:3933.
20. Tam JP, Lu YA, Yang JL, Chiu KW. An unusual structural motif of antimicrobial peptides containing end-to-end macrocycle and cystine-knot disulfides. Proceedings of the National Academy of Sciences of the United States of America. 1999;96(16):8913-8.
21. Craik DJ. Plant cyclotides: circular, knotted peptide toxins. Toxicon. 2001;39(12):1809-13.
Recibido: 7 de mayo de 2014.
Aprobado: 15 de septiembre de 2014.
Escarleth Contreras Puentes, Antonio Díaz Caballero. Universidad de Cartagena, Facultad de Odontología campus de Zaragocilla, Cartagena, Bolívar. Colombia. Teléfono: 057 + (5)6698191 EXT 110.
Correos electrónicos: scarleth.contreras@gmail.com, adiazc1@unicrtagena.edu.com