Introducción
A pesar de los avances en el tratamiento antibiótico y las medidas para modular la respuesta inmunitaria, la sepsis continúa teniendo una elevada mortalidad, que alcanza más del 40 %, con una incidencia en aumento.1,2,3,4 Existe en la actualidad suficiente evidencia científica para afirmar que la aplicación precoz y dirigida de una serie de medidas preventivas, diagnóstico-terapéuticas, mejoran de manera significativa la supervivencia. También existe la certeza de que el seguimiento de estas medidas tiene un cumplimiento insuficiente en el entorno hospitalario.5,6,7
La sepsis requiere una identificación rápida y un tratamiento como enfermedad tiempo-dependiente, o sea, en la que el retraso diagnóstico o terapéutico influye negativamente en la evolución del proceso y, por tanto, es de especial interés para las áreas de urgencias. Las sociedades científicas, conscientes de esta situación, lanzaron en el año 2002 una campaña, la Surviving Sepsis Campaign, centrada en el manejo de la sepsis en los centros asistenciales, fundamentalmente en el ámbito de la Unidades de Cuidados Intensivos (UCI).8 Por su importancia, las maneras en que estos temas son enfocados se someten constantemente a revisión y actualización.9
Las infecciones asociadas a los cuidados sanitarios (IACS) son las que se adquieren en el hospital, ocasionadas por la flora intrahospitalaria y en ocasiones condicionadas por el microbiota del personal de salud y del mismo paciente. Esto representa un problema de gran importancia clínica y epidemiológica, debido a que condicionan mayores tasas de morbilidad y mortalidad, con extensión de los días de hospitalización y dispendio de los recursos económicos. Ningún país escapa a tal situación en constante ascenso.1,3,6
La situación actual plantea un incremento multifactorial de las infecciones en las UCI, pues constituyen áreas de alto riesgo, de dos a cinco veces mayor que otras áreas de un hospital. Las UCI están relacionadas con el uso de métodos invasivos: accesos vasculares, catéteres urinarios y tubos endotraqueales, entre otros procederes que incrementan de forma significativa el riesgo de adquirir infecciones nosocomiales.7
El Centro de Control de Enfermedades de Atlanta comunicó que solo en los Estados Unidos más de 80 000 pacientes mueren anualmente debido a una infección asociada a los cuidados médicos, las cuales originan, además, un prolongado tiempo de hospitalización, con una carga económica de unos 5000 millones de dólares al año.10)
El conocimiento de la importancia de las UCI en la génesis de las IACS y el interés de intensivistas y epidemiólogos en la enfermedad infecciosa del paciente crítico han facilitado el diseño de programas específicos de recogida de información para el registro de las infecciones en los pacientes ingresados en los servicios de cuidados intensivos. Estos programas permiten, además del control de las infecciones adquiridas en la UCI, el seguimiento administrativo, el registro de los microorganismos aislados, incluida la sensibilidad a los antibióticos de referencia y los antibióticos que se han prescrito para cada enfermo, tanto en la UCI como en otros servicios del hospital.1,3,5
La información obtenida sobre sepsis nosocomial facilitará al personal del hospital, médicos, enfermeras, administradores y otros investigadores el conocimiento de la evolución de las tasas de estas infecciones, así como los cambios en los patrones de sensibilidad-resistencia de los agentes patógenos endémicos de cada UCI.
La poca información al respecto constituyó la motivación principal para el diseño y ejecución del presente estudio, que se propuso identificar los gérmenes más frecuentes en los cultivos y su resistencia a los antimicrobianos en la terapia intensiva del Hospital “Dr. Joaquín Albarrán”.
Métodos
Se realizó un estudio descriptivo, retrospectivo en el periodo comprendido de enero 2015 a diciembre del 2018, en el servicio de terapia intensiva del Hospital Clínico Quirúrgico Provincial “Dr. Joaquín Albarrán”. El universo estuvo constituido por 1847 cultivos realizados, de los cuales se seleccionaron 654 en los que se obtuvo crecimiento.
Se analizaron las siguientes variables: gérmenes aislados en el total de cultivos positivos y según tipo de muestra (esputo, hemocultivo, urocultivo) y resistencia antimicrobiana en los cinco gérmenes más frecuentes según año.
Los datos recogidos se analizaron mediante el procesador estadístico SPSS v.21.0. Para el análisis descriptivo se calcularon las distribuciones de frecuencias absolutas y relativas expresadas en porcentajes. Se utilizaron tablas para la presentación de la información.
Se tuvo en cuenta la aprobación de la institución y el consejo científico para el desarrollo y presentación de la investigación. No se necesitó consentimiento informado escrito de los pacientes, ya que no se realizó intervención distinta a la establecida en el servicio para la toma de muestra para cultivos.
Resultados
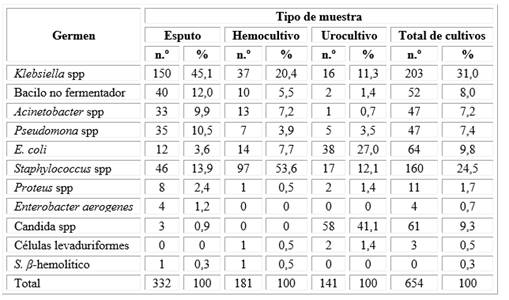
Del total de cultivos realizados, la Klebsiella Spp fue el germen más frecuente (31 %) seguido del Staphylococcus spp (24,5 %) y de la E. coli (9,8 %). Al analizar los gérmenes según tipo muestra, en los esputos, se mantuvo la Klebsiella spp (45,1 %) como la bacteria de mayor frecuencia de aparición, en los hemocultivos el Staphylococcus spp (53,6 %) y en los urocultivos, la candida spp (41,1 %) (Tabla 1).
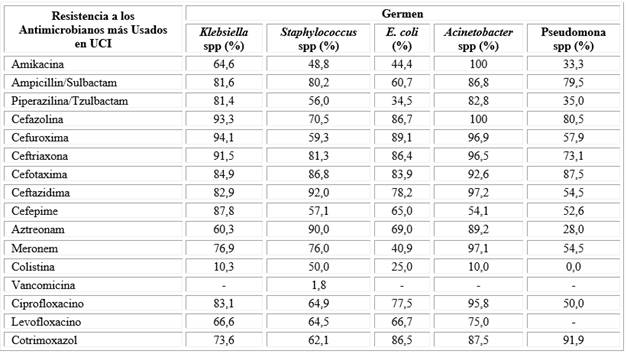
La Klebsiella spp fue el germen que con más frecuencia se aisló en el total de cultivos realizados, existiendo más de un 60,0 % de resistencia para todos los antibióticos más usados, excepto para la colistina (10,3 %). En orden de frecuencia le sigue el Staphylococcus spp. De los antimicrobianos más usados para tratar las infecciones por Staphylococcus spp, la vancomicina es la droga más recomendada con solo un 1,8 % de resistencia reportada.
El siguiente germen más aislado fue la E. coli. De los antimicrobianos disponibles, los que menos resistencia reportaron fueron la colistina (25,0 %), la piperazilina/tzobactam (34,5 %), para los demás existió más de un 40 % de resistencia. Aunque el Acinetobacter spp no fue tan frecuente en el servicio, tuvo más de un 70 % de resistencia para todos los antibióticos, excepto para la colistina, que se reporta cercano a un 10 % y el cefepime (54,1 %).
De los antimicrobianos más empleados contra la Pseudomona spp, la droga más segura fue la colistina (0 % de resistencia), otra opción fue el aztreonam (28 %) y la amikacina (33,3 %) de resistencia (Tabla 2).
Discusión
La literatura reporta que los microorganismos aislados con mayor frecuencia son los gram negativos intrahospitalarios, con una alta resistencia antibiótica. Weyland y otros11 realizaron un estudio en la UCI y reportaron como los gérmenes más frecuentes al Acinetobacter baumannii, Staphylococcus aureus, y pseudomona aeruginosa con un 37,9 %, 21,3 % y 20,9 %, respectivamente. Similares resultados fueron reportados por Leon-Chaua y otros12 en un estudio realizado en el Hospital Guillermo Almenara en Lima , Perú en el 2015, y por Guzman-Teran y otros, en Colombia.13)
En una investigación realizada en el Hospital Clínico Quirúrgico “Hermanos Ameijeiras” en el año 2012, la especie microbiana Acinetobacter baumanii causó más Neumonía Asociada a la Ventilación Mecánica (NAVM) con respecto a Pseudomona aeruginosa.14) En el estudio publicado por el proyecto DINUCIs,15) los gérmenes más frecuentes aislados en la NAVM de inicio precoz fue el Staphylococcus aureus y en la de inicio tardío, fue el Acinetobacter spp. En el Hospital Clínico Quirúrgico Docente “Dr. Salvador Allende” también se realizó un estudio similar de febrero a junio del 2015 por Monte y Martínez,16) en el que se encontraron resultados similares a los de los estudios mencionados ut supra. Lo anterior no coincide con lo reportado en el presente estudio donde la Klebsiella spp fue el germen más frecuente en el total de cultivos y en los esputos realizados, en los cuatro años analizados, sin embargo, llama la atención que los porcentajes reportados son similares a los descritos en la literatura.
Magret y otros17 aislaron en los hemocultivos el Staphylococcus aureus (22,6 %), Acinetobacter baumanii (17,9 %) y Pseudomona aeruginosa (14,3 %). Los estafilococos, en especial los coagulasa-negativos, son los más frecuentes en las infecciones relacionadas con dispositivo intravascular (DIV). En España, los cocos grampositivos suponen el 55-60 % de las bacteriemias relacionadas con catéter (BRC), seguidos de los bacilos gramnegativos (35 %) y de los hongos (8-9 %). Lo anterior coincide con lo encontrado en el presente estudio, donde se reportó el Staphylococcus en un 53,6 %.18
El factor de riesgo más importante para el desarrollo de la Infección del Tracto Urinario (ITU) nosocomial en un porcentaje que oscila entre el 72-73 % en los pacientes de UCI, según el Estudio Nacional de Vigilancia de Infección Nosocomial-Unidad de Cuidados Intensivos (ENVIN-UCI) de 2014, es la inserción del catéter. Una inadecuada higiene de manos por parte del personal sanitario puede dar lugar a episodios de bacteriuria de origen nosocomial. Además, este mecanismo es más frecuente en pacientes ancianos que tienen una colonización uretral por uropatógenos. La mayoría de las infecciones urinarias, tanto las adquiridas en la comunidad como las nosocomiales, son monomicrobianas, representando las polimicrobianas entre el 5 % y el 12 %. Existen numerosos microorganismos que pueden infectar las vías urinarias, los más frecuentes suelen ser los bacilos gramnegativos. Escherichia coli provoca alrededor del 80 % de las infecciones agudas de pacientes que no padecen anomalías urologías y no son portadores de sondas. Otros bacilos gramnegativos, como por ejemplo Klebsiella, Proteus y Enterobacter, provocan un porcentaje menor, y las pseudomonas y la serratia están asociadas a la manipulación, sondaje de larga evolución y obstrucción urológica por cálculos. Es frecuente la colonización de la orina por candida, sobre todo en pacientes diabéticos, los cuales han recibido varios tratamientos antibióticos y son portadores de una sonda urinaria que puede causar infección del tracto urinario.19
Un aspecto importante en el presente estudio fue la alta frecuencia de cultivos en los que no se obtuvo crecimiento bacteriano. Si bien la conducta ante el diagnóstico presuntivo de una sepsis es tomar la muestra y luego iniciar la terapia antibiótica sin esperar el resultado de esta, el aislamiento del germen constituye una necesidad para precisar la conducta terapéutica adecuada, particularmente en los casos en los que no responden a la selección antimicrobiana inicial.
En el estudio realizado por Guzmán-Terán y otros13 en una UCI de Colombia se evidenció una resistencia de un 50 % para la Cefuroxima, 20 % para la Ceftazidima, 25 % para la Ceftriaxona, 20 % para el Cefepime. Todos son niveles de resistencia mucho más bajo que los expuestos en nuestro estudio.
En otro estudio realizado en Pereira, Colombia, se constató una resistencia en el caso de la Klebsiella spp para las cefalosporinas de tercera y cuarta generación entre un 23-46 %: meropenem (8 %), aztronam (38 %), piperacilina + tazobactam (46 %). En el caso del Staphylococcus spp solo reportó un 50 % de resistencia para el oxacillin, niveles que se muestran más bajos que los expuestos en los resultados de la presente investigación.20
El uso de antibióticos frente a las infecciones (ya sea de forma empírica, preventiva o tras el diagnóstico de la infección y su evidencia microbiológica) es otro factor importante al analizar la trascendencia de la infección nosocomial. En Estados Unidos se estimó que en los hospitales se prescribe antibióticos al 23-37,8 % de los pacientes.19).Según la evaluación de diferentes protocolos, más de la mitad de las terapias antibióticas se consideran inapropiadas.19,21) Muchos de estos casos se dan en las prescripciones empíricas y sin previa consulta al laboratorio de microbiología, lo que puede favorecer el riesgo de infección.21 También hay que considerar un número de efectos colaterales tras el inicio del tratamiento antibiótico, tales como la emergencia de resistencias, la posibilidad de infecciones complejas y los efectos locales desagradables.
La política antibiótica llevada a cabo en cada hospital o unidad en los años anteriores condiciona la emergencia de nuevos patógenos. Los antibióticos más usados seleccionan unas cepas de bacterias o levaduras resistentes a dichos antibióticos que son los que se presentarán con mayor frecuencia. Las fuerzas interdisciplinarias formadas por farmacéuticos, microbiólogos y especialistas en enfermedades infecciosas deben monitorizar y evaluar el uso de antibióticos.22
El estudio mostró que la Klebsiella spp es el germen más frecuente en la terapia y en los esputos, en los hemocultivos predominó el Staphylococcus spp, en los urocultivos la candida. Existe más de un 40 % de resistencia in vitro para todos los antibióticos, siendo de elección para el tratamiento de los gram negativos la colistina y para el Staphylococcus spp, la vancomicina.