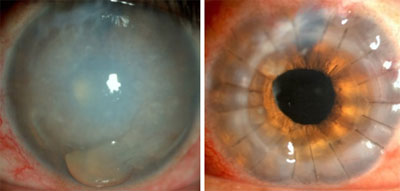
Introducción
La córnea es una estructura compleja que, además de tener un papel protector, es responsable de alrededor de las tres cuartas partes del poder óptico del ojo. La córnea normal no tiene vasos sanguíneos; el aporte de nutrientes y la eliminación de los productos metabólicos se realizan principalmente a través del humor acuoso en la cara posterior y por las lágrimas en la cara anterior, con un gradiente de oxígeno descendente anteroposterior. La córnea es el tejido más densamente inervados del cuerpo, con un plexo subepitelial y estromal más profundo, inervado ambos por la primera división del nervio trigémino. Por esta razón, las abrasiones y las afecciones corneales como la queratopatía bullosa se asocian con dolor, fotofobia y lagrimeo reflejo.1
Queratopatía bullosa pseudoafáquica
El grosor central promedio de la córnea humana adulta normal es de aproximadamente 550 µm para los caucásicos y permanece constante entre la segunda y la sexta décadas, pero varía con la hora del día y la raza.
La córnea se compone de seis capas de anterior a posterior: epitelio, capa de Bowman, estroma, membrana de Descemet, endotelio y la sexta membrana corneal entre la estroma y la membrana de Descemet, la que se ha propuesto recientemente, aunque algunas autoridades creen que es una continuación de la estoma posterior. La composición del estroma no es uniforme; el estroma anterior contiene una proporción más alta de dermatán y queratán sulfato, lo que hace que el estroma posterior sea más propenso a hincharse con el exceso de agua en los estados de disfunción endotelial.1,2,3
Los estudios inmunohistoquímicos mostraron depósitos de un componente específico de la matriz extracelular, como la fibrilina-1, la cual pertenece a la familia de proteínas de la matriz extracelular asociadas con microfibrillas elásticas y tenascin-C, que es una glicoproteína que tiene gran importancia en la curación y se encuentra en la parte posterior en las áreas fibróticas subepiteliales de las córneas con queratopatía bullosa.4
Los factores de crecimiento y las citoquinas influyen en la proliferación celular, la inflamación, la cicatrización y la fibrosis. Los niveles elevados de interleucina-2 (IL-2), interleuquina-8 (IL-8), insulina factor de crecimiento (IGF-1), factor de crecimiento transformante (TGF-β) y factor de médula ósea-4 (BMP-4) se encuentra en córneas con queratopatía bullosa. Las interacciones entre los factores de crecimiento y la matriz extracelular degradan las metaloproteínas por lo que pueden ser un mecanismo para la pérdida de transparencia corneal.4
La capa de células endoteliales comprende una zónula de oclusión incompleta que permite que las moléculas entren en el estroma corneal desde la cámara anterior. La bomba de Na +/ K ± ATPase activa extrae osmóticamente agua e iones del estroma corneal al humor acuoso, lo que ayuda a mantener el grosor y la transparencia de la córnea.5
La densidad celular endotelial normal es unas 3 000 células/mm2en adultos jóvenes. Este número disminuye un 0,6 % por año, y el tamaño de las células aumenta porque no pueden regenerarse. Con una densidad celular de alrededor de 500 células/mm2, se desarrolla edema corneal y se reduce la transparencia.1
Etiopatogenia
La principal causa de la queratopatía bullosa es la pérdida de células endoteliales por cirugía, trauma, distrofia corneal o degeneración. Es la cuarta causa del trasplante de córnea en un centro de referencia nacional.6 ocurre más frecuentemente en la sexta década de la vida o después de la cirugía de catarata con implantación de lente intraocular por cualquier técnica quirúrgica, aunque el aumento localizado de la temperatura, asociado con la sonda de facoemulsificación, puede provocar más daños térmicos en el tejido corneal adyacente. También se daña el endotelio, causado por una alta irrigación/aspiración que pueden resultar en un flujo turbulento con partículas de la catarata. De igual forma, el tiempo de duración de la facoemulsificación utilizada durante la cirugía es muy importante porque la energía del ultrasonido está asociada con la producción de radicales libres, que son reactivas con uno o más electrones no pareados en sus órbitas externas y pueden dañar el endotelio corneal por estrés oxidativo.7,8
Otras etiologías incluyen distrofias endoteliales, como la distrofia de Fuchs, las anomalías congénitas, las microcórneas, el glaucoma agudo, la endotelitis herpética o las cirugías, que pueden conducir a la pérdida endotelial, como la trabeculectomía, la lente intraocular con fijación escleral, los implantes de lente de cámara anterior para la corrección afáquica y fáquica de alta ametropía, así como después del láser de argón y la queratotomía radial.4
La queratopatía bullosa puede ocurrir en alrededor del 1 al 2 % de los pacientes sometidos a cirugía de cataratas, lo que representa alrededor de dos a cuatro millones de pacientes en todo el mundo.4
Opciones de tratamiento de la queratopatía bullosa pseudoafáquica
Soluciones osmóticas
El tratamiento clínico para el edema corneal debe basarse en agentes hipertónicos tópicos como el cloruro de sodio (5 %), los medicamentos antinflamatorios antiglaucoma, tópicos y/o sistémicos, ya que el aumento de la presión intraocular puede comprometer la función de las células endoteliales y lubricantes, que son útiles temporalmente ante el dolor experimentado por los pacientes. Las lentes de contacto terapéuticas mejoran los síntomas.8
Vendas de lentes de contacto
Las lentes de contacto como vendaje se han utilizado durante mucho tiempo en pacientes con queratopatía bullosa. Se pueden usar en combinación con una solución salina hipertónica sin conservantes para reducir la incomodidad del paciente y mejorar la agudeza visual de manera más efectiva.5
Punción del epitelio estromal anterior
La punción estromal anterior se utilizó inicialmente para tratar pacientes con erosión corneal recurrente; este abordaje quirúrgico puede aumentar la capacidad de adhesión del epitelio corneal con membrana basal. Más tarde, se utilizó la punción del epitelio estromal anterior (PEA) para tratar la queratopatía bullosa. Es un procedimiento simple, seguro, efectivo y de bajo costo para aliviar los síntomas en pacientes que no son elegibles para el trasplante de córnea. El mecanismo más importante para la PEA en el tratamiento de la queratopatía bullosa es la fibrosis inducida por cirugía, la cual hace que las células epiteliales formen un contacto directo con el estroma del sustrato. Esto puede formar una adhesión estable y servir para fortalecer los filamentos de hemidesmosomas. Las cicatrices fibróticas, como una nueva capa de formación de barrera, impiden que el humor acuoso se filtre hacia el subepitelio; por lo tanto, las ampollas corneales desaparecen gradualmente. La exposición a los nervios corneales podría eliminarse con la fibrosis, y reducir así la percepción del dolor de la córnea.9
Para los pacientes con queratopatía bullosa con mala función visual, y que no apliquen además para el trasplante de córnea por otras afecciones generales o mentales, la cirugía de PEA con el uso de lentes de contacto como vendaje es un tratamiento eficaz, reutilizable y económico, que puede mejorar la incomodidad ocular del paciente y tiene una clínica evidente de valor práctico.9
La queratectomía fototerapéutica (QF) puede mejorar el dolor al reducir el grosor de la córnea y esto ayudaría a las células endoteliales restantes a mantener la hidratación de la córnea.4 Varios estudios informaron que la QF era electiva en el tratamiento de pacientes con queratopatía bullosa de una variedad de etiologías. Informaron que las ampollas se resuelven y el dolor se elimina en una gran proporción de pacientes tratados con una ablación superficial.10,11)
El plexo nervioso sensorial principal en la córnea, que se deriva de la rama nasociliar de la división oftálmica del nervio trigémino, se encuentra en el estroma, en la región inmediatamente subepitelial, con un plexo de densidad más baja y más profundo en el estroma.10) El fundamento de este tratamiento es la ablación de estos plexos nerviosos, lo que reduce la sensación corneal. La cicatrización induce un aumento de proteínas extracelulares como la laminina, la fibronectina, el colágeno de tipo IV y las hemidesmosomas, que promueven una mayor adhesión entre el epitelio y el estroma.4,10
La QF profunda parece ser más exitosa en comparación con la QF superficial, a partir de la mayor cicatrización asociada, que también puede resultar en una mayor estabilidad del epitelio, y una ablación profunda tiene un efecto superior en la disminución del dolor por la ablación del plexo neural en la córnea.10
El mismo razonamiento que en la QF se usa también para la queratectomía lamelar automatizada, pero en este caso se usa un microquerátomo tradicional para la extracción del tejido corneal. Es un procedimiento rápido, que puede ser un factor importante para algunos pacientes ancianos que presentan dificultades para someterse a cirugías más prolongadas mientras permanecen en decúbito dorsal.4
Recubrimiento conjuntival según Gundersen
El colgajo o recubrimiento conjuntival de Gundersen cubre toda la córnea. En este procedimiento, la conjuntiva bulbar se diseca y se moviliza desde la cápsula de Tenon subyacente previo debridamiento epitelial pericorneal.12) Este colgajo puede aliviar el dolor en pacientes con queratopatía bullosa al cubrir las terminaciones nerviosas corneales expuestas con una superficie conjuntival intacta (Fig. 1).
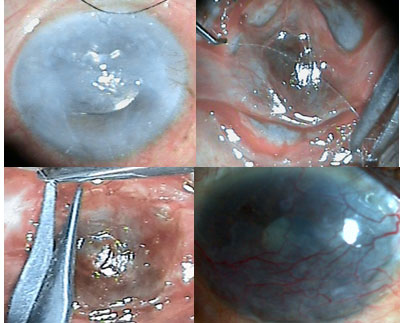
Fig. 1 Las imágenes representan el edema corneal crónico pseudoafáquico transoperatorio y el resultado posrrecubrimiento conjuntival bipediculado.
El procedimiento se puede combinar con el implante de membrana amniótica.(13) Las complicaciones posoperatorias incluyen un fórnix acortado, la retracción del colgajo y la posible pérdida de la conjuntiva sana para la posterior trabeculectomía. La tasa de retracción del colgajo varía del 10 al 15 %. Esta complicación responde a una tracción excesiva en el colgajo, los ojales y las fusiones de la mucosa conjuntival, por el crecimiento epitelial.(13) El recubrimiento se puede remover para un trasplante de córnea posterior en pacientes con potencial de recuperación visual, que alcanzó 0,2 con corrección y sin suturas, como se muestra en la Figura 2. La vascularización que permanece después de la eliminación del colgajo aumenta el riesgo de un rechazo posterior del injerto. También existe el riesgo de que la deficiencia de células madre del limbo requiera autoinjertos de este. Por lo tanto, un colgajo conjuntival es más apropiado para ojos con poco o ningún potencial visual.(13)
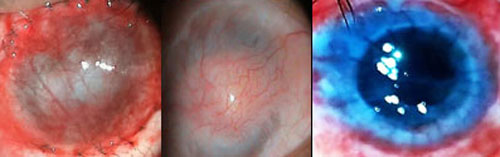
Fig. 2 Final de recubrimiento conjuntival ocho meses después. Remoción del recubrimiento y trasplante penetrante con fin óptico.
Implante de membrana amniótica
En el año 1999, Pires y otros usaron con éxito la membrana amniótica (MA) para controlar el dolor en pacientes con queratopatía bullosa. Ellos atribuyeron sus resultados a varios inhibidores de la proteasa ubicados en la matriz estromal de la MA, que son importantes para promover la curación epitelial y reducir la ulceración e inflamación del estroma.(14)
La membrana amniótica facilita la epitelización al proporcionar un sustrato adecuado, y una membrana basal normal al promover la migración y la adhesión de las células epiteliales. También se cree que la membrana produce varios factores de crecimiento que soportan el epitelio. Cuando se aplica la membrana amniótica a la córnea, se sabe que los fibroblastos derivados de queratocitos y los miofibroblastos migran desde el estroma corneal al estroma amniótico. Según Dos Santos, Paris y otros,(15) esto contribuye a la fibrosis subepitelial y también ancla la lámina epitelial de amnios a la superficie corneal. El implante de membrana amniótica es eficaz para controlar el dolor en pacientes con queratopatía bullosa pseudoafáquica; no induce neovascularización, pero no es la primera opción de tratamiento, teniendo en cuenta el costo de su adquisición, esterilización, preservación, adecuada aplicación y el tiempo de evolución posoperatorio para evaluar los resultados.(15)
Inhibición de la quinasa asociada a Rho
La vía Rho/Rho-kinase (ROCK) regula la migración y la proliferación celular, así como la apoptosis. Y-27632. Un inhibidor selectivo de ROCK puede promover la adhesión y la proliferación de células endoteliales de la córnea al disminuir la apoptosis inducida por disociación.(16) Este agente se puede usar in vivo como gotas oculares o ex vivo para expandir las células endoteliales de la córnea humana en medio de cultivo.
En un estudio clínico,(17) la congelación transcorneal se realizó con una varilla de acero inoxidable con un diámetro de 2 mm en ocho ojos de ocho pacientes con descompensación corneal, causada por distrofia corneal endotelial de Fuchs de inicio tardío, láser de argón o queratopatía en síndrome de pseudoexfoliación. Luego se aplicaron las gotas para los ojos Y-27632 seis veces al día durante una semana. Tres de cada cuatro ojos con edema corneal central causado por distrofia corneal endotelial de Fuchs demostraron una disminución significativa en la paquimetría central, que se mantuvo con el tiempo. Los cuatro ojos restantes con edema corneal difuso no tuvieron mejoría en la agudeza visual ni en la paquimetría corneal. Las células endoteliales corneales humanas no demostraron alteraciones celulares ni toxicidad después del tratamiento con un inhibidor de ROCK. Por lo tanto, la inhibición tópica de ROCK se puede utilizar como una alternativa al trasplante de córnea en pacientes con descompensación corneal temprana.(17)
Recientemente, se inyectaron células endoteliales corneales humanas cultivadas suplementadas con un inhibidor de ROCK en la cámara anterior en 11 ojos con queratopatía bullosa. Después de 24 semanas de inyección, todas las córneas estaban despejadas y nueve ojos lograron una mejoría en la agudeza visual mejor corregida de más de dos líneas.(18) La combinación de ácido hialurónico y Y-27632 puede mejorar la eficiencia de la adhesión celular como resultado de la unión, lo que permite el cultivo de células endoteliales de córneas de donantes más viejas.(19)
Enlace cruzado de colágeno corneal
El enlace cruzado de colágeno corneal (CXL) con las radiaciones de riboflavina y ultravioleta A (UVA) es un proceso fotoquímico que introdujeron Seiler y Spoerl en la Universidad de Dresde para el tratamiento de trastornos ectásicos de la córnea, como queratoconos y ectasias pos LASIK.(20)
La CXL corneal se considera una nueva herramienta en la lucha por la reducción temporal del edema corneal en pacientes con queratopatía ampollosa. Se ha encontrado que mejora la transparencia corneal, el grosor corneal y el dolor ocular después de la cirugía.(21)
El mecanismo de acción propuesto es que la riboflavina absorbe la luz UVA, lo que resulta en la producción de radicales de oxígeno libres. Estos radicales de oxígeno altamente reactivos inducen la reticulación del colágeno del estroma corneal y fortalecen la córnea.
Diferentes estudios demostraron que el CXL corneal mejora la transparencia, el grosor corneal y el dolor ocular un mes después de la operación. Este alivio sintomático fue probablemente el resultado de la compactación del estroma inducida por CXL y la reducción de la formación de bullas. Sin embargo, no parece tener un efecto duradero para disminuir el dolor y mantener la transparencia corneal.(21)
Trasplante de córnea
El trasplante de córnea sigue siendo el tratamiento de referencia para los pacientes con queratopatía bullosa y potencial visual, ya que proporciona alivio sintomático y rehabilitación funcional de la agudeza visual.(22) Algunas limitaciones, como la recuperación de la agudeza visual, responden al alto astigmatismo y, aunque la córnea es el tejido trasplantado más común del cuerpo humano, la tasa de éxito de los injertos corneales está influida por el riesgo de rechazo(6,23,24,25,26,27) (Fig. 3,4 y 5).
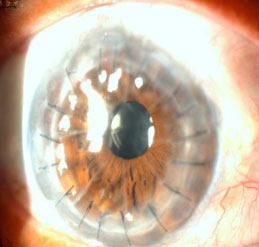
Fig. 5 Queratoplastia penetrante al año y medio. Se utilizó donante con queratotomía radial y buen endotelio central. Se observa transparencia postrasplante penetrante.
En los procedimientos de queratoplastia lamelar posterior (LK) y la queratoplastia endotelial recientes (EK), solo se trasplantan las capas internas de la córnea y existen múltiples variantes de este procedimiento, que incluyen la EK lamelar profunda, la extracción de Descemet (automatizada) EK (DSEK o DSAEK),23) los que no han tenido la evaluación conclusiva en el decursar del tiempo y que de no lograr el objetivo restaurador queda la posibilidad del trasplante penetrante de todas las capas corneales.
La técnica de queratoplastia lamelar posterior requiere tejido donante con alta celularidad endotelial; habilidad y experiencia quirúrgica; instrumental automatizado o no, pero adecuado y de preferencia cápsula posterior íntegra, pues la presencia de vítreo dificulta cualquier acción necesaria en la cámara anterior. Tiene la ventaja de la preservación de la superficie del receptor. Es una técnica prometedora, pero la pérdida de células endoteliales es mayor que en la queratoplastia penetrante de acuerdo con el parecer de Domingues y otros.4
Conclusiones
Se demuestra que el trasplante penetrante de córnea es un tratamiento generalizado para mejorar la sintomatología y la agudeza visual en la queratopatía pseudoafáquica. Los tratamientos alternativos para los pacientes sin potencial visual, como la terapia clínica medicamentosa, el uso de lentes de contacto terapéuticas, la punción del estroma anterior y los colgajos conjuntivales demuestran efectividad. El trasplante de membrana amniótica y la queratectomía fototerapéutica pueden mejorar la calidad de vida.