INTRODUCCIÓN
La hernia discal intradural es una condición rara, y representa el 0,26-0,30 % de todas las hernias;1 de ellas, solo el 3 % son cervicales, y en un 8,7 % se expresan clínicamente por radiculopatía; la gran mayoría de los pacientes son diagnosticados durante el acto transoperatorio como portadores de esta.2
Los nuevos déficits neurológicos son complicaciones poco frecuentes después de la cirugía de columna. Ocurren en una tasa inferior al 1%.3
La incidencia de daño por isquemia-re perfusión secundario a una descompresión cervical varía desde 2 a 5,7 %, aunque en laminectomía descompresiva para estenosis torácica puede ser del 14,5 %.4
El deterioro neurológico pos cirugía puede ser atribuido a la reperfusión de la médula espinal; en imagen de resonancia magnética la isquemia y el edema muestran aumento de la intensidad de señal, explicando el término White Cord Syndrome (WCS).5
El presente caso muestra una combinación altamente inusual, además de ser el primero reportado en la literatura nacional, y la primera vez que se observa esta complicación secundaria a cirugía por hernia discal intradural.
PRESENTACIÓN DEL CASO
Se presenta una paciente femenina de 53 años, con antecedentes de hipertensión arterial e hipotiroidismo; intervenida desde hacía dos años por osteofito cervical posterior a C4-C5. Acudió en busca de asistencia médica por intenso dolor cervical de tres meses de evolución, que irradiaba hacia ambos miembros superiores, con sensación de calambres sobre todo del derecho.
Examen físico: escala visual analógica (EVA) 5/10; Índice de masa muscular (IMC): 23,3kg/m2sc; fuerza muscular: 4/5 en deltoides y bíceps braquial D. Resto de músculos claves 5/5 según resonancia magnética cerebral (RMC) reflejos osteotedinosos: hiperreflexia tricipital, bicipital a predominio derecho. Signo de Hoffman y Trömmer derecho. No clonus; no signo de Babinski; escala de Nurick: grado 1; mJOA: 17 puntos; ASIA: E.
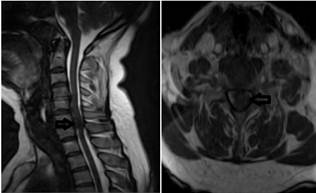
En la imagen de resonancia magnética (IRM): se informó hernia discal extruida C6-C7 que comprimía el cordón medular, provocando cambios en la intensidad señal medular. (Fig. 1).
Se realizó disectomía C6-C7 e injerto de cresta iliaca; se procedió a la entubación sin extensión cervical, se mantuvo la tensión arterial media (TAM) en 80-100 mmHg, se utilizó microscopio Carl Zeiss para la disectomía, y control fluoroscópico para la colocación del injerto autólogo. No ocurrieron complicaciones durante el acto quirúrgico.
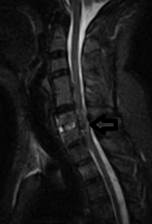
Al despertar, la paciente presentó monoparesia crural derecha 1/5 y signo de Babinski derecho, por lo cual se solicitó de inmediato estudio de resonancia magnética nuclear (RMN), y se colocó metilprednisolona según esquema NASCIS III. La IRM se obtuvo 24 horas después, e informó la presencia de restos de disco y compresión medular. (Fig. 2).
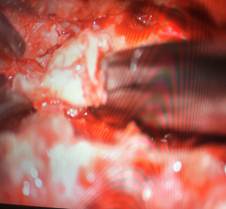
Se sospechó contenido intradural de la hernia, por lo cual se realizó corporectomía C6, injerto y fijación con placa de titanio y tornillos. Se completó el proceder 48 horas después de la primera cirugía, obteniendo efectivamente restos discales intradurales (Fig. 3), sin presenciar salida de líquido cerebroespinal a través del sitio por el cual perforó la hernia a la duramadre.
La paciente presentó mejoría clínica a las 12 horas del proceder, con 3/5 en el miembro afecto, con rehabilitación y medicamentos neurotróficos; a los 6 días comenzó nuevamente con disminución de la fuerza muscular, esta vez con afectación de todas las extremidades: MI 0/5, MS 3/5 a predominio distal, globo vesical, arreflexia en miembros inferiores e hiperreflexia en superiores. Mantuvo signo de Hoffman.
Se indicó de urgencias tomografía axial computarizada, en la cual no se observó hematoma, acumulo de líquido pre-vertebral o mal posición del instrumental, o del injerto. Se re intervino en búsqueda de alguna causa que explicara el deterioro clínico; en el acto de la cirugía solo fue notable la expansión de la duramadre hacia el área de la corporectomia y la tensión de esta.
Se solicitó nueva IRM (Fig. 4), donde fue evidente hiperintensidad de señal en el T2, aumento de volumen del cordón, y pérdida de las columnas liquidas anterior y posterior a este nivel, lo cual confirmó el diagnostico de White Cord Syndrome. Se instauró nuevamente el esquema de metilprednisolona por 48 horas, y luego se continuó con dexametasona hasta su retirada escalonada, además de agregar drenaje espinal continuo al tratamiento.

Fig. 4 Se observa el edema y la pérdida de las columnas líquidas (T1) (a la izquierda); y señalada por la flecha, la hiperintensidad medular en T2 (a la derecha).
La paciente egresó a las dos semanas con Nurick grado 5, y signos vitales estables. Pese a la rehabilitación, a los dos meses de seguimiento continuó con el mismo estatus neurológico.
DISCUSIÓN
Las principales causas asociadas al deterioro neurológico brusco postquirúrgico son el fallo de la fijación, el hematoma epidural, el edema medular, y el daño por isquemia reperfusión;4,6 este último, crucial cuando se realizan descompresiones multiniveles.
Para arribar al diagnóstico del White Cord Syndrome (o daño por isquemia reperfusión) es necesario excluir las tres primeras causas anteriormente citadas, y contar con IRM en la cual se identifique la hiperintensidad medular en la imagen ponderada en T2.6
Los pacientes con déficits neurológicos agudos después de una cirugía de columna cervical, deben someterse a estudios de RM para descartar patología extrínseca del cordón antes de ser diagnosticados con WCS. En particular, dos de los nueve casos analizados por Nancy Epstein requirieron cirugía adicional para abordar la estenosis y osificación del ligamento longitudinal posterior, por lo tanto, no tenían la patología en cuestión.7
Papaioannou y colaboradores indican que los principales diagnósticos diferenciales son: los traumatismos iatrogénicos que producen pérdida de líquido cefalorraquídeo, pseudomeningocele, lesión cerebrovascular y enfermedades desmielinizantes.8
Esta complicación podría atribuirse a un fenómeno a largo plazo causado por la reperfusión de un tejido sometido a isquemia crónica, como un "robo" de flujo del área comprimida a la descomprimida.5
Esto podría ser imputable a una variedad de mecanismos, como la oclusión de pequeños vasos por el edema extraluminal e intraluminal, disfunción de autorregulación arterial, pérdida rápida de trifosfato de adenosina (ATP), despolarización de la membrana celular y acumulación de Ca ++ intracelular, y estrés oxidativo debido al aumento repentino de la presión arterial después de la reperfusión que conduce a la sobreproducción de especies reactivas de oxígeno (radicales libres) y muerte celular.5
Fan y colaboradores demostraron que tras el inicio de la isquemia, existe disminución del flujo sanguíneo local en la médula espinal, casi el 77,48 % del basal, que se revierte parcialmente por la reperfusión inicial, superando incluso el nivel basal. Sin embargo, una hora después de la reperfusión, el flujo sanguíneo se redujo nuevamente al nivel por debajo de la línea de base, seguido de una disminución durante tres horas sin recuperación.9
Uno de los factores que se asocia al desarrollo de esta entidad es el tiempo de evolución de la mielopatía hasta el acto quirúrgico.
Vidal y colaboradores, en su serie experimental observaron que la descompresión produce de forma aguda un aumento de 1,5 a 2 veces los niveles de citoquinas inflamatorias dentro de la médula espinal, y al realizarla de forma tardía se asocia a lesión por reperfusión agravada, astrogliosis y peor recuperación neurológica; además, produce elevación prolongada de las citocinas inflamatorias y una respuesta inflamatoria monocítica periférica exacerbada.10
Por el contrario, la descompresión temprana condujo a la resolución de la inflamación mediada por reperfusión, mejoría neurológica y reducción de la hiperalgesia,10 razón por la cual se procura una reducción en el tiempo, desde el diagnóstico hasta la cirugía, en el presente caso este fue de tres meses.
Resulta contradictorio que el agravamiento de los síntomas ocurriese seis días luego de la segunda cirugía, al ser frecuente la aparición del defecto pos operatorio inmediato, sin embargo, otros autores han reportado periodos de instalación que superan el fin del acto quirúrgico, tales como Papaioannou y colaboradores,8 con una evolución subaguda del daño a las 24 horas; y Sepúlveda y colaboradores,11 quienes observaron inicio de los síntomas 24 horas después y empeoramiento al mes y nueve días de la cirugía. Ello muestra los complejos mecanismos fisiopatológicos de esta entidad, que aún están por estudiar y comprender.
Entre las opciones para tratar esta complicación se encuentra el uso de esteroides, entre ellos, la metilprednisolona resulta muy eficaz, pues reduce la proteína S-100β y la enolasa neuronal específica, inhibe la interleucina (IL) 1β y aumenta IL-8 e IL-1RA. Por tanto, preserva y mejora la calidad de vida de los pacientes.12
Otra de las opciones terapéuticas es el uso del drenaje espinal continuo, teniendo en cuenta que la perfusión de la médula espinal depende en parte de la presión del líquido cerebro raquídeo (LCR).13
La colocación preoperatoria de un drenaje de LCR puede ayudar en el manejo anestésico de un paciente con una médula espinal muy comprimida. Las presiones elevadas del LCR inhiben la perfusión al cordón edematoso, por lo que la reducción gradual de la presión del LCR antes de la descompresión completa, puede mitigar el edema medular.13
Esta variante fue usada en el presente caso, aunque de forma pos quirúrgica, teniendo en cuenta que en el protocolo de trabajo del departamento no está contemplado su uso transoperatorio.
El síndrome por isquemia reperfusión es más frecuente en las intervenciones por vía posterior, siendo solamente reportado en abordajes anteriores5,14,15 y en el caso presentado.
No existe evidencia de que la descompresión por vía posterior brinde una solución definitiva a la injuria; solo esquemas de altas dosis de esteroides y rehabilitación pueden revertir o mejorar el cuadro,4,5,15 razón por la cual no se realizó laminectomía C6 y C7.
El White Cord Syndrome es una complicación rara. Este caso es el primero en ser reportado en el país. Su presentación luego de cirugía para hernia discal intradural no ha sido referida. El diagnóstico se realiza luego de la exclusión de complicaciones trans operatorias, y al observar hiperintensidad del cordón medular ponderado en T2 en la resonancia magnética. La fisiopatología esta mediada por la aparición de radicales libres. El manejo radica en una adecuada descompresión, uso de esteroides y rehabilitación. La correcta identificación de este síndrome es crucial para un tratamiento oportuno y precoz, evitando así consecuencias fatales.