Introducción
La Enfermedad por coronavirus 2019 (COVID-19) fue declarada como una pandemia por la Organización Mundial de la Salud (OMS), el 11 de marzo de 2020.1) La presentación más grave de la enfermedad es el Síndrome Respiratorio Agudo Severo causado por el Coronavirus 2 (SARS-CoV-2) que se convirtió en una catástrofe mundial al provocar la sobrecarga y el colapso de los servicios médicos en la mayoría de los países. La terapéutica médica ha evolucionado rápidamente; sin embargo, la ventilación mecánica sigue siendo el principal pilar del manejo del paciente con la COVID-19 severo.2
El principal propósito del manejo ventilatorio del Síndrome de Distres Respiratorio Agudo (SDRA) es garantizar el intercambio de gas sin provocar daño adicional a los pulmones del paciente. La ventilación mecánica se asocia a serias complicaciones, en parte porque es administrada a pacientes con alto riesgo de compromiso respiratorio o cardiovascular. Estas complicaciones pueden relacionarse con el efecto mecánico directo de la presión intratorácica generada por el ventilador, sobredistención de los alveolos, inflamación sistémica o estimulación neuronal. Muchas de las complicaciones pueden ser potencialmente evitadas o minimizadas. Este hecho es importante desde la perspectiva clínica y es un área investigativa fundamental en la actualidad.3
Las causas reconocidas de lesión pulmonar inducida por el ventilador incluyen: presión, volumen, flujo y frecuencia respiratoria. La presión de conducción dinámica, definida como la presión aplicada por el ventilador necesaria para entregar el volumen corriente, refleja la fuerza que reciben los pulmones en cada respiración. Todos estos factores mecánicos pueden considerarse partes de una sola entidad física: Poder mecánico, el cual se define como la cantidad de energía por unidad de tiempo transferida desde el ventilador al sistema respiratorio; parte de esta energía actúa directamente sobre el tejido pulmonar donde puede causar daño.3
La Intensidad de la ventilación mecánica está reflejada por la presión de conducción dinámica y el poder mecánico.
El Síndrome de Disfunción Múltiple de Órganos puede definirse como la incapacidad de uno o más órganos para mantener su funcionamiento de manera espontánea, sin intervención. Entre los sistemas de evaluación de Disfunción Multiorgánica los más comúnmente usados son el SOFA (Sequential Organ Failure Assessment) y el LODS (Logistic Organ Dysfunction Score).4
Al reportarse el SOFA en días predefinidos, nos permite comparar con la media de disfunción orgánica; mientras el ΔSOFA nos permite comparar la trayectoria de la disfunción orgánica a partir de la puntuación de base. El ΔSOFA refleja confiablemente las diferencias de mortalidad entre grupos. Describe los cambios en la disfunción de órganos a lo largo del tiempo. Se asocia fuertemente con la mortalidad y explica 32 % de los efectos del tratamiento sobre la mortalidad.5
Resulta intuitivo que un agravamiento de la disfunción multiorgánica evaluada con la escala SOFA, se manifiesta en un aumento de la puntuación con respecto al estado previo, lo cual se traduce en un valor de ΔSOFA> 0.
Nos propusimos evaluar la repercusión que tiene la ventilación mecánica sobre el Síndrome de Disfunción Múltiple de Órganos, así como el papel de la lesión pulmonar inducida por el ventilador en la génesis de este síndrome; todo esto a partir del empleo de la Intensidad de la ventilación mecánica como predictor de VILI. De esta manera, podemos crear un precedente para optimizar el tratamiento de los pacientes con SDRA, lo cual sería útil para futuras pandemias de Síndromes Respiratorios Agudos Severos, así como para el manejo del SDRA de otras causas.
El objetivo de esta investigación es determinar la relación entre Intensidad de la ventilación mecánica y ΔSOFA>0 (agravamiento) en los pacientes con la COVID-19 a las 72 horas después de la intubación.
Material y Métodos
Se realizó un estudio observacional, analítico, longitudinal y retrospectivo en los pacientes ingresados con la COVID-19 en la Unidad de Cuidados Intensivos (UCI) del Hospital “Aleida Fernández Chardiet” desde el 1/7/2021 hasta el 30/9/2021.
Este hospital atiende una población de 191 540 habitantes, comprendidos entre los municipios de Melena del Sur, Batabanó, Madruga, San Nicolás de Bari, Nueva Paz y Güines, pertenecientes a la provincia de Mayabeque, Cuba. En el período de estudio ingresaron en el hospital 641 pacientes sospechosos de COVID-19 (test rápido de antígeno positivo), de ellos 68 pacientes fueron tratados en la UCI del hospital.
El grupo de estudio de 35 pacientes estuvo conformado por los ingresados en la UCI con el diagnóstico de neumonía por la COVID-19 (PCR positivo) que requirieron ventilación mecánica invasiva, durante el período en cuestión y que no fallecieron antes de las 72 horas tras la intubación.
Las variables analizadas en nuestro estudio fueron: edad (Años cumplidos hasta la fecha); sexo (Género al que pertenece el paciente); presión pico (Presión máxima alcanzada en la vía aérea durante la inspiración [Pp]); presión positiva al final de la espiración (Presión alcanzada en la vía aérea al final de la fase espiratoria, la cual es prefijada por el operador [PEEP]); presión de conducción dinámica (Presión aplicada por el ventilador necesaria para entregar el Volumen Tidal [ΔP]); volumen tidal (Volumen de la mezcla de aire insuflada a los pulmones en cada ciclo respiratorio [Vt]); frecuencia respiratoria (Número de respiraciones que efectúa el ventilador mecánico durante un minuto [Fr]); poder mecánico (Cantidad de energía por unidad de tiempo transferida desde el ventilador al sistema respiratorio [PM]); y delta SOFA (Diferencia entre el SOFA obtenido a las 72h de ventilación mecánica invasiva y el SOFA del día en que se inició esta [ΔSOFA]).
Se calculó la presión de conducción dinámica (ΔP) a partir de:
Δ P = Pp - PEEP6
El poder mecánico se calculó a partir de las fórmulas:
PM = 0,098 * Fr * (Vt/1000)* (Pp - ½ *ΔP)6) para modos ventilatorios controlados por volumen.
PM = 0,098 * (Vt/1000) * Fr* (ΔP + PEEP)6) para modos ventilatorios controlados por presión.
La variable de medición de la respuesta que se escogió fue ΔSOFA para el tercer día de ventilación mecánica y se categorizó en ΔSOFA> 0 y ΔSOFA≤ 0, correspondiéndose con el agravamiento o no de la disfunción multiorgánica, respectivamente.
El ΔSOFA para el tercer día de ventilación mecánica se calculó a partir de:
Δ SOFA = SOFA día3 - SOFA día15
SOFA día1: SOFA registrado a las 24 h de ventilación mecánica.
SOFA día3: SOFA registrado a las 72 h de ventilación mecánica.
Los datos fueron recogidos directamente de las historias clínicas. Las variables demográficas y parámetros ventilatorios fueron recogidos en la primera hora tras la intubación y ventilación mecánica y la variable SOFA a las 24 y 72 horas posteriores a la ventilación. Luego fueron digitalizados en una computadora en el programa Excel.
Los datos recogidos fueron procesados en el programa SPSS Statistics versión 25. Las variables cualitativas fueron resumidas en frecuencias absolutas y relativas. Las variables cuantitativas se representaron como media y desviación estándar o mediana y rango intercuartílico, según se cumpliera la hipótesis de normalidad o no (prueba de Kolmogorov-Smirnov). La información fue presentada en tablas estadísticas.
Para identificar relación entre las variables cualitativas estudiadas se confeccionaron tablas de contingencias y se obtuvo el valor de la prueba estadística de Chi cuadrado (X 2 ) o el test exacto de Fisher, según correspondió. La comparación de variables cuantitativas se realizó con la prueba t de Student y U de Mann Whitney, según su distribución. Se estableció un intervalo de confianza para los resultados de 95 %, con un nivel de significación asintótica bilateral de p˂0,05.
Se realizó una regresión logística binaria simple para cada una de las variables cuantitativas, que difirieron significativamente, para comprobar cuáles se relacionaron de forma independiente con ΔSOFA dicotomizada para ΔSOFA≤ 0 y SOFA> 0; empleando el método “introducir”. Se estimó la proporción de varianza de la variable dependiente (ΔSOFA) explicada por las variables predictoras mediante la R2 de Cox y Snell. Se consideró que existía riesgo cuando el OR ajustado y el límite inferior de su IC eran mayores que 1 con una p<0,05.
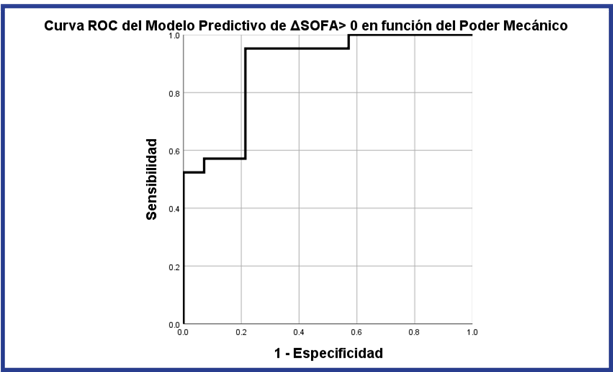
La capacidad discriminativa de los modelos de Regresión Logística se evaluó mediante la Curva ROC y el área bajo la curva.
La investigación fue sometida a revisión, valoración y aprobación por el Comité de Ética del Hospital. Se garantizó la protección de la confidencialidad y el anonimato de los pacientes cuyos documentos clínicos fueron utilizados en esta investigación.
Resultados
De los 35 pacientes que conformaron el grupo de estudio, 74,3 % (26) fueron hombres y 25,7 % (9) mujeres. Presentaron ΔSOFA>0 60 % (21) y ΔSOFA≤0 40 % (14). No existieron diferencias significativas entre los dos grupos en cuanto al sexo o edad de los pacientes.
No hubo diferencias significativas con respecto a la presión de conducción entre ambos grupos (15 vs. 18, U=94,00, z= -1,795, p=0,77).
Existieron diferencias significativas entre ambos grupos en cuanto al volumen tidal (417 [±26] vs. 462 [±39]), diferencia de medias de -45,47 (95 % IC [-69,47 a -21,47]), t (33) = -3,855, p =0,001); el Poder Mecánico (11,62 [±1,28] vs. 14,34 [±2,14]), diferencia de medias de -2,72 (95 % IC [-4,02 a -1,42]), t (33) = -4,25, p<0,001); y Frecuencia Respiratoria (medianas: 15 vs. 16), U= 79,00, Z= -2,394, p = 0,022).(Tabla 1).
Tabla 1 Comparación de las variables registradas en función del ΔSOFA
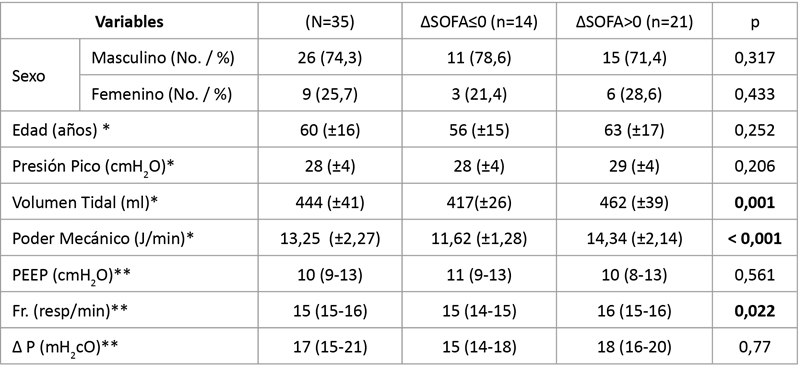
Leyenda: * media (± desviación estándar) ** mediana (rango intercuartílico 25 %-75 %),
PEEP: Presión Positiva al Final de la Espiración, Fr: Frecuencia respiratoria.
De las variables significativamente diferentes, solo fueron buenas predictoras de ΔSOFA> 0, el poder mecánico (OR 3,421, 95 % [1,510 a 7,750, p= 0,003]) y el volumen tidal (OR 1,03, 95 % IC [1,012 a 1,068], p= 0,005) (Tabla 2). Para el modelo con la variable independiente poder mecánico el valor de R2 de Cox y Snell fue de 0,417; o sea, un valor de ΔSOFA>0 depende en 41,7 % de la variación del poder mecánico.
Tabla 2 Regresiones logísticas binarias para cada variable independiente con respecto a ΔSOFA dicotomizada (ΔSOFA ≤ 0 o ΔSOFA>0)

Leyenda: B*: coeficientes estimados del modelo de regresión logística que expresa la probabilidad de ΔSOFA>0 en función de cada variable, Sig.†: significación estadística, Exp(B)‡: Odds Ratio (OR) independiente para cada variable.
La probabilidad de ΔSOFA> 0 aumenta 3,421 veces por cada unidad en que se incrementa del poder mecánico.
Se evaluaron los Modelos de Regresión Logística mediante la Curva ROC. El Área Bajo la Curva (AUC) del Modelo Predictivo de ΔSOFA> 0 en función del Poder Mecánico (Figura 1) (AUC 0,888, 95 % IC [0,775 a 1], p< 0,001) evidencia una buena capacidad discriminatoria.
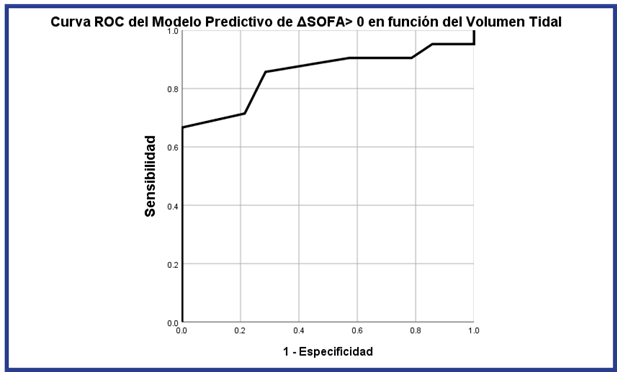
El Modelo Predictivo de ΔSOFA>0 en función del volumen tidal (Figura 2) también tiene una buena capacidad discriminatoria (AUC 0,852, 95 % IC [0,722 a 0,982], p <0,001).
Discusión
En el estudio sobre pacientes con la COVID-19 en el Reino Unido se evaluaron 633 pacientes admitidos en Unidades de Cuidados Intensivos que requirieron ventilación mecánica invasiva. Fueron hombres 76 % y la edad promedio estuvo entre 51 y 66 años.7 Otro estudio donde se recoge la edad de pacientes ventilados con la COVID,8 muestra una edad media de 63 años, en este fueron hombres 77,2 %. En un estudio en Andorra y España, con 742 pacientes ventilados, la mediana de la edad fue 64, con 504 hombres para 68.9 En ninguno de estos trabajos ni en el nuestro se encontraron diferencias significativas en cuanto a la distribución del sexo con respecto a los grupos en que se distribuyeron los pacientes.
Los parámetros ventilatorios registrados en los estudios antes referidos, se comportaron: frecuencia respiratoria (media de 18,8 resp/min), la presión pico (media de 26 cmH2O) oscilando entre 23 y 30 cmH2O. La PEEP media de 10 cmH2O, variando entre 8 y 12 cmH2O.7 Lascarrou y col. recogieron en su estudio una PEEP mediana de 12 (10 a 14) y presión de conducción de 12 (9-14).8 La mediana de la frecuencia respiratoria en la investigación realizada por Ferrando y col. fue de 24 (20-30) y la presión de conducción máxima registrada fue de 15 como mediana y un rango (12-19).9
Como puede observarse, en estos trabajos la PEEP prefijada a los pacientes en general no varió mucho respecto a los valores empleados por nosotros. Sin embargo, la presión de Conducción fue muy por debajo de la registrada en nuestro estudio. Esto se debe a que nosotros evaluamos la presión de conducción dinámica, a partir de la presión pico, como componente de la Intensidad de la ventilación mecánica; en dichos estudios se evaluó la presión de conducción en función de la presión meseta.
Se han realizado varios estudios para determinar asociación entre presión de conducción y poder mecánico y mortalidad en pacientes con Síndrome de Distres Respiratorio Agudo antes de la Pandemia de la COVID-19. En uno llevado a cabo por Guerin y col., con un total de 787 pacientes; la media de la frecuencia respiratoria fue de 27 (±6), el volumen tidal de 397 (±76), la presión de conducción promedio de 13 (±4) y el poder mecánico de 13,4 (±5);10) tanto la presión de conducción como el poder mecánico se asociaron a un incremento de la mortalidad. Sin embargo, en el trabajo de Coppola y col. no se encontró asociación entre poder mecánico y mortalidad en UCI, ya que no se hallaron diferencias significativas de esta variable entre el grupo de fallecidos (14,03) y sobrevivientes (14,97).11) En ambas investigaciones la PEEP mediana fue de 10, similar a la reportada entre los pacientes con SDRA por la COVID-19.7,8,9
Resulta notable la elevada frecuencia respiratoria registrada en los estudios de Ferrando y col.9 y Guerin y col.10 muy por encima de la media del resto de los trabajos, incluyendo el nuestro.
El trabajo de Yildirim y col. evalúa el efecto de la presión de conducción en el SDRA por la COVID-19 en 58 pacientes. Entre el grupo de sobrevivientes y fallecidos no hubo diferencias significativas en cuanto a la PEEP empleada; si hubo una diferencia significativa en cuanto a la mortalidad para el día 28 entre los grupos con Presión de Conducción de 15 (12-17) vs. 19 (14-22); siendo mayor en el grupo con la Δ P más alta.12
En nuestra investigación, no hubo diferencias significativas entre el grupo de pacientes con agravamiento de la disfunción multiorgánica (ΔSOFA>0) y los que no empeoraron (ΔSOFA≤ 0) con respecto a la presión de conducción
En una investigación realizada por Boscolo y col. también se encontró relación directa entre la presión de conducción y la mortalidad en pacientes intubados con la COVID-19, demostrándose una asociación lineal entre ambas variables. También se evidenció que el volumen tidal no se asoció con un riesgo incrementado de muerte.13
En nuestra investigación, sin embargo, se halló una significativa relación entre el volumen tidal y el agravamiento de los pacientes, siendo entre todas las variables a partir de las cuales se calcula el Poder Mecánico, la de mejor relación independiente. Hay que señalar que los pacientes que entraron en nuestro estudio recibieron un volumen tidal, como promedio, ligeramente superior al registrado en los trabajos anteriormente analizados, aunque siempre se mantuvo en el rango establecido de ventilación protectora (4 - 6 ml/Kg de Peso Ideal).
La asociación entre la intensidad de la ventilación mecánica y la mortalidad se ha investigado tanto en pacientes con SDRA por la COVID-19 como por otras causas. En el trabajo de Urner y col. se estudiaron 13 408 pacientes, la presión pico promedio fue de 20 (14-25), ΔP dinámica de 13 (9-17), poder mecánico de 11 (8-16). Se encontró que un aumento significativo del riesgo de muerte se asoció a un incremento diario de la Presión de Conducción o el Poder Mecánico.14
En el trabajo de Schujit y col. la presión pico fue de 27 (24,2-30), ΔP de 14 (12-16) y poder mecánico de 18,5 (15,5-22,2), la frecuencia respiratoria prefijada de 22 (20-24). El poder mecánico se asoció de manera independiente a la mortalidad para el día 28; sin embargo, la presión de conducción no.6 Similar a como sucedió con nuestro grupo de estudio respecto al agravamiento de la disfunción multiorgánica.
La principal fortaleza de nuestro estudio es que se realizó en una única Unidad de Cuidados Intensivos, por lo que no hubo variabilidad en los protocolos de ventilación mecánica, y resultó en uniformidad de la práctica clínica. Esto nos permite descartar influencias externas. Otra fortaleza fue que las variables estudiadas se ajustaron a una adecuada revisión para determinar asociación teórica, antes de llevar a la práctica los modelos logísticos.
La principal limitación de nuestro estudio es el pequeño tamaño de la población; lo cual no nos permite generalizar los resultados alcanzados.
Nuestro trabajo tiene aplicación inmediata en la práctica clínica al evidenciar relación entre el poder mecánico y la disfunción múltiple de órganos. Teniendo en cuenta nuestros resultados, se pueden modificar las variables ventilatorias prefijadas por el operador para limitar el daño que provoca la ventilación mecánica sobre los pacientes con la COVID-19 grave y así garantizar una mejor atención. Así pues, mientras menor sea el valor del poder mecánico calculado para cada paciente, menor será el daño provocado, teniendo especial importancia la limitación del volumen tidal administrado y la frecuencia respiratoria prefijada. Así podemos garantizar una atención segura y de calidad.