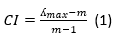Introducción
La malaria es una enfermedad infecciosa causada por varias especies de parásitos apicomplejos del género Plasmodium. En humanos, existen seis especies de Plasmodium responsables de causar malaria: P. falciparum, P. knowlesi, P. malaria, P. ovale curtisi, P. ovale wallikeri y P. vivax. Juntos, causan aproximadamente medio millón de muertes al año. Entre todas las especies, P. falciparum y P. vivax son los parásitos más estudiados debido a la alta frecuencia de infección y complicaciones clínicas que ocasionan en los pacientes (Wilson, et al., 2021)
El ciclo de vida de las especies de Plasmodium es complejo ya que los parásitos transitan entre etapas sexuales y asexuales y evolucionan para sobrevivir en diferentes ambientes celulares. Esto comienza cuando un mosquito hembra Anopheles, que lleva los esporozoítos del parásito (Spz) en sus glándulas salivales, ingiere sangre, lo que resulta en la inyección de Spz en el torrente sanguíneo de un huésped humano . Los Spz infectan primero las células hepáticas, donde se multiplican asexualmente durante los siguientes 7-10 días, período en el que el paciente está asintomático (Mordecai, et al., 2020).
Diferente de otros Especies, P. vivax y P. ovale pasan por una etapa latente llamada hipnozoítos que pueden detener la progresión de la infección durante semanas o incluso años después de la transmisión. Ahora, en forma de merozoítos (Mrz), los parásitos se liberan de las células hepáticas en vesículas y viajan a los capilares. Las vesículas eventualmente estallan, descargando el Mrz para ingresar al torrente sanguíneo donde se dispersan y entran a los eritrocitos. Aquí adentro, los parásitos se reproducen asexualmente generando trofozoítos que maduran a esquizontes. Los esquizontes estallan generando merozoítos que salen de la célula e invaden más eritrocitos, repitiendo el ciclo de crecimiento, replicación, salida e invasión. La llegada de Mrz al torrente sanguíneo y la ruptura de los eritrocitos inyectados desencadenan síntomas clínicos que se desarrollan en la enfermedad de la malaria (Moxon, et al., 2020).
P falciparumy P. vivax el tiempo de incubación es de 12-18 y 9-14 días, respectivamente. La patología incluye signos como fiebre intermitente, dolor de cabeza, vómitos, escalofríos, dolor abdominal y síntomas de sudoración que pueden desarrollar potencialmente una hemólisis crónica y fatal. Finalmente, un pequeño número de parásitos en etapas asexuales se comprometen con el ciclo sexual, formando microgametocitos (masculino) y macrogametocitos (femenino). Una vez maduros, los gametocitos del torrente sanguíneo pueden ser absorbidos por mosquitos hembra, continuando la transmisión de los parásitos (Bustillos & Navarro, 2021).
La distribución de casos de malaria se reporta alrededor del mundo especialmente en países con áreas tropicales y subtropicales, ambientes en los que se distribuyen los mosquitos. En América del Sur, P. vivax es la especie más común y afecta especialmente a la selva tropical y las regiones costeras durante la estación seca. Se confirma la presencia de P. falciparum en esta región. Sin embargo, un estudio publicado en 2019 sugiere una disminución de la población de esta especie en Brasil y Argentina, países donde la mayoría de los casos de malaria son asintomáticos (Wimberly, et al., 2021).
En 2015, la Organización Mundial de la Salud (OMS) informó que el 83% de los casos de malaria en esta región corresponden a: Venezuela (30%), Brasil (24%), Perú (19%) y Colombia (10%). Adicionalmente, un estudio realizado en 2018 mostró una asociación entre la migración humana y un aumento de casos de malaria (96%) en la frontera entre Ecuador y Perú (Jaramillo-Ochoa et al, 2018).
Para luchar contra la malaria, los métodos más utilizados siguen siendo el control de vectores y las terapias farmacológicas. Sin embargo, P. falciparum desarrolló resistencia a monoterapias y sesquiterpenos como las terapias combinadas a base de artemisinina (ACT), incluso en estrategias alternas, convirtiéndose en un problema para eliminar la enfermedad. La principal causa de la resistencia es el uso irresponsable de medicamentos antipalúdicos como la cloroquina, lumefantrina, amodiaquina, sulfadoxina-pirimetamina, quinina, piperaquina y mefloquina, y la falta de control sanitario incluso en países con componentes farmacéuticos de calidad y sistemas sanitarios sólidos (Moxon, et al., 2020).
Debido al desarrollo de resistencia a los medicamentos antiparasitarios, es importante mejorar el control de la malaria más allá de la administración y la prescripción o el programa de eliminación para hacer frente a la resistencia emergente, el tratamiento antipalúdico nuevo inadecuado, o cumplimiento deficiente en los países afectados. Si bien los parásitos pueden ser sensibles a los medicamentos al inicio de la aplicación, dosis más prolongadas y altas de los medicamentos pueden desarrollar resistencia parasitaria, lo que significa el fracaso del tratamiento (Camargo, et al., 2019).
Los países latinoamericanos, por encontrarse en una amplia zona selvática, además boscosa,donde abundan los ríos y pantanos, conviven en ella diferentes familias de insectos, entre las que se encuentran diversas especies de mosquitos transmisores de muchas enfermedades endémicas, los cuales se encuentran distribuidos en toda la región amazónica y en diversas ciudades aledañas, lo que tiende a infectar la salud de los seres humanos. Para evitar estas situaciones, se proyectan acciones que intentan contrarrestar los efectos negativos de estas plagas. En este sentido es importante destacar, que luego de haber estado entre los más destacados, Ecuador, es uno de los países que desde el 2017 hasta la actualidad, muestra una situación que tiende al incremento de la enfermedad en algunas regiones endémicas (Jadan-Solis, et al., 2019)
De hecho, la eliminación de la enfermedad requiere una mejor solución para reemplazar las terapias con medicamentos que fallan, especialmente para tratar los casos no detectados. Así, el desarrollo de una vacuna representa un paso significativo y crucial de un mecanismo profiláctico de protección contra la malaria, inhibiendo el desarrollo de gametocitos a partir de los parásitos y la aparición de síntomas duros (Gómez, et al., 2020).
Para que el proceso sea efectivo, además de crear los mecanismos de acción para enfrentar esta situación, se hace necesario realizar actividades educativas en las comunidades, por lo que esta investigación tiene como objetivo describir las últimas vacunas contra la malaria, su mecanismo de acción y la fase de estudio que ha llegado hasta estos días. Y además, realizar una propuesta de intervención educative que propicie la información adecuada a la población respecto a esta enfermedad y los medios para prevenirla.
Materiales y métodos
Métodos teóricos
Método analítico sintético: el método analítico permite la descomposición del todo en aspectos específicos para entender y comprender la estructura; facilitó la observancia para comprender mejor los componentes. En este contexto este método implica la síntesis, es decir la unión de los elementos dispersos para conformar un componente total.
Método inductivo deductivo: este método de investigación permite un razonamiento lógico. Mientras el método inductivo parte de premisas específicas para llegar a aspectos generales, el método deductivo es lo opuesto, pues parte de lo genérico hasta llegar a los aspectos particulares. Sin embargo, ambos métodos son esenciales en la construcción del conocimiento.
Método histórico lógico: estos métodos permiten la construcción de la investigación a partir de los elementos históricos que construyen la investigación para comprender los elementos esenciales de la misma y su evolución histórica. Hernández, Fernández, & Baptista (2006)).
Métodos empíricos:
Entrevistas: se aplicará al grupo de expertos seleccionados a participar en la investigación, para tomar sus puntos de vista en consideración para la elaboración de la propuesta educativa.
Observación: para comprobar cómo se comporta el fenómeno objeto de la investigación. Se pretende realizar una observación de campo.
Métodos para el procesamiento de la información
El Proceso Analítico Jerárquico (AHP Saaty) (Tabla 1)
Es uno de los métodos más extendidos para resolver problemas de toma de decisiones de múltiples criterios. Esta técnica modela el problema que conduce a la formación de una jerarquía representativa del esquema de toma de decisiones asociado. Esta jerarquía presenta en el nivel superior el objetivo que se persigue en la solución del problema y en el nivel inferior se incluyen las distintas alternativas a partir de las cuales se debe tomar una decisión. Los niveles intermedios detallan el conjunto de criterios y atributos considerados ( Beltrán, Acurio, & Alulema, 2021); Estupiñán, et al., 2021).
El AHP es una teoría orientada hacia el responsable de la toma de decisiones y sirve para identificar la mejor alternativa de acuerdo con los recursos asignados. Este método puede aplicarse a situaciones que involucran factores de tipo técnico, económico, político, social y cultural. Es decir, pretende ser una herramienta científica para abordar aquellos aspectos que son difícilmente cuantificables, pero que a veces requieren una unidad de medida.
Algunos autores plantean que el AHP no ha sido bien comprendido, ya que va más allá de ser una simple metodología para situaciones de elección. Se plantea entonces, que la mejor manera de entender el método es describiendo sus tres funciones básicas: estructurar la complejidad, medir en una escala y sintetizar. La jerarquía está construida de manera que los elementos sean del mismo orden de magnitud y puedan relacionarse con algunos del siguiente nivel. Los pasos son:
Priorización de los elementos del modelo jerárquico.
Comparación binaria de los elementos.
Evaluación de los elementos mediante la asignación de pesos
Ranking de las alternativas de acuerdo a los pesos dados
Síntesis y análisis de sensibilidad
Tabla 1 - Escala de evaluación de Saaty (Tasa juicio verbal)
| Escala | |
|---|---|
| 9 Extremadamente más preferido | 3 Moderadamente más preferido |
| 7 Muy poderosamente más preferido | 1 Igualmente preferido |
| 5 Poderosamente más preferido |
Nota: Saaty (Saaty, 2008).
A continuación, se presenta un algoritmo para el cálculo de éste (este debe aplicarse para todos los criterios):
Para cada línea de la matriz de comparación por pares determinar una suma ponderada con base a la suma del producto de cada celda por la prioridad de cada alternativa o criterio correspondiente
Para cada línea, dividir su suma ponderada por la prioridad de su alternativa o criterio correspondiente
Determinar la media ʎmax del resultado de la etapa anterior
Calcular el índice de consistencia (CI) para cada alternativa o criterio
Donde m es el número de alternativas
Determinar el Índice Aleatorio (IA) de la tabla 2
Tabla 2 - Índice aleatorio para el cálculo del coeficiente de consistencia
| Número de alternativas para la decisión n | Índice aleatorio | Número de alternativas para la decisión n | Índice aleatorio |
|---|---|---|---|
| 3 | 0.58 | 7 | 1.32 |
| 4 | 0.9 | 8 | 1.41 |
| 5 | 1,12 | 10 | 1,49 |
| 6 | 1,24 |
Determinar el índice de cociente de consistencia (la razón entre el índice de consistencia y el índice aleatorio).
Resultados y discusión
Para la presente revision, se analizaron los siguientes documentos (Aguilar, 2021; Cartagenova, 2021; Hidalgo, 2021; Llonch, van der Sluis, & Fernández, 2008; Camargo, et al., 2019), de los cuáles se pone a consideración la siguiente información sobre la enfermedad y las vacunas que se han puesto en práctica.
Ciclo de vida de Plasmodium: P. falciparumy P. vivax pasan por dos ciclos que se desarrollan en el interior de dos huéspedes. En el vector ocurre el ciclo sexual y, en el humano, el asexual (Fig.1).
Ciclo sexual de Plasmodium: El ciclo de vida sexual de Plasmodium comienza cuando un mosquito Anopheles hembra ingiere sangre que contiene gametocitos del torrente sanguíneo de un huésped humano infectado. Los gametocitos masculinos y femeninos tomados llegan al intestino medio del mosquito y se someten a fertilización y maduración, formando oocinetos. Los ooquinetos migran al hemocele para formar ooquistes. Una vez maduros, los ooquistes revientan liberando esporozoítos, que migran a las glándulas salivales del mosquito donde están listos para la transmisión.
Ciclo asexual de Plasmodium: La infección por malaria comienza cuando el mosquito Anopheles hembra que porta Spz se deposita debajo de la piel humana. Este ciclo se divide en dos procesos que ocurren dentro del hígado (etapas preeritrocíticas) y en el torrente sanguíneo (etapas eritrocíticas). Después de la invasión, comienza la fase preeritrocítica por la migración de Spz al hígado para infectar las células hepáticas que experimentan el desarrollo de merozoítos (Mrz). Los P. falciparum Mrz son liberados al torrente sanguíneo para entrar en los estadios eritrocíticos, mientras que los P. vivax Mrz tienen la capacidad de permanecer como hipnozoítos (Hpz) en el tejido hepático a la espera de su reactivación lo que refiere casos asintomáticos. En consecuencia, la fase eritrocítica se coloca por invasión de Mrz que ingresa a los eritrocitos por interacción de baja afinidad receptor-ligando que induce la deformación de la membrana con (EBA-175, EBA-140 y EBA-181) antígenos y familias de homólogos de unión a reticulocitos (Rh1, Rh2a/Rh2b y Rh4). La consiguiente invasión sufre la formación secuencial de etapas de anillo, trofozoítos y esquizontes (Scz). Las Scz infectadas maduras van a infectar más eritrocitos.
Etapa de gametocitosse desarrolla durante 10 días en el interior de los eritrocitos y su maduración tiene lugar en fases V. Estos corresponden a la etapa infecciosa que puede transmitirse desde el torrente sanguíneo humano al mosquito Anopheles hembra. Sin embargo, los eritrocitos infectados con gametocitos inmaduros (GIE) de las fases I a IV se ocultan en tejidos profundos para evitar su eliminación por el bazo. Un estudio in vitro sugiere que para pasar a la fase V, los parásitos Plasmodium interfieren en la eritropoyesis al infectar los eritroblastos primarios, completar su maduración en ellos y llegar a la circulación sanguínea. Mientras circulan en el torrente sanguíneo, pueden transmitirse a un mosquito Anopheles hembra. (Fig. 1)
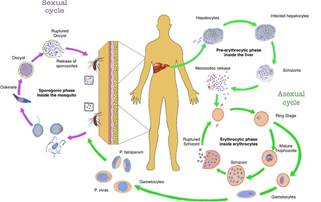 Fuente: Esquema modificado del Departamento de Salud y Servicios Humanos de EE. UU. de los CDC 2020
Fuente: Esquema modificado del Departamento de Salud y Servicios Humanos de EE. UU. de los CDC 2020Fig. 1 - Plasmodiociclo de vida en dos huéspedes (vector: mosquito Anopheles hembra y humano)
En la siguiente figura se ilustran los principals síntomas y complicaciones causadas por Plasmodium falciparum y Plasmodium vivax
 Fuente: (Jadan-Solis et al, 2019)
Fuente: (Jadan-Solis et al, 2019)Fig. 2 - Características clínicas presentadas en la infección por malaria causada por cepas de Plasmodium falciparum y Plasmodium vivax
Vacunas contra Plasmodium
La eficiencia y eficacia de las vacunas depende de una serie de estudios tales como los mecanismos moleculares y celulares de invasión que utilizan los parásitos para ingresar a las células huésped, análisis de los componentes de la vacuna, dosis y forma de administración y respuesta inmune de los pacientes. Algunas de las principales estrategias utilizadas para la generación de dichas vacunas son: proteínas contra la fase preeritrocitaria, vacunas atenuadas contra parásitos y vectores virales.
Vacunas preeritrocíticas: Las vacunas preeritrocíticas tienen como objetivo obstruir los esporozoitos de manera rápida y competente, justo después de la inoculación en la dermis antes del tránsito de los lechos capilares venosos al hígado. Cómo se previene la invasión de hepatocitos es un asunto por dilucidar, pero lo más probable es que se logre a través de anticuerpos que opsonizan los esporozoitos. El blanco principal de la vacuna es la proteína circumsporozoite (CSP).
Vacuna SRT, S: RTS, S/AS01 es la vacuna antipalúdica más estudiada, publicitada y líder. Fue creado en 1987 y fue desarrollado contra la malaria por P. falciparum. Los primeros estudios en esta vacuna mostraron que los esporozoitos atenuados por radiación demostraron protección contra la malaria. Posteriormente, el antígeno CSP se identificó como un objetivo de la respuesta inmune, por lo que esta proteína fue secuenciada, clonada y analizada con mayor detalle. A continuación, se utilizó el antígeno de superficie de la hepatitis B como matriz portadora para la región de repetición central CSP y la región C-terminal, que contenía epítopos de células T y B y un adyuvante inmunogénico AS01. La eficacia de esta vacuna está limitada por el polimorfismo en los epítopos de células T y sus respuestas de células T.
La vacuna RTS, S/AS01 se encuentra actualmente en implementación piloto (fase 4) en Ghana, Kenia y Malawi para abordar la seguridad en la salud pública. Después de la eficacia mostrada en las pruebas de Fase 3 en países africanos. El estudio registró 15.459 participantes, contando 8.922 niños de 5 a 17 meses de edad y 6.537 lactantes de 6 a 12 semanas de edad. Los resultados de la fase 3 muestran una eficacia superior al 36 % en niños de entre 5 y 17 meses de edad después de 4 dosis entregado como una inyección liofilizada administrada por vía intramuscular. Sobre la seguridad de la vacuna, esta vacuna conlleva un aumento de convulsiones febriles dentro de los 7 días posteriores a la vacunación, después de 7 días todos los sujetos se recuperaron y no mostraron ningún segundo efecto. (Tabla 4)
Tabla 4 - Posible vacuna contra la malaria contra P. falciparum y P. vivax dirigida a la etapa de preeritrocitos durante el ciclo asexual.
| Vacuna | Antígeno | Auxiliar | Mecanismo de acción | Estado |
|---|---|---|---|---|
| Estrategia en tiempo real, S | Pf CSP (207- 395) & HepBsAg | AS01E | Inhibe la motilidad de los esporozoitos, previene la invasión de hepatocitos | Implementación piloto, fase 4 base de referencia de farmacovigilancia |
| Estrategia en tiempo real, S Regímenes de dosis fraccionadas | Pf CSP (207-395) & HepBsAg | AS01B/ AS01E | Inhibe la motilidad de los esporozoitos, previene la invasión de hepatocitos | Pruebas clínicas de fase 2b en áreas endémicas |
| ChAd63 | TRAMPA + YO epítopos (CS, | MVA | Inhibe el esporozoito | Fase 2b pruebas clínicas |
| LSA1, LSA3, STARP, EXP1, pb9) | ME-TRAP | motilidad, previene la invasión de hepatocitos | En endemic áreas | |
| PfSPZ Vacuna | PfSPZ (esporozoitos de organismo completo atenuados por radiación) | AS01B | Inhibe la motilidad de los esporozoitos, previene la invasión de hepatocitos | Pruebas clínicas de fase 2b en áreas endémicas |
| PfCelTOS FMP012 | CelTOS (proteína transversal celular) para ookinetesy esporozoitos) | GLA-SE | Inhibe la motilidad de los esporozoitos, previene la invasión de hepatocitos | Fase 1a pruebas clínicas |
| CSVAC | CS | Inhibe la motilidad de los esporozoitos, previene la invasión de hepatocitos | Fase 1a pruebas clínicas | |
Fuente: (Camargo et al, 2019).
Vacunas eritrocíticas: El desarrollo de síntomas y complicaciones clínicas de la enfermedad aparece durante la infección parasitaria en estadio sanguíneo. Por esa razón, es importante recibir vacunas que puedan prevenir complicaciones como la muerte. Las vacunas eritrocíticas actúan sobre las proteínas de superficie de los merozoítos, que atacan a los glóbulos rojos, generando mímicos y adquiriendo inmunidad adquirida neutralizando anticuerpos que bloquean la invasión y limitan la replicación del parásito después de salir del hígado controlando la parasitemia.
Vacunas MSP1, MSP2, MSP3 y GLURP: Este tipo de vacunas incluyen antígenos como proteína de superficie de merozoito 1, 2 y 3 (MSP1, MSP2 y MSP3); y la proteína rica en glutamato (GLURP), el principal epítopo de células B que se encuentra durante el parásito en etapa sanguínea, su propósito es controlar la multiplicación del parásito cooperando con los receptores FcyII en la generación de anticuerpos IgG que reconocen los epítopos de glóbulos rojos. Existe evidencia importante sobre las respuestas de anticuerpos contra MSP3 y GLURP en el sudeste de Asia con más del 50% de los resultados, MSP1 muestra resultados altos en Gambia, Sierra Leona y Ghana con baja parasitemia y ataques de malaria. Sin embargo, el MSP3 ya es el único que permanece en fase II de evaluación.
Vacuna GMZ2: Esta vacuna corresponde a una combinación híbrida entre la región N-terminal de GLURP y la región C-terminal de MSP-3, aplicada 3 veces con 1 mes por intervalo, actúa produciendo altas cantidades de anticuerpos citofílicos (IgG) contra GLURP y MSP- 3 antígenos que protegen de las características clínicas presentes durante la enfermedad mediante el proceso de inhibición celular dependiente de anticuerpos (ADCI). Ha demostrado buena tolerabilidad, seguridad e inmunidad en las pruebas de Alemania y África, pero su eficacia aún es baja para ser utilizada como una vacuna segura contra la malaria aprobada por salud pública, es necesario mejorar la formulación o la posibilidad de un adyuvante potente porque no completa un mayor protección con inmunidad adquirida de forma natural.
Vacuna AMA1: Es creado por la proteína de superficie de los merozoítos del antígeno de membrana apical 1 (AMA1) que se encuentra en el cuello de las roptrias durante las últimas cuatro horas del desarrollo del ciclo eritrocitario de Plasmodium, que se considera un objetivo principal debido a la capacidad de activar la respuesta celular humoral y más fuerte. produciendo anticuerpos inhibidores del crecimiento del parásito que neutralizan AMA1 evitando que los merozoítos invadan los glóbulos rojos. Incluye tres dosis aplicadas por inyección intramuscular durante dos meses. Además, esta vacuna muestra proliferación de células T y respuesta inmune humoral y celular. Sin embargo, los efectos secundarios que presenta son eritema e hinchazón correspondientes a la hipersensibilidad. Por ello, es necesario desarrollar más estudios sobre el número de dosis que se van a aplicar y el tiempo entre ellas.
Vacuna spf66: La vacuna SPf66 fue publicada por primera vez en 1987 por el científico colombiano Manuel Elkin Patarroyo del Instituto Nacional de Inmunología en Bogotá. Es una vacuna química sintetizada creada para reducir la cantidad de parásitos presentes en la sangre, lo que lleva al desarrollo de inmunidad natural para Plasmodium falciparum. Esta vacuna fue probada durante la década de los 90 demostrando su seguridad, inmunogenéticamente y logros protectores, donde tres dosis de la vacuna donde bien tolerado en Tailandia y Colombia para Plasmodium falciparum con 38-60% de eficacia. Sin embargo, nuevos estudios no mostraron evidencia de mayor protección contra Plasmodium falciparum en África, donde aparecen nuevos episodios de malaria, ha mostrado una baja eficacia del 28% y no brinda protección en áreas endémicas.
Por otro lado, se sugiere el uso de un nuevo adyuvante QS-21 en lugar del hidróxido de aluminio (alumbre) o adyuvante de Freud que podría mejorar su funcionalidad y especificidad. Pero, el producto fabricado en EE. UU. probado para SPf66 no era idéntico al colombiano, lo que sugiere la implementación de procedimientos de estandarización adecuados para obtener una comparación correcta entre los resultados.
Vacuna PvDBP: Es el único proyecto en desarrollo contra Plasmodium vivax, sus mecanismos corresponden a la producción de anticuerpos que bloquean la interacción con el ligando eritrocitario DARC. Pero permanece en el ensayo clínico en humanos de fase 1 a pesar de que es el candidato más prometedor. (Tabla 5)
Tabla 5 - Posible vacuna contra la malaria contra Plasmodium falciparum y Plasmodium vivax dirigida a etapas sanguíneas durante el ciclo asexual
| Vacuna | Antígeno | Adyuvantes | Mecanismo de acción | Estado |
|---|---|---|---|---|
| MSP3 | Proteína de merozoito | Hidróxido de aluminio (Al(OH)3) | Inhibe la invasión de eritrocitos | Pruebas clínicas de fase 2 |
| Superficie 3(MSP3) | ||||
| MSP2 | Superficie de proteína de merozoito 2 | Hidróxido de aluminio (Al(OH)3) | Inhibe la invasión de eritrocitos | Pruebas clínicas de fase 1 |
| GLURP | Proteína rica en glutamato (GLURP) | Hidróxido de aluminio (Al(OH)3) | Inhibe la invasión de eritrocitos | Pruebas clínicas de fase 1 |
| GMZ-2 | Proteína rica en glutamato (GLURP) y MSP3 | Hidróxido de aluminio (Al(OH)3) | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 2 |
| pfAMA1- dico | Antígeno de membrana apical 1 (AMA1) | AS01B AS01A Hidróxido de aluminio (Al(OH)3) GLA-SE | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 2b |
| P27A | Proteína de malaria PFF0165c (P27A) | Hidróxido de aluminio (Al(OH)3) GLA-SE | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 1a/1b |
| SE36 | Dominio N-terminal del antígeno de repetición de serina (SERAS) | Hidróxido de aluminio (Al(OH)3) gel | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 1b |
| Chad63 Th5 +/- MVA RH5 | Homólogo 25 de proteína de unión a reticulocitos (RH5) | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 1a | |
| pfs25 | Proteína de superficie 25 | Inhibir el desarrollo de ookinete en el intestino medio del mosquito | Pruebas clínicas de fase 1 | |
| PRIMVAC | VAR2CSA fragmento | Alhidrogel y GLA-SE | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 1a/1b |
| PAMVAC | VARCSA fragmento | Alhidrogel GLA-SE GLA-LSQ | Inhibir la invasión de eritrocitos | Pruebas clínicas de fase 1a/1b |
| SPf66 | Antígenos de merozoitos | Hidróxido de aluminio (Al(OH)3) QS-21 | Reducir los Monto de parásito ensangre | Clínico inactivo |
| PvDBP | Dominio de unión al receptor de pags. Vivax Proteína de unión Duffy | glucopira nosil lípidoemulsión estable adyuvante (GLA-SE) | Inhibe el parásito | Pruebas clínicas de fase 1 |
Fuente: (Camargo et al, 2019) .
Gametocitos Vacunas
Tabla 6 - Posible vacuna contra la malaria contra P. falciparum y P. vivax dirigida a las etapas sexuales durante el ciclo asexual
| Proyecto vacuna | Antígeno | Adyuvantes | Estado actual |
|---|---|---|---|
| Pfa24 VLP | Pfs25 | Alhidrogel | Fase 1 clínico Fase 2 aclínico |
| Pfs25-EPA/Alhidrogel | Pfs25 | Fase 1b Clínico | |
| Pfs230D1M- EPA/Alhidrogel y/o Pfs25/EPA/Alhidrogel | Pfs25M Pfs230D1M | Fase 1 Clínico | |
| Pfs230D1K- EPA/Alhidrogel y Pfs25-EPA/AS-1 | Pfs25M Pfs 230D1M | Fase 1 Clínico | |
| ChAd63 Pfs25=IMX313/MVA Pfs25-IMX313 | Pfs25 | Fase 1 a Clínico | |
| Pfs25 | Pfs25 | Montanida ISA-51 | Fase I1 Inactivo- Clínico |
Fuente: (Camargo et al, 2019).
Este artículo revisó el ciclo de vida y las posibles vacunas contra P. vivax y P. falciparum (Tabla 6). En términos médicos, durante las etapas eritrocíticas, las características clínicas representan interés de la salud pública y privada por la alta prevalencia de casos durante décadas. Por ello, es necesario erradicar la afección mediante vacunación. Sin embargo, es destacable establecer prioridades para las vacunas ya terminadas y aceptadas para su uso en cada una de las etapas de desarrollo de plasmodium durante la transmisión. RST, S es una vacuna preeritrocítica que previene la invasión de hepatocitos correspondiente a la vacuna más estudiada y probada (fase 4) en Ghana, Kenia y Malawi consiguiendo alta eficacia con 4 dosis intramusculares con bajos efectos secundarios, excepto meningitis. Es importante resaltar que esta vacuna no funciona contra la malaria grave.
Por otro lado, las vacunas eritrocíticas contra la invasión de glóbulos rojos representan una solución para la evolución de los síntomas y complicaciones clínicas. Se están evaluando varias cantidades de vacuna. Pero la mayoría de ellos permanecen en estadios preclínicos que no garantizan su eficacia. SPf66 fue la primera vacuna contra la malaria generada para el estadío eritrocitario que comenzó con resultados efectivos, pero ya no se evalúa ni investiga por su baja eficacia en ensayos en EE.
Las vacunas creadas en base a MSP1, MSP2, MSP3 y GLURP continúan en evaluación por su especificidad al parásito, pero es necesario mejorar la investigación dado que solo MSP3 se encuentra en un alto nivel de ensayo clínico. AMA-1 representa una vacuna desarrollada con buenos resultados en diferentes países, pero es necesario seguir demostrando su eficacia debido a los efectos secundarios que podrían retrasarse con éxito.
Sólo existe un tipo de vacuna desarrollada para Plasmodium vivax PVDBP, que ha mostrado buenos resultados, pero se encuentra en una fase baja de evaluación. La vacuna más desarrollada en esta etapa es la GMZ2 la cual funciona en base a una combinación entre MSP3 y GLURP debido a la evidencia demostrada durante cada evaluación, donde su interacción presenta un importante nivel de respuesta frente al desarrollo de la enfermedad al bloquear los eritrocitos.
Según lo planteado en la revisión bibliográfica, existen numerosas investigaciones respecto al tema de la prevención de la Malaria a través de vacunas, donde se ha conocido la efectividad de muchas. Pero aún existe poco nivel de conocimiento e información de la población, y en otros casos, se hace difícil el acceso a este tipo de tratamiento. Como parte de los objetivos de esta investigación, se propuso una estrategia educativa, que implique a los estudiantes y profesores de las ciencias de la salud, para posibilitar que llegue la información a la población, en todas las comunidades del país. Teniendo como premisa la política que se viene estableciendo del ¨buen vivir¨, y los derechos constitucionales de los ciudadanos en nuestro país.
La estrategia educative propuesta tiene como objetivos fundamentales los siguientes:
Importancia de la vacunación para prevenir la enfermedad
Brindar información en cuanto al uso indebido e irresponsible de medicamentos antipalúdicos
Promoción para la prevención de vectores
Importancia de acudir consulta médica ante la aparición de los síntomas, teniendo en cuenta la gravedad de esta enfermedad
Los objetivos anteriores fueron expuestos en consulta a expertos bajo los siguinetes criterios para validar la propuesta de intervención educativa.
Brinda la posibilidad de informar a la población
Sencibiliza en cuanto a la importancia de la vacunación para evitar la enfermedad
Posibilita implicar a los estudiantes en la difusión de la información
Involucra a todos los miembros de la familia en el proceso
Permite el trabajo en equipos multidisciplinarios
El análsis a través del método AHP de Saaty quedó de la siguiente manera. (Tablas 7 y 8)
Tabla 7 - Matriz A de comparación por pares de los criterios
| Criterios | Criterio 1 | Criterio 2 | Criterio 3 | Criterio 4 | Criterio 5 |
| Criterio 1 | 0 | 0.9 | 0.7 | 0.8 | 0.9 |
| Criterio 2 | 1 | 0 | 1 | 0.9 | 0.9 |
| Criterio 3 | 0.9 | 1 | 0 | 1 | 0.7 |
| Criterio 4 | 0.5 | 0.7 | 0.6 | 0 | 0.5 |
| Criterio 5 | 0.6 | 0.8 | 0.8 | 0.5 | 0 |
| Suma | 3.00 | 3.40 | 3.10 | 3.20 | 3.00 |
Fuente: consulta a expertos.
Tabla 8 - Matriz Normalizada
| Criterios | Criterio 1 | Criterio 2 | Criterio 3 | Criterio 4 | Criterio 5 | PESO |
| Criterio 1 | 0.00 | 0.26 | 0.23 | 0.25 | 0.30 | 0.21 |
| Criterio 2 | 0.33 | 0.00 | 0.32 | 0.28 | 0.30 | 0.25 |
| Criterio 3 | 0.30 | 0.29 | 0.00 | 0.31 | 0.23 | 0.23 |
| Criterio 4 | 0.17 | 0.21 | 0.19 | 0.00 | 0.17 | 0.15 |
| Criterio 5 | 0.20 | 0.24 | 0.26 | 0.16 | 0.00 | 0.17 |
Fuente: consulta a expertos.
El análisis realizado mediante expertos mostró un valor propio de 2.014147265, donde IC= -0.75 y RC= -0.67 resultando consistencia, lo que indica que el método fue aplicado de forma adecuada.
El criterio de mayor peso obtenido fue el número 2, y en segunda posición el criterio 3, que se traducen en:
Sencibiliza en cuanto a la importancia de la vacunación para evitar la enfermedad.
Posibilita implicar a los estudiantes en la difusión de la información
Para lograr mayor efectividad en la prevención de la Malaria en las diferentes comunidades; se consideró de gran utilidad la aplicación de este método educativo en las comunidades, debido a que este posibilita sencibilizar a la población respecto a la importancia de participar en las campañas de vacunación que se lleven a cabo en el país, además de que los protagonistas de llevar a cabo la estrategia serán en gran medida los estudiantes de las ciencias de la salud, lo que contribuye a su desarrollo professional, posibilitando la realación con sus pacientes a través de la medicina comunitaria y de prevención de salud.
Conclusiones
El desarrollo de vacunas contra la malaria avanza, pero es necesario mejorar la investigación e invertir en recursos para ello, debido a la importancia de obtener una vacuna totalmente aprobada que pueda desencadenar en la población la disminución del número de pacientes infectados por plasmodium.
Cada persona es vulnerable a ser infectada por cualquiera de las manchas de los parásitos donde P. falciparum y P. vivax se convierte en el parásito más peligroso que se desarrolla en un humano por un vector portador que afecta los eritrocitos resultando en posibles enfermedades que también afectan durante el embarazo. Sin embargo, es necesario seleccionar la vacuna que tenga mejor acción y resultados como RST, S durante la etapa preeritrocítica que es la vacuna más avanzada.
La propuesta de intervención educativa en las comunidades puede llegar a ser efectiva en la prevención de la Malaria, pues con esta se pretende sencibilizar a la población en cuanto a la importancia de la vacunación como medio más eficaz de evitar la enfermedad. Además de que posibilita implicar a los estudiantes en trabajo comunitario, siendo ellos los principals agentes trasmisores de la información, preparándoles para su futuro desarrollo professional como promotores de salud en los lugares de más difícil acceso.