INTRODUCCIÓN
Las tecnologías ómicas, surgidas para dar soporte al Proyecto Genoma Humano (PGH), se definen por la evaluación de conjuntos específicos de moléculas, el empleo de métodos a gran escala o alto flujo (high throughput) para el procesamiento de muestras complejas, la generación de altos volúmenes de datos, y la necesidad de grandes capacidades de cómputo, herramientas computacionales especializadas y bases de datos para el almacenamiento de sus resultados.1
Las tecnologías ómicas aparecieron a partir de la investigación de las moléculas biológicas objeto de su estudio, según el progreso del PGH y las iniciativas que le siguieron: genómica (a partir del estudio inicial del genoma), transcriptómica (ácido ribonucleico, ARN), proteómica (proteínas) y metabolómica (metabolitos). La lista se extiende hoy a más de 200 tecnologías que configuran nuevas áreas del conocimiento y la investigación; por sus aplicaciones ya en fase de ensayos clínicos destacan entre ellas la microbiómica y la edición del genoma. Por su parte, la farmacogenómica se relaciona con la influencia de las características del genoma del individuo en la respuesta a los medicamentos y, por tanto, en la dosis que aquel necesita; sin embargo, en la literatura se emplean indistintamente los términos farmacogenética y farmacogenómica, a pesar de que el primero tiene menor alcance y debe ser considerado una subcategoría del segundo.2
Entre las tecnologías ómicas, la bioinformática se distingue porque aporta un conjunto de herramientas y recursos computacionales que permiten adquirir, almacenar, organizar, procesar, analizar, observar, modelar, predecir o relacionar los datos obtenidos con el resto de las tecnologías para generar información valiosa. Su naturaleza es interdisciplinar, pues es un área de confluencia de las ciencias de la vida, las tecnologías de la informática y las comunicaciones, así como de otras ciencias: matemática, estadística, física, química, inteligencia artificial, etc.2
Las tecnologías ómicas connotan las potencialidades de lo que se ha dado en llamar “la revolución genómica” en términos de aplicaciones en el diagnóstico y la terapéutica de las enfermedades humanas, particularmente significativas para las ciencias médicas. La incorporación de los datos ómicos a los clínicos, sociales y ambientales permite una comprensión sistémica, integradora, de los procesos de salud y enfermedad. Se habla entonces del modelo de medicina genómica, de precisión o medicina personalizada.3
La Medicina Personalizada de Precisión (MPP) se relaciona con la integración de los datos genómicos y otras ciencias ómicas, con el conjunto de datos clínicos del paciente y su entorno para una práctica clínica adaptada a las características individuales de cada paciente; aporta eficacia, seguridad, eficiencia y sostenibilidad a la atención médica;4) sin embargo, con la MPP aparecen y se diversifican varios dilemas éticos vinculados con la confidencialidad, la protección de la privacidad de los pacientes y los riesgos potenciales de discriminación, así como las decisiones en torno al diagnóstico prenatal y presintomático, la manipulación del genoma y otras formas de tratamiento antes de la aparición de las enfermedades.
Por todo ello, los profesionales de la salud deben prepararse para enfrentar los nuevos escenarios que impondrá la introducción de las tecnologías ómicas en la práctica clínica. Una reunión de expertos de 26 países llamó a los gobiernos y agencias internacionales a reconocer la importancia de la implementación de la medicina genómica y a promover la educación al respecto en la formación inicial y la permanente.5 Ello se debe a la identificación de la falta de información en el personal sanitario como una de las limitaciones para su aplicación en la práctica clínica.2
En este trabajo se muestran los resultados de una exploración de los conocimientos sobre las tecnologías ómicas y la medicina personalizada en estudiantes de Medicina en la Universidad de Ciencias Médicas de Las Tunas, Cuba.
MÉTODOS
Se realizó un estudio exploratorio, cuanticualitativo, para el que se seleccionó, por muestreo no probabilístico, una muestra de 29 estudiantes de segundo año de la carrera Medicina de la Universidad de Ciencias Médicas de Las Tunas, durante el segundo semestre del curso académico 2018-2019. Se obtuvo el consentimiento informado para participar en la investigación.
Se aplicaron métodos teóricos:
Análisis-síntesis e inductivo-deductivo: para el estudio de las fuentes de información y la fundamentación teórica.
Inductivo-deductivo: para la interpretación de los resultados y la formulación de las conclusiones.
Entre los métodos empíricos se aplicaron una prueba de conocimientos y una encuesta en forma de cuestionario. En el primero de esos instrumentos, se preguntó sobre:
Una definición sobre la secuencia del genoma humano, la edición del genoma, la farmacogenética y la bioinformática.
La posibilidad de secuenciar el genoma completo de una persona.
El nombre y dirección electrónica de bases de datos sobre estructuras de proteínas u otras moléculas, genes y sus funciones normales o patológicas, enfermedades humanas y farmacogenética.
Algún gen implicado en la patogenia de una enfermedad humana.
Un medicamento que, para su prescripción, requiera de realizar alguna prueba genética o se haya descrito alguna influencia genética que afecte su farmacología.
Alguna ley o norma sanitaria que regule los estudios sobre el genoma humano, en Cuba u otro país.
En el cuestionario se indagó sobre las asignaturas que habían recibido en la carrera y trataron contenidos sobre:
Técnicas de diagnóstico molecular.
Pruebas genéticas para la prescripción de algún medicamento.
Un gen cuya detección permita diagnosticar alguna enfermedad o el riesgo de padecerla.
Los sitios web o bases de datos con información sobre el genoma humano.
También se les preguntó si consideraban correcto informar a los pacientes sobre los hallazgos de alteraciones en su genoma que signifiquen un riesgo para enfermar, modificar el genoma de una persona para curar una enfermedad o para evitar que enferme.
Los resultados se procesaron por estadística descriptiva y se presentan en frecuencias absolutas y relativas.
RESULTADOS Y DISCUSIÓN
Para explorar los conocimientos de los estudiantes sobre las aplicaciones diagnósticas de las tecnologías ómicas, se relacionaron en una pregunta varias técnicas de biología molecular junto a tecnologías empleadas en la medicina personalizada. Mientras el mayor número de ellos seleccionó la secuencia entre las que conocían, ninguno refirió saber sobre los microarrays, resultados que se muestran en la Tabla 1.
Tabla 1 Proporción de estudiantes que refirieron conocer técnicas de diagnóstico molecular.
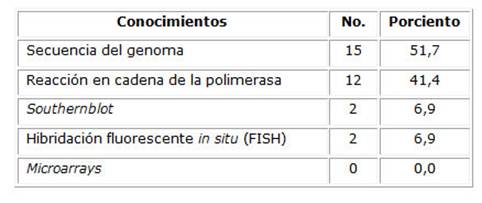
Fuente: prueba de conocimientos.
Fueron pocos los estudiantes que pudieron definir en qué consiste la secuencia y las otras tecnologías ómicas sobre las que se les preguntó, ninguno lo hizo en el caso particular de la bioinformática, datos que se aprecian en la Tabla 2.
Tabla 2 Proporción de estudiantes que definieron adecuadamente las tecnologías ómicas.
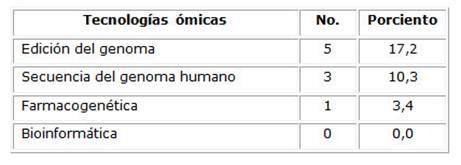
Fuente: prueba de conocimientos.
A la pregunta de si es posible secuenciar el genoma completo de una persona, 17 estudiantes respondieron afirmativamente, lo que significa el 58,6 % de la muestra. En cambio, solo dos (6,9 %) mencionaron correctamente un gen implicado en la patogenia de alguna enfermedad humana: BTK y WT1, que relacionaron de manera correcta con la enfermedad de Bruton (OMIM #300755) y el tumor de Wilms (OMIM #194070), respectivamente.
El anticuerpo monoclonal trastuzumab fue el único medicamento con influencias genéticas en su farmacología y prescripción, señalado por un estudiante (3,4 %).
En ningún caso se mencionó el nombre ni la dirección electrónica de alguna base de datos sobre estructuras de proteínas u otras moléculas, genes y sus funciones normales o patológicas, enfermedades humanas ni vinculadas a farmacogenética. Igual sucedió en relación con el conocimiento sobre la existencia de alguna ley o norma sanitaria que regule los estudios sobre el genoma humano, en Cuba o en otros países.
Genética Médica fue la asignatura identificada con mayor frecuencia por los estudiantes, entre las cinco donde refirieron que se trataron contenidos sobre las tecnologías ómicas u otros aspectos de la medicina personalizada, según expresa en la Tabla 3.
Tabla 3 Proporción (%) de estudiantes que refirieron asignaturas en las que se ofreció tratamiento a las tecnologías ómicas.
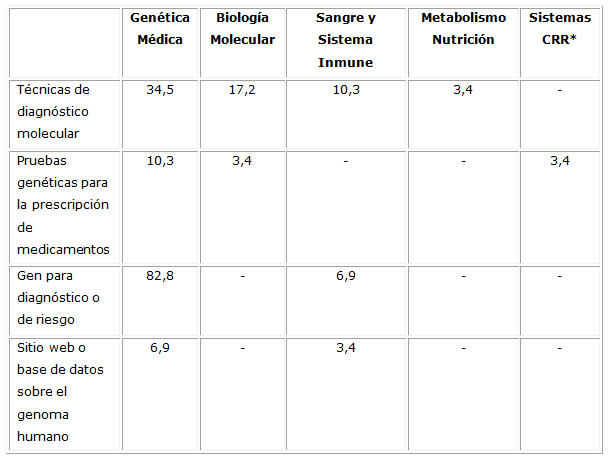
Fuente: cuestionario a estudiantes.
Leyenda: *CRR cardiovascular, respiratorio, digestivo y renal
Al indagar sobre algunos de los dilemas éticos que generan las tecnologías ómicas y la medicina personalizada, puede verse en la Tabla 4, que en todos los casos más de la mitad de los estudiantes estuvo de acuerdo con informar a los pacientes sobre los hallazgos de la secuencia que traduzcan un riesgo para enfermar, así como manipular genomas para tratar una enfermedad o evitar que se produzca.
Tabla 4 Opiniones de los estudiantes sobre algunos dilemas éticos del estudio y manipulación del genoma humano.

Fuente: cuestionario a estudiantes.
El continuo abaratamiento de las tecnologías ómicas hace pensar que en un plazo mediato se extenderán por la práctica clínica y se convertirán en un estándar entre los medios diagnósticos y las terapias para las enfermedades humanas; se llegará a un escenario en que la disponibilidad de equipamiento permitirá secuenciar un número cada vez mayor de individuos, enfermos o no, en los próximos años.
En Cuba, la transferencia de las tecnologías ómicas a la práctica clínica tiene entre sus pilares los recursos humanos altamente capacitados.6 La formación médica inicial, por tanto, está llamada a tratar contenidos que vinculen la medicina personalizada y las tecnologías que la soportan, en los planes y programas de estudio.
El bajo conocimiento sobre las tecnologías ómicas, reflejado en que ningún estudiante refiriera estar al tanto sobre los microarrays, y que menos de la quinta parte de la muestra pudiera definir adecuadamente alguna de aquellas, es un problema que ha sido identificado en varios países, incluso los que cuentan con instituciones que ofrecen servicios de secuencia u otras tecnologías relacionadas con la MPP; por ejemplo, solo el 6 % de los estudiantes de Medicina encuestados en un estudio en Estados Unidos consideró haber sido formado adecuadamente para la medicina genómica;7 ello, un lustro después de que un grupo de expertos reconociera que la enseñanza de la genética para profesionales de la salud en ese país era inadecuada.8
En opinión de estos autores esas limitaciones se deben, en primer lugar, al pobre tratamiento de las tecnologías ómicas y la MPP como contenidos en la formación médica inicial. Una evaluación de contenidos relacionados con la medicina genómica en la formación inicial en facultades médicas de Estados Unidos y Canadá, informó una escasa representatividad y sistematización, apreciada tanto por estudiantes como por profesores.9
Entre las iniciativas de formación sobre medicina genómica se identificaron dos universidades estadounidenses que incluían la secuencia del genoma personal.9) Los principios, aplicaciones e interpretación de la secuencia del genoma completo debe ser considerado en los programas de formación teniendo en cuenta, como se dijo, que en los próximos años esta tecnología será cada vez más rutinaria, tanto en la investigación como en la práctica clínica.
La falta de conocimientos sobre farmacogenética y farmacogenómica, también apreciable en los resultados mostrados en este primer acercamiento al problema, tiene implicaciones para el ejercicio de la medicina, dado el lugar que ocupa el tratamiento entre las habilidades y niveles de actuación del médico en el modelo del profesional declarado en Cuba. En tal sentido, se ha identificado que el limitado conocimiento sobre farmacogenética en profesionales de la salud en España impide una prescripción segura y eficaz en un buen número de fármacos, de acuerdo con las recomendaciones de las agencias reguladoras.10
Llama la atención que haya sido un anticuerpo monoclonal, el trastuzumab, el medicamento señalado por sus requerimientos farmacogenéticos. Se trata de un bioproducto aprobado contra el cáncer de mama con sobrexpresión de HER2, que mejora la supervivencia y reduce la recurrencia de la enfermedad, para el que se han descrito polimorfismos asociados a menor eficacia, como el rs1801274-G, o a mayor toxicidad, como rs1136201-G, sobre todo eventos cardiovasculares con baja fracción de eyección ventricular e insuficiencia cardiaca congestiva grave.11
El conocimiento sobre bioinformática, evaluado a través de preguntas sobre las bases de datos biológicos, también resultó insuficiente. Entre otras causas, ello pasa porque la mayoría de los profesores tampoco fueron formados en esa área.12) El creciente número de bases de datos biológicos, repositorios y herramientas bioinformáticas, así como las oportunidades que abren a la docencia, la asistencia y la investigación, brindan argumentos para considerar el desarrollo de iniciativas de formación que incorporen este tipo de contenidos.
El marco regulatorio es un contenido a considerar en la formación médica, sobre todo en temas relacionados con los usos de la información genética y la manipulación del genoma humano, que generan dilemas éticos y situaciones nuevas en la relación médico-paciente. Por ello es importante que los profesionales de la salud reciban, en su formación, contenidos sobre las leyes y normas sanitarias que regulan las investigaciones sobre el genoma. Dos de las normas jurídicas que pueden servir de ejemplo son:
La Resolución No. 219 del Ministerio de Salud Pública de Cuba, que contiene las normas éticas para la protección de la información genética de ciudadanos cubanos que participan en investigaciones o se les realizan diagnósticos asistenciales en las que se accede a datos relativos al individuo y a sus familiares, así como a material biológico a partir del cual puede obtenerse ADN, publicada en la Gaceta Oficial No. 29 Extraordinaria del 18 de junio de 2007.13
Genetic Information Nondiscrimination Act of 2008, conocida por sus siglas GINA, aprobada por el Congreso de Estados Unidos el 21 de mayo de 2008.14
Solo cinco asignaturas, de acuerdo con lo mencionado por los estudiantes, dieron tratamiento a las tecnologías ómicas en las actividades docentes. Ello representa el 14,3 % del total de 35 asignaturas de los currículos base y propio de la carrera Medicina hasta el cuarto semestre. Llama la atención que en ningún caso se trató de las que vinculan a los estudiantes directamente con la práctica clínica, particularmente con la atención primaria de salud, como son Introducción a la Medicina General Integral, Promoción de Salud, Prevención en Salud, Nutrición, Vacunación, Introducción a la Clínica y Medicina Comunitaria. No se aprovechan los espacios de la educación en el trabajo para abordar contenidos sobre las tecnologías ómicas y la MPP.
Varios autores han reconocido que los contenidos relacionados con genética se imparten en los primeros años de la carrera, momento en que son percibidos más por su carácter de ciencia básica, con escasa importancia para la práctica clínica. Se pierden así oportunidades para la vinculación básico-clínica y la aplicación de los contenidos aprendidos al diagnóstico, incluidas las pruebas genéticas y las terapias personalizadas, entre otros aspectos.8 En igual sentido, se ha llamado a que las universidades médicas incorporen más contenidos sobre las tecnologías ómicas en todo tipo de docencia, tanto conferencias como pases de visita.10
Una alerta sobre la formación en genómica y bioinformática para facilitar la traslación de la MPP a la práctica asistencial en las comunidades autónomas de España, considera indispensable su inclusión en los programas de posgrado.4) Los autores de esta investigación opinan al respecto que la formación médica inicial puede ser el punto de partida más efectivo por su mayor alcance, bien sea a través de asignaturas dedicadas específicamente a esos contenidos o integrados a los programas de las demás asignaturas. También deben tenerse en cuenta las posibilidades que ofrecen las tecnologías de la información y las comunicaciones para complementar y reforzar el proceso enseñanza aprendizaje, tanto presencial como a distancia.5
La mayoría de los estudiantes encuestados creyó correcto informar a los pacientes sobre los hallazgos relativos a las alteraciones en su genoma, así como la utilidad de realizar manipulaciones genéticas en bien de la salud de los individuos. He aquí un hallazgo importante, pues revela una disposición positiva hacia la utilización de las tecnologías ómicas que, sin subestimar la complejidad de los dilemas éticos que ellas traen aparejados, puede favorecer su introducción en el sistema nacional de salud y la implementación de la MPP en el país.
La resistencia de los profesionales ante el cambio de paradigma que la MPP supone para la práctica asistencial es uno de los retos detectados en otros países, al tiempo que son ellos mismos quienes impulsan mayormente este cambio de paradigma sanitario, la implicación de las instituciones, la inclusión de aspectos de MPP en las políticas sanitarias y la necesidad del cambio a nivel gubernamental.4) La formación médica inicial tiene, por tanto, el reto de fomentar actitudes positivas hacia la MPP, como parte de su tratamiento como contenido.
Puede señalarse como limitación del presente estudio el haber incluido estudiantes que solo han cursado los primeros cuatro semestres de la carrera Medicina, por lo que no han recibido los contenidos del ciclo clínico, que tiene en la educación en el trabajo su forma fundamental; además de lo comentado sobre las asignaturas que vinculan al estudiante a la práctica asistencial desde el primer semestre de la carrera, aunque se considera que la situación actual revelada en esta investigación no es diferente para los años superiores, es decir, del tercero al sexto. No obstante, queda por indagar al respecto y mostrar las evidencias. Un reporte recién publicado deja ver que los conocimientos entre médicos residentes, recién graduados o con experiencia asistencial, son igualmente insuficientes.15
CONCLUSIONES
A partir de los resultados encontrados en esta exploración se constató que es bajo el nivel de conocimientos en los estudiantes de segundo año de Medicina en relación con las tecnologías ómicas, tanto las empleadas con fines diagnósticos como terapéuticos, así como sobre el marco legal que regula los hallazgos en torno al genoma humano, en Cuba como de otros países; sin embargo, los estudiantes mostraron una actitud positiva hacia la importancia de informar a los pacientes sobre los resultados del estudio del genoma, así como de la posibilidad de modificarlo, si existieran criterios médicos que lo justificaran.














