INTRODUCCIÓN
A finales del siglo XIX, en el Hospital Kasr El Aini, de El Cairo, Egipto, un oficial médico del ejército imperial inglés, prácticamente aislado y obligado por la necesidad1, realizó por primera vez, la más empleada de todas las incisiones sobre la caja torácica. En sendos artículos de los años 1897 y 1901, Herbert Meyrick Nelson Milton (octubre 1857 - 20 de diciembre de 1921) describió la técnica de esternotomía longitudinal media para el abordaje al mediastino, primero para la resección de un enorme nódulo linfático tuberculoso y posteriormente para la extracción, a través de la tráquea, de un cuerpo extraño alojado en un bronquio2-4.
Aunque a todas luces esta incisión ofrece un fácil acceso a los órganos del mediastino ántero-superior, no fue hasta 1953 que Harry B. Shumacker (20 de mayo de 1908 - 14 de noviembre de 2009) la utiliza en valvulotomías pulmonares cerradas en 8 pacientes, y la propone para la cirugía cardíaca, describiéndola erróneamente como un nuevo abordaje. Sin embargo, curiosamente las ventajas de la exposición en la línea media habían sido tibiamente recibidas un tiempo antes, cuando el cirujano estadounidense presentó por primera vez su manuscrito en el mitin anual de la Asociación Americana de Cirugía Torácica5, y se continuó empleando -durante las primeras décadas de operaciones sobre el corazón- la incisión preferida hasta el momento: la toracotomía bilateral anterior transesternal6.
Según Dalton et al7, en octubre de 1957, Ormand Clinkenbeard Julian (6 de mayo de 1913 - 18 de diciembre de 1987) retomó el debate y propuso la reintroducción de la incisión de Milton en la incipiente cirugía cardíaca con circulación extracorpórea, con el objetivo fundamental de evadir las complicaciones pulmonares secundarias a la abertura de ambas hemicavidades torácicas durante el abordaje en «concha de almeja». Mencionó en su artículo, que el mayor beneficio que se obtenía con el acceso al corazón a través del esternón, provenía de evitar todo trauma sobre el pulmón, especialmente en el grupo de pacientes cianóticos, entiéndase enfermos con cardiopatías congénitas más graves. La posibilidad de operar sin necesidad de abrir las pleuras le permitiría al anestesiólogo insuflar manualmente los pulmones en momentos claves de la cirugía, lo cual eludía el colapso alveolar y las atelectasias7. No obstante, aún en 1958 se evitaba la esternotomía y mediante incisiones en «concha de almeja» se realizaron las primeras anastomosis entre arterias mamarias y coronarias, cuando a Longmire se le complicaron algunas de sus endarterectomías abiertas8,9.
A finales de la década de 195010 un grupo de la Clínica Cleveland de Ohio, dirigido por William H. Sewell propuso la modificación de la técnica de implantación de una arteria torácica (mamaria) interna esqueletizada en el miocardio (Vineberg)11, mediante la tunelización del vaso, ahora preparado en forma de una banda tisular conformada por la mencionada arteria, sus venas, fascia endotorácica-pleura parietal, linfáticos y otros tejidos perivasculares («operación del pedículo»)12,13. Con el desarrollo posterior de la cirugía de injertos aorto-coronarios, la práctica de diseccionar la arteria mamaria en forma de pedículo rápidamente se convirtió en la técnica preferida por la mayoría de los grupos, por ser más rápida y teóricamente menos dañina para el hemoducto14-16.
Uno de los inconvenientes de este procedimiento es que su primer paso, usualmente, consiste en la apertura de la cavidad pleural17,18, para visualizar adecuadamente algún segmento de la arteria que se tomará como inicio de la disección. En no pocas ocasiones es posible conservar la integridad pleural con esta variante de disección, pero muchos cirujanos prefieren construir un pedículo lo suficientemente ancho como para evitar la lesión accidental de una arteria que no siempre permanece visible durante toda su preparación; en esa circunstancia es prácticamente inevitable no invadir el espacio pleural.
En pacientes con historia de nicotinismo, enfermedad pulmonar obstructiva crónica o enfisema, es prácticamente imposible acceder a las porciones más proximales de la arteria mamaria sin modificar momentáneamente la anatomía de los órganos que la rodean, en especial los pulmones hiperinsuflados que intentan ocupar su posición habitual. Algunas de las soluciones que se implementan en esta situación consisten en deprimirlo manualmente con los separadores comúnmente empleados en cirugía torácica, con una pinza larga protegida con gasa, o -más frecuentemente- con la cánula metálica de aspiración; también puede desinflarse pasivamente colocándole un peso encima, como compresas húmedas (Fig. 1). Otra práctica habitual de los cirujanos es solicitarle al anestesiólogo la disminución del volumen corriente o de la presión positiva al final de la espiración (PEEP, por sus siglas en inglés). Cualquiera de estas estrategias puede trastornar suficientemente la anatomía o fisiología del sistema respiratorio como para causar importantes complicaciones durante y después de la cirugía.
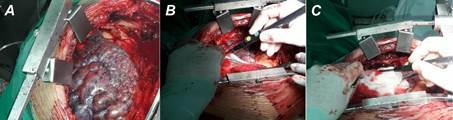
Fig. 1 A. Cuando un pulmón enfisematoso dificulta el acceso al segmento proximal de la mamaria inevitablemente debe modificarse su anatomía mediante depresión o separación. B. Depresión mediante separador pulmonar clásico. C. Depresión con la cánula metálica de aspiración al vacío.
A comienzos de la década de 1970 algunos grupos comenzaron a practicar de forma estable la disección esqueletizada de la arteria mamaria para la cirugía de revascularización miocárdica19. Esta técnica permite muchas veces conservar la integridad de la cavidad pleural20-23. Sin embargo, también durante el abordaje al segmento de la arteria comprendido en los tres primeros espacios intercostales, la ventilación del pulmón puede complicar seriamente la maniobrabilidad del cirujano y conllevar la lesión de estructuras vasculares, nerviosas o la propia pleura y pulmón, y el consumo de más tiempo del deseado para la disección.
En 1992 Cunningham y colaboradores23 señalaron que un separador retráctil estratégicamente colocado podría proveer excelente exposición en esta situación. Durante más de un cuarto de siglo, prácticamente no se ha vuelto a mencionar dicho aditamento.
En una extensa revisión de artículos relacionados con la disección de la arteria mamaria en cualquiera de sus variantes, publicados desde la década de 1940, solo se encontró un trabajo en el que se propone el empleo de pinzas hemostáticas convenientemente colocadas, para optimizar la disección extrapleural del hemoducto, donde los autores teorizan la fabricación futura de un separador más sofisticado24. La literatura analizada no permite precisar las estrategias empleadas por otros grupos quirúrgicos para lidiar con la interposición pulmonar durante la disección de la arteria mamaria.
Desde finales de 2015 nuestro grupo confeccionó y comenzó a utilizar un separador retráctil de pulmón con el objetivo de facilitar la maniobra de disección esqueletizada de la arteria mamaria interna. Según nuestro conocimiento, este es el primer dispositivo fabricado en el mundo con esa intensión. A continuación se presentan sus principales características y ventajas.
CARACTERÍSTICAS DEL SEPARADOR PROPUESTO
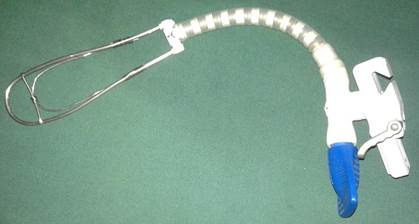
El elemento fundamental del separador pulmonar retráctil que se presenta, lo constituye el brazo articulado de los estabilizadores de arterias coronarias epicárdicas, empleados en la cirugía de revascularización miocárdica. Estos dispositivos son fabricados habitualmente para un solo uso, por lo que se prescinde de ellos muy pronto. Por tal motivo, existe una amplia disponibilidad de ese aditamento en centros de cirugía cardiovascular donde se practique cirugía coronaria sin circulación extracorpórea u otras variantes quirúrgicas a corazón latiendo. La «valva» del separador se fabrica a partir de varillas de aluminio o acero inoxidable; estos componentes y las pequeñas láminas de metal maleable empleadas para unirlos, también se obtienen de instrumentos desechados en cirugía cardiovascular: pleurótomos de pequeño calibre, ganchos de Overholt o uriómetros, cánulas de cardioplejia, y otros. En algunos de los separadores que hemos construido, sus componentes han sido unidos sencillamente con sutura de acero quirúrgico empleado para el cierre esternal (Fig. 2). El tiempo total de fabricación, con un mínimo necesario de herramientas, no ocupa más de una hora.
VENTAJAS
El diseño del soporte ajustable del estabilizador coronario le permite adherirse de forma rápida a una gran variedad de separadores esternales empleados durante la disección mamaria. Puede resultar conveniente fabricarlos en varios tamaños para que se puedan ceñir a diferentes situaciones anatómicas, pero hemos fabricado al menos uno en el que la varilla metálica curva («valva») puede deslizarse a través de los soportes plásticos del brazo articulado, lo que le permite variar su extensión (Fig. 3). Una vez que el separador ha sido adecuadamente fijado a una estructura rígida, el cirujano puede posicionarlo de forma conveniente para que no interfiera con su maniobrabilidad (Fig. 4). Debe recordarse que se coloca casi exclusivamente cuando la disección de los segmentos proximales de la mamaria se ve entorpecida por la expansibilidad pulmonar, por lo que con solo unos poco usos, el cirujano es capaz de predecir con facilidad la posición más ventajosa que le permitirá concluir el procedimiento sin mayores contratiempos.
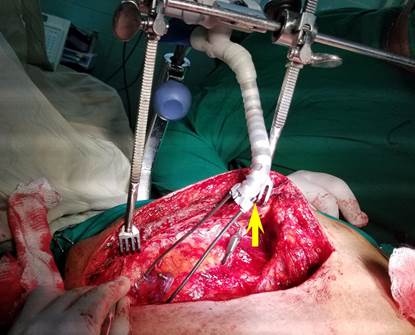
Fig. 3 Separador facilitando la disección del segmento proximal de la arteria mamaria izquierda. Obsérvese que la varilla curva en forma de «valva» puede deslizarse a conveniencia del cirujano (flecha), lo que modifica el alcance del separador. En este paciente, el extremo distal de la mamaria ha sido pinzado al inicio de la disección, en consonancia con el nuevo método de disección mamaria propuesto por el autor principal de este artículo.
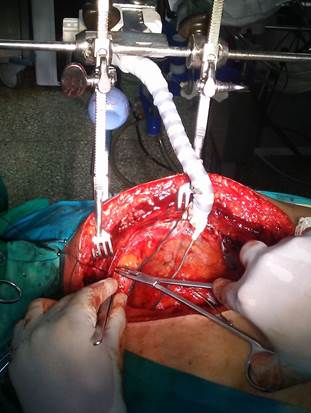
Fig. 4 La adecuada disposición del separador no interfiere con la maniobrabilidad del cirujano. En este paciente, además, la vena mamaria ha sido separada de la arteria mediante un punto de tracción anclado al borde de la herida, maniobra que también facilita la disección del segmento proximal del hemoducto.
En las situaciones que ameritan su despliegue, el separador, al conservar cierta flexibilidad, disminuye o elimina los traumas sobre el pulmón, mediante una depresión más gentil de la víscera, de forma estable, y solo estrictamente necesaria para descubrir el trayecto de la mamaria, con evidentes ventajas sobre la dinámica ventilatoria durante ese tiempo. Esto juega un papel importante en pacientes enfisematosos o con abundantes bulas en las porciones superomediales del pulmón, que al insuflarse disminuyen considerablemente la visualización del cirujano, y que al separarse bruscamente pueden lesionarse con facilidad.
Una mejor visualización del cirujano, obviamente facilita la disección de la arteria mamaria en cualquier variante, disminuye la duración del procedimiento, así como el riesgo de lesión de estructuras periarteriales y la incidencia de atelectasias, al reducir los traumas pulmonares y prescindir de la necesidad de disminuir la PEEP o el volumen corriente pulmonar durante la disección.
Un dispositivo ajustable que asuma la separación de estructuras anatómicas siempre racionalizará la utilización del personal del equipo quirúrgico en cualquier intervención; en nuestro caso, al eliminarse la necesidad de que una enfermera deprima el pulmón durante la preparación del segmento proximal de la mamaria, se optimiza su función de instrumentista para apoyar la extracción de los hemoductos que se diseccionan sincrónicamente (arteria mamaria y radial, vena safena).
En muchas ocasiones, una separación gentil del pulmón permitirá conservar la integridad de la cavidad pleural lo que redundará en muchos beneficios, durante y -especialmente- después de la cirugía. En el transoperatorio, una pleura cerrada evitará la acumulación desapercibida de sangre en la cavidad torácica, lo que indirectamente obliga al cirujano a localizar y controlar puntos imprecisos de sangrado, cuando la hemorragia comienza a rebosar el mediastino anterior; esto disminuirá la posibilidad de anemia y la necesidad de transfusiones. Siguiendo esta misma lógica, la pleura intacta impedirá la mezcla de la papaverina empleada para irrigar el hemoducto, con cantidades de sangre que posteriormente puedan ser aspirados al reservorio de cardiotomía, e infundidas nuevamente al paciente. Este aspecto ha sido poco estudiado, pero en teoría es posible que el antiespasmódico empleado durante la disección de hemoductos, si es incorporado al torrente sanguíneo del paciente, pueda ser responsable de vasoplejia transoperatoria hemodinámicamente significativa.
La apertura de la cavidad pleural durante la disección mamaria puede también ser responsable de una elevada morbilidad durante el posoperatorio. Se han informado derrames pleurales en cerca de un 90% de los pacientes en la primera semana de la cirugía, algunos son catalogados de crónicos persistentes y relacionados con la preparación mamaria; y en muchas ocasiones requieren abordaje quirúrgico25. Además la abertura del espacio pleural puede ocasionar neumotórax y fístulas entre arterias sistémicas y vasos pulmonares, entre otras complicaciones. La consecuente colocación de drenajes a través de espacios intercostales, contradictoriamente, puede entorpecer la resolución de derrames al interferir con la capacidad absortiva de la pleura25, y puede ser un origen importante de síndromes dolorosos torácicos posoperatorios26,27 causantes de neumonías, ventilación mecánica invasiva y estadía prolongada en sala de cuidados intensivos, entre otras complicaciones.
Por último, no debe dejar de mencionarse la amplia versatilidad que ofrece el dispositivo para su empleo en otras especialidades donde se requiera la separación de órganos sin comprometer las habilidades bimanuales de los cirujanos, especialmente durante la cirugía torácica, donde puede acoplarse al clásico separador de Finochieto.
CONCLUSIONES
La evidencia demuestra que la preservación de la integridad pleural durante la preparación de la arteria mamaria interna se asocia a menor incidencia de disfunción pulmonar y de complicaciones respiratorias en el postoperatorio28; comentar completamente los beneficios de esta estrategia está más allá de los objetivos de este trabajo.
En cirugía cardiovascular, pacientes en los que se logre conservar la integridad de la cavidad pleural prescindirán del clásico drenaje intercostal, e incluso ocasionalmente podrá colocárseles una sola sonda en mediastino anterior16. Las probabilidades de desarrollar derrame pleural unilateral, complicaciones respiratorias infecciosas, neuralgias intercostales o atelectasias serán mínimas, así como el sangrado y la necesidad de transfusiones. Una pleura intacta disminuirá considerablemente la formación de adherencias pulmonares y la distorsión de la anatomía intratorácica29, lo cual resulta extremadamente beneficioso para el paciente y cirujano si posteriormente surge la necesidad de un procedimiento quirúrgico oncológico, situación cada vez más frecuente en la cirugía torácica actual30,31.
A esto deben agregársele los conocidos beneficios de la disección esqueletizada de la arteria mamaria en prácticamente cualquier estrategia de revascularización que se emplee, en relación con la poca incidencia de dolor o parestesias torácicas32,33, y de complicaciones profundas de la herida esternal34-36.
Desde finales del 2015, el separador de pulmón se ha empleado en cerca de un centenar de pacientes operados en nuestro servicio. Un análisis preliminar de su efectividad mostró beneficios transoperatorios en relación con la conservación de la integridad pleural, disminución del tiempo de disección y protección de la vena mamaria28, situación esta última que también se puede traducir en una mayor protección del esternón, pues algunos autores han señalado la existencia de una posible teórica relación entre lesión del drenaje venoso retroesternal y complicaciones profundas del hueso36,37. Quizás deba señalarse también que durante todo este tiempo no han existido casos de mediastinitis en nuestro servicio, complicación con consabidas repercusiones tanto médicas como económicas38,39. Además, como norma general, los enfermos en los que se ha usado el dispositivo han permanecido menos días en sala de cuidados intensivos posoperatorios y se han egresado más precozmente, lo que indudablemente ha significado una cuantiosa disminución de los costos hospitalarios en este importante grupo de pacientes.