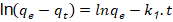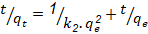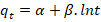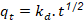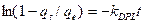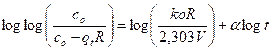INTRODUCCIÓN
Los últimos años han permitido el desarrollo de métodos para la obtención de carbón dada la amplia gama de aplicaciones. La demanda ha llevado a buscar materias primas de bajo costo y amplia disponibilidad, donde los materiales renovables juegan un papel importante García, (2004), (Prieto y col., 2020), (Sharma y Janveja, 2008). Ha sido poco estudiada la factibilidad de obtener carbones activados a partir de algunos recursos biomásicos de las regiones tropicales con amplia disponibilidad y mínima competencia con otros usos (Reinoso, 2002).
La contaminación por metales pesados puede deberse de manera natural al medio ambiente (litogénica) y por la actividad del hombre (antropogénica). Lo anterior conduce a dos índices de contaminación por metales según la Environment Protection Agency (EPA): Índice potencial de contaminación (IPC) e Índice de tecnofilidad (IT).
Las propiedades adsorbentes de los carbones pueden ser utilizadas para la eliminación de metales pesados potencialmente tóxicos como el plomo, el cual ocupa el primer lugar en el IPC y el segundo lugar en el IT.
Como consecuencia de lo planteado el objetivo de este trabajo es obtener carbón activado con buenas propiedades adsortivas a partir de bagazo de caña de azúcar, bambú y marabú, recursos renovables de disponibilidad en el país, que permita la eliminación de iones Pb (II) de soluciones acuosas.
MATERIALES Y MÉTODOS 1 2 3 4 5 6
La preparación del carbón parte de bagazo de caña de azúcar (BC), marabú (M) y bambú (B) previamente secados, molidos y tamizados para la obtención de una granulometría adecuada. Se utilizan procesos “químicos” con ácido fosfórico 0,1 mol/L y parámetros operacionales de 120 minutos a temperatura de 673 K. Con ácido nítrico 0,2 mol/L se activa para aumentar la superficie específica de los materiales Los adsorbentes obtenidos son sometidos a un proceso de caracterización donde se evalúa la densidad aparente por aprisionamiento (g/mL), la densidad picnométrica (g/mL), densidad aparente (g/mL), porosidad (%), compresibilidad (%), tortuosidad, factor de forma, humedad (%), material volátil (%), ceniza (%), carbón fijo (%) , índice de yodo, índice de azul de metileno, superficie específica respecto al azul de metileno y pH (Prieto y col., 2020).
Una vez caracterizada la fracción menor de 0,20 mm de diámetro se estudia la cinética de adsorción de iones Pb (II) al determinar sus concentraciones en disoluciones acuosas mediante la técnica de absorción atómica siendo utilizado el espectrofotómetro Perkin Elmer 372. Se aplican diferentes modelos cinéticos y difusivos: seudoprimer orden, seudosegundo orden, Elovich, difusión en la película de liquido, difusión intrapartícula, modelo de Bangham y difusividad efectiva, mediante las siguientes expresiones (Avon, 1997), (Azizan, 2004), (Chen y Wang, 2007), (Chun-I ( Li-Hua, 2008), (Rivera-Utrilla y col., 2003), (Lavado y col., 2010), (Prieto y Lestayo, 2017).
Modelo de seudo primer orden
Modelo de seudo segundo orden
Modelo de Elovich
Modelo de difusión intrapartícula
Modelo de difusión en la película de líquido
Modelo de Banhgam
Donde:
qe = cantidad de metal adsorbido en el equilibrio (mg/g)
qt = cantidad de metal adsorbido en cualquier instante (mg/g)
t = tiempo (minutos)
k1 = constante de velocidad de seudo primer orden (min-1)
k2 = constante de velocidad de seudo segundo orden (g/mg-min)
kd = constante de velocidad de difusión intrapartícula (mg/g s1/2)
α = velocidad de sorción inicial (mg/g min)
β = constante de desorción (g/mg)
kDPL= constante de velocidad de difusión en la película de líquido (s-1)
k0 y α son constantes de la ecuación de Bangham. Los valores de α deben estar entre 0 y 1.
R: relación entre la masa del adsorbente y el volumen de la solución (g/L).
RESULTADOS Y DISCUSIÓN
Las diferentes fracciones se caracterizan y los resultados se muestran en la Tabla 1.
Tabla 1 Parámetros físicos y químicos de las fracciones de carbones empleadas en la adsorción de iones Pb (II)
| Densidad aparente por aprisionamiento | 0,33 g/mL | 0,75 | 0,48 |
| Densidad picnométrica | 1,09 g/mL | 1,34 | 0,72 |
| Densidad aparente | 0,28 g/mL | 0,38 | 0,34 |
| Porosidad total | 74 % | 71% | 52,5% |
| Factor de forma | 0,47 | 0,49 | 0,60 |
| Compresibilidad | 15 | 49 | 29,8 |
| Tortuosidad | 1,67 | 1,25 | 1,52 |
| Humedad | 6,5 % | 8,9 % | 9,2 % |
| Material volátil | 31,3 % | 42,9 % | 29 % |
| Ceniza | 50,2 % | 10,6 % | 12,6 % |
| Carbón fijo | 12 % | 37,6 | 49,18 |
| pH | 6 | 2,9 | 6,2 |
| Índice de azul de metileno | 15 | 18 | 16 |
| Índice de yodo | 834 | 1001 | 918 |
| Superficie específica | 202 m2/g | 305 | 223,5 |
| Radio promedio de poro | 535 nm | 107 nm | 297 nm |
El carbón de bambú presenta la más alta densidad picnométrica, con alta porosidad, solo superada por el carbón de bagazo de caña de azúcar. Es destacable su compresibilidad, que es la más alta de todas. Presenta el mayor por ciento de material volátil. Es el más ácido de los carbones, al presentar pH de 2,9. Posee el más alto índice de yodo, índice de azul de metileno y superficie específica. Es necesario destacar dado el radio de poro que el carbón de bagazo de caña de azúcar corresponde a un material macroporoso, en cambio los carbones de bambú y marabú es mesoporoso.
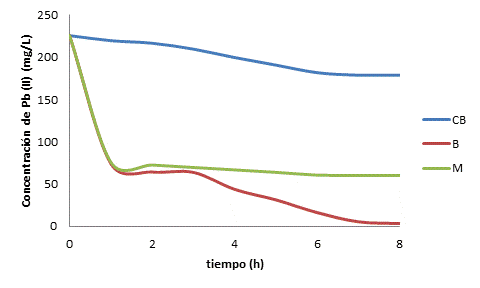
A continuación se aprecia la dependencia de la concentración con el tiempo para los tres carbones a la temperatura de 298 K:
En la Figura 1 se aprecia como el mejor adsorbente es el carbón de bambú, cuya capacidad de adsorción es de 111,15 mg/g.
El estudio cinético y difusivo permite obtener los siguientes modelos evaluados por los coeficientes de determinación (Tabla 2).
Tabla 2 Coeficientes de determinación de los modelos cinéticos de la adsorción de iones Pb (II) en los diferentes carbones activados
| Seudoprimer orden | 0,988 | 0,981 | 0,977 |
| Seudosegundo orden | 0,818 | 0,972 | 0,901 |
| Elovich | 0,88 | 0,951 | 0,841 |
| Difusión intrapartícula | 0,969 | 0,978 | 0,957 |
| Difusión en la película de líquido | 0,818 | 0,769 | 0,782 |
| Modelo de Bangham | 0,959 | 0,928 | 0,764 |
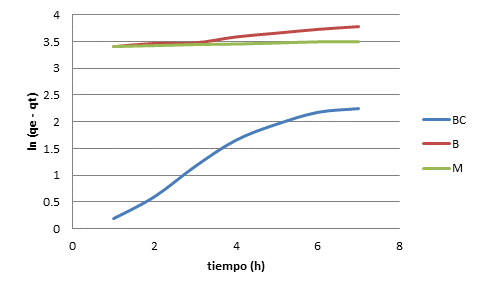
Como se aprecia hay dos aspectos importantes en la adsorción de iones Pb (II) en soluciones acuosas utilizando carbón obtenido por activación “química”. La adsorción de iones Pb (II) responde a una adsorción de tipo física de seudoprimer orden dado el alto coeficiente de determinación. Las constantes de velocidad “aparente” de seudoprimer orden son 0,361, 0,059 y 0,016 min-1 para el carbón de bagazo de caña de azúcar, marabú y bambú, respectivamente. El tiempo de vida media para los carbones anteriormente mencionados son 1,92, 11,75 y 43,32 minutos. Lo anterior permite afirmar que el proceso de adsorción de iones Pb (II) en solución acuosa desde el punto de vista de rapidez esta beneficiado para el carbón de caña de azúcar, no así para el carbón de bambú, que es el más lento de los tres carbones empleados. En cuanto a la capacidad de equilibrio de adsorción (qe) muestran un valor de 9,48 meq/g, 0,85 meq/g y 44,52 meq/g, para carbón de bagazo de caña de azúcar, marabú y bambú, respectivamente. Lo anterior se infiere de los análisis reflejados en la Figura 2.
Al atender a las concentraciones de equilibrio (Ce) para cada carbón se tienen los valores de 179 mg/L, 59,7 mg/L y 3,69 mg/L para carbón de bagazo de caña de azúcar marabú y bambú, respectivamente.
Al establecer los valores de las constantes de equilibrio a partir de los valores de qe y Ce se obtiene valores de la energía libre (ΔG) de +7,28 kJ/mol, -6,17 kJ/mol, y +10,52 kJ/mol para el proceso de adsorción para los carbones de bagazo de caña de azúcar, bambú y marabú, respectivamente. Lo anterior responde a los valores de las constantes de equilibrios de 0,053, 12,07 y 0,014 L/g, respectivamente. Si solo se considera al valor de esta variable de estado el proceso es espontaneo para el bambú.
En cuanto a los mecanismos difusivos se aprecia que la difusión intrapartícula juega un papel importante en los tres carbones, por lo que la aplicación del modelo rotacional conduce a los siguientes coeficientes de difusión, los cuales son para el carbón de bagazo de caña de azúcar, marabú y bambú los valores de 3,0•10-10, 3,3•10-11 y 2,8•10-12 m2/s. Un análisis comparativo sobre los coeficientes de difusión efectivo sobre otro adsorbente como la ceniza de bagazo de caña de azúcar a la temperatura de 298 K, se obtiene el valor de 4,5 • 10-18 m2/s, cuyo valor está condicionado por el pequeño tamaño de radio de poro del adsorbente.
CONCLUSIONES
El carbón obtenido de bambú presenta los mayores índices de azul de metileno y de iodo.
El carbón de bambú muestra la mayor capacidad de adsorción de equilibrio para los iones Pb (II), 111,15 mg/g, siendo la superficie específica (305 m2/g) el factor fundamental de este resultado.
El análisis estadístico a través de los coeficientes de determinación permite establecer una fisisorción de los iones Pb (II) con orden de adsorción de seudoprimer orden para los tres carbones utilizados. Para los carbones de bagazo de caña, bambú y marabú los valores son 0,988, 0,981 y 0,977, respectivamente.
La difusividad efectiva se presenta con menor valor en el carbón de bambú (2,8•10-12 m2/s), lo cual es atribuible al presentar el menor radio de poro.