INTRODUCCIÓN
En las últimas décadas la batalla por la salud se ha visto impulsada por la investigación científica,1 sobre todo en ramas de la Medicina como la Microbiología clínica. La creación de líneas de trabajo en el laboratorio, que trasciendan más allá de la recomendación habitual o lo convencional, es clave para el progreso que demanda la actual Revolución Científico-Técnica con la aparición de novedosos métodos diagnósticos.
La necesidad de contar con nuevas técnicas de laboratorio más rápidas, sensibles y específicas para la detección de agentes patógenos de difícil aislamiento, cultivo e identificación por los métodos convencionales llevó a la Salud Pública cubana, con el IPK (Instituto de Medicina Tropical “Pedro Kourí”), a implementar el diagnóstico molecular en todo el país.
Para lograrlo se decidieron la descentralización del Laboratorio Nacional de Referencia y la construcción de Laboratorios de Biología Molecular en los CPHEM (Centros Provinciales de Higiene, Epidemiología y Microbiología) de La Habana, Villa Clara y Santiago de Cuba como parte del Proyecto MediCuba Europa para el fortalecimiento y el desarrollo de la Microbiología molecular en Cuba.
Con la inauguración y la puesta en marcha de este Laboratorio en el CPHEM de Villa Clara, en junio de 2018, se le dio un nuevo rol protagónico a la técnica PCR (reacción en cadena de la polimerasa) en tiempo real en la Región Central de Cuba porque permitió disminuir el tiempo de respuesta y la demora en la emisión de los resultados de determinaciones clínicas que anteriormente se tributaban al Laboratorio Nacional de Referencia del IPK. Desde sus inicios se aplicó como una importante herramienta para la vigilancia activa clínico-epidemiológica al diagnosticar, a nivel genómico, agentes infecciosos.
En este sentido la PCR en tiempo real cumple sobrados requisitos de rapidez, sensibilidad, especificidad y confirmación diagnóstica2 porque permite la detección de material genético (ácidos nucleicos), tanto (ADN) ácido desoxirribonucleico como (RNA) ácido ribonucleico, que constituyen la característica inequívoca de especie y sus modificaciones genéticas, lo que tiene diferentes aplicaciones según la situación estudiada.3
En el campo de la Microbiología se define su aplicación para poder detectar microorganismos o agentes de difícil desarrollo en medios de cultivo, tanto artificiales como celulares, en los que las técnicas serológicas de detección de antígenos y anticuerpos carecen de suficiente validez diagnóstica. De ahí que tenga vital importancia su uso en Virología.3
Con la emergencia que determinó la llegada de la COVID-19 a Cuba, la Biología molecular villaclareña se dispuso, de inmediato, a procesar las muestras de exudado nasofaríngeo; resultó ser el Laboratorio el primero en detectar el primer caso autóctono el 11 de marzo de 2020. Desde ese momento la RT-PCR (PCR tras transcripción inversa) en tiempo real para la detección del SARS-CoV-2 fue crucial para lograr el desenlace efectivo de la pandemia en la Región Central hasta su definitiva contención epidemiológica.
Actualmente se han diversificado las determinaciones clínicas estudiadas por técnicas moleculares en el CPHEM de Villa Clara con la incorporación de nuevas plataformas diagnósticas basadas por igual en la PCR en tiempo real, pero utilizando sistemas tanto cualitativos como cuantitativos, lo que ha contribuido a elevar el desarrollo de la Microbiología molecular en la Región Central del país.
Esta investigación tiene el objetivo de caracterizar la evolución y la importancia de la Microbiología molecular en el Laboratorio del CPHEM de Villa Clara de junio de 2018 a diciembre de 2023.
MÉTODOS
Se realizó un estudio descriptivo transversal en el Laboratorio de Biología molecular del Centro Provincial de Higiene, Epidemiología y Microbiología (CPHEM) de Villa Clara en el período comprendido de junio 2018 a diciembre 2023.
La población estuvo constituida por el total de muestras procesadas en el Laboratorio de Biología molecular para la detección de patógenos virales y bacterianos de interés clínico-epidemiológico.
Variables investigativas:
Años: 2018, 2029, 2020, 2021, 2022 y 2023
Plataformas tecnológicas de diagnóstico microbiológico: Rotor-Gene-Q (QIAGEN), SLAN, Gene Xpert® MTB/RIF y COBAS 4800®; se utilizaron varios estuches comerciales para los procesos de extracción, amplificación y detección de las dianas moleculares
Provincias: Villa Clara, Cienfuegos, Santi Spíritus, Ciego de Ávila y Camagüey
Diagnósticos moleculares: virus respiratorios no SARS-CoV-2, citomegalovirus y herpes simple, infecciones de trasmisión sexual (ITS), Toxoplasma gondii, panel VIASURE de 18 virus, dengue y panel ITS bacteriana
Diagnóstico de virus específicos: virus de inmunodeficiencia humana (VIH), virus de la hepatitis C (VHC), virus de la hepatitis B (VHB) y virus del papiloma humano (VPH)
Resistencia a la rifampicina
Se crearon bases de datos para analizar las variables clínico-epidemiológicas de interés. Se utilizó la estadística descriptiva para expresar los resultados.
La investigación fue aprobada por el Comité de Ética y el Consejo Científico de la Unidad de Salud Pública.
RESULTADOS
En la Tabla 1 se aprecia la evolución cronológica de las plataformas empleadas en el diagnóstico molecular y en las muestras procesadas. En el año 2018 se analizaron 4 636 muestras por el termociclador Rotor Gene-Q®, sobre todo para el diagnóstico del virus Zika.
Simultáneamente a la apertura del Laboratorio de Biología molecular se implementa el diagnóstico de la tuberculosis (TB), con la plataforma Gene Xpert® MTB/RIF; se realizaron inicialmente 281 estudios.
Posteriormente, en 2020, se procesan 147 837 muestras de exudados nasofaríngeos mediante la RT-PCR en tiempo real debido a la aparición del SARS-CoV-2 en el ámbito epidemiológico cubano. Ante esto el laboratorio realizó su estrategia organizacional para el enfrentamiento a la pandemia a fin de dar respuesta en tiempo real, siempre con el objetivo de disponer del diagnóstico oportuno clave.
La pandemia de la COVID-19 representó un aumento significativo de las determinaciones realizadas en el laboratorio, sobre todo en el año 2021, con la circulación de la variante Delta del virus, de alta transmisibilidad y gravedad, y llegaron a procesarse 409 440 casos.
En un primer momento se contó con la plataforma Rotor Gene-Q® para la amplificación y la detección específica de sus dianas genéticas, en el año 2021, ante la compleja situación, se introdujo la plataforma SLAN, que permitió dinamizar y agilizar el trabajo al aumentar la capacidad resolutiva en medio de un escenario de incremento significativo de casos.
A pesar de la difícil contingencia sanitaria existente en la provincia el desarrollo de la Microbiología molecular no se detuvo porque dio pasos agigantados con la introducción de la tecnología COBAS 4800® y se creó el Laboratorio de carga viral en noviembre de 2021; se procesaron, desde su apertura, 13 669 muestras para el diagnóstico de VIH, de VHB, de VHC y de VPH.
Tabla 1 Evolución cronológica de las plataformas diagnósticas y las muestras procesadas en el Laboratorio de Microbiología molecular del CPHEM de Villa Clara
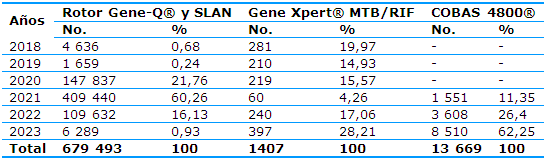
Fuente: Bases de datos y Libros de Registro del Laboratorio de Biología molecular
El número de determinaciones realizadas en Villa Clara tuvo un incremento notable a partir de 2020 y hasta 2021, año en que llegaron a procesarse 338 228 muestras, con la circulación del SARS-CoV-2, porque el centro se estableció como laboratorio territorial para su diagnóstico, al que tributaban, inicialmente, todas las muestras provenientes del resto de las provincias (Tabla 2).
A partir de 2021 ocurre un decrecimiento progresivo producto a la descentralización del diagnóstico del SARS-CoV-2 con la inauguración de Laboratorios de Biología molecular en todas las provincias. Ya en 2023 el número de muestras analizadas procedentes de Villa Clara disminuyó a 14 603 también debido al control epidemiológico de la pandemia.
Tabla 2 Distribución por provincias de las determinaciones diagnósticas realizadas en el Laboratorio de Biología Molecular del CPHEM de Villa Clara
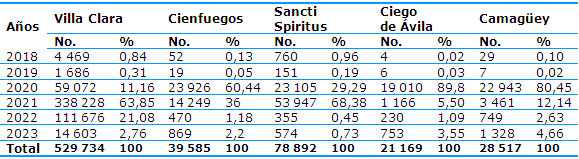
Fuente: Bases de datos y Libros de Registro del Laboratorio
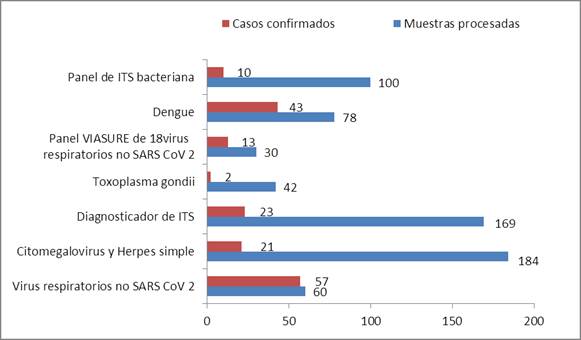
En la Figura 1 se representan los diagnósticos moleculares realizados en el período de estudio mediante el empleo de las plataformas de amplificación Rotor Gene-Q® y SLAN. Se destacan en este caso la elevada positividad que mostró el panel de virus respiratorios implementado en 2019 para el diagnóstico de los virus sincitial respiratorio (RSV) e influenza A y B. Con este estuche comercial se detectaron 22 casos de influenza A, cinco de influenza B y 30 de RSV.
Con el empleo de otro estuche comercial se implementó también el diagnóstico de los patógenos de transmisión sexual: Chlamydia trachomatis (13), Mycoplasma genitalium (3), Neisseria gonorrhoeae (4) y Trichomonas vaginalis, diagnosticándose (3), para un total de 23 positivos, de 169 muestras procesadas.
En 2023 se introduce un panel para la detección genómica de 18 virus respiratorios, lo que permitió identificar la circulación comunitaria de 13 positivos de 30 analizados: 10 de influenza B, uno de influenza A, uno de parainfluenza virus tipo 4 y uno de coronavirus OC 43.
Además, se estudiaron 100 muestras con el panel de ITS bacteriana y se confirmaron tres infecciones por Neisseria gonorrhoeae y siete por Chlamydia trachomatis.
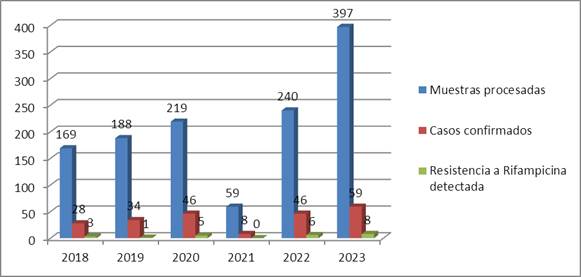
Para la vigilancia de casos activos de tuberculosis en la Región Central la plataforma Gene Xpert® MTB/RIF ha analizado un total de 1 272 muestras desde 2018, se destacó un aumento progresivo en el número de determinaciones realizadas porque ya el año 2023 se destacaron con 397 casos procesados, 59 confirmados y ocho con resistencia a la rifampicina detectada (Figura 2).
 Fuente: Bases de datos y Libros de Registro del Laboratorio
Fuente: Bases de datos y Libros de Registro del LaboratorioFig. 2 Diagnóstico molecular realizado por la plataforma Gene Xpert® MTB/RIF en el Laboratorio de Biología molecular del CPHEM de Villa Clara
En noviembre de 2021 se realizó la puesta en marcha del Laboratorio de carga viral, mediante la implementación de la plataforma diagnóstica COBAS 4800®System. En el período en estudio se procesaron 9 909 muestras de VIH, 1 791 de VHC, 1 270 de VHB y 1 598 de VPHPV (Figura 3).
DISCUSIÓN
El diagnóstico molecular en Villa Clara comenzó en junio de 2018 con la inauguración del Laboratorio de Biología Molecular en el CPHEM con alcance territorial (abarcaba la Región Central del país). En este año las primeras muestras procesadas coincidieron con la epidemia de Zika en Cuba. El diagnóstico se enfocó inicialmente en la vigilancia activa del virus; se analizaron 4 596 muestras de suero y orina. También se analizaron 40 para detectar citomegalovirus y virus del herpes simple, lo que suma un total de 4 636 determinaciones realizadas.
En 2019 continúan el perfeccionamiento y el desarrollo de la Biología molecular en Villa Clara al introducirse nuevos kits diagnósticos para la vigilancia de virus respiratorios (influenza A y B y virus sincitial respiratorio) y de patógenos responsables de infecciones de transmisión sexual (Neisseria gonorrhoeae, Chlamydia trachomatis, Mycoplasmas genitalium y Trichomonas vaginalis). Se aumentó el número de estudios realizados; sin embargo, en ese año decreció el número total de muestras procesadas al disminuir la transmisión comunitaria del virus Zika.
Posteriormente, en 2020, con la aparición del SARS-CoV-2 en el ámbito epidemiológico cubano, es de destacar el aumento notable de exudados nasofaríngeos procesados mediante PCR en tiempo real. Esta contingencia sanitaria constituyó un reto para el colectivo de trabajadores porque destacaron su capacidad y su preparación ante una situación de salud tan compleja.
Ya a mediados de 2021 se hizo necesario ampliar aún más la capacidad resolutiva del Laboratorio por la aparición de la variante Delta, de alta transmisibilidad y gravedad. En este escenario la preparación de los recursos humanos fue vital para el manejo de la pandemia. Diferentes centros de investigación en el país han analizado positivamente también la capacitación del personal de laboratorio como factor principal para lograr mayor eficiencia en el diagnóstico.4,5
En medio de la situación que representó la pandemia, el Laboratorio realizó una estrategia organizacional para dar respuesta en tiempo real las demandas diagnósticas y epidemiológicas; dentro de ella jugó un rol importante el proceso de capacitación de los recursos humanos de la Región Central como personal técnico, Licenciados en Bioanálisis clínico, Residentes y Especialistas, en el diagnóstico molecular por PCR en tiempo real en colaboración con el IPK.
Estuvo dirigido a los temas: toma de muestras, Bioseguridad, extracción de ácido nucleico, preparación de mezcla de PCR, amplificación y análisis e interpretación de los resultados teniendo siempre en cuenta las Normas de buenas prácticas de laboratorio y los requerimientos indispensables de Bioseguridad para el manejo de agentes infecciosos.
Este proceso se mantiene de forma continua como herramienta clave para garantizar la calidad del trabajo.
Primeramente, Villa Clara asumió todo el diagnóstico del SARS-CoV-2 de la Región Central; después, con la creación de Laboratorios de Biología molecular en el resto de las provincias, se descentraliza el estudio de la COVID 196 y disminuye consecuentemente las muestras analizadas, como se observa de forma significativa en 2023.
A partir de inicios de este año, como parte del Proyecto para el fortalecimiento y el desarrollo de la Biología molecular en Cuba, se reciben nuevos medios diagnósticos para la detección de citomegalovirus, de virus herpes simple tipos 1 y 2 de Toxoplasma gondii, de virus del dengue, de Chlamydia trachomatis, de Neisseria gonorrhoeae y de Mycoplasma genitalium y un panel para el estudio de 18 virus respiratorios.
Esto abre paso al continuo desarrollo ascendente y al perfeccionamiento de la Microbiología en la era molecular en la Región Central, con énfasis en el campo de la Virología, porque cada vez son más los estudios que describen la utilidad de los métodos moleculares.
También posee importancia para la búsqueda simultánea de varios patógenos. Tal es el caso del panel virus respiratorios, que cambia la visión de la etiología, mejora la capacidad de detección de agentes potencialmente pandémicos o emergentes y permite su notificación inmediata lo que reduce, de forma significativa, la utilización indiscriminada de antimicrobianos en la práctica clínica diaria.
Estas técnicas permiten un buen sistema de vigilancia en poblaciones claves vulnerables y como apoyo a programas prioritarios como el PAMI (Programa de atención materno infantil) y los Programas de prevención de las ITS-VIH/síndrome de inmunodeficiencia adquirida (SIDA) y hepatitis, de cáncer y de prevención y control de la tuberculosis.
Simultáneamente a la apertura del Laboratorio de Biología molecular, se implementó el diagnóstico de la tuberculosis con la plataforma Gene Xpert® MTB/RIF, lo que consolida la vigilancia molecular activa de casos de tuberculosis en la Región Central con múltiples beneficios porque con esta tecnología se simplifica en un paso la aplicación de la técnica de PCR, además de poseer elevadas sensibilidad y especificidad diagnósticas, hecho que ha sido corroborado internacionalmente.7,8,9,10
Esta técnica molecular, Gene Xpert MTB/RIF, es un ensayo automatizado para el diagnóstico de la TB basado en la detección de ácidos nucleicos específicos de Micobacterium tuberculosis, a partir de muestras clínicas. Esta novedosa herramienta diagnóstica logra simplificar la identificación del ADN micobacteriano, integra y automatiza los tres procesos requeridos para pruebas moleculares basadas en PCR (extracción, amplificación y detección), reduce la complejidad de las pruebas moleculares, el riesgo de contaminación cruzada y las limitaciones de bioseguridad y detecta la presencia del bacilo directamente de una muestra clínica, es que conjuntamente es capaz de identificar al gen rpoβ, el que codifica la resistencia a la rifampicina; todos estos valiosos resultados tan solo en dos horas.11 Esta técnica ha demostrado tener muy buenos y confiables resultados.12,13
En noviembre de 2021 se realiza la puesta en marcha del Laboratorio de carga viral mediante la implementación de la plataforma diagnóstica COBAS 4800® System, lo que representó un gran avance para la provincia por la mejoría de los tiempos de respuesta y el incremento de la capacidad de muestras. En el Laboratorio se procesó la carga viral de VIH a pacientes en seguimiento de su tratamiento antirretroviral, a las gestantes seropositivas y serodiscordantes, a todos los casos nuevos confirmados y a los pacientes con marcada sospecha clínica y con pruebas serológicas negativas. También se asume la confirmación diagnóstica y el seguimiento de los pacientes con antígeno de superficie de hepatitis B positivo y anticuerpo anti C positivo para VHB y VHC, respectivamente. Además se realiza la vigilancia de ambos tipos de hepatitis en los pacientes sometidos a hemodiálisis para detectar brotes que puedan surgir oportunamente a fin de lograr la estratificación de estos pacientes.
Con esta tecnología se introduce, en 2023, el análisis cualitativo por PCR de muestras de exudado endocervical para el diagnóstico del virus de papiloma humano y para detectar sus genotipos de alto riesgo oncogénico, método de laboratorio que ha dado muy buenos resultados según señalan algunos estudios.14,15
CONCLUSIONES
El aumento progresivo de la capacidad resolutiva del Laboratorio de Biología molecular de Villa Clara, junto a la implementación de nuevas plataformas diagnósticas, ha permitido fortalecer la detección de patógenos de interés clínico como el SARS-CoV-2.
Se ha perfeccionado la vigilancia centinela virológica con la capacitación continua del personal, con la creación de una estrategia organizacional para contribuir a la prontitud en la emisión de los resultados y con la imposición de la conducta terapéutica oportuna.