Introducción
El infarto en la arteria de Percheron (IAdP), o síndrome de Percheron, o infarto talámico bilateral, o infarto bitalámico, es una patología infrecuente, que se caracteriza por variaciones anatómicas, donde una arteria tálamo-perforante originada de la arteria cerebral posterior, vasculariza los núcleos talámicos con perfusión variable del mesencéfalo,1 y representa el 0,1 a 0,4 % de los primeros episodios del accidente cerebrovascular isquémico.2
Debido a sus hallazgos neurológicos inespecíficos se le conoce como “camaleón de apoplejía” porque no presenta los signos típicos de un ictus: mutismo, confusión, disfunciones del movimiento, bradicardia, parkinsonismo, convulsiones y otros;3) sin embargo, cuando se establece el cuadro clínico del IAdP se describe una tríada clásica: alteración de la conciencia, deterioro de la memoria y parálisis de la mirada vertical; lo que hace importante el diagnóstico oportuno de esta patología y así evitar complicaciones innecesarias e incluso la muerte.4
Esta investigación tuvo el objetivo de describir un caso clínico de infarto en la arteria de Percheron.
Presentación de caso
Se presenta una mujer de 67 años de edad en compañía de su hijo, quien refiere que al percatarse que su madre no acude al desayuno, y la encuentra acostada, tratan de despertarla, pero reacciona con bostezos; su hijo describe que la ve con mucho sueño y que no responde adecuadamente sus preguntas, en un tiempo de 2 h aparece con estos síntomas, y decide llevarla a emergencia al Hospital IV Augusto Hernández Mendoza - EsSalud - Ica.
En el hospital son interrogados e indican que la paciente examinada tiene antecedentes de hipertensión arterial (HTA), con tratamiento irregular de losartan 50 mg vía oral por la mañana y por la noche, acompañado de clonazepam 2 mg (1/2 tableta) vía oral al acostarse de manera regular; no padece de diabetes mellitus.
La paciente fue intervenida quirúrgicamente hace 17 años de histerectomía, y de colecistectomía 13 años respectivamente. El examen clínico presentó: presión arterial (PA): 140/90 mmhg, frecuencia cardíaca (FC): 62 latidos/min, frecuencia respiratoria (FR): 14 respiraciones/min, temperatura (T°): 36,5 °C, sato2: 95 % con Fio2: 21 %; con piel tibia; murmullo respiratorio: rudo en ambos hemitórax; ruidos cardíacos, rítmicos, de buena intensidad, con tendencia a la bradicardia; ruidos hidroaéreos: presentes, no doloroso a la palpación, no visceromegalias; puño percusión lumbar (-); somnolienta, con escala de Glasgow: 12/15, apertura ocular: 3, respuesta verbal: 4, respuesta motora: 5; pupilas: hiporreactivas sin signos de focalización, por lo que se inició un tratamiento con solución salina al 0,9 % 1000 cc vía endovenosa a xv gotas por min, con protector gástrico también por vía endovenoso.
Se amplían otros estudios con los siguientes paraclínicos: hemograma: leucocitos: 10,75/mm3 (VN: 5-10/mm3); hemoglobina: 9,50 g/dL (VN: 13-16 g/dL); hematocrito: 30,10 % (VN: 36-45 %); plaquetas: 232/mm3 (VN: 150-450/mm3); glucosa: 185,00 mg/dL (VN: 70-110 mg/dL); urea: 24,30 mg/dL (VN: 5-45 mg/dL); creatinina: 0,86 mg/dL (VN: 0,3-1,4 mg/dL); sodio: 139 mmol/L (VN: 135-145 mmol/L); potasio: 4,2 mmol/L (VN: 3,5-5,1 mmol/L); proteína C reactiva: 0,90 mg/dL (VN: 0,0-0,5 mg/dL); grupo sanguíneo: O, factor Rh: positivo; tiempo de coagulación: 7 min (VN: 5-10 min); tiempo de sangría: 2 min (VN: 2-7 min); sedimento urinario: leucocitos: 0-2 por campo, hematíes: 0-1 por campo, bacterias: escasas; prueba antigénica para el coronavirus dos del síndrome respiratorio agudo severo (SARS-CoV-2): no reactiva; la radiografía de tórax informó: que no tiene signos de condensación; la tomografía axial computarizada (TAC) de cabeza sin contraste informó que tomográficamente es adecuada para su edad, con signos de angioesclerosis.
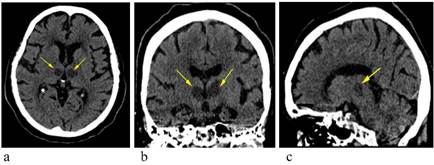
Se vuelve a evaluar, no presenta cambios clínicos significativos; se deduce posible intoxicación por clonazepam 2 mg (tomado probablemente al acostarse), por tanto se indica flumazenilo 0,2 mg EV en bolo rápido, hasta por 04 dosis, pero la paciente no reacciona como se esperaba en el transcurrir de las horas y el compromiso neurológico empeoró, se van agregando otros síntomas como: confusión, desorientación, deja de hablar, la mirada se mantiene fija y va ingresando del coma superficial al coma profundo; por esto se decide repetir la TAC de cabeza sin contraste 36 h después de la primera, donde se informa: hipodensidades en la región paramediana de ambos tálamos, sin compromiso de mesencéfalo: infarto en la arteria de Percheron; en vista del mayor compromiso neurológico, se le asegura la permeabilidad de la vía aérea, se decide intubar a la paciente y colocarla en ventilación mecánica con previa autorización y con la firma de consentimiento informado por parte de los familiares; se realiza la interconsulta a los médicos de la Unidad de Cuidados Intensivos (UCI), quienes indican que pase a UCI, para su manejo. La paciente a los dos días fallece por infección sobreagregada (fig. 1).
Discusión
Los tálamos son conglomerados de sustancia gris, divididos por sustancias blancas hasta en 60 núcleos, ubicados entre los hemisferios cerebrales y el mesencéfalo; comprometidos con la transmisión de los estímulos motores y los sensitivos, así como la regulación de la consciencia, el sueño y el estado de alerta.5
Las primeras descripciones de la vascularización del tálamo fueron realizadas en 1900 por Dejerine y Roussy. Después, el neurólogo francés Gérard Percheron realizó la descripción más completa entre los años 1960 y 1964,6 describió que la arteria cerebral posterior y la arteria comunicante posterior participan en su vascularización (fig. 2).
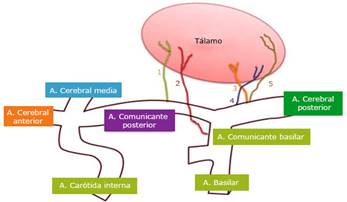
Fig. 2 Vascularización del tálamo: 1) arteria polar; 2) arteria paramediana; 3) arteria del pedículo tálamo geniculado; 4) arteria coroidea posteromedial; 5) arteria coroidea posterolateral. (Modificado del esquema de Lazorthes).7
Esta última, la arteria comunicante posterior con un 60 a 70 % por intermedio de la arteria polar, cuyo territorio comprendía el polo rostral de la región lateral del tálamo, actualmente sustituida por la arteria paramediana.8
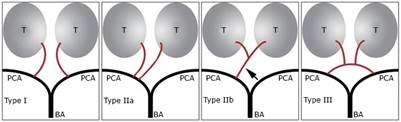
La arteria de Percherón (AdP) (Tipo IIB) es una variante rara de la arteria paramediana, se llama también arteria óptica interna de Duret o arteria tálamo perforante de Foix y Hillerman. Esta arteria se origina de la arteria cerebral posterior; en esta circunstancia Gérard Percheron observó tres variantes de la anatomía vascular del tálamo8 (fig. 3).
Se desconoce la prevalencia de la AdP; por tanto, los IAdP son raros; representan el 0,1 % al 0,4 % de los eventos isquémicos cerebrales; y del 4 % al 18 % de todos los eventos isquémicos talámicos;9 su etiología suele ser embolización desde el corazón, la aorta o las arterias carótidas, o también podría ser por trombosis de placas microateromatosas. Se consideran factores de riesgo como: la hipertensión arterial, la diabetes mellitus, la hipotensión sistémica, la fibrilación auricular, las neoplasias, las coagulopatías, la disección de arteria vertebral, los aneurisma de arteria basilar, entre otros.10
Las manifestaciones clínicas del IAdP son variadas en la fase aguda y pueden comprender alteraciones del estado de conciencia como: confusión, desorientación, hipersomnolencia, mutismo, acinesia y “coma vigil”, que puede progresar a coma profundo; en la fase ya establecida presenta la triada clásica que incluye: parálisis vertical de la mirada (65 %), alteración de la memoria (58 %) y coma (42 %).6
Debido a sus hallazgos neurológicos inespecíficos al inicio y posteriormente ya establecidos, se le conoce como “camaleón de apoplejía.”3
El diagnóstico se realiza por: tomografía axial computarizada la que puede ser normal, en fase inicial o se evidencian hipodensidades en ambos tálamos con o sin compromiso de mesencéfalo, cuando el cuadro clínico se encuentra establecido;11 el gold estándar es la resonancia magnética nuclear donde se muestra la hiperintensidad en las secuencias T2 y FLAIR con o sin afectación de mesencéfalo.
Se describe un hallazgo distintivo, el signo de la “V”, en la secuencia FLAIR y DWI, sobre la superficie pial del mesencéfalo en la fosa interpeduncular.12 Se conocen cuatro patrones de IAdP:
Patrón I: talámico paramediano bilateral con mesencéfalo rostral (43 %).
Patrón II: talámico paramediano bilateral sin mesencéfalo (38 %).
Patrón III: bilateral paramediano y anterior talámico con mesencéfalo (14 %).
Patrón IV: bilateral paramediano y talámico anterior sin mesencéfalo (5 %).
Dentro del diferencial se deben considerar los grupos etiológicos:
Vascular: síndrome del tope de la basilar, trombosis venosa cerebral profunda.
Tóxicas: intoxicación por monóxido de carbono, depósito por metales pesados (plomo, hierro, cobre), radioterapia y quimioterapia.
Metabólicas: alteración del metabolismo del calcio, encefalopatía de Wernicke, encefalopatía hepática, hiperamonemia, hipoglicemia.
Infecciosas: por virus de la influenza, citomegalovirus, toxoplasmosis cerebral.
Desmielinizantes: síndrome de desmielinización osmótica, esclerosis múltiple, encefalomielitis aguda diseminada.
Neoplasias: linfoma cerebral primario, glioma talámico bilateral.13,14
El tratamiento es el estándar para el accidente cerebrovascular isquémico, es decir, agentes trombolíticos intravenosos o intraarteriales (activador del plasminógeno tisular) durante las primeras 4 h; la trombectomía endovascular, después de 4-6 h, pero se usa solo para grandes vasos, y después de transcurrido ese tiempo está indicada la anticoagulación; según las pautas que la American Heart Association (AHA, por sus siglas en inglés) y American Stroke Association (ASA, por sus siglas en inglés).15,16
Se concluye que el IAdP es poco frecuente; se presenta con síntomas inespecíficos en la etapa inicial, que hace pasarlo desapercibido en la evaluación clínica; debe ser considerado como diferencial en todo paciente con alteración del estado de conciencia acompañado de una tomografía axial computarizada normal; por tanto, el diagnóstico y el tratamiento deben ser oportunos para lograr resultados favorables y evitar procedimientos adicionales innecesarios o incluso la muerte.