INTRODUCCIÓN
La hepatitis autoinmune (HAI) es una enfermedad inflamatoria cónica del hígado. Se caracteriza por la pérdida de la tolerancia a los autoanticuerpos, en individuos con predisposición genética y puede ser desencadenada por un factor ambiental.1,2) La etiopatogenia exacta no está bien esclarecida. Se conoce que es una lesión hepática inmunomediada, impulsada por los linfocitos T, aunque los linfocitos B también están involucrados en la inmunopatología.1,3,4
La terapia de primera línea con prednisona o azatioprina es eficaz en el 80-90 % de los pacientes. Los que no controlan la enfermedad por mala respuesta, intolerancia a los medicamentos o fracaso terapéutico, tienen indicación de terapia de segunda línea con 6-mercaptopurina (6-MP), micofenolato mofetilo, ciclosporina o tacrolimus, aunque con resultados menos favorables.2,5
Existe un reducido número de casos de difícil manejo: los verdaderos no respondedores a pesar de cumplir el tratamiento y los que desarrollan un síndrome de superposición por una posible vía de inmunopatogénesis impulsada por células B dominantes, que no es un objetivo eficaz de la terapia estándar. Estos pacientes pueden necesitar un tratamiento alternativo basado en terapias biológicas como el rituximab y el infliximab, pero con datos de eficacia y seguridad aún no concluyentes, por lo que su uso es limitado.2,3,4
Se conoce que la HAI se debe a un fallo en la tolerancia autoinmune periférica, lo que ha condicionado una hipótesis, la cual plantea que, en los casos de evolución tórpida, lo que se requiere es la restauración de la tolerancia inmunológica hepática y no la inmusupresión. La terapia celular como la infusión de células T reguladoras autólogas, específicas de antígeno y que se alojan en el hígado para restaurar la tolerancia inmunológica hepática, se perfila como un posible tratamiento futuro para controlar la etiología en la HAI.3,4,6
La velocidad de progresión de la enfermedad no es similar en todos los pacientes a pesar de tener un tratamiento específico. La rapidez de la respuesta al tratamiento, expresada por la mejoría de los niveles séricos de aminotransferasa en 2 semanas, es el predictor más importante del resultado, aunque la remisión bioquímica a los 6 meses es más utilizada en la práctica clínica.2,7,8,9) Se ha demostrado que determinar la etiología de las enfermedades hepáticas es determinante en su tratamiento y evolución clínica.10,11)
Esta investigación se realiza con el objetivo de describir la respuesta al tratamiento inmunosupresor de pacientes con hepatitis autoinmune.
MÉTODOS
Diseño
Se realizó un estudio descriptivo, longitudinal y ambispectivo. Se revisaron las historias clínicas de todos los pacientes con diagnóstico de hepatitis autoinmune que se habían valorado en la consulta de Hepatología del Centro de Investigaciones Médico Quirúrgicas desde el año 2000 y los que se incorporaron a partir de ese momento.
El periodo de estudio abarcó desde el año 2000 hasta el 2021 (con evaluaciones trimestrales). La media de seguimiento fue de 11,25 años, mínimo de 5 y máximo de 18 años.
Sujetos
Fueron examinados 44 enfermos y se incluyeron 32 individuos que cumplieron con los siguientes criterios:
Tabla 1 - Criterios simplificados de Hennes
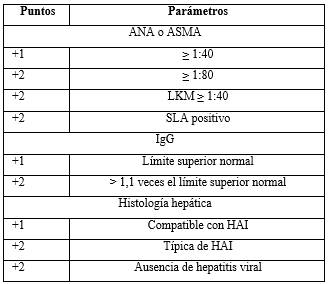
Leyenda: ANA: anticuerpos antinucleares; ASMA: anticuerpo antimúsculo liso; LKM: anticuerpo microsomal anti-hígado/riñón; SLA: anticuerpos hepáticos antisolubles; IgG: inmunoglobulina G; HAI: hepatitis autoinmune.
Criterios de exclusión:
Variables
Las variables incluidas fueron: tipo de hepatitis autoinmune, forma de presentación, respuesta al tratamiento y estado actual de los pacientes con hepatitis autoinmune según la respuesta al tratamiento inmunosupresor.
Los tipos de HAI considerados son:13
HAI I: se caracteriza por presentar ANA o ASMA positivos, aunque hasta el 20 % de los casos de HAI son negativos para los autoanticuerpos ANA, ASMA y anticuerpos anti-microsomales tipo 1 (LKM1). Es la forma más frecuente y afecta tanto a niños como a adultos.
HAI II: se caracteriza por tener LKM1 o antihígado-riñón positivos y anticuerpo anticitosol hepático tipo 1 (LC1). Es más común en edades pediátricas.
La forma de presentación clínica fue definida como:2
Asintomáticos: ausencia de síntomas con aumento ocasional de las enzimas hepáticas.
Sintomáticos: síntomas crónicos inespecíficos, manifestaciones clínicas de enfermedad hepática avanzada o síntomas de otras enfermedades autoinmunes concurrentes.
Enfermedad aguda: menos de 30 días de evolución de los síntomas e incluye los que debutan con hepatitis aguda grave, fallo hepático agudo y exacerbaciones de una hepatopatía crónica subyacente.
El estadio de enfermedad hepática al momento del diagnóstico se determinó según las características clínicas, ecográficas o histológicas. Se agruparon a los pacientes en no cirróticos y cirróticos:
No cirróticos: pacientes con hallazgos histológicos compatibles con hepatitis de interfase, con infiltrado necroinflamatorio a predominio linfoplasmocitario y presencia o no de tractos fibrosos. Se clasificaron según score de Metavir14 en pacientes con actividad histológica importante (A2-A3/FO) y hepatitis crónica (F1-F3).
Cirróticos: pacientes con hallazgos ecográficos característicos como distorsión de la arquitectura hepática, esplenomegalia o várices, o histología compatible que incluye estadio F4 de Metavir.14
La respuesta al tratamiento fue evaluada a los 6 meses. Se tuvo en cuenta la respuesta clínica y bioquímica. Se categorizó en:
Respuesta: cuando los pacientes estaban asintomáticos con remisión bioquímica expresada por normalización de la aspartato aminotransferasa (ASAT), la alanina aminotransferasa (ALAT) y la inmunoglobulina G.
No respuesta: los enfermos que presentaron disminución de las transaminasas, pero sin cumplir criterios de remisión bioquímica y el fracaso o intolerancia al tratamiento.2,7
Se consideró fracaso al tratamiento cuando hubo empeoramiento clínico, bioquímico o histológico a pesar del tratamiento inmunosupresor.
Se definió la evolución clínica (variable de interés para el estudio de la supervivencia) según las manifestaciones clínicas, hallazgos imagenológicos o histológicos en la evaluación actual y se clasificó en:
Progresión: aquellos pacientes que evolucionaron a estadios más avanzados de la enfermedad (enfermos con hepatitis crónica que progresaron a cirrosis hepática o cirróticos que presentaron complicaciones mayores de la cirrosis, trasplante o muerte).
No progresión: se incluyeron los pacientes que se mantuvieron en el mismo estadio de la enfermedad.
El estado actual de los pacientes con hepatitis autoinmune según la respuesta al tratamiento inmunosupresor se expresó como: vivo, fallecido y trasplante hepático.
En este estudio el trasplante hepático se consideró una muerte relacionada con el hígado y se consideró un fallo en el tratamiento.
Procedimientos
Se recogieron los datos generales (sexo y edad). Se determinó tipo de HAI, forma de presentación clínica y el estadio de la enfermedad. En la evaluación actual se definió la evolución clínica según la progresión o no de la enfermedad y su relación con la respuesta al tratamiento a los 6 meses.
Para la recopilación de la información se confeccionó una base de datos con las variables establecidas y se procesaron en el programa SPSS versión 19.0.
Procesamiento
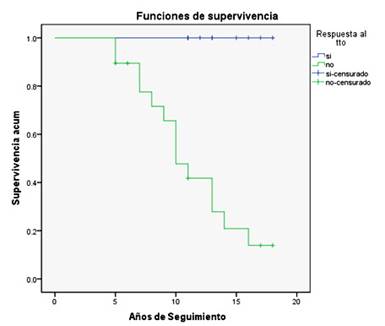
Se utilizaron medidas descriptivas de resumen: media y desviación estándar (DS), para variables cuantitativas y porcentaje para las variables cualitativas. Para estimar la función de supervivencia se utilizó la curva de Kaplan-Meier (programa SPSS versión 19.0) y Log-rank para la comparación de medias. Para el análisis de la supervivencia no se incluyeron los pacientes que fallecieron por causas no relacionadas con la enfermedad hepática.
Aspectos bioéticos
La investigación se realizó según los preceptos establecidos en el Código Internacional de Ética Médica y los que competen a las investigaciones biomédicas en humanos contemplados en la Declaración de Helsinki.15 Fue aprobada por el Comité de Ética del Centro de Investigaciones Médico Quirúrgicas.
RESULTADOS
Predominó el sexo femenino 31 (96,9 %) pacientes. La edad media fue de 34 años (edad mínima de 18 y máxima de 74 años) y el 87, 5 % de los enfermos tenían HAI tipo I.
La forma de presentación clínica predominante fue la sintomática con 27 (84,4 %) enfermos, seguida de 3 pacientes que comenzaron de forma aguda (hepatitis aguda grave) y 2 asintomáticos al inicio de la enfermedad. El 71,9 % de los individuos estudiados estaban cirróticos en el momento del diagnóstico. Presentaron respuesta a los 6 meses de tratamiento 13 (40,6 %) pacientes (tabla 2).
Tabla 2 - Características generales de los pacientes con hepatitis autoinmune al inicio de la enfermedad
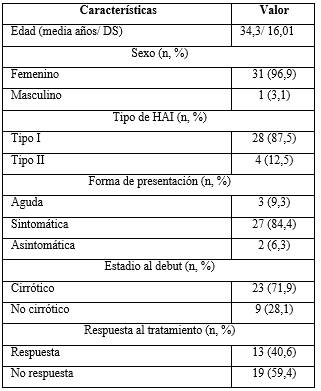
n= 32; Leyenda: DS (desviación estándar); HAI (hepatitis autoinmune).
De los 16 pacientes que se encontraban vivos, 11 (34,4 %) tuvieron respuesta al tratamiento; de 12 que fallecieron, 10 (31,3 %) no tuvieron respuesta y en los 2 con respuesta al tratamiento la muerte no estuvo relacionada con la enfermedad hepática. Los 4 que requirieron trasplante hepático no respondieron al tratamiento (tabla 3).
Tabla 3 - Estado actual de los pacientes con hepatitis autoinmune según la respuesta al tratamiento inmunosupresor
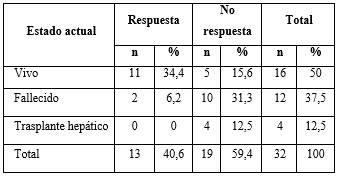
Para el análisis de la supervivencia se excluyeron los 2 pacientes que habían tenido respuesta al tratamiento y fallecieron por causa no relacionada con la enfermedad hepática: una por fractura de cadera y otra por un melanoma de la piel.
Los resultados a diferentes niveles de respuesta al tratamiento inmunosupresor fueron estadísticamente significativos (p< 0,005) como se muestra en la tabla 4.
Tabla 4 - Prueba de igualdad de distribuciones de supervivencia para diferentes niveles de respuesta al tratamiento inmunosupresor

Los enfermos con respuesta al tratamiento presentaron una supervivencia del 100 % a los 5 y 10 años de la primera evaluación, con una media de seguimiento de 11,25 años, representada por la pendiente más plana con una tasa de eventos (mortalidad) baja y mejor pronóstico de supervivencia. En el caso de los pacientes no respondedores solo el 89,5 %, estaban vivos a los 5 años y el 47,5 % a los 10 años, representados por la pendiente más pronunciada, una tasa de mortalidad alta y peor pronóstico de supervivencia (Fig. 1).
DISCUSIÓN
Las características generales de los pacientes (predominio del sexo femenino y de la tercera década de la vida) no difieren de lo reportado en la literatura.1,2,11,16 El sexo femenino es un factor de riesgo para la HAI en todas las poblaciones (3 cuartas partes de los pacientes con HAI son mujeres jóvenes).
La presencia de cirrosis al comienzo de la enfermedad, en la mayoría de los pacientes estudiados, sugiere que el diagnóstico etiológico fue tardío. Es criterio de los autores que, esto se debe a que la enfermedad probablemente pasó desapercibida en los estadios iniciales o quizás por un comportamiento más agresivo en esta región, no bien documentado aún por la no disponibilidad de estudios.
Las revisiones del tema muestran resultados contradictorios, Sharma y otros17 reportan que el 70 % de los pacientes de toda la cohorte tenían cirrosis al momento de la presentación y el 45 % de estos enfermos tenían evidencia clínica de descompensación. Castellanos y otros18 mostraron similares resultados en un estudio retrospectivo cubano, pues la mayoría de los pacientes tenían enfermedad hepática avanzada en el momento del diagnóstico o la desarrollaron durante su seguimiento. Sin embargo, según estudios evaluados por la guía americana,2 solo entre el 28 y 33 % de los adultos tenían cirrosis hepática al inicio de la enfermedad.
La presencia de cirrosis en el momento del diagnóstico es un factor de mal pronóstico, pero en esta investigación los pacientes cirróticos que respondieron al tratamiento, consiguieron detener el curso de la enfermedad con una buena evolución clínica y una excelente supervivencia. Desde hace varios años, se plantea que en la cirrosis la respuesta terapéutica es similar a la de los no cirróticos cuando se usan esteroides.19
Los pacientes que respondieron al tratamiento tuvieron una evolución favorable sin progresión de la enfermedad. Esto se atribuye a que, en la HAI, el control de la inflamación hepática y la necrosis hepatocelular puede inhibir el estímulo fibrogénico y favorecer la degradación del tejido fibrilar constituido por colágeno tipo I y III en la matriz extracelular. Los corticoides reducen la inflamación e inhiben la acción del factor de crecimiento transformante ß, que activa las células estrelladas, con lo que se alcanzan respuestas favorables en la regresión de la fibrosis.20,21) Esto quedó demostrado desde hace años por Valera y otros20 en su estudio de 54 pacientes con HAI tratada con inmunosupresores, en el cual el 41 % disminuyó la fibrosis hepática y no hubo progresión en el 50 %; similar resultado reportan Rodríguez y otros11 en 24 pacientes evaluados, de los cuales 14 (58 %) en estadio de cirrosis hepática compensada con respuesta al tratamiento, no presentaron progresión de la enfermedad.
Entre los pacientes que no respondieron al tratamiento de primera línea se encuentran los diagnosticados en edades tempranas (3 de los 4 con HAI tipo II) que tuvieron mala adherencia al tratamiento inmunosupresor. Algunos de estos pacientes durante su evolución desarrollaron síndrome de solapamiento y aunque se les agregó el ácido ursodesoxicólico, no tuvieron control de la enfermedad y por tanto su evolución clínica fue desfavorable, como se describe en esta entidad.22) Un menor número de pacientes sin respuesta al tratamiento se habían diagnosticado en estadio de cirrosis descompensada y 4 de ellos requirieron trasplante hepático. Solo 2 de las pacientes fueron tributarios de tratamiento de segunda línea, sin mostrar respuesta favorable. La cirrosis y la no respuesta terapéutica son predictores de progresión en la HAI.23
Cuando se comparan los enfermos con respuesta al tratamiento con aquellos que no respondieron, se evidencia el impacto de la terapéutica con un aumento significativo de la sobrevida de los enfermos con control de la etiología. Este beneficio en la supervivencia se demostró en ensayos controlados con placebo desde 1970, que informaron una mortalidad de hasta un 56 % en pacientes no tratados, en comparación con el 14 % de los que recibieron tratamiento.24 En un estudio de cohorte, Biewenga y otros25 concluyeron que los valores de aminotransferasas bajas durante el tratamiento se asocian con una mejor supervivencia a largo plazo en la HAI.
Por el contrario, el fracaso de la respuesta terapéutica evaluado a los 12 meses, constituyó un factor predictor de trasplante y muerte relacionada con el hígado. Otras investigaciones26,27,28 reafirman estos resultados, al demostrar que las recaídas se asociaron con un con mayor índice de mortalidad en los pacientes con HAI.
Este trabajo confirma que la buena respuesta al tratamiento inmunosupresor inicial evita la progresión de la enfermedad, lo que impacta de manera positiva en la supervivencia de los pacientes con hepatitis autoinmune.