Introducción
La fractura abierta de tibia distal (FATD) constituye actualmente un verdadero flagelo, debido al aumento gradual de la velocidad del transporte motorizado y la práctica de deportes o trabajos de alto riesgo, que producen lesiones por traumatismos de alto valor energético. Su evolución clínica está sujeta a múltiples factores y complicaciones, con una propensión hacia la osteoartritis del tobillo con el transcurso del tiempo.1,2,3
La tibia, por su propia localización, está expuesta a lesiones frecuentes y el tercio distal de superficie es subcutánea. Las fracturas abiertas son más frecuentes en ella que en cualquier otro hueso y además la irrigación es más precaria que en otros lugares rodeados de musculatura importante.1,4
Las FATD también llamadas la pesadilla de los ortopédicos, fracturas del pilón o plafón, se caracterizan por su severidad y el complejo y prolongado tratamiento que requieren sus complicaciones, a pesar del avance tecnológico existente. Actualmente constituyen un problema de salud reconocido y representan una de las principales causas de morbilidad y secuelas funcionales en traumatología, lo que significa un incremento de los gastos por concepto de tratamiento, como resultado de una prolongada estadía hospitalaria del enfermo, necesidad de medicamentos y reintervenciones, además del costo social por incapacidad laboral y la tragedia que para el paciente representa.5,6
En el tratamiento de las FATD es importante la fijación o estabilización esquelética, en el resultado final influyen varios factores como; el mecanismo de producción, la región anatómica que se produce la lesión, el tamaño de la herida, las posibles lesiones asociadas y finalmente, el tipo y grado de contaminación de las heridas. Existen experiencia de que el hueso fracturado se define mejor con una buena fijación, además la estabilización quirúrgica rápida permite que el daño asociado a los tejidos blandos no progresen, así como también favorece la cicatrización de la herida.7,8
La fijación externa (FE) de los huesos es una técnica que se ha perfeccionado mucho y ha modernizado tanto los materiales utilizados en su construcción, como la estructura de los equipos, lo que ha posibilitado unir la seguridad, con la sencillez en su uso; por ello cada día gana más adeptos y cosecha más éxitos, pero como cualquier técnica necesita de: respeto, planificación preoperatoria adecuada, selección inteligente de los equipos, accesorios, técnica quirúrgica adecuada y cuidados postoperatorios correctos.2,7,9,10
En la década de los 80 es cuando verdaderamente en Cuba, así como en el mundo, la técnica de FE de los huesos se difunde e invade de forma masiva los diferentes servicios en todas las latitudes, fundamentalmente, a partir de las experiencias de Gavril Ilizarov en Kurgan, de Vidal en Francia y de Roaul Hoffman en Suiza, entre otros precursores no menos importantes. A partir de estas experiencias del método europeo, introducidas por los profesores Ceballos Mesa, Vidal Ramos, Pedrera, Zayas Guillot y Álvarez Cambras, surge el modelo de fijador externo RALCA®, el más difundido en el país.7,10,11
Las principales indicaciones de los FE son: fracturas expuestas (por excelencia), fracturas inestables, desplazadas, de difícil contención por métodos conservadores, lesiones de piel y tejidos blandos, fracturas con pérdida de sustancia ósea, infecciones, lesiones vasculares o nerviosas, retardo en la consolidación, seudoartrosis, artrodesis, etc.5,8
Son múltiples las ventajas ya que: posibilita la fijación rígida de los huesos, en casos en que otras formas de inmovilización son inadecuadas. Ejemplo: fracturas expuestas tipo III; severas, en las que el yeso o los metales de tracción no permitirían el acceso. Provoca una compresión selectiva en el eje axial que anula los movimientos de angulación y cizallamiento, y permite una formación de callo óseo rápida. Posibilita la realización de una vez o por separado, de diferentes funciones: compresión, neutralización o distracción de los fragmentos de las fracturas. Los fijadores externos de múltiples planos, IIizarov o RALCA® pueden realizar a la vez más de 6 funciones.10
El método permite el control directo del estado del miembro y la herida, incisión antero lateral, incluida cicatrización, estado vascular, nervioso, viabilidad de los colgajos cutáneos y compartimentos musculares tensos. Permite tratamientos asociados: cambio de vendajes, injerto de piel, injerto óseo, irrigación de la zona; todos los cuales se pueden practicar sin afectar la irrigación de la zona. La FE permite el tratamiento agresivo y simultáneo del hueso y las partes blandas, y el tratamiento de lesiones vasculares.1,6,8)
Permite la rehabilitación precoz, el movimiento inmediato de las articulaciones proximales y distales, contribuyendo a reducir el edema, mejora la nutrición de las superficies articulares, retarda la fibrosis capsular, reduce la rigidez articular, la atrofia muscular y la osteoporosis. Además la utilización simultánea de diferentes medios físicos utilizados en fisioterapia y rehabilitación (estimulación eléctrica: exitomotriz o analgésica, laserterapia, etc.).1
En el retardo de la consolidación hay descalcificación de los extremos óseos, el canal medular no está cerrado, no hay fibrosis marginal y se encuentran sombras de calcificaciones en las partes blandas en torno al foco de fractura (callo óseo incipiente). Mientras que en la seudoartrosis se observa descalcificación y esclerosis de los extremos óseos que se ven redondeados, uno de ellos adopta la forma convexa y el otro cóncavo, simulando una articulación condílea, hay cierre del canal medular, ausencia de sombra de osificación en torno al foco de fractura, separación de los extremos óseos y a veces engrosamiento de los extremos óseos (hipertrófica) por calcificación del tejido fibroso cicatricial.5
El retardo de consolidación y la seudoartrosis, son dos procesos que difieren en su fisiopatología, pronóstico y tratamiento. No hay una definición universalmente aceptada de seudoartrosis; en general se acepta si la consolidación ósea no se realiza en 6-8 meses. Este proceso puede ser alterado o perturbado por factores mecánicos, biológicos o una combinación de ambos. El tratamiento debe ser individualizado teniendo en cuenta todas las causas presentes en el paciente, para abordar de manera integral el problema. La seudoartrosis de los huesos largos se puede tratar con un procedimiento quirúrgico único en más del 90 % de los pacientes, con buenos o excelentes resultados en la restauración del eje mecánico y longitud del miembro afectado, en 80 % de los casos. Además existen múltiples alternativas para el tratamiento de fracturas complejas de pilón tibial.2,5,8,12
En los casos en los que no estén muy claras las imágenes de radiología simple, es útil la realización de una tomografía axial computarizada (TAC) la cual presenta mayor especificidad con lo que nos ayudará a confirmar el diagnóstico.2
En general, aproximadamente 53 % de las seudoartrosis ocurren en los miembros inferiores y es la tibia la más afectada; además, es el hueso del que más fracturas se reportan, debido a su anatomía, (ausencia de músculos en su cara anterior e interna), presenta factores de riesgo para que se produzcan dichos trastornos de consolidación, y aún más en el tercio distal o pilón tibial.2,13
Según Volkow entre 3-11 % de los casos en donde se realiza apertura del foco fracturario puede desarrollarse seudoartrosis. Esto se explica por la pérdida del hematoma y la vascularización local, esencial en la formación del callo óseo, además de las inserciones musculares y del periostio, tener muchos cuidados con los abordajes quirúrgicos.14,15,16,17,18
A la vez se puede observar necrosis focal, que no solo es ósea, sino también de las estructuras intraóseas, lo cual retrasa el proceso regenerativo pudiendo detenerse en cualquier momento; según varios autores esta es la principal causa de seudoartrosis.2,5,19
En esta investigación los autores realizaron el método de estudio observacional, descriptivo; en ella se describen todos los procederes y se muestran las figuras durante dos años de la evolución del paciente.
El consentimiento informado fue aprobado y firmado por el paciente y la investigación fue aceptada por el Consejo Científico y el Comité de Ética Médica, previo al proceder quirúrgico.
Campo electromagnético pulsátil
Los científicos Yasuda y Fukada, en 1953, demostraron por inducción eléctrica la aparición de hueso de neoformación en la vecindad del cátodo (electrodo negativo), con una corriente de un rango de 1 miliampere (1 mA) durante tres semanas en el fémur de un conejo. También descubrieron un fenómeno conocido como piezoeléctrico. Luego definieron la presencia de potenciales, que aparecen en relación con las solicitudes mecánicas del hueso. En otros estudios observaron que su aparición depende de la estructura colágeno-mineral del hueso, dichos potenciales son independientes de la viabilidad celular y se demuestran desde el hueso como órgano y hasta el hueso como tejido. Posteriormente reforzó la idea con la ley de Wolf y los fenómenos eléctricos en el hueso.1,2,3,4,5,17
Todos los autores están de acuerdo en que, inmediatamente después de la fractura hay una inversión de la polaridad, la diáfisis se hace negativa en relación con la epífisis, microcorrientes alternas y directas tienen un efecto de osteogénesis.1,4
Los investigadores Bassett CAL y Becker RO, en 1962, fueron los primeros en aplicar la estimulación eléctrica al hueso y le llamaron “callo óseo eléctrico”. A partir de entonces −refiere Ceballos Mesa− esta terapéutica ha tenido un acelerado desarrollo en la especialidad de Ortopedia y Traumatología.17
En Cuba, en el año 1985, se comienza la producción de campos magnéticos pulsátiles, llamados ECMP-01 y los de corriente directa bipolar, llamados CDB-402. En 1988 se fabricaron los modelos ECMP-02 y CDB-04; en la segunda mitad de la década de los 90, aumentó la producción y fue objeto de estudio su aplicación y resultados logrados en varias investigaciones en el país.1
Explicar la formación del callo eléctrico no constituye un problema fácil, dado que su mecanismo, aún poco conocido, queda inmerso en los distintos eventos físicos, químicos y biológicos, que participan en las variadas formas de callos y procesos osteogénicos.
Basset CAL y otros, como cita Ceballos Mesa en su publicación, (17 se dedicaron al análisis profundo de las particularidades eléctrica del hueso, afirmaron que los potenciales piezoeléctricos se relacionan con procesos fisiológicos importantes en los tejidos vivos, tales como: síntesis de proteínas, distribución de iones libres, características especiales de las membranas, funciones de las hormonas y enzimas, comunicaciones o enlaces celulares, acción de las mitocondrias y otras. Todo esto pone de relieve la infinidad de posibilidades que existen con respecto a estimulaciones de los procesos fisiológicos y bioquímicos vinculados a la regeneración del tejido óseo por traumatismos.1,6
Marad5 señala que la electricidad y los campos electromagnéticos regulan la síntesis de la matriz extracelular y estimulan la reparación de las fracturas. En sus estudios realizados explican que:
1.Regulan las proteínas, síntesis de colágenos e incrementan la formación en los modelos de la osificación endocondral.
2.Aceleran la formación y reparación celular.
3. Incrementan la unión en las fracturas.
4. Producen resultados equivalentes a los injertos óseos.
Sin embargo, no se han emitido conclusiones definitivas acerca de este proceso terapéutico, cada autor establece sus propios parámetros, las distintas ventajas y desventajas de su equipo.1,5
La estimulación por campo electromagnético pulsátil (CEMP) para formar el callo óseo, se obtiene mediante un generador y dos bobinas de inducción, la corriente generada es de 10 voltios. Las dos bobinas colocadas en forma paralela, tan pronto como la corriente comienza a pasar por ellas, crea un campo magnético que se extiende hacia fuera en ángulo recto a la cara de contacto de la bobina superior, este es captado por la bobina inferior de forma que produce un campo electromagnético constante entre ambas, esto induce en el hueso un campo eléctrico sin tener necesidad de realizar ningún implante en profundidad, sino por medios externos puros, por lo que es menos invasivo. Se verifica colocando un imán entre los dos campos y este comienza a vibrar.1,5,17
El mecanismo de acción responde a distintas tesis:
Estimulación de gruesas moléculas proteicas.
Estimulación de vainas de Schawn.
Alcalinidad local.
Disminución de la tensión de oxígeno.
Los efectos biológicos de los campos electromagnéticos son originados por varios mecanismos de acción, entre los cuales figuran:
Efecto de magnetización (primario): responsable de la orientación de moléculas y átomos bipolares.
Efecto piezoeléctrico (secundario): efecto directo que produce la polarización de la masa de un cuerpo, o la creación de cargas eléctricas en su superficie cuando se somete a fuerza mecánica.
Efecto inverso: deformación de un cuerpo cuando es sometido a un campo eléctrico. Orientación arquitectónica de las trabéculas óseas en zonas dañadas.
Efecto metabólico: responsable de todos los procesos tróficos estimulantes y de la reparación tisular mediante; control del riego sanguíneo de cada tejido, control nervioso de grandes segmentos de circulación y control hormonal de determinadas sustancias que aumentan o disminuyen el riego sanguíneo.
Efecto analgésico: se plantea como hipótesis el aumento de los aminoácidos del grupo mórfico de las endorfinas y las encefalinas.1,17)
Entre las ventajas de la estimulación por CEMP se menciona que tiene una influencia fisiológica que estimula al organismo en el sentido de su propia curación; prácticamente, no tiene contraindicaciones y se puede asociar muy bien con otros métodos terapéuticos. La terapia es indolora, de ejecución sencilla y no es necesario el contacto con el cuerpo. Los CEMP tienen un elevado poder de penetración (de hasta 15 cm) y los efectos obtenidos perduran más allá del final del tratamiento.
La aplicación clínica de los CEMP en el tratamiento de las enfermedades óseas se encuentra ampliamente referida en la bibliografía, que expresa la interacción campo-célula, como una regulación de la osteogénesis, mediante su acción sobre los factores de crecimiento.
La intervención transforma el foco seudoartrósico en un estado fisiopatológico idéntico a la fractura primitiva, empezando de nuevo todo el proceso de consolidación. Para lograr esto, debemos abordar tanto el componente quirúrgico como el biológico. Existe una gama amplia de intervenciones quirúrgicas e implantes las cuales se aplicarán según los requerimientos de cada paciente; y para optimizar el componente biológico se pueden utilizar métodos clásicos como decorticación, injertos óseos, coralina, células madre, preparados ricos en plaquetas, o utilizar las nuevas sustancias.3,5
En la búsqueda bibliográfica realizada se describen otras formas de tratamientos y abordajes quirúrgicos, algunas de estas son:
1. Alternativas para el tratamiento de fracturas complejas de pilón tibial.12
2. Combinación de la fijación externa e interna en el tratamiento de una fractura expuesta del pilón tibial.10
3. Fijación externa en pacientes con fracturas del pilón tibial.11
4. Tratamiento de fracturas por alta energía del pilón tibial con el método de Ilizarov.13
5. Manejo quirúrgico temprano de las fracturas del pilón utilizando el enfoque anterolateral.14
6. Abordajes quirúrgicos anterolaterales versus anteromediales para fracturas de pilón.18
7. Fracturas de extremo distal de tibia tratadas con placas de estabilidad angular. Estudio retrospectivo observacional entre técnica abierta y mínimamente invasiva.15
8. External fixation versus open reduction and internalfixation of pilon fractures.19
9. Tratamiento de las fracturas articulares de la tibia mediante fijación externa.18
10. Clavado intramedular para no uniones de pilones.20
11. Artrodesis con clavo transcalcáneo en artrosis postraumática de tobillo y retropié.21
En la bibliografía revisada no se encontró ningún trabajo de este tipo, con la técnica quirúrgica realizada por nosotros u otra similar; con el injerto de peroné como estabilizador y estimulador de la osteogénesis en la artrodesis del tobillo.
Presentación del caso
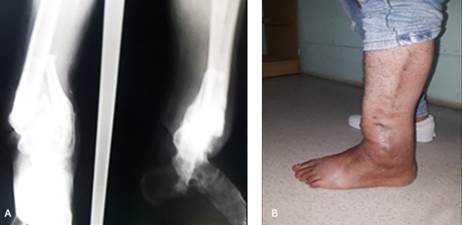
Se trata de un paciente de 38 años, blanco, masculino, con antecedentes de salud que sufrió un accidente de tránsito en moto, fue tratado en el cuerpo de guardia, por una herida con exposición del hueso a nivel del tobillo izquierdo, se realizan los exámenes complementarios de laboratorio e imagenología (Fig. 1-A y B).
Ingresado de urgencia, se lleva al salón, se le realiza cura con abundante suero y sustancias antisépticas, desbridamientos y curetaje óseo; se le diagnostica una fractura abierta, contaminada, conminuta en tercio distal de la tibia, grado III-B, según la clasificación de Gustillo y Anderson. Le colocaron un fijador externo temporal, antibióticos y cura local de los colgajos de piel. Curas en días alternos hasta ver la cicatrización, que fue de forma irregular con gran fibrosis de la epidermis, en la región distal de la pierna (Fig. 1-C y F). Sufrió una infección profunda que fue tratada con antibioticoterapia específica, según cultivo, para un estafilococo áureo positivo sensible a la vancomicina, la evolución fue favorable.
A los ocho meses comienza con dolor, que no cedía a los analgésicos, claudicación a la marcha, lesión crónica de la piel y deformidad en varo por la inestabilidad articular del tobillo debido a la seudoartrosis. Se le realizan radiografías y TAC (Fig. 1-D y E).
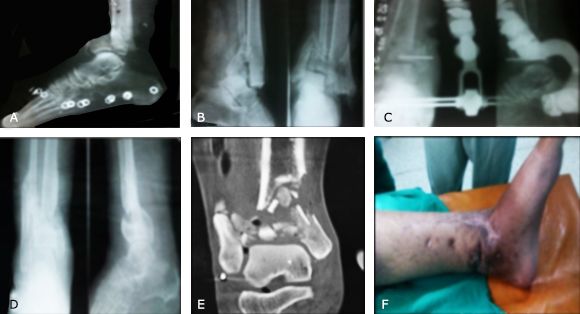
Fig. 1 A. Radiografía inicial de urgencia, con el zapato. B. Control preoperatorio. C. El primer fijador que le colocaron. D. Radiografía con seudoartrosis e imagen antes del tratamiento quirúrgico. E. Corte de la TAC. F. Fotografía antes del tratamiento quirúrgico (ver cicatrices).
Por el mal estado de la piel en las posibles zonas de abordajes quirúrgicos se decidió realizar artrodesis transcalcánea con injerto libre del peroné en la seudoartrosis distal, con la técnica quirúrgica que se describe a continuación:
Previa anestesia, se efectúa desinfección local, se colocan paños de campos y se procede a la extracción del injerto: previamente mesuramos a nivel de la cara externa de la pierna en el tercio medio-superior del peroné, incisión longitudinal, por planos separamos las estructuras musculares, ligamos vasos sanguíneos, desperiostizamos y realizamos la ostectomía de 10 cm. Cierre por planos (Fig. 2-A).
Bajo control radiológico se realiza transfixión con un Staiman grueso, hacer una corrección de la deformidad con el tobillo en 90°, o ligera extensión plantar de 5°. Por la región medioplantar en el calcáneo, una vez visualizado en el lugar ideal y deseado (transcalcáneo a través del astrágalo y de la tibia), se amplía la incisión en el centro del calcañal y colocamos una broca o trefina (de 1,2 cm de diámetro) para perforar circularmente a través de los tres huesos, hasta 6 cm por encima de la articulación del tobillo. Tomamos el injerto del peroné y lo ponemos guiándonos por el Staiman intramedular con un guiador y un martillo gentilmente, hasta lograr el injerto en el lugar deseado. Realizamos radiografía de control (Fig. 2-B, C y D).
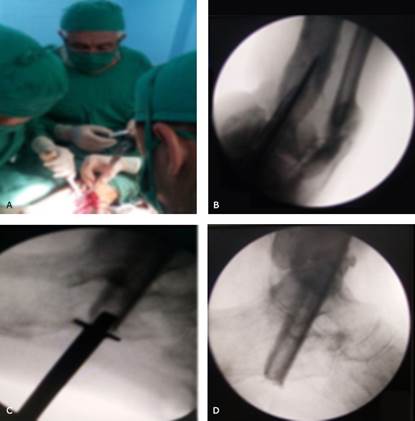
Fig. 2 A. Durante el acto quirúrgico tomando 10 cm el peroné. B. Radiografías de control en el salón, AP y lateral, mostrando el Staiman guía. C. Impactando el injerto de peroné. D. Colocado.
Colocación del fijador externo: con transfixor eléctrico y de baja velocidad o revoluciones, para no producir efectos térmicos en la piel ni en el hueso, se colocan los Staiman del modelo RALCA®, a nivel de la tibia y el calcáneo con barras en T, para luego realizar compresión a nivel de la articulación (Fig. 3-A).
Se cura al paciente y se le cambia el vendaje al día siguiente (Fig. 3-B).
Se muestra orificio de la entrada del injerto de peroné transcalcáneo (Fig. 3-C).
Después de la cura se le explica la metodología de aplicación del CEMP sobre la zona operada (Fig. 3-D).
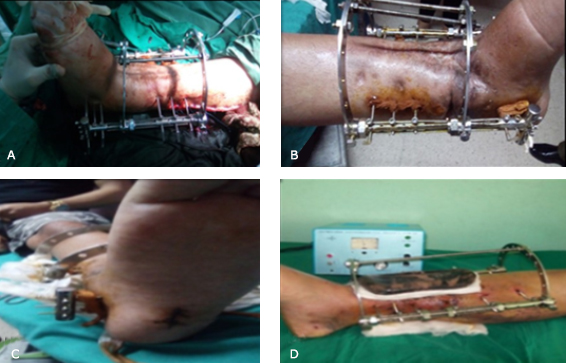
Fig. 3 A. Recién colocado el fijador externo RALCA® en el salón de operaciones. B. La cura al día siguiente de la operación. C. Orificio de entrada del injerto del peroné transcalcáneo. D. El CEMP colocado.
Comienza el apoyo a las 3 semanas de operado (Fig. 4-A). A las 16 semanas de operado se le retira el fijador externo y se observa el callo óseo favorable, o sea, hay consolidación y artrodesis de la articulación (Fig. 4-B-C).
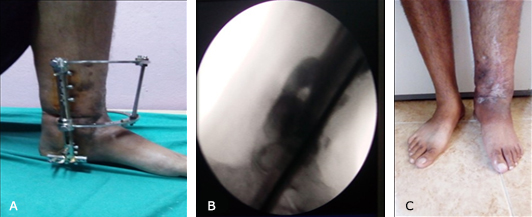
Fig. 4 A. Apoyando a las 3 semanas con el fijador colocado. B y C. Radiografía de control y fotografía de pie, a las 16 semanas de operado con callo óseo favorable. Artrodesis del calcáneo-astrágalo-tibia.
Se le realizaron radiografías de control y fotografía a los dos años de su seguimiento en las que se observa el excelente resultado final (Fig. 5-A-B).
Conclusiones
Se cumplió el objetivo del trabajo, al lograr la formación del callo óseo en un tiempo menor que el promedio, en esta zona anatómica con precaria irrigación sanguínea y severas lesiones de piel.
El uso combinado de la fijación externa, los injertos óseos, la estimulación eléctrica con campos magnéticos y la fisioterapia con apoyo precoz, es el método ideal para el tratamiento de seudoartrosis de la tibia en su tercio distal.
A pesar de los múltiples estudios y avances en este campo en los últimos tiempos es necesaria aún mayor investigación para determinar cuál es el mejor método que se pueda aplicar para un determinado tipo de seudoartrosis.
No se encontró en la bibliografía revisada otra técnica quirúrgica similar.