Introducción
La nueva especie de coronavirus, denominada COVID-19, ha generado escenarios de emergencia sanitaria en muchos países de todos los continentes. Las preocupaciones de las autoridades salubristas y otros decisores se justifican por la velocidad rápida de su propagación, las tasas de mortalidad registradas y la implementación de intervenciones de alta complejidad. La estrategia epidemiológica incluye, además de la vigilancia poblacional, la identificación de casos positivos con la prueba de reacción en cadena de polimerasa con transcriptasa inversa (PCR-RT, por sus siglas en inglés).1
Potencialmente, la carga viral puede ser un marcador útil para el pronóstico de la enfermedad. Al respecto, los científicos advierten que el genoma viral está presente en secreciones respiratorias, deposiciones, sangre, saliva y orina, y se puede excretar por el aparato respiratorio por 2 semanas; también hay presencia viral en pacientes asintomáticos.2) Mediante el hisopado nasofaríngeo se ha informado el desprendimiento prolongado de ácido desoxirribonucleico viral hasta 37 días en adultos y más de un mes (en heces) después de la infección en niños.3,4
Rojas et al5 resaltan las valoraciones hechas por investigadores chinos en una serie de 99 pacientes. Para ellos los resultados de la PCR-RT fueron concluyentes para definir el diagnóstico de neumonía por la COVID-19, así como el registro de la magnitud de aquellos enfermos con necesidades de oxigenoterapia, ventilación artificial mecánica y la terapia de reemplazo renal. Señalan, además, que en los pacientes con infección activa, la prueba es de alto valor evolutivo y sugieren repetir las muestras cada 2 o 4 días hasta obtener 2 resultados negativos. La opinión de especialistas brasileños coincide con lo anterior, a pesar de reconocer resultados falsos-negativos debido a material celular insuficiente o técnicas inadecuadas de extracción y detección.6
En el Hospital Militar Dr. Joaquín Castillo Duany de Santiago de Cuba fueron admitidos los pacientes con COVID-19, pertenecientes al territorio del oriente sur de Cuba. La PCR-RT evolutiva fue un valioso padrón de referencia para la toma de decisiones médicas durante la estadía hospitalaria; sin embargo, las sucesivas observaciones permitieron identificar limitaciones para su valor evolutivo como el tiempo para el procesamiento de las muestras e información del resultado ante una demanda creciente, la positividad mantenida superior a los días promedios de hospitalización, el registro de las frecuencias por grupos poblacionales (adultos y niños), entre otros. Por estas razones, se realizó la presente investigación con el objetivo de caracterizar la variabilidad de los resultados de la PCR evolutiva en pacientes con la COVID-19.
Métodos
Se efectuó un estudio observacional, descriptivo longitudinal y prospectivo de 68 pacientes con la COVID-19 atendidos en el Hospital Militar Dr. Joaquín Castillo Duany de Santiago de Cuba, entre el 12 de marzo y el 30 de abril de 2020, para caracterizar la variabilidad de los resultados de la PCR evolutiva. El universo incluyó niños y adultos de ambos sexos.
La colecta de la muestra virológica se realizó mediante el hisopado faríngeo y nasal; se procedió al análisis de la PCR-RT en el centro de referencia territorial designado por las autoridades del Ministerio de Salud Pública. Los resultados positivos permitieron confirmar la COVID-19 en estos pacientes.
Se incluyeron variables sociodemográficas (edad, sexo, grupo poblacional), epidemiológicas (condición del contacto) y de gestión (tiempo para el informe de resultados), entre otras. Las fuentes de información incluyeron la historia clínica, la encuesta epidemiológica y una base de datos digitalizada y actualizada, en tiempo real, por el grupo asesor del consejo de dirección en conjunto con especialistas informáticos, donde se registraron los datos principales de cada paciente desde el día del ingreso hospitalario.
La información se recogió en formato digitalizada y se procesó en Microsoft Office Excel; asimismo, se realizó un análisis estadístico descriptivo, mediante medidas de tendencia central y distribución de frecuencias.
Resultados
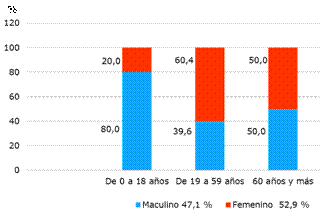
En la serie (Fig.1.), hasta la fecha de cierre, predominó el sexo femenino (52,9 %); sin embargo, 80,0 % de los menores de 18 años fueron del sexo masculino y entre los mayores de 60 años se obtuvo similar frecuencia de observación (50,0 %).
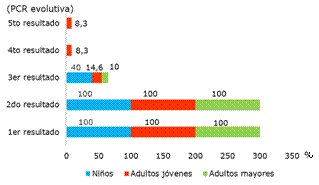
Resultó notable que a todos los pacientes se les realizaron 2 pruebas de PCR, pero, evolutivamente, 40 % de los niños y 10 % de los adultos mayores requirieron de un tercer resultado; mientras que en 8,3 % de los adultos jóvenes precisaron de 5 pruebas (Fig.2).
Durante el período de observación de los pacientes afectados (Fig.3.) en el primer tercio de tiempo se promedió 1 día para la comunicación del resultado; en tanto, en el segundo y tercero hubo una tendencia al incremento de la unidad de análisis para el informe de la PCR-RT desde el laboratorio de referencia, con un valor medio de 1,5 días (DE± 0,6) y 3,2 días (DE± 1,6), respectivamente.

Fig. 3 Tiempo promedio para la comunicación del resultado de la PCR-RT durante los días de observación clínica y epidemiológica.
A los 15 días de tratamiento (Fig.4.) se registraron casos positivos activos en todos los grupos poblacionales y 40 % de los niños mantuvieron positividad de la PCR-RT. Posteriormene, este suceso se mantuvo entre los adultos jóvenes y 6,3 % registró una carga viral activa con más de 20 días de tratamiento.
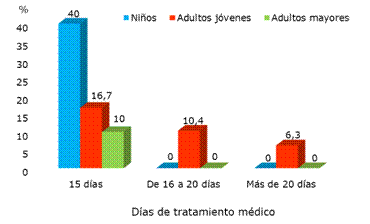
Fig. 4 Positividad de la PCR evolutiva por grupos poblacionales en diferentes etapas del tratamiento
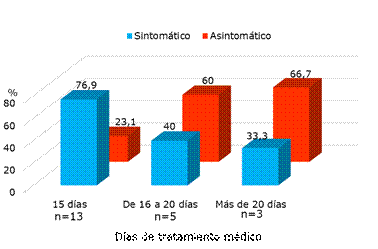
Entre los pacientes con resultados positivos de la PCR-RT a los 15 días del tratamiento, 76,9 % fueron sintomáticos. Nótese que 60,0 % de los que permanecieron con carga viral entre 16-20 días de terapia medicamentosa resultaron ser asintomáticos al igual que 66,7 % de aquellos con más 20 días de medicación (Fig.5).
Discusión
El coronavirus-2 (SARS-CoV-2) conserva gran homología con otros virus de la familia de los betacoronavirus, y los individuos infectados presentan manifestaciones clínicas similares a las identificadas en otros brotes epidémicos descritos en el pasado (SARS en el 2003 y MERS en el 2012), por ello, su diagnóstico se centra en la detección del material genético viral en muestras respiratorias de personas sospechas.7
La positividad registrada en el presente estudio es un indicativo de que el virus afecta sin distinción a niños y adultos de ambos sexos, con una mediana de edad de 30 años para los varones (DE±21) y de 37 para las féminas (DE±19,7). La escasa información sobre resultados de sensibilidad y especificidad en la población infantil (60,5 % varones) pudiera estar relacionada con lo infrecuente de la COVID-19 en estas edades.8
En España, en una serie retrospectiva en pacientes confirmados mediante PCR, la mayoría fueron varones (56,9 %) con más de 65 años de edad;9en tanto, Guzmán et al10 hallaron predominio de las femeninas (52,0 %), con una mediana de edad de 44 años, un suceso diferente a las exposiciones descritas en muchos artículos científicos.
Los autores de la presente investigación consideraron suficiente una PCR-RT evolutiva durante los inicios de la respuesta a la COVID-19; sin embargo, sucesivas ediciones recibidas del protocolo nacional de actuación (versión 1.3) y las experiencias acumuladas condujeron a realizar más de una prueba evolutiva, de manera que por cada persona en cada grupo poblacional se registraron 2,4 PCR-RT en niños, seguidos de adultos jóvenes (2,3) y adultos mayores (2,1). Al igual que el resto, la segunda prueba de ácido nucleico patógeno respiratorio se combinó con las observaciones clínicas y la información epidemiológica de cada paciente, pues, en concordancia con la opinión de expertos, un primer resultado negativo no excluye la infección por el SARS-CoV-2 y descarta la infección por otros agentes causantes de neumonía atípica.11
Por otra parte, a pesar de la probada utilidad de la PCR-RT para confirmar la infección viral en una muestra humana, surgieron algunas limitaciones en el proceso. En el segundo y tercer tercios del período de observación clínica y epidemiológica se extendió el tiempo para la comunicación del resultado superior a las 24 horas. Es probable que el suceso haya sido consecuencia de otros eventos simultáneos: un aumento del número de casos sospechosos, por consiguiente, un mayor volumen de muestras a procesar y saturación de las capacidades instaladas en el laboratorio de referencia. Al respecto, otros autores advierten sobre similar situación en la mayoría de los países, ya que los test solo se pueden procesar en laboratorios certificados y los resultados llegan con retrasos, lo cual es perjudicial para los pacientes y para los sistemas de salud y de vigilancia.12
Si bien el tratamiento de los afectados incluyó una combinación de kaletra, cloroquina e interferón alfa 2b recombinante, la PCR continuó detectando fragmentos del virus en pacientes de todas las edades. Proporcionalmente, en los niños (p=0,4) fue mayor la positividad a los 15 días con la triple terapia anti COVID-19, aunque en conjunto con los adultos mayores (p=0,1) se registraron resultados negativos antes del día 20 del esquema general de tratamiento.
Esta persistencia pudiera explicarse, a juicio de los autores del presente estudio, por la carga viral y la magnitud con que afecta al huésped o susceptible. En su serie, Osejo13 destaca los resultados de especialistas chinos, quienes establecen una relación directamente proporcional entre las variables, cantidad de partículas del virus recibida y gravedad de la afectación, que son determinantes de la duración del episodio infeccioso con influencia directa en la estancia hospitalaria de los enfermos.
En correspondencia con lo expuesto, la condición del contacto fue una de las variables que por sí misma expresó la ley dialéctica de la unidad y lucha de contrarios. Del universo en estudio, más de una decena de pacientes (19,1 %) siguieron dando positivo a los 15 días de tratamiento, y la mayoría que mantuvieron positividad, superados los 20 días, fueron los asintomáticos. Por su parte, Tan et al14 en su serie 67 pacientes confirmados, aseguraron que la eliminación viral media fue de 20 días y tuvieron varias muestras positivas.
Según se plantea hay personas infectadas que no transmiten la enfermedad, mientras que otras pueden llegar a transmitirla a muchas más.15 Lo cierto es que estimaciones fiables sitúan el valor R0 de la COVID-19 superior a 1 (1,4-2,5), indicativo de gran capacidad de transmisión y extensión de la enfermedad infecciosa. Para Madrigal et al,16 el nivel de evidencias es suficiente para repetir la prueba de la PCR-RT, pero con precaución, pues se han descrito varios informes de falsos negativos atribuidos a razones multifactoriales.
Finalmente se concluye que, independientemente de la edad y la duración del tratamiento médico, algunos individuos se mantienen con carga viral detectable. Por la variabilidad descrita y por la incertidumbre de muchas características epidemiológicas del SARS-CoV-2, no es aconsejable el egreso de pacientes sin que la PCR-RT resulte negativa, sobre todo para los casos asintomáticos, en quienes el seguimiento evolutivo ha sido menos favorable.