INTRODUCCIÓN
Las enfermedades periodontales han afectado a la humanidad desde tiempos remotos.1) La enfermedad periodontal inflamatoria crónica constituye uno de los padecimientos de mayor frecuencia en la cavidad bucal, comprende un grupo de entidades caracterizadas por una respuesta inflamatoria de los tejidos, que incluyen a la encía, ligamento periodontal, cemento radicular y hueso alveolar.2,3
Suelen presentarse en diferentes formas, y esto obedece a las posibilidades de ruptura del equilibrio hospedero-microorganismo que se manifiesta sobre todo, en los tejidos periodontales, los cuales experimentan cambios progresivos y constantes que pueden afectar el mantenimiento de la salud.3
La periodontitis crónica es una enfermedad de sitios, la destrucción periodontal no ocurre al mismo tiempo en todas las partes de la boca, sino en algunos dientes a la vez o incluso, solo en algunas de sus caras en un momento determinado; 3,4) puede afectar a toda la dentición, pero en general, los molares e incisivos son los más susceptibles, mientras que los caninos superiores e inferiores y los primeros premolares inferiores son más resistentes a la enfermedad.4,5) Clínicamente, se caracteriza por la presencia de sangramiento al sondeo, bolsas periodontales, movilidad dentaria, pérdida de inserción clínica y en la radiografía se observa la destrucción del hueso alveolar.6
Los defectos óseos verticales o angulares son corroborados mediante las radiografías periapicales; estos tienen dirección oblicua y dejan en el hueso un surco socavado a lo largo de la raíz; la base del defecto es apical al hueso circundante.7) Los defectos angulares se catalogan sobre la base del número de paredes óseas. Dentro de las bolsas infraóseas, las de tres, y dos paredes y media ofrecen mejor protección y mayores probabilidades de éxito. El tratamiento de los defectos óseos verticales subyacentes a bolsas infraóseas consiste en obtener regeneración del hueso perdido.8
La búsqueda de tratamientos eficaces y perdurables sostenidos en procesos naturales y poco invasivos ha sido una premisa a lo largo de la historia. En correspondencia con lo planteado, el surgimiento de la medicina regenerativa ha ocupado el interés de múltiples especialistas de las ciencias médicas; los nuevos conocimientos sobre la biología de estos procesos, su factibilidad y aceptación desde su concepción autóloga han propiciado el diseño de estrategias terapéuticas sostenidas en la integración multidisciplinaria que permiten modificar con éxito, tratamientos convencionales.
El uso de los concentrados plaquetarios, como sustratos básicos para la obtención de biomateriales inductores de procesos biológicos que conducen a la regeneración, ha irrumpido en varias especialidades y la periodoncia ha sido pionera en su aplicación.9
En el año 2001, Joseph Choukroun y cols., citados por Martínez-Hernández y cols., 10) dieron inicio a una segunda generación de los concentrados plaquetarios; la propuesta fue acogida con gran aceptación, por primera vez se obtenía un biomaterial sólido autólogo con múltiples ventajas, entre las que se destacan la atoxicidad, la ausencia de inmunorreactividad y su fácil obtención. La fibrina, rica en plaquetas y leucocitos (FRP-L), ha permitido desde entonces el logro de una cicatrización más rápida y segura de los tejidos óseos y blandos.11
La composición básica que posee de forma exitosa la FRP-L, se estructura en un ordenamiento celular contenido en una matriz de fibrina enriquecida en plaquetas, leucocitos, células madre y proteínas de bajo peso molecular, esenciales para el logro efectivo de una adecuada comunicación intercelular, las citocinas. Cada uno de los componentes del concentrado tiene funciones específicas que abarcan desde la liberación activa de factores de crecimiento hasta el control de funciones fisiológicas vitales, como los procesos de diferenciación y maduración celular, respuesta inmune local y sistémica, hematopoyesis y participación activa en la reparación tisular y ósea.
Varios estudios han demostrado, que estos procesos de liberación de factores de crecimiento se mantienen vitales hasta 28 días posteriores al implante del biomaterial, ponderándose el efecto regenerador.12
La aplicación de la FRP-L autóloga en periodoncia, ofrece grandes ventajas sobre los tratamientos convencionales, al ser obtenida a partir de la propia sangre del paciente, de una forma sencilla, rápida y económicamente factible, con diversas propiedades biológicas inductoras de la regeneración ósea y tisular.8
Múltiples estudios han demostrado desde la evidencia, que la aplicación de la FRP-L autóloga incrementa la cantidad de factores de crecimiento, conduciendo a una rápida cicatrización ósea con reducción del tiempo de curación y consecuentemente, una mayor satisfacción del paciente.13,14) Sin embargo, en Villa Clara, que cuenta con la Unidad de Investigaciones Biomédicas (UNIB) donde se procesan diferentes agregados plaquetarios, se desconoce cuál será la efectividad de la membrana de fibrina rica en plaquetas en el tratamiento de las periodontitis crónica; en el presente estudio se persigue el objetivo de evaluar la efectividad de una membrana de fibrina rica en plaquetas y leucocitos asociado al tratamiento quirúrgico convencional en los defectos óseos angulares de la periodontitis crónica.
MÉTODOS
Se realizó una investigación cuasi-experimental. La población de estudio estuvo constituida por 88 pacientes que acudieron a la consulta de Periodoncia de la Facultad de Estomatología de la Universidad de Ciencias Médicas de Villa Clara, con diagnóstico de periodontitis crónica, tributarios a tratamiento quirúrgico, en el período comprendido entre marzo de 2016 a septiembre de 2018. Se utilizó un muestreo no probabilístico intencional por criterios; fueron seleccionados 21 pacientes, que cumplían con los criterios de inclusión establecidos para este estudio. La inclusión definitiva de los sitios en el estudio se decidió en el momento de la realización del colgajo.
Criterios de inclusión
Pacientes entre 21-64 años de edad.
Pacientes con diagnóstico de periodontitis crónica con defectos óseos angulares mesio-distal.
Sitios con bolsas de 4 mm y más, ubicados en dos sextantes diferentes pero análogos.
No haber recibido tratamiento periodontal en los últimos 6 meses.
Consentimiento informado y libre aceptación de la participación en el estudio
Criterios de exclusión de pacientes:
Fumadores y/o alcohólicos.
Trasplantados y/o inmunodeprimidos.
No tributarios a tratamiento quirúrgico por comorbilidades asociadas descompensadas de alto riesgo, con hemodinamia inestable.
Con trastornos cuantitativos o cualitativos plaquetarios, trastornos de la coagulación o tratados con anticoagulantes sistémicos.
Con trastornos psiquiátricos severos.
Mujeres embarazadas o en período de lactancia materna.
Con diagnóstico de patología oncológica o sometidos a tratamiento con citostáticos
Criterios de salida
Decisión de salida del estudio por voluntad del paciente.
Incumplimiento en el cronograma de control.
Fallecimiento del paciente durante el estudio
La muestra quedó constituida por 21 pacientes que cumplieron los criterios establecidos para el estudio. En ellos se seleccionaron 265 sitios: 132 recibieron tratamiento quirúrgico convencional más aplicación de una membrana de fibrina rica en plaquetas y leucocitos como biomaterial autólogo (grupo estudio) y 133 recibieron, exclusivamente, el tratamiento quirúrgico convencional (grupo control).
Los pacientes incluidos en el estudio siguieron la secuencia de tratamiento normada para los servicios de salud; se destaca, el ingreso en el segundo nivel de atención, con la confección de la historia clínica realizada por los investigadores, cumpliendo los requerimientos en el orden clínico e imagenológico.
En la presente investigación se utilizaron tres unidades de análisis.
Fueron consideradas las variables clínicas:
Presencia de sangramiento al sondeo, profundidad de las bolsas periodontales y movilidad dentaria.
-Para determinar la pérdida de inserción clínica se tuvieron en cuenta los criterios establecidos por la Academia Americana de Periodontología en cada sitio a tratar: antes del tratamiento, al mes, 3, 6 y 12 meses después de haber recibido el mismo.
-Para la evaluación radiográfica se estandarizó el estudio. Se realizó una evaluación radiográfica del nivel óseo antes del tratamiento a los 3, 6 y 12 meses después de recibir el mismo
Antes del tratamiento, se midió la distancia del ápice al fondo del defecto que se denominó distancia al fondo del defecto inicial (DAFDi). Una vez realizado el tratamiento en ambos grupos, se midió la ganancia ósea (GOx) a los tres, seis y 12 meses, calculada a través de la siguiente fórmula: GOx= DAFDx-DAFDi
Donde:
GOx: Ganancia ósea a los x meses después del tratamiento.
DAFDx: Distancia del ápice al fondo del defecto a los x meses después del tratamiento.
DAFDi: Distancia del ápice al fondo del defecto tomado como referencia inicial.
i: Inicial
x: Evolución a los 3, 6 y 12 meses
La membrana de fibrina rica en plaquetas fue elaborada en la UNIB, según protocolo establecido en dicha institución.
Una vez obtenida la membrana, los investigadores realizaron todos los pasos de un colgajo de espesor total que permitió acceder al defecto óseo y adaptar la membrana en el mismo. Se indicó antibioticoterapia con amoxicilina (500 mg cada ocho horas); en aquellos pacientes con alergia a los betalactámicos, se indicó metronidazol (250 mg cada ocho horas por vía oral, durante 10 días).
Procesamiento estadístico
Los datos recolectados en este estudio fueron registrados en un libro de Microsoft Excel 2010 y posteriormente, fueron procesados mediante el software estadístico SPSS versión 15.0.
Para determinar la efectividad de los sitios tratados, se evaluaron parámetros clínicos (bolsas periodontales y sangramiento al sondeo) y la ganancia ósea. Se consideró efectivo, cuando radiográficamente existió una ganancia ósea de dos mm o más, y no se detectaron clínicamente bolsas periodontales y sangramiento al sondeo. Resultó medianamente efectivo, cuando radiográficamente existió una ganancia ósea de 1-1,9 mm y no se detectaron parámetros clínicos o existió uno de ellos. Resultó no efectivo, cuando radiográficamente existió una ganancia ósea de 0-0,9 mm y persistieron los parámetros clínicos.
La efectividad general se determinó a partir de la sumatoria de la efectividad de los sitios efectivos y medianamente efectivos, siendo efectivo si el porciento de estos era mayor o igual a 85 %.
RESULTADOS
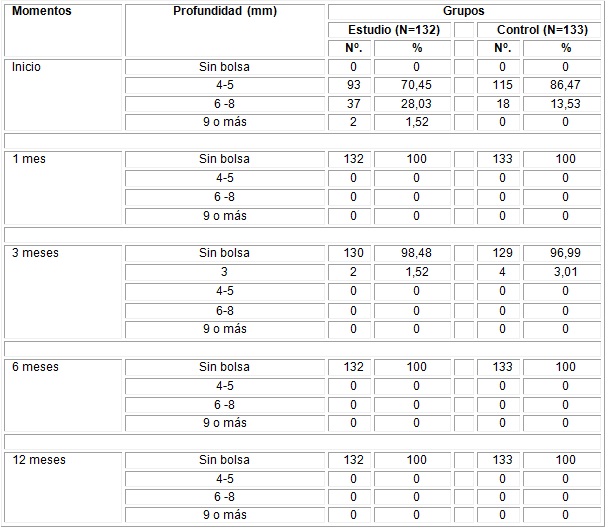
La profundidad al sondeo, en los diferentes momentos en los grupos estudiados aparece representada en la siguiente tabla; se aprecia que dicha variable, al inicio del estudio estaba presente en todos los sitios que se incluyeron en la investigación; prevalecen las bolsas de 4 a 5 mm, tanto en el grupo estudio como control; sin embargo, en ambos grupos, a los 3 meses, solo existieron bolsas periodontales de 3 mm, con predominio en el grupo control con un 3,01 %; menor en el grupo estudio con un 1,52 %. Cabe destacar, la ausencia de bolsas periodontales luego de la aplicación del biomaterial. Esto sucede en ambos grupos. (Tabla 1)
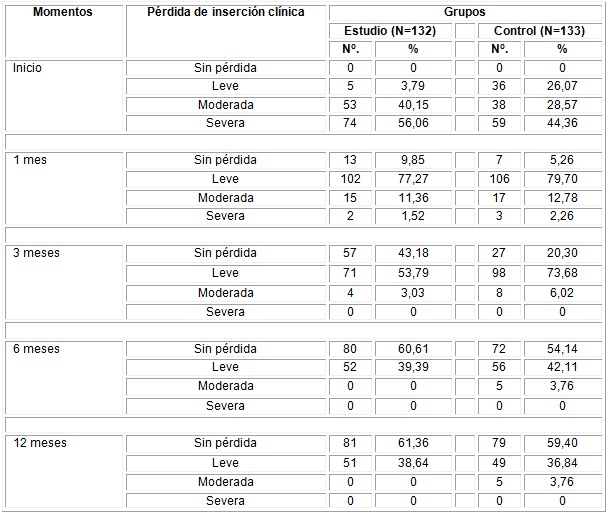
En la siguiente tabla aparece reflejada la pérdida de inserción clínica en los distintos momentos del estudio; se puede apreciar la pérdida de inserción clínica antes del tratamiento en el grupo estudio, con 74 sitios con pérdida de inserción clínica severa para el 56,06 % y en el grupo control con 59 sitios (44,36 %). Hubo un incremento de los sitios sin pérdida de inserción clínica, en posteriores momentos en ambos grupos estudiados, aunque superior en el grupo estudio, para un 61,36 %. (Tabla 2)
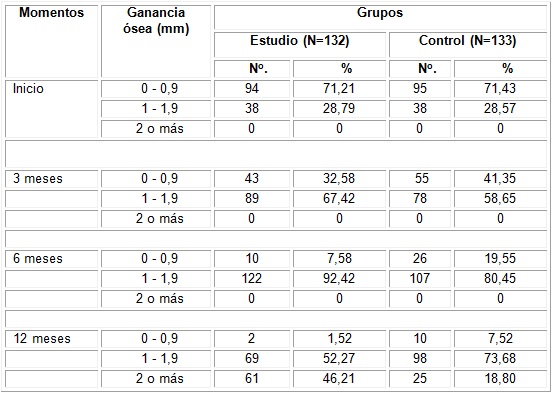
En cuanto a la distribución de los grupos estudiados, de acuerdo a la ganancia ósea evaluados en los distintos momentos, se corrobora que los sitios pertenecientes al grupo estudio, donde se aplicó la membrana de fibrina rica en plaquetas, mostraron mejores resultados que aquellos que solamente recibieron tratamiento convencional (grupo control). A los 3 meses, en el grupo estudio, 89 sitios (67,42 %) tuvieron una ganancia ósea entre 1-1,9 mm, mientras, en el grupo control, 78 sitios (58,65 %) se encontraban en esta categoría; similares resultados se observaron a los 6 meses al alcanzarse un 92,42 % (grupo estudio) y 80,45 % (grupo control). A los 12 meses de recibir el tratamiento, la ganancia ósea de 2 mm o más en el grupo estudio superó al grupo control: 61 sitios (46,21 %), 25 sitios (18,80 %), respectivamente. Es válido aclarar, que la información recogida en el momento inicial se tomó como valor referencial del nivel óseo. (Tabla 3)
Según grupos estudiados, se aprecia a los 12 meses de tratamiento, la siguiente efectividad en los sitios: en el grupo estudio fue efectiva, para un 46,21 % (61 sitios) y notablemente inferior en el grupo control, con el 18,80 % (25 sitios); se demuestra una relación muy significativa para x2=25,44 p=0,000. (Tabla 4)
Tabla 4 Distribución de los sitios según efectividad del tratamiento y grupos estudiados
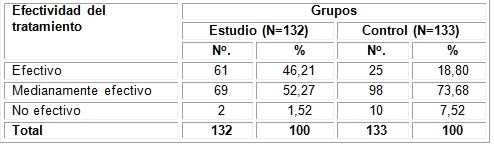
Fuente: Formulario del estudio
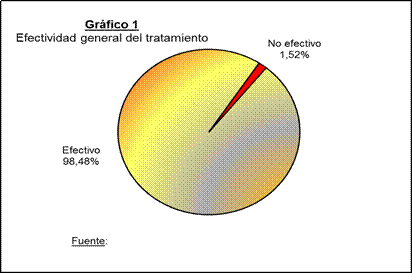
La efectividad con la utilización de membrana de fibrina rica en plaquetas se expresó en el siguiente gráfico; se muestra, que en los sitios del grupo estudio que recibieron la membrana de fibrina rica en plaquetas (130 sitios, 98,48 %) fue efectivo el tratamiento (mayor que el 85%) y solamente, 1,52 % (2 sitios) no fue efectivo (menor que el 85 %). (Gráfico 1)
DISCUSIÓN
La periodontitis crónica es la más frecuente entre todas las enfermedades periodontales; afecta a los tejidos de soporte dentario y su principal característica clínica es la pérdida progresiva, tanto de la inserción clínica como ósea, esta última evidenciada radiológicamente, en detrimento de la estructura dentaria en pacientes adultos. Presenta modelos cíclicos de exacerbaciones y remisiones, sin consenso sobre la causa de esta progresión que puede tardar años.15,16
La inflamación crónica es la causa más frecuente de hemorragia al sondeo. En la inflamación gingival existen varias alteraciones histopatológicas que producen hemorragia gingival; se destaca, la dilatación e ingurgitación de capilares y el adelgazamiento o ulceración del epitelio del surco; los anterior depende de los capilares, los cuales se encuentran dilatados y más próximos a la superficie y el epitelio delgado y degenerado, aportando menor protección; en ellos, los estímulos en condiciones normales son inocuos, causan rotura de los capilares y hemorragia gingival. Los sitios con hemorragia al sondeo presentan un área mayor de tejido conectivo inflamado, que las zonas sin hemorragia; la intensidad de la misma y la facilidad con que se producen dependen de la gravedad de la inflamación. En los casos de periodontitis crónica severa o moderada, la presencia de hemorragia al sondeo se identifica como un signo de enfermedad activa.3,17,18
En el tejido de inserción periodontal, la respuesta inflamatoria se caracteriza por grandes cantidades de leucocitos neutrófilos polimorfonucleares y macrófagos, funciones destructivas y fagocitosis en el sitio de interacción con el tejido superficial que origina la presencia de un infiltrado inflamatorio con la activación del sistema inmune y la producción, y liberación de citocinas.19
La formación de la bolsa da lugar a la pérdida de inserción clínica y denudación de la superficie radicular.17 La magnitud de la pérdida de inserción suele tener relación, si bien no siempre, con la profundidad de la bolsa. Esto se debe, a que el grado de pérdida de inserción depende de la localización de la base de la bolsa en la superficie radicular, en tanto, la profundidad de la bolsa es la distancia entre el fondo de la misma y la cresta del margen gingival.20,21
Según los hallazgos encontrados en relación con los niveles de inserción clínica, la literatura consultada plantea que, mientras más altos sean los niveles de la misma, radiográficamente se evidencia mayor pérdida ósea; en el estudio se mostró concordancia entre estos dos parámetros clínicos. Inicialmente, en el grupo de estudio existió una pérdida de inserción clínica severa en un 56,06 %; sin embargo, a los 12 meses de realizado el tratamiento, se evidenció, que el 61,36 % se encontraba sin pérdida de inserción clínica; no se observó este parámetro en su forma moderada ni severa.7
Los investigadores plantean, que el éxito del tratamiento periodontal depende en gran medida, de la capacidad de analizar el caso de manera global. El paciente debe estar sometido a un estricto control de higiene oral para controlar la acumulación de microorganismos, eliminar o controlar los factores de riesgo e influyentes, así como seleccionar el tratamiento adecuado; hay que tener en cuenta, que los pacientes con estas patologías -en ocasiones- tienen un pronóstico individual dudoso, en dependencia del tipo de defecto óseo y la cantidad de hueso remanente. Por ello, es de estricto cumplimiento eliminar el proceso inflamatorio, prevenir la progresión de la enfermedad y regenerar la pérdida de los tejidos periodontales.14
Desde el punto de vista microscópico, el defecto óseo tratado es llenado inicialmente por el coágulo sanguíneo, el cual es reemplazado por un tejido de granulación que eventualmente da origen a nuevas fibras colágenas, laminillas de cemento y trabéculas óseas. Por encima de este proceso, el epitelio que recubre el área se adhiere al diente por medio de hemidesmosomas y una lámina basal, se produce con mayor facilidad en bolsas infraóseas que en supraóseas, pues el hueso lateral protege el coágulo y permite su favorable evolución.8,9
Las plaquetas liberan factores de crecimiento, presos en el interior de la matriz de fibrina, después de su activación. Estos factores de crecimiento son considerados estimulantes para la respuesta mitogénica en el periostio y son responsables por la reparación del hueso durante la cicatrización normal de las heridas.
Los concentrados de plaquetas aumentan la cicatrización del tejido, debido a una mayor proliferación de progenitores del tejido conectivo que estimulan la actividad de los fibroblastos y los osteoblastos, y mejoran la osteogénesis, tienen actividad antimicrobiana contra especies bacterianas involucradas en infecciones orales, modifican el mecanismo de defensa del huésped, mediante la administración de péptidos de señalización que atraen a las células de los macrófagos y modifican la reacción inmune (liberando leucocitos que sintetizan interleuquinas).
La aplicación de adhesivos de fibrina -en el tratamiento quirúrgico- está bien documentada, es un mecanismo biológico natural de polimerización de fibrina, amplificado de forma artificial; contiene los componentes sanguíneos mediante la centrifugación y proporciona una oportunidad para ampliar los componentes ricos y ventajosos de la propia sangre del paciente.
Se ha evidenciado, que las propiedades estructurales de la fibrina pueden ser un parámetro de diseño importante para maximizar la invasión de los tejidos óseos durante la cicatrización de las heridas. Inicialmente, este biomaterial fue utilizado en la cirugía implantológica, principalmente, para favorecer y acelerar los procesos de recambio y cicatrización ósea. Su uso ha sido científicamente comprobado, presenta grandes beneficios clínicos para promover la regeneración ósea y mejorar la cicatrización de los tejidos blandos.13,22
En la muestra estudiada se corroboró, que los pacientes que recibieron tratamiento quirúrgico periodontal, más la aplicación de una membrana de FRP-L como biomaterial autólogo, tuvieron mejores resultados a los 12 meses de evolución, en comparación con aquellos que recibieron tratamiento quirúrgico convencional, solamente, para un 46,21 % de efectividad.
La utilización de la membrana de FRP-L, como biomaterial autólogo en el tratamiento quirúrgico de los defectos óseos angulares de la periodontitis crónica, demostró tempranamente, una mejoría durante la fase de cicatrización, el logro de una adecuada coloración gingival y posteriormente, un aumento de la inserción clínica y mayor ganancia ósea, asociado a bienestar posoperatorio y favorable aceptación del tratamiento por el paciente.
CONCLUSIONES
En la muestra estudiada prevalecieron los sitios con periodontitis crónica severa. Los sitios que recibieron tratamiento con la membrana de FRP-L, como biomaterial autólogo, mostraron mejores resultados en los parámetros clínicos, fundamentalmente, el aumento de la inserción clínica y radiográficamente, mayor ganancia ósea. El tratamiento con la membrana de FRP-L fue efectivo; puede ser una alternativa eficaz, especialmente, en situaciones donde los signos y síntomas de la enfermedad periodontal avanzada sean notables.