INTRODUCCIÓN
La epidemia global de las enfermedades cardiopulmonares no solamente se incrementan en número absoluto, sino que se estima que a mediados del siglo actual uno de cada cuatro individuos del planeta tendrá 65 años de edad o más.1,2 En Cuba, la expectativa de vida es comparable a la de muchos países del primer mundo y sigue en ascenso.3 Villa Clara, provincia en la que se realiza el presente estudio, tiene una de las poblaciones más envejecidas del país, con una expectativa de vida promedio de 77 años.3
En el Anuario Estadístico de 2017 se afirma que entre los habitantes de uno a 79 años hay un promedio de pérdidas de años de vida potenciales, de 13,59 años por causas cardiovasculares.3
En la actualidad, en los ancianos se realizan intervenciones quirúrgicas mayores, cada vez más complejas y riesgosas. Así lo demuestran los procederes endovasculares realizados por los cardiólogos intervencionistas con mayor auge y desarrollo,2 al punto de poder realizar intervenciones quirúrgicas a pacientes más añosos, con pronóstico de morbilidad y mortalidad muy elevado.
La muerte de las células miocárdicas secundaria a la isquemia transitoria ocurre en los primeros minutos de la reperfusión en forma de necrosis en bandas de contracción. Los mecanismos involucrados en la ruptura del sarcolema y la necrosis durante la reperfusión inicial son debidos a alteraciones del ión Ca2+ (intercambiador de iones Na+/H+-, Na+/Ca2+WQen el retículo sarcoplásmico) o que interfiere con sus consecuencias (hipercontracturas, activación de la cascada calpain, y la apertura de la permeabilidad de los canales mitocondriales).4,5
En los pacientes en que ya se identificó que se le van a realizar procederes diagnósticos o terapéuticos que conllevan agresiones isquémicas al miocardio, de intensidad y duración significativa, el condicionamiento isquémico (CI)6 puede ser una ventana terapéutica de gran utilidad para mejorar los índices de morbilidad y mortalidad, sobre todo en la prevención, reducción del tamaño del infarto tipo cuatro o cinco y disminución de la incidencia y severidad del bajo gasto cardíaco (BGC) que se puede presentar, muchas veces asociados a las lesiones de reperfusión inherentes a la revascularización coronaria.4,5,6
Dicho CI se puede inducir de forma local, condicionamiento isquémico local (CIL) por pinzamiento y despinzamiento de la arteria aferente del corazón, pinzamiento aórtico o insuflación del balón de angioplastia (con los cuidados extremos que estos conllevan para evitar traumas vasculares o tensiones excesivas) o por medios farmacológicos, condicionamiento isquémico farmacológico (CIF).5,6 Algunos estudios2,5,6,7,8 demuestran que se puede limitar el tamaño del infarto mediante estrategias no farmacológicas, como el poscondicionamiento isquémico y el condicionamiento isquémico a distancia (CIAD).
El CIAD se ha evaluado en humanos con resultados satisfactorios y se muestra su efectividad como cardioprotector en pacientes a los que se les realiza angioplastia primaria. Este proceder a distancia tiene múltiples ventajas sobre el CI clásico: es seguro, muy económico y puede aplicarse fácilmente a todos los pacientes con infarto de miocardio que reciban tratamiento de reperfusión.5,6
Constituye el objetivo de este artículo, analizar si existen diferencias entre los dos grupos (control y estudio) teniendo en cuenta el consumo de inotrópicos y/o vasopresores durante los períodos intra y posoperatorio, así como la incidencia de eventos adversos cardiacos mayores y mortalidad en el postoperatorio.
MÉTODOS
Se realizó un estudio cuasiexperimental, explicativo, comparativo con control histórico. Se recoge la muestra del grupo control (control histórico) de forma retrospectiva. El grupo estudio del CIAD se evaluó de forma prospectiva en ambos casos de acuerdo al orden de llegada, en la unidad quirúrgica del Cardiocentro “Ernesto Ché Guevara” de Villa Clara.
El universo estuvo constituido por todos los pacientes con diagnóstico preoperatorio de enfermedad arterial coronaria multivasos, programados para revascularización coronaria de forma electiva.
Se incluyeron los pacientes que de modo electivo fueron intervenidos por cirugía cardiaca de revascularización coronaria, en el caso del grupo estudio, pacientes que estuvieron de acuerdo con otorgar el consentimiento informado para la investigación. Se excluyeron a los que además de la revascularización coronaria, se les realizó procedimientos de ablación intraoperatorio de focos arrítmicos, implantación de válvulas o injertos aórticos u otros, presencia de una fístula arteriovenosa o linfedema del brazo derecho en el caso del grupo estudio, cirugía cardiaca previa endovascular o convencional, cirugía de urgencia o emergencia, insuficiencia renal y disfunción neurológica previa. Como criterio de salida se tuvo en cuenta a los pacientes que fallecieron durante el período intraoperatorio y en la primera semana del posoperatorio.
La muestra quedó conformada por 494 pacientes, muestra representativa de la población estudiada que fueron intervenidos quirúrgicamente de revascularización coronaria.
Operacionalización de las variables
- Eventos adversos cardiacos mayores: Fueron aquellas complicaciones que se presentaron en los primeros 7 días del período posoperatorio, desde que se trasladó el paciente a la sala de cuidados intensivos quirúrgicos (UCIQ) y luego a la sala posoperatoria, después de intervenido quirúrgicamente, entre las que se encontraron:
Taquicardia ventricular (TV): Se consideró cuando el ritmo cardiaco se inició por debajo del haz de Hiss, con traducción eléctrica en el ECG, de ensanchamiento del complejo QRS y con onda T invertida y deformada, frecuencia cardiaca superior a 100 latidos por minuto, siendo sostenida si esta duró más de 30 seg, con deterioro importante de la hemodinamia del paciente, con necesidad de usar terapia medicamentosa, mecánica o eléctrica y no sostenida cuando duró menos de 30 seg, sin deterioro importante de la hemodinamia del paciente, sin necesidad de usar terapia medicamentosa, mecánica o eléctrica.
Fibrilación ventricular (FV): Se consideró cuando se deforma completamente la morfología ECG del complejo QRS y de la onda T, puede ser un trazado de ondas gruesas o finas.
Bajo gasto cardiaco reversible (BGCR): Se definió como el trastorno clínico humoral y hemodinámico caracterizado por los siguientes criterios: índice cardíaco < 2,2 l/min/m2, presión arterial sistólica < 80 mmHg o PAM < 65 mmHg, presión media en aurícula izquierda > 18 mmHg, necesidad de usar balón de contrapulsación intraórtica o fármacos inotrópicos positivos para soporte hemodinámico. Presencia de gradiente térmico en los miembros inferiores y pulsos pedios finos o ausentes. Oliguria (diuresis < 0,5 mL/kg peso corporal/h). Acidemia metabólica.
Bajo gasto cardiaco real (BGC real): Definida para todos los pacientes con BGC posterior a la revascularización coronaria, independientemente de los resultados previos del test de BGC.
Criterios electrocardiográficos. Nuevo IMA. Se consideró, nuevo IMA el que apareció en el ECG, posterior a la cirugía, en los pacientes que no tenían IMA previo, con cambios específicos que incluyeron aparición de nuevas ondas Q patológicas (duración ≥ 0,04 segu y profundidad ≥ 25 % del voltaje de la onda R o complejos QS) en más de una derivación. Cambios inespecíficos que incluyeron elevación del segmento ST ≥ 1,5 mm de la línea isoeléctrica en dos o más derivaciones de una misma región, depresión del ST ≥ 2 mm en las derivaciones precordiales o inversión de la onda T por más de 48 h; decapitación de la onda R en las derivaciones precordiales, presencia de arritmias ventriculares o trastornos de la conducción auriculoventricular.
Criterios enzimáticos: se consideraron valores patológicos si estos fueron superiores a cinco veces la cifra normal: troponina I > 1 μg/L, CK total ≥ 250 U/l, CK MB ≥ 133 U/l, troponina T> 240 μg/L, LDH ≥ 800 U/l, LDH1 /LDH2 mayor a uno en muestras recogidas entre el segundo y tercer día del postoperatorio y TGO ≥ 90 U/l.
Extensión del IM antiguo: Se consideró extensión del IM antiguo el que apareció en el ECG, posterior a la cirugía, en derivaciones diferentes a las ya afectadas, previo a la intervención quirúrgica, con cambios específicos que incluyeron aparición de nuevas ondas Q patológicas (duración ≥ 0,04 seg y profundidad ≥ 25 % del voltaje de la onda R o complejos QS) en más de una derivación de la misma localización del IM antiguo, o en otra cara anatómica. Cambios inespecíficos que incluyeron elevación del segmento ST ≥ 1,5 mm de la línea isoeléctrica en dos o más derivaciones de una misma región, depresión del ST ≥ 2 mm en las derivaciones precordiales o inversión de la onda T por más de 48 h; decapitación de la onda R en las derivaciones precordiales, presencia de arritmias ventriculares o trastornos de la conducción auriculoventricular.
Criterios enzimáticos: iguales a los criterios presentados anteriormente.
Uso del balón de contrapulsación intraórtico (BIA): Se consideró según se usó el BIA durante la cirugía y en el postoperatorio. Se clasificó en dos categorías: Balón de contrapulsación intraoperatorio: Cuando se implantó antes, al finalizar o durante las maniobras de interrupción de la CEC como medida de tratamiento del fallo ventricular agudo y postoperatorio cuando se implantó en la sala de cuidados postoperatorios.
Uso de medicamentos en el intraoperatorio y posoperatorio: Se consideró cuando se le administró al paciente algunas de los siguientes medicamentos: dobutamina, norepinefrina, epinefrina o todos.
Mortalidad: Se consideró el número de fallecidos y sus causas generales en:
Sépticas: Se definió como tal a la muerte causada por un foco infeccioso en cualquier parte del organismo en el que se demostrara la presencia de bacterias, asociado a manifestaciones clínicas de sepsis.
Bajo gasto cardiaco fatal (BGCF) o irreversible: Se definió como el trastorno clínico humoral y hemodinámico caracterizado por los siguientes criterios: índice cardíaco < 2,2 l/min/m2, presión arterial sistólica < 80 mmHg o PAM < 65 mmHg, presión media en aurícula izquierda > 18 mmHg, necesidad de usar BIA, fármacos inotrópicos positivos o vasopresores para soporte hemodinámico. Presencia de gradiente térmico en los miembros inferiores y pulsos pedios finos o ausentes. Oliguria (diuresis < 0,5 mL/kg peso corporal/h). Acidemia metabólica. No mejoría con tratamiento médico habitual y evolución hacia la muerte.
Falla multiorgánica: Se clasificó en presente y ausente. Se consideró fallo de órganos cuando el paciente reflejó, al menos uno de los siguientes criterios (independientemente de si se anotaba o no en la hoja de egreso):
Fallo cardíaco: Frecuencia cardiaca (FC) < 50 latidos/min (lat/min), taquicardia ventricular, fibrilación ventricular, paro cardíaco e IMA.
Falla respiratoria: Frecuencia respiratoria (FR) < 5/min o > 50/min. Ventilación mecánica por 3 o más días o flujo inspiratorio de oxígeno FiO2 (Fracción de oxígeno que se inspira en una mezcla de gases) > 0.4 o presión positiva al final de la espiración (PEEP) > 5 cm/agua.
Falla Renal: creatinina sérica > 280 mmol/L o 3,5 mg/dL. Diálisis, hemodiálisis/ ultrafiltración.
Falla Neurológico: Glasgow < 6 en ausencia de sedación.
Falla Hepática: Bilirrubina > 51 mmol/L o 3 mg/dL en ausencia de hemólisis. TGP > 100 U/L.
Técnicas de procesamiento
La información fue llevada a una base de datos mediante la aplicación Microsoft Excel 2010 y procesada con el programa estadístico SPSS versión 20.
Análisis estadístico
Las variables cualitativas fueron resumidas mediante números absolutos y porcentajes, las cuantitativas con la media y desviación estándar. Para la comparación de los grupos de estudios según variables cualitativas se empleó la prueba chi cuadrado ((2). La comparación de los grupos de estudio según variables cuantitativas se realizó con la prueba t de Student.
Protocolo anestésico establecido
La inducción anestésica se realizó con la administración por vía endovenosa en dosis única de lidocaína 2 % 1 mg/kg, fentanyl 5 μg/kg de peso corporal, propofol a 2 mg/kg, bromuro de vecuronio 0,1 mg/kg, luego se colocó el tubo orotraqueal. La ventilación pulmonar mecánica se efectúo con un ventilador Fabius GS; el volumen corriente inicial se calculó a 7 mL/kg, la FR de 12 a 16 ciclos por minuto y la FiO2 50 %, luego se colocó un catéter venoso profundo en la vena yugular interna derecha (vía intermedia) para monitorizar la presión venosa central (PVC) y dos centímetros debajo se colocó introductor calibre ocho F para colocar un catéter en la arteria pulmonar (Swan Ganz) con el que se midió índice cardiaco (IC) y resistencia vascular sistémica (RVS). El mantenimiento de la anestesia se realizó con Isofluorano entre 1 y 1,5 concentración alveolar mínima. Después de estabilizado el paciente posterior a la instrumentación anestésica se procedió a colocar a los del grupo estudio, un torniquete en el brazo derecho (preCIAD), el cual se insufló hasta alcanzar una presión de 200 mmHg, esta presión se mantuvo durante 5 min, luego se desinfló y se dejó reperfundir la extremidad por 5 min, más tarde se repite este ciclo dos veces más. Después de clampeada la arteria coronaria para su revascularización (evento isquémico mayor), se repitió el procedimiento de insuflar/desinsuflar el torniquete (perCIAD) y posteriormente al momento del cierre, se realizó por tercera y última vez igual proceder (posCIAD). Concluida la cirugía se trasladó el paciente a la UCIQ donde fue tratado según protocolo establecido.
RESULTADOS
Se conformaron dos grupos de 247 pacientes cada uno (muestra representativa de la población estudiada). No se encontraron diferencias significativas (p>0,05) según un conjunto de variables que representan el estado inicial de los pacientes: (edad, sexo, fevi, dm, HTA, EPOC, antecedentes patológicos familiares de cardiopatía isquémica, hiperlipidemia, duración cec, arteriopatía extracardíaca o periféricas, número de vasos con lesiones angiográficas significativas, número de vasos revascularizados, nyha, ima reciente, angina inestable, im antiguo, hábito de fumar), tratamientos previos que tuvieron los pacientes, lo que garantizó la homogeneidad de los grupos y pudo realizarse las comparaciones entre ellos.
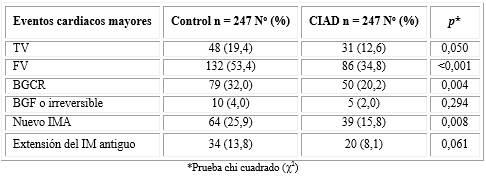
Los eventos adversos cardiacos mayores (Tabla) más frecuentes fueron la FV, BGCR y nuevo IMA en ese orden, con diferencias significativas entre ambos grupos control y CIAD respectivamente, a favor del grupo estudio.
Con respecto al uso de medicamentos de apoyo a la función cardiovascular (dobutamina) en el periodo intra-posoperatorio, se observó que hubo diferencias significativas (p<0,001) entre los dos grupos, con mayor consumo de medicamento en el grupo control.
En relación con los valores de norepinefrina se observó diferencia significativa (p< 0,05), entre los dos grupos, el CIAD fue el de menor consumo tanto en el intra como en el posoperatorio.
En el caso de la epinefrina intraoperatorio, no se encontró diferencia significativa entre los grupos, sin embargo; en el posoperatorio sí hubo diferencias muy significativas p<0,001 a favor del grupo estudio.
Para la mortalidad, primero se realizó una predicción de esta con el test EUROSCORE, no se encontró diferencia significativa, correspondiéndose con el análisis de la mortalidad total sin diferencias significativas entre los grupos (p=0,090). No hubo fallecidos en los primeros 7 días del estudio, estos aparecieron en el período comprendido después de la primera semana hasta el egreso del paciente.
Como no se encontraron diferencias significativas en cuanto a la mortalidad total y teniendo en cuenta que en el grupo control existió el doble de fallecidos con relación al grupo CIAD, se analizó la contribución de cada grupo a la mortalidad mediante la diferencia relativa porcentual de esta variable entre el grupo CIAD con respecto al control y fue de -96 %, es decir, la diferencia entre la mortalidad del grupo control y el CIAD con respecto al grupo control, tiene una contribución del -96 % [(Mortalidad del grupo CIAD) - (Mortalidad del grupo control)/(Mortalidad del grupo control) X 100] [(4 %-8,1 %/8,1 % X 100], esto quiere decir, que el grupo estudio contribuyó menos al incremento de la mortalidad total.
DISCUSIÓN
Los primeros experimentos de laboratorio con oclusión coronaria transitoria permitieron observar que durante esta se producía una exacerbación de las alteraciones funcionales asociadas a la isquemia, en particular arritmias.3,4 En 1960 fueron descritos los cambios histológicos producidos por la reperfusión del territorio miocárdico isquémico en perros2,3,4,5 y se da entrada a un nuevo concepto: la restauración del flujo de un determinado territorio isquémico puede en sí misma producir muerte celular, lo que podría ensombrecer parcialmente los beneficios de la reperfusión.4,5,6
Las lesiones miocárdicas sufridas durante la cirugía cardiaca, la mayoría atribuibles a la isquemia y/o lesión posreperfusión,4 asociadas a peores resultados clínicos a corto y largo plazo fue objeto de estudio por Balakumar,4 en el año 2012 en su artículo: “Curando el corazón diabético: ¿Funciona el precondicionamiento miocárdico en el diabético?”, reafirmó categóricamente que la lesión posreperfusión resultado de la realización de injertos coronarios, imprescindibles para mejorar la salud del paciente, producen el doble de daño miocárdico que la isquemia previa, de esta forma, la incidencia de lesión miocárdica, BGC y con ello el aumento significativo de las necesidades de apoyo inotrópico y vasoactivo por un período mayor de tiempo, son elementos que hay que tener en cuenta en el manejo anestésico del revascularizado.4
Para evaluar el carácter protector que pudiera tener el CIAD en la disminución de complicaciones, sobre todo de origen cardiovascular, se estudió la incidencia de eventos adversos cardiacos mayores. Stephen y otros7 posterior a la cirugía, encuentran una disminución en la incidencia de eventos adversos cardiacos mayores al igual que lo encontrado en este estudio, para algunos de ellos como: la FV, BGCR y nuevo IMA. El autor7 demostró además, menor frecuencia de dolor precordial (p=0,0006), menos cambios del segmento ST (p=0,005) en el electrocardiograma y menor incidencia de eventos cerebrales, en el grupo CIAD, cuatro contra 13 en el control y diferencias significativas (p = 0,018).7
Algo muy relacionado con lo anterior significó el uso del BIA. Está demostrado que la pronta utilización de este, disminuye la incidencia y mejora el pronóstico del BGCR y/o irreversible, sin embargo; la mayor utilización del BIA se traduce muchas veces como inadecuada protección miocárdica y por ende, peores resultados pronósticos, este estudio se comporta similar a lo recogido en la bibliografía. Se demuestra así, que el uso del CIAD es capaz de disminuir la incidencia de BGC7 y con ello el uso del BIA.
Stephen y otros7) autor del anterior estudio, coincide con los resultados de esta investigación y sugiere, que es mejor “apretar un brazo para proteger el corazón” que prescindir de este, pues con él se puede disminuir la incidencia de eventos adversos cardiacos mayores hasta en un 50 %.7,8
En relación con el uso de los medicamentos de apoyo a la función cardiaca en investigaciones realizadas, hay autores como Bei Li y otros9 que consideran, que el uso de drogas de apoyo cardiovascular, disminuye considerablemente con la implementación del CIAD, por estar el miocardio mejor preparado para enfrentar la lesión que se produce posterior a la reperfusión (atontamiento miocárdico y/o isquemia miocárdica). En su artículo realizado con 99 pacientes divididos en dos grupos, demuestra la disminución del consumo de inotropos (p = 0,019) en el grupo estudio, al igual que en esta investigación.
De forma semejante avalan el comentario anterior los cuatro metanálisis revisados al respecto.10,11,12,13 El más destacado realizado por Stewart y otros10 también perteneciente a la Universidad de Cambridge; de 6506 citas revisadas, 22 trabajos resultaron elegibles con 933 pacientes, 19 reportes con CIL (clampeo y desclampeo de la aorta), concluyen con disminución del consumo de inotropos.10,11,12,13
La mortalidad como entidad multicausal no responde solamente a razones de tipo cardiovasculares (isquémicas) donde el CIAD tiene una función de vital importancia, sino que es un proceso mucho más complejo donde también influyen determinantemente la edad, sepsis, sangramientos y complicaciones de tipo quirúrgicas (no isquémicas). Por tal motivo, para un análisis adecuado de esta variable sería necesario excluir las causas no isquémicas de muerte posoperatoria, aspecto muy difícil de lograr al ser esta una cirugía muy compleja, con muchas comorbilidades y con un tiempo bastante prolongado de recuperación, donde la incidencia de factores externos pueden influenciar de forma muy significativa en la mortalidad de estos pacientes.
Al desglosar la mortalidad total, por las diferentes causas de muerte, no se encuentran diferencias significativas, sin embargo; si se tiene en cuenta que la predicción preoperatoria de mortalidad según el test EUROSCORE era igual para ambos grupos, se concluye que el CIAD fue el que menos contribuyó de forma directa al incremento de la mortalidad total y además, el que menos contribuyó de forma indirecta en el aumento de esta al impedir que eventos adversos cardiacos mayores como el BGCR, nuevo infarto agudo de miocardio y FV, atenuadas por el CIAD, pudieran haberse convertido en complicaciones letales como lo fue el BGCF o fallo multiorgánico.
Resultados muy parecidos a los de esta investigación obtiene Takagi y otros11 en un metanálisis realizado del CIAD en cirugía cardiovascular, evalúa investigaciones recientes y concluye que el CIAD fue muy útil en la disminución del daño miocárdico pero no de la mortalidad. Sin embargo, Man y otros12 refiere en un metanálisis realizado en el año 2017 que el CIAD en pacientes con infarto agudo de miocardio es capaz de disminuir la mortalidad de cualquier etiología.
Se concluye que el condicionamiento isquémico a distancia es un procedimiento útil para la protección miocárdica en la revascularización coronaria, demostrado por una disminución significativa del uso de medicamentos de apoyo a la función cardiovascular. Con su aplicación se constató una disminución significativa de eventos adversos cardiacos mayores fundamentalmente la fibrilación ventricular, bajo gasto cardiaco reversible, nuevo infarto agudo de miocardio y con ello la disminución de la mortalidad por esta causa.