INTRODUCCIÓN
El café (Coffea arábica L.) es un ejemplo de los cultivos agrícolas que se desarrollan en Colombia desde el siglo XVIII hasta la actualidad. En la actualidad, los departamentos del Huila, Nariño y Cauca conforman el nuevo ‘Eje Cafetero’. Las superficies cultivadas han crecido 63,6 % en los últimos 13 años, lo que conlleva a una mayor expansión del territorio agrícola local, comprometiendo el recurso suelo. Gracias a su vocación agrícola y tradición cafetera, el departamento ha del Huila se ha consolidado en los últimos años como el principal productor de café en Colombia (Cerquera et al., 2020).
La transformación de los paisajes nativos por la intensificación de los monocultivos de café, ha sido una de las principales causas de la perdida de la biodiversidad en los ecosistemas altoandinos. Los macroinvertebrados edáficos, que son invertebrados del suelo con un tamaño superior a 2 mm, pueden desempeñar un papel importante como bioindicadores. Su abundancia, riqueza taxonómica y distribución vertical varían en función de la cobertura vegetal, los diferentes usos y manejos del suelo, así como de las variaciones estacionales (Doblas et al., 2009); Cabrera et al., 2017; Velásquez y Lavelle, 2019).
Los sistemas agroforestales (asociación de cultivos y árboles) representan una oportunidad para la producción de café con criterios de sostenibilidad. Estos sistemas se correlacionan positivamente con la biodiversidad Campera et al., (2022) y la abundancia de macrofauna del suelo (Rojas et al., 2021). En contraste, en los monocultivos de café predominan los organismos bioindicadores que señalan desequilibrio y perturbación en el suelo (Rodríguez et al., 2019).
El objetivo de esta investigación es evaluar la incidencia de dos sistemas productivos de café en la composición, riqueza, abundancia y distribución vertical de los macroinvertebrados edáficos en el municipio de Garzón, Huila, Colombia.
MATERIALES Y MÉTODOS
Zona de estudio
Se encuentra localizada a 15 Km al Este del municipio de Garzón - Huila (Colombia). Se identificaron nueve fincas con una superficie promedio de 1,0 ha. Estas se ubicaron entre las coordenadas 02º20'52" de latitud norte y 75º54'17" de longitud oeste del Greenwich, en una altitud de 1 460 a 1 668 m.s.n.m. Todas las fincas se encuentran dentro de la zona de vida de Bosque Húmedo-Premontano (Bh-P) conforme a la clasificación de Holdridge. Predominan temperaturas medias entre los 18 °C y 24 °C y las precipitaciones anuales oscilan entre 2 000 y 3 500 mm. Los suelos de la zona son superficiales a profundos, bien drenados, ligeramente ácidos y de una fertilidad moderada (IGAC, 1994 y IGAC 2014).
Sistemas evaluados
Se evaluaron monocultivos de café (MC) con una distancia de plantación de 1,2 m x 1,8 m y densidad de 4 630 árboles por hectárea, sistemas agroforestales de café y plátano (Musa paradisiaca L.) (SAFC), establecidos a una distancia de 1,2 m x 1,8 m y 5,6 m x 3 m, respectivamente, y superficies de bosque secundario (BS) medianamente intervenido como control positivo. Los cafetales correspondieron a plantaciones de la variedad Catimor, establecidas hace 11 años, con dos años del último zoqueo (poda total de los tallos a 30 centímetros del suelo para estimular el rebrote de nuevos tallos).
El manejo agronómico de MC y SAFC fue realizado por los productores siguiendo las recomendaciones de los asistentes técnicos de la zona, así: aplicaciones de 100 cm3 de glifosato en 20 L de agua para el control de arvenses, dos veces al año y podas con guadañadora cada cuatro meses; el control de plagas se realizó mediante aplicaciones de plaguicidas a base de Fenilpirazol, Clorpirifos y Tiametoxam + Ciproconazol, en dosis de 25 ml por 20 L de agua, con aplicaciones anuales en SAFC y semestrales en MC. La fertilización se realizó con urea, fosfato diamónico (DAP) y óxido de calcio (CaO). En cada caso se empleó una dosis de 50 gramos por planta, cada cuatro meses.
El bosque secundario (B.s) tiene 40 años aproximadamente; Ararat y Prager (2002) encontraron en estos bosques de la zona, especies como Goupia glabra A. (cedro blanco), Cedrela odorata L. (cedro rosado), Erythrina poeppigiana W. (cachingo), Persea caerulea R&P (aguacatillo), Chrysophyllum cainito L. (caimo), Inga marginata W. (guamo) y Jacaranda copaia A. (gualandai).
Establecimiento del diseño y muestreo en campo
Se estableció un diseño de Bloques Completos al Azar (BCA) en arreglo factorial con cuatro (4) replicas. El factor A correspondió a los sistemas evaluados (M.c, S.A.F.c y B.s) y el factor B a las cuatro profundidades de muestreo de invertebrados (hojarasca, 0-10 cm, 10-20 cm y 20-30 cm).
Los muestreos, se llevaron a cabo en el mes de octubre de 2018 (se contó con permiso de colecta, según Resolución 01140 de 2016), en época lluviosa, antes de iniciar la segunda cosecha significativa de café del año para evitar disturbaciones antrópicas.
Los macroinvertebrados edáficos se recolectaron mediante el método sugeridos por Velásquez y Lavelle, (2019). En cada sistema se recogieron tres monolitos (de 25 x 25 cm) o submuestras por replica; los monolitos se dividieron en cuatro estratos: hojarasca, 0-10, 10-20 y 20-30 cm. Para la recolección de los macroinvertebrados edáficos emplearon pinzas entomológica y pinceles. Estos se conservaron en alcohol al 70 %, con excepción de las lombrices las cuales se conservaron en viales con formol al 5 %. Posteriormente se trasladaron al Laboratorio de Entomología de la Universidad de la Amazonía (LEUA) para su caracterización a nivel de orden y familia. Se utilizaron las claves y descripciones taxonómicas de Ruiz et al. (2008) y Borror et al. (1992).
Variables de respuesta y análisis de los datos de biológicos
Para el análisis de la población de macroinvertebrados se determinaron los valores de riqueza (número de familias), abundancia específica (individuos m-2), densidad (número de individuos m-2) y distribución vertical de los macroinvertebrados en función de la abundancia en cada perfil o estrato del suelo. Se calcularon y presentaron los resultados generales en cada uno de los sistemas.
Además, se validaron los supuestos de normalidad y de homogeneidad de las varianzas de los datos mediante un análisis residual exploratorio (gráfico de Q-Q plot, la prueba Shapiro-Wilk y gráfico de valores predichos frente a residuos). Los datos que presentaron una distribución normal y homogeneidad de varianza (riqueza), se analizaron mediante la prueba LSD de Fisher (p<0,05) y los datos que no presentaron una distribución normal, se analizaron mediante la prueba no paramétrica Kruskall-Waill (p<0,05).
Se empleó un análisis multivariado con el objetivo de reducir la información y facilitar su interpretación. Para el caso de la diversidad, se realizó un análisis de correspondencia (AC) basado en la presencia - ausencia de las familias de macrofauna del suelo. Este permitió identificar aquellas familias exclusivas o compartidas entre sistemas. Todos los análisis se realizaron con el software InfoStat, versión 2018.
RESULTADOS Y DISCUSIÓN
Composición de la riqueza y abundancia de macroinvertebrados edáficos
La riqueza taxonómica estuvo representada por dos phylum, siete clases, 22 órdenes y 53 familias de macroinvertebrados edáficos. La mayor riqueza se presentó en B.s, seguido de S.A.F.c y M.c. A pesar de ello, los sistemas evaluados no presentaron diferencias estadísticamente significativas (p>0,072) en la riqueza de grupos taxonómicos (Tabla 1). Este tipo de comportamiento puede corresponder a un esfuerzo de muestreo o de potencia estadística insuficiente, sin embargo, estos resultados presentan una tendencia en la cual la riqueza disminuye a medida que aumenta el grado de perturbación y las diferencias en la vegetación como ocurre con la alta heterogeneidad de B.s y la homogeneidad de M.c. Lo anterior coincide con reportes de Delgado et al. (2011) y Cabrera et al. (2011) quienes indican que la riqueza de especies es más alta en el bosque y en los sistemas agroforestales que en sistemas de producción sin presencia de árboles, gracias a la diversidad de la vegetación, la disponibilidad de alimento para las especies, la compleja estructura de la vegetación que provee sitios de hábitat y brinda mejor protección que en sistemas agropecuarios más simples. Rojas et al. (2021) también afirman que los agroecosistemas cafeteros con vegetación compleja, ayudan a mantener una alta riqueza de macroinvertebrados lo que permite una mayor similaridad con el bosque, como es el caso de S.A.F.c (Tabla 1).
Tabla 1. - Abundancia (individuos m2) y riqueza de la macrofauna del suelo en los sistemas productivos de café (M.c y S.A.F.c) y en bosque secundario (B.s) en el departamento del Huila
| Familia | M.c | S.A.F.c | B.s | ||
|---|---|---|---|---|---|
| Amaurobiidae | 1,33 ± 1,33 | 2,67 ±1,8 | - | ns | |
| Anisolabididae | 1,33 ± 1,33 | 5,33 ±5,33 | - | ns | |
| Araneidae | 2,67 ±2,67 | - | - | ||
| Bdellidae | - | - | 5,33 ±1,54 | ||
| Cantharidae | - | 1,33 ± 1,33 | - | ||
| Carabidae | 4 ± 2,28 | 1,33 ±2,28 | 10,67 ± 4,55 | ns | ns |
| Cheliferidae | - | - | 5,33 ± 1,54 | ||
| Chthoniidae | - | 1,33 ± 1,33 | - | ||
| Cixiidae | 1,33 ± 1,33 | - | - | ||
| Clubionidae | - | 2,67 ± 2,67 | - | ||
| Coccinellidae | - | 1,33 ± 1,19 | 5,33 ± 2,37 | ns | |
| Crhysomelidae | 8 ± 6,95 | 10,67 ± 6,95 | 5,33 ± 13,9 | ns | ns |
| Cryptopidae | 8 ± 3,96 | 10,67 ± 3,96 | 16 ± 7,93 | ns | ns |
| Curculionidae | - | 8 ± 3,68 | - | ||
| Cybaeidae | 1,33 ± 1,33 | 2,67 ± 1,8 | - | ns | |
| Cydnidae | - | 5,33 ± 4,1 | 10,67 ± 10,67 | ns | |
| Dictynidae | 12 ± 9,26 | 4 ± 2,09 | - | ns | |
| Ectobiidae | 8 ± 6,3 | 9,33 ± 6,3 | 42,67 ± 12,59 | ns | ns |
| Elateridae | 1,33 ± 1,33 | 4 ± 2,87 | - | ns | |
| Forficulidae | 1,33 |
- | 10,67 |
** | |
| Formicidae | 205,33 |
325,33 |
138,67 ± 151,99 | * | ns |
| Geometridae | 2,67 ± 1,8 | - | - | ||
| Geophilidae | 1,33 |
1,33 |
21,33 |
ns | * |
| Gryllidae | - | - | 10,67 ± 1,54 | ||
| Hubbardiidae | 2,67 ± 2,67 | - | - | ||
| Isotomidae | 21,33 ± 8,22 | 5,33 ± 8,22 | 5,33 ± 16,44 | ns | ns |
| Julidae | - | - | 10,67 ± 1,54 | ||
| Labiduridae | 6,67 ± 5,38 | 16 ± 16 | - | ns | |
| Largidae | - | 8 ± 2,83 | - | ||
| Lepidopsocidae | 1,33 ± 1,33 | - | - | ||
| Linyphiidae | 17,33 ± 8,77 | 25,33 ± 8,77 | 10,67 ± 17,54 | ns | ns |
| Lumbricidae | 165,33 |
352 |
666,67 |
** | * |
| Lycosidae | 1,33 ± 1,33 | - | - | ||
| Mycetophagidae | 2,67 ± 1,8 | 5,33 ± 3,01 | - | ns | |
| Nabidae | 1,33 ± 1,33 | 1,33 ± 1,33 | - | ns | |
| Noctuidae | 5,33 ± 2,27 | 17,33 ± 6,67 | - | ns | |
| Nymphalidae | 13,33 ± 13,33 | 5,33 ± 5,33 | - | ns | |
| Parajulidae | - | 17,33 ± 17,33 | - | ||
| Pentatomidae | 1,33 ± 1,33 | - | - | ||
| Pisauriidae | - | 13,33 ± 4,33 | - | ||
| Polydesmidae | 8 |
2,67 |
21,33 |
ns | * |
| Porcellionidae | 13,33 |
10,67 |
80 |
ns | * |
| Ptiliidae | - | 5,33 ± 4,10 | - | ||
| Salticidae | - | - | 5,33 ± 5,33 | ||
| Scarabaeidae | 8 ± 8,36 | 13,33 ± 8,36 | 48 ± 16,72 | ns | ns |
| Siphonotidae | - | 8 ± 8 | - | ||
| Spirobolidae | - | 1,33 ± 1,19 | 5,33 ± 2,37 | ns | |
| Staphylinidae | 45,33 ± 14 | 52 ± 14 | 53,33 ± 28,01 | ns | ns |
| Superstitioniidae | - | - | 5,33 ± 1,54 | ||
| Tetragnathidae | 2,67 ± 3,16 | 6,67 ± 3,16 | 5,33 ± 6,32 | ns | ns |
| Theridiidae | 4 ± 4,35 | 8 ± 4,35 | 16 ± 8,69 | ns | ns |
| Trogositidae | - | 1,33 ± 1,33 | - | ||
| Trombidiidae | 1,33 ± 1,33 | - | - | ||
| Abundancia total | 586,67 |
969,33 |
1216 |
* | * |
| Riqueza | 8,58 ± 0,84 | 10,17 ± 0,84 | 13 ± 1,69 | ns | ns |
* = P < 0,05; ** = P < 0,01; ns = no significativo. † corresponde a las comparaciones entre los sistemas productivos; †† corresponde a las comparaciones entre B.s, M.c y S.A.F.c.
Medias ± error estándar. Medias seguidas por la misma letra en minúscula no difieren significativamente entre M.c y S.A.F.c; y medias seguidas por la misma letra en mayúscula no difieren significativamente entre B.s, M.c y S.A.F.c según la prueba LSD de Fisher p<0,05.
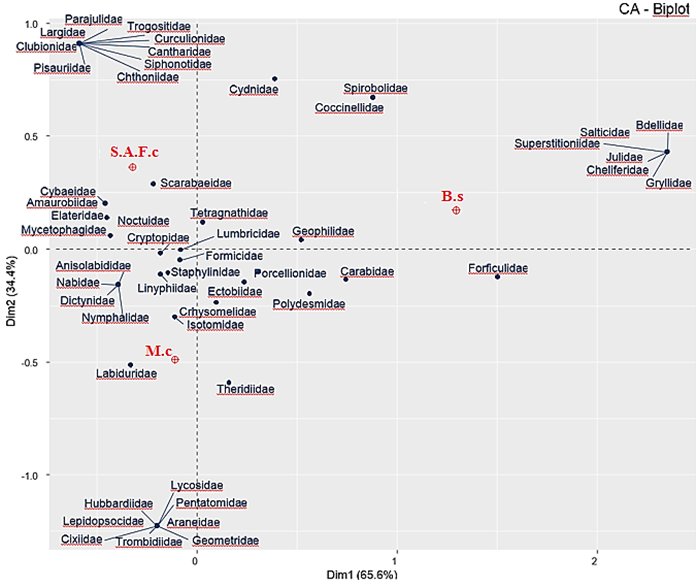
El análisis de correspondencia (Figura 1) demostró que ocho familias (Araneidae, Lycosidae, Hubbardiidae, Trombidiidae, Cixiidae, Pentatomidae, Geometridae y Lepidopsocidae) se encontraron asociadas a un solo sistema, el M.c; diez familias (Clubionidae, Pisauriidae, Chthoniidae, Parajulidae, Siphonotidae, Cantharidae, Curculionidae, Ptiliidae, Trogositidae y Largidae) sólo fueron registradas en S.A.F.c, mientras que Salticidae, Superstitioniidae, Cheliferidae, Bdellidae, Julidae y Gryllidae sólo fueron registradas en B.s (Figura 1). La escasa representatividad de las familias reportadas señala que son más susceptibles a las perturbaciones ambientales. También se registraron familias asociadas a M.c y S.A.F.c (Tabla 1 y Figura 1), esto puede deberse a que C. arábica se encuentra cubriendo la mayor parte del suelo proporcionando un hábitat similar en los dos sistemas ideal para estos organismos (Campera et al., 2022).
Abundancia de individuos por sistema
Se registraron 22.320 individuos m-2(Figura 2), con un promedio general de 826,7 individuos m-2 por monolito. La mayor abundancia en promedio se presentó en el B.s, seguido del S.A.F.c, siendo estos dos sistemas similares estadísticamente, pero presentando diferencias significativas con M.c (p<0,014) (Tabla 1).

Fig. 2. -Abundancia total de macrofauna del suelo (a nivel de familia) en sistemas productivos de café y bosque secundario
Se presentaron diferencias (p<0,049) entre los sistemas productivos de café (Tabla 1, Figura 2), evidenciando que las comunidades de macroinvertebrados presentes en los sistemas de uso del suelo están determinadas por la disposición de recursos para su supervivencia y los niveles de intervención del suelo en el desarrollo de las actividades agrícolas. Los resultados demuestran que existe una relación positiva directa entre sistemas menos disturbados con la abundancia de macroinvertebrados edáficos como lo argumentaron otros autores (Delgado et al., 2011).
En este sentido, se sugiere que el principal factor que influyó en el patrón de abundancia fue la heterogeneidad vegetal; el resultado obedece a que la diversificación de los sistemas productivos con otras especies vegetales mejora la abundancia de macroinvertebrados (Delgado et al., 2011), aunque estos efectos también están condicionados por la aplicación de insecticidas y fertilizantes.
Las familias taxonómicas que presentaron la mayor abundancia en los tres sistemas fueron: Lumbricidae, Formicidae, Staphylinidae, Porcellionidae, Scarabaeidae y Ectobiidae. De igual manera, Rojas et al. (2021) encontraron que en la mayoría de la macrofauna hallada en sistemas cafeteros de Colombia dominan en abundancia las lombrices de tierra y las hormigas. Estas seis (6) familias representaron el 80,7% de los macroinvertebrados edáficos identificados en todo el estudio, mientras que los grupos de “Otros” correspondientes a 47 familias representaron el 19,3 % de los grupos taxonómicos al presentar baja densidad en los sistemas evaluados (> 2 %).
Sin embargo, tan sólo tres familias (Lumbricidae, Formicidae y Porcellionidae) de las más abundantes y tres de la categoría de “otros” (Forficulidae, Geophilidae y Polydesmidae) presentaron diferencias significativas (p< 0,01) evidenciando un uso potencial como bioindicadores de calidad de suelo y perturbaciones antrópicas en sistemas cafeteros. La abundancia de Lumbricidae presentó diferencias estadísticas significativas entre los sistemas evaluados, alcanzó mayor valor en el B.s, seguido del S.A.F.c y menor abundancia en M.c (p< 0,01) (Tabla 1). Este orden taxonómico se caracteriza por participar en la regulación de la dinámica de la materia orgánica y del ciclo biogeoquímico de los nutrientes, en la neutralización de las toxinas generadas por los productos agroquímicos y en la modificación de la estructura del suelo.
Por otro lado, las familias de Geophilidae, Polydesmidae y Porcellionidae fueron similares estadísticamente dentro de las mismas familias tanto en el S.A.F.c como en el M.c, no obstante, se encontraron diferencias significativas frente al B.s (Tabla 1), con p<0,031, p<0,045 y p<0,036 respectivamente; lo anterior se debe a que estas familias requieren ambientes húmedos debido a su pérdida de agua, atributo que proporciona el B.s.
Respecto a la familia Formicidae presentó mayor abundancia en el S.A.F.c frente al M.c con encontrándose diferencias significativas entre sí (p<0,046) (Tabla 1). La familia de Forficulidae presentó mayor abundancia en el B.s frente al M.c encontrándose diferencias significativas entre sí (p<0,001) (Tabla 1); principalmente a que son organismos sensibles al uso del suelo debido que en muchas ocasiones viven en túneles profundos (Cabrera, 2011) .
El grupo Otros corresponde a los 47 grupos familias restantes que individualmente aportan menos del 2 % cada uno. La abundancia de individuos en S.A.F.c no presentó diferencias estadísticas con B.s, resultado similar presentó (Delgado et al., 2011) en un sistema agroforestal de café con banano evidenciando que la macrofauna presente en los diferentes sistemas de uso del suelo está determinada por la disposición de recursos para su supervivencia y por la intensidad de las actividades agrícolas, lo que sugiere que los sistemas agroforestales con café pueden ser una opción viable para conservar la abundancia de macroinvertebrados edáficos.
General
La mayor abundancia se encontró en el estrato de 0-10 cm, con diferencias significativas respecto al estrato de hojarasca y demás profundidades (Figura 3); esto concuerda con los hallazgos de Olayemi et al., (2022) quienes establecen que la macrofauna se encuentra confinada en la parte superior, en los primeros centímetros del suelo. De igual manera se presentó diferencias significativas en la hojarasca con relación a las profundidades de 10-20 cm y 20-30 cm. Estos dos últimos estratos fueron estadísticamente similares entre sí.
M.c.
Se encontró mayor abundancia en el estrato de hojarasca debido, probablemente, al mayor aporte de hojarasca en la parte superficial incidiendo de esta manera en la formación de un hábitat más propicio para el desarrollo de estos organismos, sin embargo, es estadísticamente similar a la profundidad de 0-10 cm, no obstante, se presentó diferencia estadística significativa en hojarasca respecto a los estratos de 10-20 cm y 20-30 cm; también entre el estrato de 0-10 cm respecto al estrato de 20-30 cm (Figura 3). Esta disminución de macrofauna en los estratos profundos puede deberse que a medida que se profundiza en el perfil del suelo disminuyen la porosidad, el contenido de oxígeno y de materia orgánica que proporciona el hábitat y alimento (Vanolli et al., 2023).
Lo anterior sustenta lo mencionado por Armbrecht y Perfecto (2001), que el monocultivo de café es un caso ejemplar de cómo la intensificación de la agricultura afecta negativamente a la biodiversidad tropical, porque al reducir la presencia de los árboles de sombra se disminuye la fauna asociada a los cultivos. En parte, esto se explica por la disminución de la complejidad estructural del cultivo y, por tanto, de los nichos ecológicos de la fauna residente en él (Rodríguez et al., 2019). En este contexto de simplificación, es posible estudiar cómo se afectan las relaciones interespecíficas entre los macroinvertebrados que habitan los agroecosistemas y cómo estas relaciones pueden favorecer o perjudicar los intereses del agricultor.
S.A.F.c.
Se encontró mayor abundancia en el estrato de 0-10 cm, presentándose diferencias estadísticas significativas con respecto al estrato de hojarasca y demás profundidades. De igual manera se presentaron diferencias significativas en la hojarasca con relación a las profundidades de 10-20 cm y 20-30 cm, estas dos últimas profundidades a pesar de tener abundancias distintas fueron estadísticamente similares (Figura 3). Doblas (2009) señalan que una de las causas que conlleva a tener mayor presencia de organismos en los primeros estratos (superficial y 0-10 cm) se debe a la cantidad de materia orgánica debido a la cobertura vegetal la cual aporta biomasa y genera microhábitats favorables para la vida de la macrofauna. Duran et al., (2023), sugieren que la mayor complejidad estructural y composición botánica de los sistemas agroforestales promueven la riqueza y diversidad de la macrofauna edáfica al mejorar las condiciones físicas, el contenido de materia orgánica del suelo potenciando esta al mejorar sus procesos de agregación y porosidad.
B.s
El estrato que presentó mayor abundancia fue 0-10 cm de profundidad (Figura 3). Este comportamiento puede estar relacionado con el suelo que se forma por la adición de hojarasca, además, la presencia del árbol en los sistemas hace que las temperaturas y el impacto de la lluvia disminuyan en comparación a los terrenos abiertos, constituyéndose en alternativas para lograr la colonización (Lavelle et al., 2022).
CONCLUSIONES
La abundancia y distribución de la macrofauna edáfica son atributos altamente sensibles cuando se sustituye el bosque por sistemas de producción de café. Sin embargo, la implementación del cultivo de café en sistemas agroforestales emerge como una estrategia importante para la conservación de estos organismos.
Las familias más abundantes (Lumbricidae, Formicidae y Porcellionidae) y menos abundantes (Forficulidae, Geophilidae y Polydesmidae) presentan una alta susceptibilidad a los cambios de coberturas en los sistemas.
En el sistema agroforestal de café, se observa la mayor diversidad de macroinvertebrados en los primeros 10 cm de suelo, mientras que en el monocultivo se encuentra la mayor diversidad en la hojarasca.











 texto en
texto en