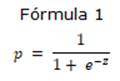Introducción
El síndrome de bajo gasto cardíaco (SBGC), es una manifestación clínica de gasto cardíaco insuficiente y perfusión tisular periférica, fue propuesto por primera vez por Rao et al.1 Estudios previos han demostrado que la mortalidad por todas las causas en SBGC varía de 14,8 a 62,5 % a corto plazo (un mes después del inicio) y 21,4 a 36,6 % a largo plazo (dos meses a un año después del inicio).2 El SBGC después de la cirugía cardíaca no solo conduce a la mal perfusión tisular, sino también a la disfunción orgánica múltiple del cerebro, los pulmones, el hígado, los riñones y el tracto gastrointestinal, lo que aumenta la utilización de los recursos de atención médica y los costos asociados.3
Más importante aún, el SBGC puede ser un estado de reducción reversible del gasto cardíaco después de la cirugía cardíaca y el reconocimiento temprano y el tratamiento adecuado del SBGC pueden evitar su progresión a shock cardiogénico refractario y mejorar los resultados clínicos, siendo la detección temprana de gran importancia.4
Según estudios de Norteamérica (EE.UU y Canadá), existió una reducción de la actividad quirúrgica de un 45 % global entre marzo y abril de 2020 frente a la realizada en 2019, evidenció un incremento de hasta siete veces en cirugía coronaria, probablemente a expensas de cirugía urgente, con descensos importantes en cirugía valvular de hasta el 7,5 %.5
En España en el año 2020,6 la cirugía de sustitución valvular y coronaria mostró una mortalidad del 13,61 %. La cirugía polivalvular y coronaria también presenta cifras similares (12,07 %) al tener relación con las complicaciones intra y postoperatorias, entre ellas el bajo gasto cardíaco.
Según Vera et al.,7 Cuba es uno de los pocos países en vías de desarrollo capaz de realizar colaboración en el campo de la cirugía cardiovascular y con la creación de los cardiocentros en diferentes regiones del país.
Según datos estadísticos resumidos en el Anuario Estadísticos,8 en el periodo 2019-2020 a un total de 3 004 pacientes, se les realizó tratamiento quirúrgico por alguna enfermedad cardiovascular.
Dada la situación antes descrita, se planteó realizar esta investigación con el objetivo diseñar y validar un modelo predictivo del síndrome de bajo gasto cardíaco a través de elementos de riesgo clínicos y ecocardiográficos.
Métodos
Se realizó un estudio analítico de casos y controles en pacientes que presentaron síndrome de bajo gasto cardíaco en el estado posoperatorio luego de recibir intervención quirúrgica cardiovascular y circulación extracorpórea en el Servicio de Cardiología y Cirugía Cardiovascular del Hospital Provincial Docente Saturnino Lora de Santiago de Cuba, en el período comprendido de enero 2019 a diciembre 2021.
Shoonen et al.,9 definió como síndrome de bajo gasto cardíaco postquirúrgico: aquel paciente con oliguria (diuresis inferiores a 0,5 ml/kg/h), saturación venosa central < 60 % (con saturación arterial normal) o lactato > 3 mmol/l.
Para el diseño muestral de los estudios de casos y testigos: Según lo recomendado por Bacallao,10 se trató de disponer de no menos de 10 casos por cada variable de estudio (10 variables, por tanto 100 casos), dado que existían 114 pacientes con síndrome de bajo gasto cardíaco, provenientes de la muestra del estudio. De acuerdo a los recursos disponibles en el momento de la investigación, se decidió tomar de forma aleatoria el 50 % del total (en suma 56 casos). Se escogieron (de manera aleatoria también) dos testigos por caso para un total de 112 controles, quedando conformada la muestra definitiva por 168 pacientes. El procedimiento para el muestreo fue la generación de números aleatorios con el programa SPSS 22.
Para validación del modelo predictivo y su eficiencia, se realizó en una muestra de pacientes seleccionada a través de un muestro simple aleatorio (alrededor de 108 que representa el 30 % de la muestra de elaboración), utilizándose para ello el programa SPSS 22, estos cumplían con los requisitos del estudio y no pertenecían a la muestra con la cual se construyó el modelo.
Se tomó como variable dependiente la presencia de bajo gasto cardíaco postquirúrgico. Según Shoonen et al.,9 la cual se dividió en dos fracciones: presencia de bajo gasto cardíaco (1) o ausencia de bajo gasto cardíaco (0).
Para dar cumplimiento a los objetivos de la investigación se definieron y operacionalizaron las variables las cuales fueron dicotomizadas teniendo como punto de corte estudio previo realizado:11
1. Edad: mayor de 65 años; menor igual de 65 años.
2. Sexo: masculino; femenino.
Comorbilidades de interés en la investigación:
3. Antecedentes enfermedad pulmonar obstructiva crónica (EPOC): Sí o No.
4. Antecedentes de diabetes mellitus (DM): Sí o No.
5. Antecedentes de fibrilación auricular: Sí o No.
Variables ecocardiográficas:
Las ecocardiografías se realizaron con un equipo de ecocardiograma Philips iE33, 48 horas antes de la operación en los pacientes programados para cirugía electiva y el día de la intervención en los que requirieron ser operados de urgencia.
1. Fracción de eyección del ventrículo izquierdo (FEVI):
a. FEVI ≤ 40 %.
b. FEVI > 40 %.
2. Excursión sistólica del plano anular tricúspideo (TAPSE) por sus siglas en ingles permite la evaluación de la función sistólica del ventrículo derecho preoperatorio, valores superiores a 17 mm son considerados normales.
a) TAPSE ≥17 mm (función sistólica del ventrículo derecho conservada).
b) TAPSE < 17 mm (función sistólica del ventrículo derecho deprimida).
3. Hipertensión pulmonar: al calcular el gradiente de presión sistólica entre la aurícula derecha y el ventrículo a partir de la velocidad pico del flujo regurgitante transtricuspídeo estima la PSAP sistólica. Valores inferiores a 2,8 cm/s son considerados normales; entre 2,9-3,4 cm/s se considera como valores intermedios y valores > 3,4 cm/s se consideran diagnóstico de hipertensión pulmonar valores gradiente medio transtricuspídeo ≥ 25 mmHg y valor normal presiones menores de 25 mmHg.12
4. Tiempo de pinzamiento aórtico: mayor de 90 minutos o menor igual de 90 minutos.
5. Volumen de sangrado intraoperatorio: ≥ de 500 ml o < de 500 ml.
La información sobre las variables de interés epidemiológico, clínicas, ecocardiográficas y de procedimiento intraoperatorio se obtuvo de las historias clínicas y se introdujo en un formulario de recolección diseñada para ese fin. La hoja de cálculo de Microsoft Office Excel contenía la información primaria, tanto de los casos como de los controles, fue importada con el paquete estadístico SPSS versión 22, con el cual se realizó todo el procesamiento.
Todos los análisis estadísticos se hicieron a dos colas (bilateral) y se consideraron estadísticamente significativos los valores de p < de 0,05, además se realizó el análisis bivariado con los factores de riesgo y se obtuvieron los de mayor relación con la variable dependiente, según los valores de la razón de productos cruzados (Odds ratio) y la significación del estadígrafo de Wald. Para la elaboración del modelo se realizó un análisis de regresión logística binaria multivariada ajustada a la incidencia real, donde la presencia de bajo gasto cardíaco fue considerada como variable dependiente (1- presente, 0- ausente). Para confirmar el rendimiento del modelo pronóstico del bajo gasto cardíaco se realizó una regresión logística binaria.
Se definió de nuevo como variable dependiente la presencia de bajo gasto cardíaco postoperatorio (sí o no), como posible factor el valor del modelo. Se centró el análisis en la significación del estadígrafo de la prueba de Hosmer-Lemeshow para su calibración y en el área bajo la curva ROC para su poder de discriminación; práctica común en la validación y comparación de un conjunto de criterios diagnósticos y pronósticos.10
Se elaboró el modelo predictivo a partir de un estudio de casos y controles, lo que permitió determinar la ocurrencia del evento de salud, dando como salida una ecuación matemática a partir de regresión logística binaria.
Se realizó validación interna por partición de la muestra (data splitting). El conjunto de casos y sus correspondientes controles se dividió en dos grupos de datos, uno con el 70 % para elaborar el modelo (desarrollo) y el otro con el 30 % restante para la validación (prueba).
Los autores declaran su compromiso de confidencialidad y protección de la información recogida durante la investigación. También se solicitó la autorización a la dirección del centro y la aprobación del Comité de Ética de la investigación y del Consejo Científico para la ejecución de la misma.
Resultados
En el estudio se observó que el bajo gasto cardíaco fue más frecuente en pacientes mayores de 65 años, observándose en 34 (60,4 %) mostrando alta significación estadística. Tuvieron antecedentes de diabetes mellitus 44 (26,2 %) con p ≤ 0,05 mostrando asociación significativa en relación con presencia de bajo gasto cardíaco.
El antecedente de diabetes mellitus se observó en 44 (26,2 %) pacientes con p valor ≤ 0,05 mostrando asociación significativa con la presencia de bajo gasto cardíaco. Por otro lado, la presencia de fibrilación auricular como antecedente se presentó en 34 pacientes (20,2 %), siendo la mayoría del grupo de casos con 18 pacientes (32,1 %) con valor p=0,007, obteniéndose alta significación y asociación entre ambas variables. Otras variables presentaron significación estadística tales como; FEVI ≤ 35 % con 26 pacientes para un 15,5 %, FEVD disminuida 19 pacientes (11,3 %); el tiempo de pinzamiento aórtico > de 90 minutos con 50 pacientes (29,8 %); el sangrado peri operatorio y la presencia de cirugía de emergencia con 21(12,5 %) y 76(45,2) pacientes respectivamente; todas presentaron un valor de p ≤ 0,05 y tuvieron asociación causal (Tabla 1).
Tabla 1 Diseño y validación de riesgo de síndrome bajo gasto cardíaco en la cirugía valvular. Análisis bivariado según Grupos. Centro de Cardiología y Cirugía Cardiovascular de Hospital Docente Saturnino Lora. Universidad de Ciencias Médicas. Santiago de Cuba. 2019- 2021
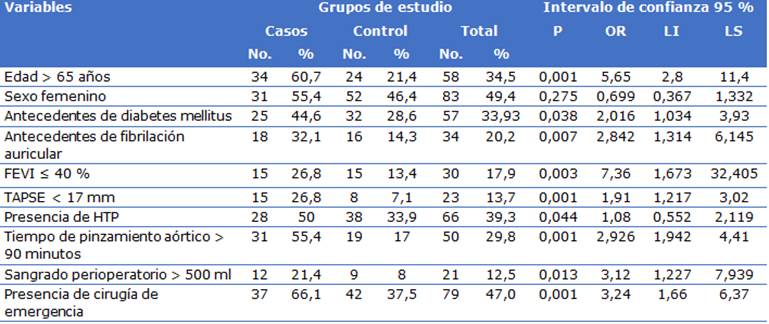
Fuente: Historias clínicas.
Ji cuadrado: p ≤0,05; % por columnas; TAPSE: Excursión Sistólica del Plano Anular Tricúspideo; FEVI: fracción del ventrículo izquierdo; HTP: hipertensión pulmonar; OR: Odds ratio; LI: límite inferior; LS: límite superior.
Como se observó en la tabla, se obtuvo a través de una regresión logística binaria el 77,4 % en la aparición de síndrome de bajo gasto cardíaco en pacientes operados; con sensibilidad de 77,9 % y especificad 74,5 %. Se mostraron valores de p ≤ 0,05 en variables tales como: Edad ≥ 65 años, FEVD, tiempo de pinzamiento aórtico, sangramiento perioperatorio ≥ 90 minutos; por lo cual se concluyó que estas variables tienen una asociación estadísticamente significativa con las complicaciones (Tabla 2).
Tabla 2 Modelo predictivo de síndrome de bajo gasto cardíaco y su ecuación
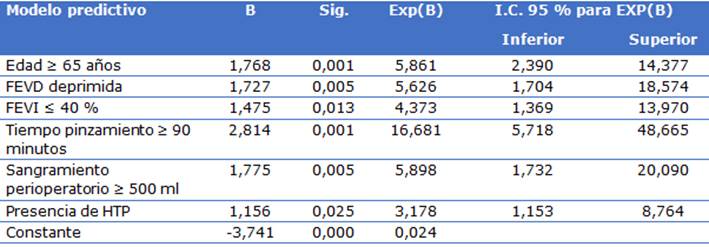
Fuente: Hoja de resultados del IBM SPSS versión 22.0
HTP: hipertensión pulmonar FEVI: función sistólica del ventrículo izquierdo; FEVD: función sistólica del ventrículo derecho. OR = Exp (B).
Se puede decir que el perfil de pacientes que presentan síndrome de bajo gasto cardíaco, se caracteriza por la presencia de una edad ≥ 65 años, FEVD deprimida, tiempo de pinzamiento aórtico mayor o igual 90 minutos y sangramiento perioperatorio mayor o igual a 500 ml. Entonces el modelo de regresión logística ajustado será (Fórmula 1):
Dónde: p es la probabilidad de aparición de síndrome de bajo gasto cardíaco.
Siendo: Z= β0+ β1 X1+… + βkXk
Dónde: β0 y βk son los coeficientes estimados a partir de los datos.
Entonces la fórmula matemática con todos los datos es:
Z= (3,741+1,768 x (edad)+1,727 x (FEVD) +2,814 x (tiempo de pinzamiento aórtico)+1,775 x (sangramiento perioperatorio) + 1,156 x (presencia de HTP) +1,475 x (FEVI); dando paso a la (Ecuación 1).
Ecuación del modelo predictivo de SBGC
Dónde:
X1: Edad mayor o igual a 65 años.
X2: FEVD.
X3: tiempo de pinzamiento aórtico.
X4: sangramiento perioperatorio.
X5: Presencia de HTP.
X6: FEVI.
Este valor de 0,7 nos indica las probabilidades de presentar síndrome de bajo gasto cardíaco con las seis variables del modelo matemático predictivo para un punto de corte de 0,05.
Al evaluar el rendimiento de modelo predictivo, con calibración y capacidad de discriminación. Entre los criterios que se determinaron para evaluar el ajuste del modelo están el R2 de Nagelkerke, cuyo valor de 0,526 explica que alrededor de más del 50 % de la variabilidad de los datos es contemplada por el modelo; y el estadígrafo correspondiente de la prueba de Hosmer-Lemeshow, con valor de 0,674; que al sobrepasar a 0,05 denota una buena calibración (Tabla 3).
Tabla 3 Pruebas estadísticas aplicadas para evaluar rendimiento y calibración del modelo en construcción y validación

Fuente: Hoja de resultados del IBM SPSS versión 22.0.
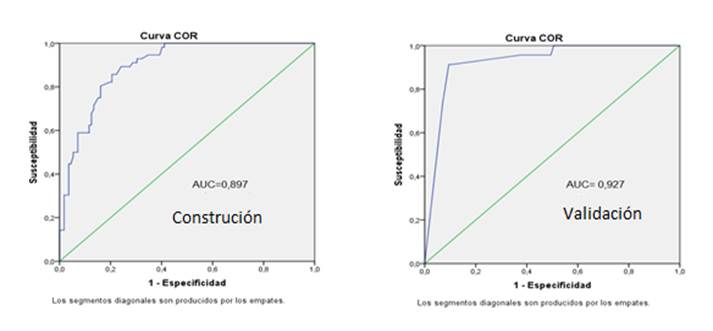
Al analizar el área bajo la curva y la curva operativa del receptor, a partir de la sensibilidad y especificidad, se comprobó que el AUC (área bajo la curva) en el modelo de construcción AUC=0,897 y en el modelo de validación AUC= 0,927; de ahí la capacidad en ambas fase del estudio para predecir el riesgo de síndrome de bajo gasto cardíaco (Figura 1).
Se realizó una validación interna del modelo por el método de data splitting con conjunto de casos y sus correspondientes controles se dividió en dos subconjuntos de datos, uno para elaborar el modelo (entrenamiento) y el otro con para la validación (prueba). Se pudo observar que los porcentajes correctos para ambos subconjuntos son muy parecidos (Tabla 4).
Discusión
Se tuvo en cuenta que variables tales como: edad ≥ 65 años, función de ventrículo derecho deprimida (TAPSE < 17 mm), el tiempo de pinzamiento aórtico ≥ 90 minutos y el sangramiento perioperatorio mayor o igual a 500 ml; en ese punto, Lorenzo,13 en un artículo de revisión refiere que la edad mayor a 65 años es uno de los elementos predisponentes de complicaciones y bajo gasto cardíaco en pacientes con cirugía cardíaca.
Pérez et al.,14 en un estudio multicéntrico publicado en 2018, señalaron la edad de 68,3 ± 9,3 años, como uno de los factores que más se asociaron a la aparición de bajo gasto postoperatorio.
Un estudio realizado por Fernández et al.,15) que incluyó 156 enfermos intervenidos de manera quirúrgica por enfermedades valvulares cardíacas izquierdas en el año 2018, de ellos 46 presentaron bajo gasto cardíaco, predominando en este grupo los pacientes mayores de 65 años. Lo anterior planteado por los diferentes autores citados, coincide con lo mostrado en el estudio.
Los autores consideran que los resultados obtenidos en la investigación pudieran estar relacionados con la mayor prevalencia de las enfermedades cardiovasculares en el sexo masculino, debido a que el sexo femenino hay una reconocida protección hormonal que declina con el climaterio, aunque a nivel mundial existe el consenso de que el sexo no debe ser un factor que altere la toma de decisiones respecto a la realización de un procedimiento quirúrgico.
En la tabla dos muestra el análisis multivariado de regresión logística donde la inclusión de variables independientes fue paso a paso a través del método wald, lo que permitió mitigar el efecto indeseado de la colinealidad y del cual quedó conformado el modelo predictivo concluyente del estudio aquel que conforman las variables: edad ≥ 65 años, función de ventrículo derecho deprimida (TAPSE < 17 mm), el tiempo de pinzamiento aórtico ≥ 90 minutos y el sangramiento perioperatorio mayor o igual a 500 ml; al coincidir en parte con EuroSCORE II; así lo reflejó López et al.16 En cuanto al modelo presentó un punto de corte en 0,5 lo que significa que por encima o igual a esta cifra, su valor predictivo es positivo y por debajo sería negativo.
En la tabla tres se realizó la prueba de Hosmer-Lemenshow, en la fase de construcción mostró una calibración correcta del modelo. 0,674 y en validación 0,571 lo que indica que los modelos posee un buen ajuste a los datos por ser mayor de 0,05. En cuanto a la sensibilidad y especificidad en ambas fases se muestra buen valor predictivo positivo. O sea, que el modelo pronostica muy bien los que van a presentar síndrome de bajo gasto cardíaco; en ese punto Cerda et al.,17 el cual coincide con lo planteado en la investigación.
Se evaluó mediante la curva ROC, que ambos modelos tiene capacidad discriminatoria. Muchos autores utilizan esta herramienta estadística para fines discriminativos tales como; García et al.18 y Toudert.19 Al tener un buen ajuste y capacidad discriminatoria traduciéndose en buen rendimiento del modelo predictivo. Según Boque et al.,20 un AUC superior al 0,70 (70 %) se considera como aceptable la capacidad de discriminación del modelo y buena si es del 0,80 (80 %). En ese mismo aspecto, Carosella et al.,21 en un estudio basado modelo en el ArgenSCORE obtuvo una curva ROC mayor de 0,80 y una adecuada relación entre la mortalidad predicha y la observada lo cual se logra en el estudio en ambos procesos de la investigación.
Se pudo observar que los porcentajes correctos para ambos subconjuntos son muy parecidos y la prueba de Hosmer-Lemeshow para ambos se encontró por encima de 0,5, lo que significa que el modelo se ajusta a los datos de la muestra de entrenamiento y de prueba; coincidiendo con los resultados de Bermúdez et al.22 Según lo referido por Sagaró y Zamora,23 en su investigación que basado en el principio de Parsimonia (el cual plantea que la solución más sencilla que explique por completo un problema es tal vez la correcta), el modelo que se obtenga, derivado de tal análisis debe ser aquel más reducido que explique los datos y que además sea clínicamente congruente e interpretable, al tener en cuenta que un mayor número de variables en el mismo implicará mayor cantidad de errores.
Por último, el estudio tiene algunas limitaciones, un tamaño de muestra pequeño y no evaluar elementos como: función renal preoperatoria y parámetros humorales, tales como: péptido natriurético y creatinina sérica, los cuales pudieran evaluarse en próximas investigaciones, aunque se debe tener en cuenta que los modelos predictivos son una herramienta muy útil en la actualidad, además de constituir el primer paso hacia la obtención de una escala matemática de predicción de riesgo, necesarios en la práctica actual.