Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Vaccimonitor
versión impresa ISSN 1025-028X
Vaccimonitor vol.22 no.1 Ciudad de la Habana ene.-abr. 2013
ARTÍCULO ORIGINAL
Caracterización de conjugados inmunogénicos de polisacárido capsular Streptococcus pneumoniae serotipo 14
Characterization of capsular polysaccharide immunogenic conjugates from Streptococcus pneumoniae serotype 14
Janoi Chang,1* Yohanna Serrano,1 Raine Garrido,1 Jessy Pedroso,1 Felix Cardoso,1 Dagmar García,1 Domingo González,2 Yanelis Herrera,2 Darielys Santana,1 Yury Valdés,1 Violeta Fernández,1† Vicente Vérez1
1Centro de Química Biomolécular. Ave. 21 y 200. Atabey, Playa, La Habana, Cuba.
2Instituto Finlay. Centro de Investigación-Producción de Vacunas y Sueros. Ave. 27 # 19805 La Lisa. La Habana, Cuba. AP 16017 CP 11600.
email:janoi.chang@cqb.cu
* Licenciado en Ciencias Farmacéuticas. Jefe del Dpto. de Glicoconjugación
RESUMEN
Las vacunas conjugadas que consisten en polisacáridos bacterianos unidos a través de un enlace covalente a una proteína portadora, han tenido un gran impacto en los esquemas de vacunación infantil, disminuyendo de forma dramática la incidencia de infecciones bacterianas. En el caso de Streptococcus pneumoniae, a pesar de que se han descrito más de 90 serotipos basados en la estructura de las cápsulas polisacarídicas y que al menos 23 tienen una importancia clínica demostrada, solo un número limitado de siete, o más recientemente 10 y 13, están incluidos en las vacunas conjugadas licenciadas. Por otra parte, la necesidad creciente de estas vacunas en el mundo requiere la incorporación de nuevos productores que se enfrentan a una elevada complejidad tecnológica, pues en todo el procedimiento de conjugación no se pueden afectar las características estructurales por las que el polisacárido es reconocido inmunológicamente. Este trabajo implementó un procedimiento de conjugación para el polisacárido de la cápsula de Streptococcus pneumoniae serotipo 14. El procedimiento comprendió la fragmentación, oxidación peryódica y posterior conjugación del polisacárido a anatoxina tetánica o diftérica. Cada intermedio fue caracterizado por métodos físico-químicos. En todas las reacciones se obtuvieron rendimientos superiores al 50%. Los conjugados generaron altos títulos de anticuerpos específicos de tipo IgG y memoria inmunológica. Se concluyó que el procedimiento permitió la obtención de conjugados inmunogénicos de serotipo 14.
Palabras clave: Streptococcus pneumoniae, vacunas conjugadas, inmunogenicidad.
ABSTRACT
Conjugate vaccines consisting of bacterial polysaccharides linked through a covalent bond to a carrier protein have a major impact on childhood immunization schemes which have dramatically decrease the incidence of bacterial infections. In the case of Streptococcus pneumoniae more than 90 serotypes have been reported, based on the structure of the polysaccharide capsules and at least 23 of them have demonstrated clinical importance. A limited number of 7 or more recently 10 and 13 are included in licensed conjugate vaccines. On the other hand, the increasing need for these vaccines worldwide requires the incorporation of new manufacturers who are facing highly complex technology since the entire conjugation process can not affect the structural features for which the polysaccharide is immunologically recognized. Our paper provides a conjugation procedure for the capsular polysaccharide of Streptococcus pneumoniae serotype 14. The process includes fragmentation, peryodic oxidation and subsequent conjugation to tetanus toxoid or diphtheria toxoid to the polysaccharide, each intermediate was characterized by physico-chemical methods. Yields higher than 50% were obtained in all reactions. The conjugates generated high titers of IgG specific antibodies and immunological memory. In conclusion, the procedure allows immunogenic conjugates of serotype 14.
Key words: Streptococcus pneumoniae, conjugate vaccines, immunogenicity.
INTRODUCCIÓN
Las vacunas conjugadas han significado un paso de avance con respecto a las vacunas de polisacáridos, pues gracias a un enlace covalente entre el polisacárido bacteriano y una proteína portadora, las mismas logran inducir respuesta protectora antipolisacárido en la población infantil y memoria inmunológica (1).
En el diseño del método para obtener una vacuna conjugada es importante tener en cuenta un grupo de parámetros como la talla del polisacárido, la selección de la proteína portadora, el método de conjugación y las propiedades del conjugado que influyen y en algunos casos determinan la inmunogenicidad del producto.
El desarrollo de un procedimiento de conjugación es complejo en la medida en que debe decidirse una combinación propia de cada uno de los elementos anteriores. El rango en que estos parámetros pueden moverse es muy amplio. Por ejemplo, en el caso de Haemophilus influenzae tipo b se puede utilizar desde un polisacárido de alto peso molecular hasta un oligosacárido obtenido por síntesis química (2, 3), cada uno con sus ventajas y desventajas.
En el caso de las vacunas conjugadas contra S. pneumoniae la complejidad adicional viene dada por la necesidad de incluir un número elevado de serotipos en la formulación. De ahí la tendencia de los productores a simplificar los procesos para la obtención de cada uno de los conjugados.
En la actualidad existen tres vacunas conjugadas licenciadas contra S. pneumoniae que incluye a los serotipos 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F y 23F. Las mismas han disminuido la incidencia de la enfermedad en muchos países que las han insertado en sus sistemas de vacunación infantil (4-6), pero la necesidad potencial de más de 300 millones de dosis anuales sigue ampliamente insatisfecha.
Para suplir esa demanda, la UNICEF ha pedido la incorporación de un mayor número de productores (7), por lo que en Cuba se está trabajando desde hace años en un proyecto conjunto entre el Centro de Química Biomolecular y el Instituto Finlay, para la obtención de una vacuna conjugada polivalente contra S. pneumoniae.
En el presente trabajo describimos el proceso de laboratorio para la obtención y caracterización de conjugados del serotipo 14 que servirá de base al desarrollo del proceso industrial.
MATERIALES Y MÉTODOS
El polisacárido capsular de S. pneumoniae serotipo 14 (PS-14), lote 806, y las proteínas portadoras anatoxina tetánica (TT), lote 6017, y anatoxina diftérica (DT), lote 6013, empleadas en la obtención de los conjugados, fueron suministradas por el Instituto Finlay, Centro de Investigación-Producción de Vacunas. Se utilizó como material de referencia PS-14 purificado, proveniente de ATCC. El suero estándar internacional de conejo específico contra S. pneumoniae serotipo 14 fue suministrado por Statens Serum Institute, Copenhagen.
Técnicas analíticas. Los métodos colorimétricos empleados fueron: determinación de carbohidratos totales por orcinol-sulfúrico (8), contenido de proteína por Lowry (9), concentración de grupos carbonilos por el método modificado de Park Jhonson (10).
El análisis estructural del PS-14 se complementó por técnicas de resonancia magnética nuclear (RMN). Las muestras se prepararon disolviendo 10 mg del producto en 0,6 mL de agua deuterada. Después de la total disolución se liofilizaron y luego se disolvieron nuevamente en agua deuterada para el análisis.
La determinación de la constante de distribución de la talla molecular (KD) se realizó por cromatografía de exclusión molecular en una columna TSK 5000 PW con NaCl 0,9%, como fase móvil y detección por índice de refracción para el polisacárido capsular, fragmentado y activado, o detección ultravioleta (206 nm) para los conjugados. Los datos y análisis se realizaron utilizando el software ClarityChrom.
Preparación y caracterización de los conjugados
Fragmentación del PS-14 a tallas entre 30-10 kDa: Se disolvieron 10 mg de polisacárido en 2 mL de agua destilada. A esta disolución se le adicionó la cantidad de ácido trifluoroacético necesaria para alcanzar la concentración definida en el intervalo 250-25 mM.
La mezcla se mantuvo con agitación a 70 oC entre 1,5_2,5 h. Transcurrido este tiempo la reacción se neutralizó utilizando una disolución de hidróxido de sodio 0,1 M. Se purificó por membranas de celulosa regenerada de 30 y 10 kDa de porosidad. Se ultrafiltró contra agua destilada hasta no detectar presencia de carbohidrato en el filtrado.
La eficiencia de la reacción se determinó de acuerdo con el contenido de carbohidrato recobrado en la fracción entre 10 y 30 kDa.
Activación del polisacárido capsular de serotipo 14 fragmentado (PS-14-frag). Se disolvieron 10 mg del PS-14-frag del paso anterior en 2 mL de disolución tampón fosfato salina pH 7,0 y se adicionaron 0,2 mL de disolución de peryodato de sodio (NaIO4) 20 mM. La reacción se mantuvo con agitación en ausencia de luz durante 2 h; luego se detuvo adicionando 0,01 mL de glicerol. Posterior a una incubación de 30 min la mezcla se purificó por ultrafiltración, utilizando membrana de 10 kDa como valor de corte, de forma similar a como se describió.
Conjugación a proteínas portadoras. Se liofilizó a sequedad una mezcla de 7,5 mg del fragmento oxidado (PS-14-ox) y 5 mg de proteína portadora en disolución tampón fosfato salina pH 7,0. Posteriormente se añadió una disolución de cianoborohidruro de sodio de 10 mg/mL.
La reacción se mantuvo con agitación a temperatura ambiente por 72 h. El conjugado resultante se purificó por ultrafiltración, utilizando una membrana de 100 kDa. El porcentaje de proteína no conjugada se calculó por cromatografía de exclusión molecular en una columna Superosa 12, con disolución tampón fosfato salina pH 7,0 como fase móvil a un flujo de 0,5 mL/min y utilizando un detector UV a una longitud de onda de 206 nm.
Inmunogenicidad de los conjugados
En estos experimentos se utilizaron ratones hembras Balb/c de 5 a 6 semanas de edad y conejos blancos Nueva Zelanda de 4 semanas de edad y de sexo femenino, proporcionados por el Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB), adaptados durante 7 días a las condiciones del laboratorio. Los ratones se colocaron en cajas de Macrolon (Panlab, España), se mantuvieron con humedad y temperatura controlada entre 22-24 ºC, con sistema de 12 h de luz y 12 de oscuridad. En el caso de los conejos fueron mantenidos en un local abierto en condiciones ambientales.
Todo el trabajo estuvo sujeto al más estricto cumplimiento de las normas éticas en la experimentación animal, regidas por guías éticas para la investigación con animales de laboratorio. Los protocolos experimentales fueron aprobados por el Comité de Ética y el Departamento de Calidad del Centro de Química Biomolecular, de La Habana.
Grupos de 10 ratones Balb/c y de 5 conejos blancos Nueva Zelanda se inmunizaron a los 0, 14 y 28 días por vía subcutánea y se tomaron muestras de sangre 7 días después de cada inmunización. Las dosis (contenido de carbohidrato) fueron de 2 µg y 5 µg, respectivamente.
En uno y otro diseño se incluyeron como controles: un grupo inmunizado con 25 µg de PS-14 y otro con suero fisiológico. Además, los conejos recibieron una dosis de refuerzo de 25 µg de PS-14 a los 120 días después de la primera inmunización; luego se realizó la extracción según fue descrito. Los sueros fueron separados por centrifugación y almacenados a -20 °C para la titulación del contenido de anticuerpos (Ac) isotipo IgG antipolisacárido serotipo 14.
Títulos de Ac isotipo IgG contra el PS-14 mediante ELISA
Se recubrieron placas de 96 pocillos de poliestireno (Maxisorp) con 50 µL/pocillo de una disolución de PS-14 (10 µg/mL) en disolución tampón fosfato salina pH 7 y se incubaron durante toda la noche a 37 ºC. Se bloqueó adicionando 100 µL/pocillo de disolución de albúmina de suero bovino al 1%. Después de incubar a 37 ºC durante 30 min se adicionaron diluciones seriadas 1/2 de los sueros comenzando por 1/100 en disolución tamponada fosfato salina pH 7,2 (BSA 1%; EDTA 0,01 M, Tween-20 0,3%) y se incubó durante 90 min a temperatura ambiente. Luego se adicionó el correspondiente anti-IgG conjugado a la enzima peroxidasa utilizando una dilución de trabajo de 1:15 000 para ratones y 1:10 000 para conejo y se incubó durante 90 min a temperatura ambiente. Se adicionó 100 µL/pocillo de orto-fenilendiamina 0,5 mg/mL en disolución citrato (Na2HPO4 52 mM y ácido cítrico 25 mM, pH 5,6) y se mantuvo la placa en la oscuridad durante 20 min.
Se detuvo la reacción adicionando HCl 3 M, se leyó la densidad óptica (DO) a una longitud de onda de 492 nm en un lector de ELISA. Al final de cada incubación se realizó el lavado de las placas con disolución tampón fosfato salina pH 7,2, Tween 20 al 0,05%.
El cálculo del título de Ac isotipo IgG se realizó mediante un análisis de regresión entre los valores de DO y el logaritmo en base a 10 del recíproco de la dilución del suero. Se consideró como criterio de selección de los animales respondedores un incremento mayor del doble del valor de DO, con respecto al valor del preinmune (t=0).
ELISA de inhibición para especificidad
Por otro lado, se evaluó la especificidad de los Ac isotipo IgG generados por los conjugados en los modelos animales. Los sueros obtenidos, luego de la tercera dosis, se preincubaron durante toda la noche a 4 oC con concentraciones conocidas de PS-14. El procedimiento se realizó igual al descrito anteriormente. Los resultados se muestran como porcentaje de inhibición, el cual se calculó según la siguiente fórmula: [DO (sin inhibidor)-DO (con inhibidor)] /DO (sin inhibidor) X 100.
Antigenicidad por método ELISA
El suero estándar internacional contra el PS-14 (1:6400) se preincubó con diferentes concentraciones del PS-14-frag y PS-14-ox en un rango de 500 µg/mL hasta 0,05 µg/mL durante toda la noche, a 4 ºC. Luego en placas recubiertas con PS-14 se desarrolló el ELISA. El procedimiento y los resultados se realizaron como ya fue descrito.
En el caso de la evaluación de la antigenicidad en los conjugados, las placas se recubrieron con 50 µL de los conjugados (PS-14-TT y PS-14-TD) en disolución tampón fosfato salina pH 7,0, a una concentración de 1 µg/mL y el PS-14 a 10 µg/mL como control y se incubaron durante toda la noche a 37 ºC. El procedimiento continuó como se describió para medir el título de anticuerpos IgG anti PS-14, pero utilizando el suero estándar internacional contra el PS-14 (1:6400).
Análisis estadístico
Las diferencias en la respuesta de Ac isotipo IgG anti PS-14 entre los distintos grupos experimentales fueron evaluadas utilizando la prueba de Kruskal Wallis y la prueba de Dunn´s. Las diferencias se consideraron significativas para p = 0,05. El procesamiento estadístico de los datos de todos los experimentos se realizó con el programa GraphPad Prism, versión 4.00.
RESULTADOS Y DISCUSIÓN
Fragmentación del PS-14
El primer paso de nuestro trabajo consistió en la confirmación de la identidad por RMN, utilizando como referencia un PS-14 (proveniente de una cepa ATCC). En el espectro se identificaron las señales correspondientes a los cuatro protones anoméricos de la unidad repetitiva (UR) en d 4,62 ppm, d 4,46 ppm, d 4,35 ppm, d 4,19 ppm y la correspondiente al CH3 del grupo N-acetamido en d 1,94 ppm, coincidiendo con lo reportado por Lindberg y col, 1977 (11). Este espectro sirvió como referencia para evaluar la conservación de la estructura en las diferentes etapas de modificación del PS-14.
La disminución de la talla molecular de los polisacáridos se utiliza como estrategia para reducir los problemas de solubilidad de los polisacáridos de alto peso molecular y, además, para facilitar la purificación del producto final durante el procedimiento de conjugación (12, 13). Como norma los productos finales para los cuales se emplea un fragmento del polisacárido son más definidos molecularmente (14). Entre los procesos de fragmentación, la hidrólisis ácida es un método muy empleado, pues tiene como ventaja ser reproducible y barato.
Se estudió la hidrólisis con ácido trifluoroacético y se encontró que 25 mM mostró el mayor recobrado de carbohidrato (95%) en la fracción 30-10 kDa (Tabla 1). Estas condiciones se repitieron y mostraron consistencia, promediando un recobrado de 91% y similar KD en todos los casos (Tabla 2).
El espectro del producto PS-14-frag se caracterizó por señales con mayor resolución, lo cual es de esperar al reducirse la talla del PS-14. Por otra parte, el espectro coincidió con el del PS-14 de referencia y se corroboró que no hubo afectación de la estructura de la UR (Fig. 1 A, B y C). Estos fragmentos inhibieron al 100% un suero estándar internacional de conejo contra PS-14, mostrando curvas de inhibición similares a la obtenida contra el PS-14, lo que confirma la conservación de la antigenicidad del PS (Fig. 2). La conclusión de este análisis fue que los fragmentos obtenidos por este procedimiento pueden utilizarse como antígenos para obtener conjugados inmunogénicos.
Oxidación del PS-14-frag con peryodato de sodio
La oxidación de PS-14-frag con NaIO4 generó entre 0,12-0,16 mol de carbonilo por mol de unidad repetitiva, con rendimientos de recobrado de carbohidrato luego de la purificación, superiores al 80% (Tabla 3). La KD determinada en columna TSK 5000 del PS-14-frag de partida y el PS-14-ox fueron de 0,40 y 0,42, lo que indica que no hay una afectación significativa de la talla molecular. El sitio más probable a ser oxidado con peryodato en la estructura de la UR de PS-14 es la ramificación b-D-Gal, según lo reportado por Kim y col (15). Este sustituyente es esencial porque forma parte del epítope del PS-14 (16), por lo que la oxidación debe ser controlada para no afectar la densidad de epítopes. La conservación de la antigenicidad de los productos oxidados a través de un ELISA de inhibición no mostró diferencias entre las curvas de inhibición obtenidas para el PS-14-ox, PS-14-frag y PS-14 (Fig. 2), lo que indica que el PS-14-ox mantiene suficientes residuos laterales b-D-Gal intactos para conservar su antigenicidad.
Conjugación de los PS-14-ox a las proteínas TT y TD
La reacción de conjugación ocurre entre los grupos aldehídos generados en el PS-14-ox y los grupos å aminos de las lisinas presentes en la proteína. Los conjugados obtenidos, tanto a la anatoxina tetánica (PS-14-TT) como diftérica (PS-14-DT), presentaron incorporación de carbohidrato de 73% para DT y 94% para TT, lo que resulta superior a los reportados en la literatura (17) (Tabla 4).
Esto puede ser atribuido a la coliofilización de la mezcla PS-14-ox y la proteína que favorece la primera etapa de formación de la imina (18) y a que los grupos carbonilos generados en el residuo lateral b-D-Gal están menos impedidos estéricamente.
Los conjugados mostraron perfiles con picos homogéneos en ambos casos, con relaciones carbohidrato: proteína y KD típicas de los conjugados (especies de mayor talla molecular) en correspondencia con la proteína empleada en cada caso (Tabla 4). Adicionalmente, el por ciento de proteína no enlazada fue menor al 5% en ambos casos.
Por otro lado, ambos conjugados son reconocidos por el suero estándar internacional anti-PS-14 (Fig 3), lo cual indica que el proceso de conjugación no afectó la antigenicidad del mismo.
Respuesta inmune en ratones y conejos
Con el objetivo de evaluar la capacidad de los conjugados de inducir anticuerpos específicos al PS-14 se inmunizaron ratones y conejos. Los títulos de IgG contra PS-14 en ratones Balb/c aumentó significativamente luego de la segunda inmunización (Fig 4) y se mantuvo hasta la tercera dosis, con un 100% de animales respondedores. Además, estos títulos de IgG fueron superiores significativamente a los medidos para el grupo control inmunizado con PS-14. En el modelo de conejo, donde solo se evaluó el conjugado PS-14-TT, se encontraron altos títulos de IgG contra el PS-14 desde la primera dosis, los cuales aumentaron con cada inmunización (p<0,05). Además, los títulos de IgG siempre fueron superiores a los obtenidos en el grupo control (Fig. 5). Los títulos de anticuerpos generados disminuyeron hasta alcanzar los niveles del grupo control a los 4 meses (Fig. 5). En ese momento se inmunizó una dosis de PS-14 que había demostrado ser poco inmunogénico, según los resultados obtenidos para el grupo control.
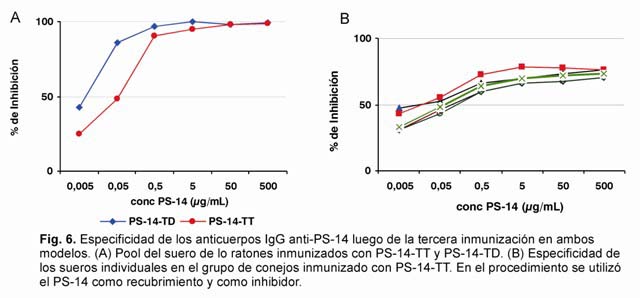
El incremento sustancial de los títulos provocados con esta inmunización con PS-14, sugieren la existencia de memoria inmunológica contra el PS-14 inducida por los conjugados. Los Ac isotipo IgG obtenidos, luego de la tercera dosis en ambos modelos, mostraron ser específicos por el PS-14 evaluado en un ELISA de inhibición (Fig. 6 A y B).
Como conclusión, se puede afirmar que por este procedimiento es posible preparar candidatos vacunales para S. pneumoniae serotipo 14, que tienen la capacidad de generar una potente respuesta T-dependiente, la cual se caracteriza por Ac isotipo IgG contra el PS-14 en ratones y conejos. Esta se corresponde con lo reportado para otros conjugados carbohidrato-proteína (19). Además, nuestro procedimiento puede servir como plataforma para la obtención de otros candidatos necesarios para la formulación multivalente contra Streptococcus pneumoniae.
REFERENCIAS
1. Greenberg DP, Vadheim CM, Partridge S, Chang SJ, Chiu CY, Ward JI. Immunogenicity of Haemophilus influenzae Type b Tetanus Toxoid Conjugate Vaccine in Young Infants. J Infect Dis 1994;170(1):76-81.
2. Schneerson R, Barrera O, Sutton A, Robbins JB. Preparation, characterization, and immunogenicity of Haemophilus influenzae type b polysaccharide-protein conjugates. J Exp Med 1980;152(2):361-76.
3. Vérez-Bencomo V, Fernández-Santana V, Hardy E, Toledo ME, Rodríguez A, Baly A, et al. A synthetic conjugate polysaccharide vaccine against Haemophilus influenzae type b. Science 2004;305:522_5.
4. García S, Levine OS, Cherian T, Gabastou JM, Andrus J, Working Group members. Pneumococcal disease and vaccination in the Americas: an agenda for accelerated vaccine introduction. Rev Panam Salud Pública 2006;19(5):340_8.
5. Vestrheim DF, Høiby EA, Aaberge, Caugant DA. Impact of a Pneumococcal Conjugate Vaccination Program on Carriage among Children in Norway. Clin. Vaccine Immunol 2010;17(3):325-34.
6. Kellner JD. Canadian Paediatric Society, Infectious Diseases and Immunization Committee. Update on the success of the pneumococcal conjugate vaccine. Paediatr Child Health 2011;16(4):233-6.
7. WHO. Target Product Profile (TPP) for the Advance Market Commitment (AMC) for Pneumococcal Conjugate Vaccines. Geneva: WHO; 2008.
8. Bruckner J. Estimation of monosaccharides by the orcinol-sulfuric acid reaction. Biochemical Journal 1995;60:200-5.
9. Lowry OH, Rosebrough NJ, Farr AL, Randall RJ. J Biol Chem 1951;193:265-75.
10. Porro M, Vitti S, Antoni G, Neri P. Modifications of Park-Johnson ferricyanide submicromethod for the assay of reducing groups in carbohydrates. Anal Biochem 1981;118:301-6.
11. Lidenberg BJ, Lonngren D and Powell A. Structural studies on the specific type 14 pneumococcal polysaccharide. Carbohydr Res 1977;58:177-86.
12. Craig A, Ramesh K, Muys JM, Francis M, Harold J. Streptococcus pneumoniae Type 14 Polysaccharide-Conjugate Vaccines: Length Stabilization of Opsonophagocytic Conformational Polysaccaride Epitopes. Infect Immu 1998;66:2441-6.
13. Biemans RL, Garcon NM, Hermand PV, Poolman J, Van Mechelen MP. Pneumococcal polysaccharide conjugates vaccine. Patent 12,097,303. 2009 june 15.
14. Wang JY, Chang AH, Guttormsen HK, Rosas A, Kasper D. Construction of designer glycoconjugate vaccines with size-specific oligosaccharide antigens and site-controlled coupling. Vaccine 2003;21:1112-7.
15. Kim JS, Laskowich ER, Michon F, Kaiser RE, Arumugham RG. Monitoring activation sites on polysaccharides by GC_MS. Anal Biochem 2006;358(1):136-42.
16. Safari D, Dekker HAT, Joosten JAF, Michalik D, Carvalho de Souza A, Adamo R, et al. Identification of the Smallest Structure Capable of Evoking Opsonophagocytic Antibodies against Streptococcus pneumonia Type 14. Infect Immun 2008;76:4615_23.
17. Che-Hung RL, Frasch CE. Polysaccharide-Protein Conjugate Vaccine. US patent 10, 566,899. 2007 jun 21.
18. Guo Z, Jennings H. Protein-Polysaccharide Conjugation. In: Pollard AJ, Maiden MCJ, eds. Meningococcal Vaccines. Methods and Protocols. Totowa, NJ: Human Press Inc; 2001. p. 49-54.
19. Moreno RL, Sampson JS, Romero-Steiner S, Wong B, Johnson SE, Ades E, et al. A murine model for the study of immune memory in response to pneumococcal conjugate vaccination. Vaccine 2004;22:3069-79.
Recibido: Agosto de 2012
Aceptado: Septiembre de 2012