INTRODUCCIÓN
En Cuba, la tasa de morbilidad por diabetes fue de 62,2 por cada 1 000 habitantes en 2017 y el número de personas tributarias a una amputación se estima en unos 1 500-3 000.1 En 2016, se trataron 49 242 pacientes cubanos con un índice de amputación de 1,68 %.1
El medicamento Heberprot-P®, Producido por el Centro de Ingeniería Genética y Biotecnología (CIGB) de Cuba, se egistró en 2006 y es usado en el país para el tratamiento de las úlceras del pie diabético (UPD).2,3 Hasta la fecha, cerca de 350 000 pacientes con UPD, en 26 países han recibido sus beneficios como parte del “Programa de Atención Integral al Paciente con UPD con el uso del Heberprot-P”.4 Esta terapia, relativamente nueva, permite un menor tiempo de tratamiento para obtener como respuesta granulación y epitelización en este tipo de lesiones.5
El riesgo relativo de sufrir una amputación ha sido reducido en 78 % de los pacientes a los cuales el Heberprot-P se les aplica, lo cual repercute directamente con la calidad de vida de los pacientes diabéticos ya que las amputaciones provocan discapacidad y dependencia, junto a trastornos psíquicos y emocionales.2
Las imágenes fotográficas de la UPD estandarizadas con el uso del marco estereotáxico FrameHeber 03®,6 producido por el Centro de Ingeniería Genética y Biotecnología (CIGB) de Cuba, permiten hacer evaluaciones cuantitativas, por Ej: medir el área de una úlcera y evaluar su cicatrización), de este y otros tratamientos.
En Cuba, la medición del área de los tejidos de la UPD se hace manualmente o de forma semiautomática.7 No existe software cubano, registrado hasta el momento, que automáticamente realice la medición de las áreas de la lesión para conocer el estado de la UPD antes y después del tratamiento.
El problema a resolver es complejo debido a las variadas formas de las úlceras y su posición en el pie, no necesariamente plana y que puede abarcar varias zonas del pie.8
El objetivo de esta investigación es comparar cualitativamente (dada la ausencia de una regla de oro) métodos de preprocesamiento y segmentación para la evaluación de la cicatrización por planimetría, y no volumétrica, mediante imágenes fotográficas de la UPD.
MÉTODOS
El presente estudio es descriptivo y transversal. Se incluyeron 6 pacientes diabéticos que asistieron al Servicio de Angiopatía Diabética del Instituto Nacional de Angiología y Cirugía Vascular (INACV) durante octubre de 2018, con lesiones de grado I-IV en la escala de Wagner.9
Se utilizó el marco estereotáxico para extremidades FrameHeber03®6 para obtener imágenes planimétricas de las úlceras de los pacientes, en momentos diferentes del tratamiento con Heberprot-P. Se obtuvieron en total 51 imágenes tomadas con una cámara SONY acoplada al FrameHeber, modelo DSC W710, de 16,4 megapíxeles y con una resolución de 4608×3456.
El FrameHeber estandariza el proceso de toma de imágenes con la existencia de una referencia posicional del miembro lesionado con una UPD y permite que todas las imágenes se tomen a la misma distancia.
Preprocesamiento
Se convirtieron las imágenes de color a escala de grises y estas fueron preprocesadas con el algoritmo ransformada Wavelet Discreta Logarítmica, dentro de un modelo S-LIP (TWDL). 10,11 Esta transformada se aplicó a las imágenes y permitió obtener información sobre el contraste local.12
En general, los algoritmos basados en wavelet tienen tres etapas. Primero, la imagen descompone en coeficientes de aproximación y de detalles horizontales, verticales y diagonales. En el segundo paso, los coeficientes se modifican, y como paso final, se aplica la Inversa de la Transformada Discreta Wavelet (ITWDL) para obtener la imagen mejorada.
A estas imágenes preprocesadas se les aplicaron los algoritmos de segmentación que se describen a continuación.
Segmentación
El algoritmo de segmentación Chan-Vese13permite obtener el borde de objetos en una imagen cuyos límites no están definidos claramente. Se basa en conjuntos de niveles que se generan iterativamente para minimizar la energía, que se define por valores ponderados correspondientes a la suma de diferencias de intensidad del valor promedio fuera de la región segmentada, la suma de diferencias del valor promedio dentro de la región segmentada y un término que depende de la longitud del límite de la región segmentada.
El algoritmo de segmentación GrabCut 14) requiere del usuario que enmarque la región de interés (ROI, por sus siglas en inglés) en una región rectangular. Luego, el algoritmo obtiene la segmentación de la úlcera. La región marcada se puede seguir modificando manualmente.
Los Modelos de Mezclas Gaussianas15 (GMM, por sus siglas en inglés) pueden ser utilizados como métodos de agrupamiento. Estos se basan en la suposición de que cada grupo d-dimensional en un conjunto de datos puede ser modelado como una distribución normal multivariada (Gaussiana). Por consiguiente, el conjunto de datos completo podrá ser modelado como una mezcla de cada una de estas gaussianas. Este algoritmo16 busca la ROI tomando como referencia el punto medio de la imagen.
RESULTADOS
Dada la poca cantidad de imágenes de que se disponen y la ausencia de una regla de oro (bordes de las úlceras anotados por expertos que permiten una comparación cuantitativa sistemática entre algoritmos para la detección automática de bordes de UPD, permitiendo conocer cuál de estos es el más adecuado, según cierta fórmula matemática), se realizó una comparación cualitativa de los algoritmos, respecto a la apreciación visual y la opinión de los autores. No se cuenta hasta el momento con una base de datos de imágenes anotadas con la que se puedan hacer estas comparaciones.
Los métodos usados en esta investigación se implementaron en el lenguaje de programación Python17 y se utilizó OpenCV18 para algunas tareas del procesamiento de las imágenes.
Todas las imágenes fueron convertidas a escala de grises para su procesamiento. Dada la iluminación no homogénea en las imágenes fue necesario un preprocesamiento para mejorar su calidad. Se usó la TWDL dentro de un modelo S-LIP.
El algoritmo Chan-Vese funcionó mejor cuando la piel del pie del paciente fue negra que cuando la piel fue blanca o clara, pues se resalta más el contraste y el algoritmo logra detectar mejor la úlcera. Este algoritmo fue sensible a la presencia de brillo y sombras propias de las condiciones no uniformes de iluminación de las imágenes.
Al igual que el algoritmo Chan-Vese, GrabCut fue sensible a los brillos y sombras y funcionó mejor en color negro de piel, pues hay mayor contraste entre la herida y la piel sana. De los métodos probados para hallar la ROI, GrabCut resultó el que mejores resultados visuales obtuvo, según los autores.
En el caso de GMM, los resultados fueron mejores que los de Chan-Vese. El método de GMM se le debe de cambiar el punto de referencia del que parte el algoritmo para segmentar, que es el centro de la úlcera, pues la mayoría de las UPD no son concéntricas y la segmentación puede no dar buenos resultados.
Teniendo en cuenta estos resultados, se decidió aplicar un preprocesamiento a las imágenes mediante TWDL en un modelo S-LIP y se ejecutaron nuevamente los algoritmos de segmentación descritos.
Los resultados obtenidos por el algoritmo Chan-Vese no fueron adecuados. El método GrabCut obtuvo buenos resultados en las imágenes preprocesadas, aunque este método es supervisado, es decir, el médico debe seleccionar una región inicial donde debe estar contenida la UPD que se desea segmentar. La figura 1 muestra el resultado de la segmentación con GrabCut luego del preprocesamiento con el modelo S-LIP, y puede observarse que se obtuvo una ROI casi perfecta. En la figura 2 se aplicó TWDL y se observa también un buen resultado.
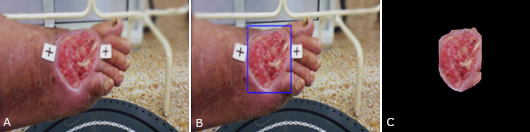
Fig. 1 Resultado de preprocesar con filtro S-LIP y segmentar con el algoritmo GrabCut: (A) imagen original, (B) imagen preprocesada, y (C) resultado de la segmentación. Foto de los autores.
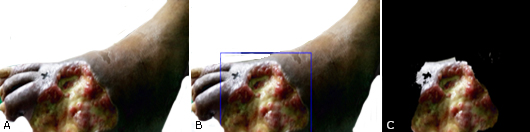
Fig. 2 Resultado de preprocesar con TWDL y segmentar con el algoritmo GrabCut: (A) imagen original, (B) imagen pre-procesada, y (C) resultado de la segmentación. Foto de los autores
Al preprocesar y luego segmentar con GMM no siempre se obtuvieron buenas segmentaciones. Las ROI detectadas, en casi todos los casos, dieron resultados mucho menos favorables que en el caso de la imagen sin preprocesar, incluso en las úlceras de personas de piel negra como se muestra en la figura 3.

Fig. 3 Imágenes procesadas con GMM, divididas en el siguiente orden de izquierda a derecha. (A) Imagen original, (B) ROI, (c) detección de las zonas amarillas según el algoritmo. Foto de los autores.
Debido a que los resultados anteriores no fueron los esperados, se decidió aplicar el filtro wavelet dentro del modelo S-LIP a las mismas imágenes y probar nuevamente. Como se ve en la figura 4, el algoritmo GMM obtuvo mejores resultados en la detección de la ROI una vez aplicado el modelo S-LIP junto con TWDL. Se puede apreciar cómo aquí se detecta la ROI de manera casi perfecta. En el caso de la detección de esfacelos,8)A hay que realizar ajustes en el algoritmo, pues solo se detectó correctamente en 13,7 % de los casos.

Fig. 4 Imágenes procesadas con GMM: (A) Imagen original, (B) ROI y (C) detección de las zonas amarillas. Foto de los autores.
Con estos resultados dedujimos que es necesario aplicar filtros a las imágenes que se deseen procesar para hallar la ROI, de preferencia TWDL con modelo S-LIP y métodos de segmentación para que estas obtengan de forma automática.
En el cuadro se muestra una comparación entre dos de los métodos del estado del arte y todos los analizados y expuestos anteriormente.
Cuadro Comparación de métodos del estado del arte y los métodos estudiados
| Métodos | Ventajas | Desventajas | Limitantes |
|---|---|---|---|
| Goyal et al.(10, 11) | Mejor precisión en selección de ROI | Requieren regla de oro con gran volumen de imágenes de UPD | No se cuenta todavía con regla de oro para las imágenes obtenidas |
| García-Zapirain et al.(9) | Mejor precisión en selección de ROI | No existe código o manual para su implementación y posterior prueba con las imágenes de este estudio | Aún en fase experimental |
| Métodos propuestos | Están disponibles en librerías reconocidas y se tiene código fuente | No detectan la ROI de forma precisa para toda la úlcera | Se necesitan más imágenes para construir una base de datos anotada y obtener resultados más fiables |
DISCUSIÓN
A continuación, se citan algunas de las formas de segmentación que se han estudiado en la literatura científica actual. En el año 2017, García-Zapirain y otros 19utilizaron técnicas de procesamiento de imágenes para segmentar las úlceras a partir de imágenes a color. Para minimizar el tiempo de ejecución del algoritmo, la ROI se identifica automáticamente según cambios de contraste. En este punto, se utiliza la frecuencia sintética de la intensidad, basándose para ello en cada píxel, la cual se calcula utilizando la energía del campo para describir la relación entre la intensidad de los píxeles.
La apariencia visual de la imagen observada es modelada por una Combinación Lineal del Modelo Discreto Gaussiano (LCDG, por sus siglas en inglés). Con el objetivo de estimar la probabilidad marginal de distribución de las tres clases de tejidos principales para la ROI en escala de grises. Luego, la probabilidad de la aparición de los píxeles de estas tres clases de clasificación para la ROI de la imagen a color, se calcula usando la imagen a color que se tiene previamente en la base de datos de imágenes segmentadas manualmente. Finalmente, para preservar la continuidad, las etiquetas se refinan y se normaliza usando el modelo generalizado de campo aleatorio de Gauss-Markov (GGMRF, por sus siglas en inglés).
En el año 2017, Goyal y otros,20) usaron Redes Neuronales Convolucionales para la clasificación de la UPD. Se propuso una arquitectura de red neuronal convolucional denominada DFUNet, que logra extraer, de manera más adecuada, características para identificar las diferencias entre la piel sana y la piel de la lesión.
Estos autores, además,21) introdujeron una base de datos de 705 imágenes que contienen UPD y proveen una regla de oro de la región de la úlcera. Además, propusieron un modelo de entrenamiento para una red convolucional completa (FCNs, por sus siglas en inglés) para segmentarla automáticamente. El modelo propuesto utiliza el coeficiente de similitud Dice de 0,794 (± 0,104) para la región de la úlcera, 0,851 (± 0,148) para la región que rodea la piel y 0,899 (± 0,072) para la combinación de las dos regiones. Esto demuestra la potencialidad de las FCNs en la segmentación de las UPD. El coeficiente Dice es utilizado para comparar la similitud de dos muestras, QS= 2C/A+B donde A y B son el número de especies en las muestras A y B, respectivamente, y C es el número de especies compartidas por las dos muestras; QS es el cociente de similitud y varía de 0 a 1.
Otras técnicas de segmentación utilizan la intensidad o variedad del color, por ejemplo, en dependencias espaciales entre arreglos MRI de elementos cerrados,22 o la entropía de imagen,23 ambas enfocadas en el objetivo de obtener el borde de la imagen. Otro estudio es el de Wannous y otros,24 para segmentar el área de la herida. Dicha investigación se basa en la combinación de segmentación no supervisada y aprendizaje automático, pero, a pesar de los buenos resultados en la práctica, no es factible debido a sus altos requerimientos computacionales.
En este estudio se abordó el problema de la segmentación de la UPD. Esta tarea hace posible la determinación del borde de la úlcera basándose en algoritmos y técnicas matemáticas, y permitiría la medición automática del área de la lesión. La observación del estado del área de la lesión permite evaluar el proceso de cicatrización de las úlceras durante un tratamiento. El software Image-J25 es actualmente el que provee una solución semiautomática. Una solución automática del problema sería lo recomendado en este caso, y lo que se propone en esta contribución, pues se evitarían los errores de imprecisión que puedan comentar los especialistas al hacer las mediciones manualmente.
Como resultado de los análisis preliminares que se han realizado con las imágenes que actualmente se tienen, se obtuvo que el mejor método es el semiautomático GrabCut, pero este no es factible para nuestro estudio ya que se desea un algoritmo automático que logre dar solución al problema. Por otra parte, se debe aplicar filtro a las imágenes para obtener mejores resultados; según las pruebas que se han hecho hasta el momento, se sugiere S-LIP.
La investigación presentada en esta contribución tiene limitaciones: el número de imágenes de UPD es relativamente pequeño y en las imágenes que se obtuvieron no están marcados los bordes de las UPD (no se tiene regla de oro), lo que no permite medir la efectividad de los algoritmos de segmentación que determinan automáticamente el borde de las úlceras. Por esta razón, y como primera aproximación al problema de segmentar UPD, se decidió hacer una evaluación cualitativa basada en la apreciación de los autores.
Aunque los resultados que aquí se exponen no son definitivos, se puede concluir que el algoritmo de segmentación automática GMM puede incluirse en un software para medir el área de la úlcera.
Por ello, se recomienda hacer nuevamente la experimentación cuando se disponga de un mayor volumen de imágenes anotadas de UPD de pacientes cubanos, y profundizar en la mejora del contraste de imágenes de pacientes con piel blanca, así como probar y comparar estos resultados con otros algoritmos de segmentación.














