Introducción
Hace medio siglo, disciplinas como la farmacovigilancia y la tecnovigilancia surgieron en el mundo ante la necesidad de garantizar la seguridad de los medicamentos, las vacunas y los dispositivos médicos disponibles en el mercado global. Estas disciplinas entran en acción desde las fases de investigación y desarrollo de los productos para la salud, hasta que se comercializan. Su finalidad es preservar y proteger la salud del paciente junto con la seguridad de los productos.1 Los sistemas sanitarios establecieron métodos para detectar y evitar reacciones adversas a los medicamentos y los ensayos clínicos constituyen la metodología que utiliza la farmacología clínica para evaluar la eficacia y seguridad de un tratamiento o intervención en seres humanos.
En los últimos años, el uso de surfactantes pulmonares exógenos se ha convertido, junto a otras medidas terapéuticas, en un tratamiento de elección en diversas afecciones respiratorias, donde se destaca la enfermedad de membrana hialina (EMH), el síndrome de dificultad respiratoria aguda (SDRA), neumonía, asma bronquial, asfixia del neonato, por lo tanto, se encuentran entre los medicamentos más evaluados. En particular, el SDRA es un problema potencialmente mortal, se caracteriza por daño pulmonar inflamatorio difuso que abarca el endotelio capilar, el epitelio alveolar y el intersticio; el incremento de la permeabilidad, el exudado inflamatorio y la fibrosis desorganizada conducen a una hipoxemia severa y progresiva.2
El surfactante pulmonar más utilizado en Cuba es Surfacen®; existen evidencias científicas que demuestran la eficacia3,4,5 y seguridad6,7,8 de este medicamento en el tratamiento de diferentes afecciones respiratorias en neonatos y adultos; en niños con SDRA la administración de Surfacen®, mejoró la oxigenación y aumentó la supervivencia; sin embargo, no hay reportes de la seguridad del tratamiento en este grupo etario.
El objetivo de esta investigación es demostrar la seguridad del tratamiento con Surfacen® en el SDRA en niños.
Materiales y Métodos
Diseño de la investigación
Se realizó un Ensayo clínico fase III, multicéntrico (unidades de cuidados intensivos pediátricos (UCIP) de los hospitales “Juan Manuel Márquez”, en La Habana, “Eduardo Agramonte Piña”, de Camagüey, “José Luis Miranda”, en Villa Clara, “Octavio de la Concepción y la Pedraja”, de Holguín, “Mártires de las Tunas”, en las Tunas, Infantil Norte e Infantil Sur, de Santiago de Cuba, abierto, controlado y aleatorizado con dos grupos de tratamiento (A y B). El protocolo de ensayo clínico está disponible en: https://rpcec.sld.cu/ensayos/RPCEC00000163-Sp. La inclusión de pacientes se ejecutó durante 33 meses (noviembre 2010 - agosto 2013).
Intervención
En el Grupo A, se incluyeron los niños a los que se les practicó tratamiento convencional de oxigenación y ventilación mecánica combinado con Surfacen® en dosis de 100 mg cada ocho horas durante tres días. En el Grupo B, los niños recibieron tratamiento convencional. Se realizó la evaluación de estas variables al momento de la inclusión y posterior a cada administración de surfactante en el grupo A y en el grupo B con igual frecuencia.
Criterios de selección de los sujetos
Pacientes entre 28 días de nacido y 18 años de edad, ambos inclusive, cuyos padres o tutores dieron su consentimiento por escrito de participación en el estudio; de cualquier sexo, residentes en Cuba, que cumplieran con los criterios diagnósticos SDRA,2 atendidos en las UCIP de las instituciones participantes. Se excluyeron los que tenían enfermedades oncohematológicas y cardiopatías congénitas.
Finalmente se incluyeron 42 pacientes: 20 en el grupo A y 22 en el grupo B.
Variables de estudio
Aparición de eventos adversos (EA), (desde el momento que se incluyó el paciente en el estudio hasta su egreso de la UCIP), tipo de EA, intensidad del EA (leve, moderado, severo), actitud seguida ante la aparición del EA (sin cambios, modificación de la dosis, interrupción temporal, interrupción definitiva), resultado del EA (recuperado, mejorado, persistente, secuelas), relación de causalidad (remota, posible, probable, muy probable), mortalidad al día 28. Estas se analizaron según los requerimientos para la notificación y el reporte de eventos adversos graves e inesperados en los ensayos clínicos.9
Recopilación, manejo y procesamiento estadístico de los datos
Los datos se registraron en los expedientes clínicos de los pacientes incluidos e igual número de cuadernos de recogida de datos.
Para el procesamiento de los datos se utilizó el sistema automatizado de cómputo SAS para Windows, versión 9.1.3. Se aplicaron análisis descriptivos, tablas de frecuencia por grupos y comparación de grupos, a través del test Chi cuadrado de bondad de ajuste de Pearson para igualdad de dos proporciones.
Principios éticos
El diseño y conducción de la investigación se realizó según establecen las directrices sobre las Buenas Prácticas Clínicas en Cuba y los principios éticos para las investigaciones médicas en seres humanos.10,11,12)
Resultados
Los EA con mayor frecuencia de aparición por grupo de tratamiento se muestran en la Tabla 1. En cada una de las 19 evaluaciones realizadas a los pacientes se verificó la ocurrencia o persistencia de EA. Se reportaron 120 EA en 27 pacientes (64,3 %), nueve del grupo A y 18 del grupo B, con influencia significativa (p=0,004; Z=2,662 prueba Z comparación entre dos porcentajes); pertenecer al grupo B implicó la ocurrencia de más EA (81,0 %; 97 de 120), mientras que los pacientes del grupo A presentaron 23 (19,0 %). En este caso, el test Chi cuadrado, de bondad para igualdad de dos proporciones complementarias, resultó significativo (p<0,0001).
La clasificación de los EA según intensidad, actitud frente al medicamento, causalidad y resultado posterior al tratamiento administrado para contrarrestarlos se muestra en la Tabla 2. Como se puede apreciar, la mayoría de los EA se manifestaron con intensidad severa, pero solo tres de ellos, 13,1%, conllevó a la interrupción definitiva del tratamiento en el grupo A. Es importante señalar que estos EA no se relacionaron con la administración de Surfacen®.
Tabla 2 Clasificación de los EA según intensidad, actitud frente al medicamento, causalidad y resultado
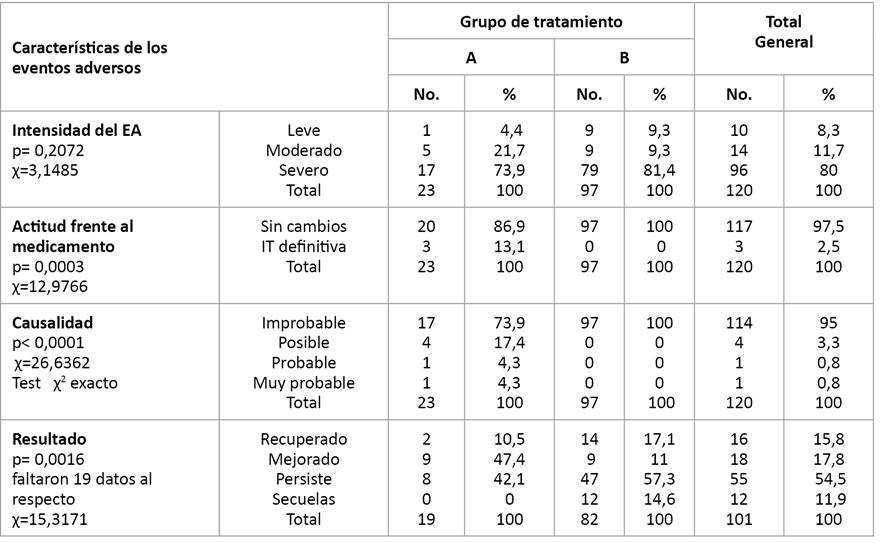
χ Chi cuadrado de Pearson
En relación con el resultado posterior al tratamiento administrado para contrarrestarlos EA, en el grupo B fue significativa la persistencia de EA y secuelas, mientras que en los pacientes del grupo A ninguno dejó secuelas. Los EA severos que se presentaron en los pacientes del grupo B se debieron a las enfermedades de base y dejaron secuelas en 12 pacientes. La proporción de ocurrencia de EA en los pacientes fallecidos fue de 83,3 % y en los pacientes vivos de 52,2 %, lo que muestra una diferencia significativa (p=0,0378).
La mortalidad al día 28 de la inclusión en el estudio fue de 41,5 %; de los pacientes incluidos, en el grupo A, 20 % y en el grupo B, 62 %. Al realizar los análisis de las causas de muerte y su posible asociación con EA graves que guarden relación de causalidad con el medicamento, se pudo constatar que en ningún caso se encontró correspondencia con la muerte. En todos los pacientes el estado clínico y la enfermedad concomitante fueron los que condujeron al fallecimiento.
Discusión
La hipertensión arterial fue el EA más frecuente en ambos grupos de tratamiento. En el grupo B casi el doble de pacientes presentó este EA, lo que se explica porque es uno de los trastornos hemodinámicos que concomitan con el SDRA, con la caída del gasto cardiaco y el aumento de la resistencia vascular periférica como su expresión más fidedigna.
En sentido general, los surfactantes pulmonares son bien tolerados y seguros con muy pocos EA debido a que su acción es local en el pulmón sin diseminación por vía hemática. Esta investigación muestra resultados similares a la realizada por otros autores.13,14)
Los autores consideran que la aplicación de Surfacen® durante 25 años en neonatología como práctica clínica habitual confirma la seguridad de este medicamento. Se advierten efectos adversos como la apertura del conducto arterioso y la hiperoxia; el primero, no traduce ninguna dificultad en los niños y el segundo, representa una necesidad en el SDRA por lo que su uso constituye una opción terapéutica asequible y confiable en las UCIP.
Teniendo en cuenta que de los reportes de EA, en el grupo A solo seis se relacionan con la instilación del medicamento, por lo que el resto de los EA, independientemente del grupo de tratamiento, fueron resultado de la sintomatología propia de las enfermedades de base que padecían y asociadas al manejo ventilatorio.
Los seis EA relacionados con Surfacen® se reportaron en dos pacientes, con tres EA en cada uno; estos fueron: desaturación, arritmias y parada cardiorrespiratoria en el paciente EA-05 e hipopotasemia, broncoespasmo y alcalosis metabólica en el paciente JLM-04. La desaturación, arritmias y broncoespasmo son EA transitorios descritos como relacionados con la administración de surfactantes exógenos, debido a la obstrucción aguda de la vía aérea (no significativos y de fácil corrección) con los consecuentes episodios de hipoxia momentánea que estos producen; resultados que muestran similitud con lo descrito por otros autores,15,16) por lo cual se recomienda, previo al tratamiento con surfactantes, estabilizar al paciente desde el punto de vista hemodinámico y metabólico, así como reajustar los parámetros ventilatorios; de no ser así, se suspende la administración del surfactante para iniciar medidas encaminadas a la estabilidad del paciente y luego, se continúa con el procedimiento una vez alcanzada dicha estabilización.14
La alcalosis metabólica, la hipopotasemia y la parada cardiorrespiratoria no se consideran relacionadas con la administración de surfactantes, más bien se reporta como propio de la fisiopatología del SDRA y del síndrome de disfunción múltiple de órganos (SDMO),2,17,18 por lo que los autores consideran que la relación de causalidad establecida con la instilación del surfactante es debido a la inexperiencia de los especialistas pediátricos en la administración de surfactantes pulmonares y en la práctica de evaluación de la causalidad de los EA detectados durante ensayos clínicos.
En una revisión del tema realizada por Willson, et al.,19) se expresaba que tanto en niños (incluidos los lactantes) como en adultos, el uso de surfactantes no mostró ningún EA significativo a largo plazo, solo apareció hipoxia transitoria y cierta inestabilidad hemodinámica al momento de la instilación del medicamento. No se reportaron reacciones alérgicas ni infecciones asociadas a la administración de los surfactantes, lo que coincide con lo descrito en esta investigación.
En 2009, Kesecioglu et al.,20) en un ensayo multicéntrico con el surfactante HL10, evidenciaron resultados desfavorables con tendencia hacia una mayor mortalidad, complicaciones y EA (51,9 % hipoxia y 34,1 % hipotensión), razón por la que se detuvo esta investigación por la Agencia Europea para la Evaluación de Productos Medicinales; resultados que no coinciden con este trabajo. Willson y Thomas,21 como expertos, comunican mediante una carta al editor en la American Journal of Respiratory and Critical Care Medicine, que la posible causa del fracaso debe estar relacionada con las características bioquímicas y propiedades biofísicas del surfactante utilizado, porque ya se ha demostrado en varios ensayos clínicos, que la administración de surfactantes mejora la oxigenación y en algunos casos, sobre todo en niños, disminuye también la mortalidad.
Varios autores22,23,24 plantean que la letalidad del SDRA se debe al daño hipoxémico mantenido que ocasiona el deterioro irreversible en la unidad celular respiratoria, la necesidad de un equipo de respiración y del uso de la ventilación protectiva con el objetivo de prolongar la vida en estos pacientes obedece al menos por categoría conceptual al fallo de dos órganos como mínimo y los clasifica dentro de la categoría de SDMO, en el grupo B más de las tres cuartas partes fallecen por esta causa, lo que concuerda con las investigaciones señaladas con anterioridad. En un metanálisis realizado por Zhang, et al.,13 no encontraron que la administración de surfactantes exógenos redujera la mortalidad en adultos con SDRA. En el ensayo clínico fase II,8) realizado con Surfacen® en adultos con el mismo esquema de tratamiento que se utilizó en este trabajo, se evidenció que el hecho de que un paciente falleciera o no, no guardaba relación con la respuesta que estos manifestaban ante el tratamiento; tal es así que 59,09 % de los pacientes fallecidos había respondido al tratamiento en el momento que se presentó el evento; de ellos, 36,36 % del grupo A, lo que puede explicarse por el hecho de que los surfactantes exógenos actúan en beneficio de la oxigenación 25) y no sobre las enfermedades desencadenantes del SDRA; razón por la cual algunos pacientes pueden superar el SDRA y fallecer como consecuencia de diversos factores intrínsecos de la condición clínica de cada paciente, lo que es característico de esta afección, donde la mayoría de las muertes es a causa del SDMO.26
El hecho de que el surfactante exógeno esté sometido a la oxidación reduce su actividad biofísica, lo que puede haber contribuido a los resultados clínicos negativos en algunos ensayos clínicos. Las proteínas del surfactante endógeno A y D tienen actividad antioxidante y su aumento u otros antioxidantes endógenos, como son la superóxido dismutasa, la vitamina E y la melatonina, entre otros, pueden moderar la descomposición por oxidación del surfactante exógeno.27
Este estudio tiene la limitación de haber incluido un número reducido de pacientes aun cuando el período de inclusión fue prolongado (33 meses), lo que se debió a la baja incidencia del SDRA en niños; lo que no impidió que los resultados fueran significativos y confiables. Tal es así, que la agencia reguladora cubana, el Centro para el Control de los Medicamentos, Dispositivos y Equipos Médicos (CECMED), evalúo los mismos y emitió el dictamen de aprobación como nueva indicación terapéutica del producto en estudio.















