Introducción
La enfermedad de Parkinson (EP) es un trastorno neurológico progresivo asociado con características motoras y no motoras que comprende múltiples aspectos de los movimientos, incluida la planificación, la iniciación y la ejecución. Durante su desarrollo se pueden observar síntomas relacionados con el movimiento como temblor, rigidez y dificultades en la iniciación, previo a alteraciones cognitivas y conductuales incluyendo la demencia.
Las características clínicas más importantes de la EP son temblor, bradicinesia, rigidez e inestabilidad postural. Estos síntomas motores afectan las extremidades superiores e inferiores y dificultan el desempeño de las tareas rutinarias de los pacientes, lo que puede ser visible desde las primeras etapas de la enfermedad (Alam et al., 2017).
Según el resumen técnico realizado por la Organización Mundial de la Salud (OMS) en 2022, la enfermedad de Parkinson (EP) es a nivel mundial, el trastorno neurológico que más rápido crece en cuanto a discapacidad y muerte de los pacientes que la padecen (Organization, 2022). Esto se debe a que la etiología (origen o causa) de la (CIE-10: G20 enfermedad de Parkinson) aún no ha sido determinado del todo, el diagnóstico de sospecha es clínico y actualmente no se disponen de marcadores biológicos específicos que detecten de forma temprana la enfermedad por lo que el diagnóstico cierto siempre es post- mórtem. Por lo tanto, realizar un diagnóstico oportuno de la enfermedad puede contribuir a mejorar los resultados del tratamiento (Cornelio et al., 2023).
El diagnóstico de la EP se basa comúnmente en las observaciones médicas y la evaluación de los signos clínicos, incluida la caracterización de una variedad de síntomas motores. Sin embargo, los enfoques de diagnóstico tradicionales pueden sufrir de subjetividad, ya que se basan en la evaluación de movimientos que a veces son sutiles para los ojos humanos y, por lo tanto, difíciles de clasificar, lo que lleva a una posible clasificación errónea (Mei et al., 2021).
Dado que los diagnósticos confiables y la detección temprana son una de las principales prioridades en la práctica médica, se está invirtiendo mucho esfuerzo en la implementación de herramientas computacionales y el desarrollo de nuevos métodos para el apoyo al diagnóstico (Aguada et al., 2023), lo que aumentaría la precisión y minimizaría el tiempo y los recursos necesarios para tratar la EP.
Los avances recientes en los campos de la inteligencia artificial y el Internet de las cosas, incluidos los subdominios del aprendizaje automático y el aprendizaje profundo, pueden ayudar a los pacientes con EP, a sus cuidadores y a los médicos en cada etapa de la enfermedad (Fonseca et al., 2019). A partir del diagnóstico temprano de la enfermedad se puede maximizar la eficacia del tratamiento y minimizar los respectivos costos de atención médica (Giannakopoulou et al., 2022).
La inteligencia artificial, específicamente el aprendizaje automático (ML), ha encontrado numerosas aplicaciones en el diagnóstico, seguimiento y tratamiento asistidos por ordenador de los trastornos del movimiento neurodegenerativos de tipo parkinsoniano.(Belić et al., 2019) El ML permite que un programa de computadora aprenda y extraiga una representación significativa de los datos de manera semiautomática.
Para el diagnóstico de la EP, se han aplicado modelos de aprendizaje automático a multitud de modalidades de datos, incluidos patrones escritos a mano, movimiento, neuroimagen, voz (Mohapatra et al., 2023), olor (Fu et al., 2022), líquido cefalorraquídeo (LCR), gammagrafía cardíaca, suero y tomografía de coherencia óptica (OCT ). El aprendizaje automático también permite combinar diferentes modalidades en el diagnóstico de la EP, como imágenes por resonancia magnética (IRM) y datos de tomografía computarizada por emisión de fotón único (SPECT).
En la actualidad, solo una gama limitada de sistemas médicos específicos basados en IA están disponibles en la práctica clínica, incluida la detección automatizada de fibrilación auricular, convulsiones o diagnóstico asistido por computadora con imágenes automatizadas. Por lo tanto, la presente revisión tiene como objetivo describir las herramientas computacionales y los algoritmos de IA específicos para el diagnóstico de la EP.
Con la realización de este estudio se pretende proporcionar a los profesionales del aprendizaje automático interesados en el diagnóstico de la EP una descripción general de los modelos y modalidades de datos utilizados anteriormente y los resultados asociados, y recomendaciones sobre cómo los protocolos experimentales y los resultados podrían informarse para facilitar la reproducción.
Métodos o Metodología Computacional
Para la realización de la Revisión Sistemática de la Literatura científica (RSL) se definió un protocolo de revisión se siguieron las pautas propuestas por el Grupo de Ingeniería de Software de la Universidad de Keele para este tipo de estudios (Keele, 2007), con el objetivo de obtener un nivel adecuado de precisión, exactitud y fiabilidad de la investigación en curso (Marcillo, 2022). El protocolo definido para esta investigación cuenta con las siguientes actividades: Definición de las preguntas de investigación; Diseño de la estrategia de búsqueda; Determinación de los criterios de selección de estudios; Reporte de estudios incluidos; Análisis y síntesis de los datos extraídos. Cada una de estas actividades son desarrolladas en detalle durante la presente investigación.
Preguntas de la investigación
Para guiar la búsqueda se determinaron las siguientes preguntas de la investigación:
Fuentes de búsqueda
En primer lugar, se seleccionaron las bases de datos y registros más adecuados de la literatura respectiva. Los autores optaron por tres bases de datos de citas académicas populares, que garantizan la alta calidad y el impacto de los artículos considerados. El primero es PubMed, una de las bases de datos más populares de literatura biomédica. El segundo es IEEE Xplore, que es una base de datos muy conocida de literatura técnica, y el tercero es Scopus, que indexa artículos académicos de una amplia gama de campos de investigación:
Criterios de búsqueda
Con base en las preguntas de investigación declaradas fueron definidas tres categorías para guiar las decisiones de inclusión/exclusión (Marcillo, 2022):
La Tabla 1 enumera las categorías definidas y brinda ejemplos sobre temas relacionados. Para incluir un estudio primario en esta investigación, debe ser relevante en al menos una categoría. Las categorías de inclusión relevantes para este estudio se muestran a continuación:
Tabla 1 - Categorías de inclusión de la revisión sistemática.
| C2 | Inteligencia Artificial |
Se implementan técnicas de IA para el diagnóstico y evaluación de la EP. Se procesan datos con IA. Se muestran las estimaciones realizadas con IA para la detección de la EP. |
| C1 | Aprendizaje automático |
Se describen los algoritmos de ML implementados para el diagnóstico de la EP. Se describen los resultados obtenidos con ML. |
| C3 | Internet de las cosas |
Se presentan estudios de casos donde se utiliza el IoT para el diagnóstico de la EP. Se describen las tecnologías de IoT utilizadas en el diagnóstico y evaluación de la EP. Discuten un caso real implementado y muestran los resultados obtenidos. Describen los sensores empleados para la recopilación de información y realizan comparaciones. |
La selección de las cadenas de búsqueda se basó en métodos y dispositivos discutidos en artículos de revisión anteriores, luego de varios ajustes para garantizar la inclusión de todas las tecnologías de interés específico para esta revisión. En la Tabla 2 se muestran las cadenas de búsqueda para cada una de las categorías de inclusión definidas.
Tabla 2 - Palabras clave utilizadas en la cadena de búsqueda para cada categoría.
|
C1 Inteligencia Artificial |
|
|
C2 Aprendizaje automático |
|
|
C3 Internet de las cosas |
|
Nota: La sintaxis de esta cadena podrá adaptarse en dependencia del motor de búsqueda que se utilice.
Criterios de inclusión-exclusión para la selección de los artículos
Los criterios definidos para la selección de las publicaciones se muestran en la tabla 3.
Tabla 3 - Criterios de inclusión y exclusión.
|
Artículos publicados en revistas o en actas de congresos. Artículos publicados en la última década (desde enero de 2013 hasta mayo de 2023) Artículos escritos en inglés o español. Deben abordar las técnicas y herramientas de diagnóstico de la EP. Deben estar relacionados con los temas de al menos una de las categorías definidas para esta investigación. Las hipótesis deben probarse en sujetos humanos adultos, bajo estrictos lineamientos éticos. Estudios que tienen como objetivo diagnosticar la EP utilizando una técnica o enfoque de IA o ML. Debe proponer al menos un algoritmo de IA específico para apoyar el diagnóstico de la DP. Sólo estudios empíricos Artículos que presentaran reportes de casos o estudios clínicos sobre la enfermedad |
|
No es un artículo de revista original o documentos de actas de congresos. En idiomas distintos del inglés o español. Artículos no revisados por pares El estudio no proporcionó descripciones de los métodos de aprendizaje automático, conjuntos de datos, o temas utilizados. Hipótesis probadas en animales. Estudios que presenten solo un análisis estadístico y ningún método de IA o ML. |
Criterios de calidad y pertinencia
¿Está claramente definido el objetivo de la investigación?
¿Está bien abordado el contexto de investigación?
¿Están los hallazgos claramente establecidos?
Con base en los hallazgos, ¿qué tan valiosa es la investigación?
Los estudios seleccionados serán evaluados en cada criterio utilizando una escala ordinal para obtener una evaluación más precisa (Inayat et al., 2015). La tabla 4 muestra la escala de puntuación para cada criterio.
Resultados y discusión
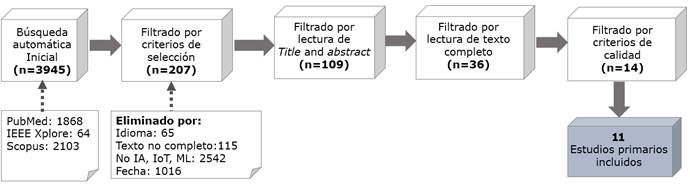
Una vez ejecutado el protocolo de búsqueda definido en el método de esta investigación, se seleccionaron 14 estudios primarios. El proceso de recuperación y selección se resume en la Figura 1.
Inicialmente, se recuperaron 3945 artículos, luego de enviar las consultas a las tres bases de datos. Se recuperaron 1868 artículos de PubMed; 64 artículos de IEEE Xplore; y 2103 artículos de Scopus. A continuación, se eliminaron 1016 artículos publicados antes de 2013. Otros 65 informes fueron excluidos por no estar redactados en inglés o español; fue necesario excluir 115 investigaciones por no poder acceder altexto completo; y un total de 2542 fueron desestimados, por no centrar su análisis en el empleo de la IA, el IoT, o el ML; lo que resultó en 207 estudios a considerar. Después de la lectura del título y el resumen el listado de artículos candidatos se limitó a 109. Finalmente, se seleccionaron 36 estudios para ser considerados en la lectura del texto completo para aplicar la evaluación de calidad y pertinencia con el objetivo de esta revisión. Finalmente se incluyeron 11 estudios primarios. Los títulos de los estudios incluidos, así como la evaluación de calidad emitida, se muestran en la tabla 5.
Tabla 5 - Reporte de estudios incluidos.
| Modelo | |
|---|---|
|
| |
| Este estudio tuvo como objetivo determinar si las enfermedades neurodegenerativas, por ejemplo, la enfermedad de Parkinson (EP), afectan la marcha y la movilidad, la enfermedad de Parkinson (EP) afecta la marcha y la movilidad en comparación con el control sano. | El error de re-sustitución de LDA durante la clasificación es del 21,11%. Además, se obtienen resultados significativos y precisos de clasificación y agrupación entre EP y control tomando la potencia en el dominio de la frecuencia del pie izquierdo-derecho como características de clasificación. |
|
| |
| Este trabajo propone un método auxiliar de clasificación de la EP mediante Inteligencia Artificial y Aprendizaje Automático supervisado. El algoritmo desarrollado en Python y Redes Neuronales Artificiales analiza los datos obtenidos de imágenes adquiridas por tomografía por emisión de positrones (PET). | Los resultados de la clasificación mediante el análisis cuantitativo de los datos muestran que el algoritmo alcanza un 90% de precisión en la predicción utilizando 11C-DTBZ y 11C-RAC como parámetros complementarios de alimentación. |
|
| |
| Se empleó el algoritmo de agrupación de k-means en mini lotes para generar automáticamente dos agrupaciones que incluían la agrupación FOG y la no FOG. A continuación, se determinó si se trataba de un evento FOG o no FOG asignando la señal actual al centro más cercano del clúster. Se empleó la validación cruzada leave-one-out para obtener la precisión, sensibilidad y especificidad del algoritmo. | Los resultados mostraron que la precisión, sensibilidad y especificidad de la detección de FOG fueron del 93,2%, 92,4% y 94,9%, respectivamente. En conclusión, el sistema desarrollado basado en el acelerómetro y el algoritmo de agrupación de k-means en mini lotes es capaz de detectar automáticamente eventos FOG sin etiquetado del conjunto de entrenamiento. |
|
| |
| En una cohorte de 119 pacientes con EP, se aplicaron algoritmos no supervisados para encontrar diferentes grupos de marcha que potencialmente incluyen la información clínicamente relevante de distintas fases de la marcha en la prueba estandarizada de marcha de 4x10 m. | Como resultado principal, analizar sólo uno de los grupos de marcha constante, no constante o de giro condujo en cada caso a un mejor rendimiento de clasificación en comparación con la línea de base (aumento del área bajo la curva (AUC) de hasta un 19% en relación con la línea de base). Además, se identificaron los parámetros de la marcha (para giros, marcha constante y no constante) que mejor predicen el deterioro motor en la EP. |
|
| |
| Presentó un nuevo método para analizar y visualizar patrones en imágenes de resonancia magnética. Para ello, este estudio adoptó la función de ganancia de información difusa (FIG) y el algoritmo de agrupación K-means. | El método propuesto alcanzó un error cuadrático medio medio de 63,49, una relación señal-ruido máxima de 30,14 y un coeficiente de similitud de Jaccard de 0,92 entre nueve IRM de EP. El rendimiento mostró una mejora del 20,73%-32,94%, 3,54%-6,20% y 6,98%-64,29% sobre el error cuadrático medio, la relación señal-ruido pico y el coeficiente de similitud de Jaccard, respectivamente, en comparación con otros métodos de segmentación de imágenes. |
|
| |
| Índices convencionales de la variabilidad de la frecuencia cardíca (VFC), además de índices de análisis geométricos y no lineales fueron calculados para ser utilizados como entrada en el clasificador denominado como máquina de soporte vectorial (SVM), donde se empleó eliminación recursiva de características (RFE) para retener las más importantes. Adicionalmente, las series de intervalos RR (diferencia en tiempo entre las ondas R adyacentes de la señal de ECG) se utilizaron como secuencias de entrada en una red neuronal basada en LSTM bidireccional (BLSTM) | Los resultados ilustran que con las características de VFC seleccionadas se obtiene un porcentaje de exactitud en el conjunto de prueba del 100% utilizando SVM en todas las maniobras. Además, el mayor porcentaje de exactitud en los datos de prueba usando BLSTM es del 75% correspondiente a la maniobra de respiración controlada. |
|
| |
| Se realizó un análisis estadístico clínico, demográfico y de los parámetros espaciales y temporales con el fin de encontrar alguna diferencia entre los pacientes de EP con y sin FoG; este último no obtuvo resultados estadísticamente significativos. Así, se implementó un análisis de aprendizaje automático empleando algoritmos basados en árboles (árbol de decisión, Random Forests, Gradient Boosted Tree, Ada-Boosting de un árbol de decisión) y utilizando como entrada las características espaciales y temporales de la marcha. | Los resultados fueron prometedores, ya que la precisión, especificidad y sensibilidad superaron el 90%, alcanzando también el 100% de sensibilidad en algunos casos. Los mejores algoritmos fueron el Gradient Boosted Tree y el Ada-Boosting de un árbol de decisión, mientras que los Random Forests y el árbol de decisión obtuvieron resultados inferiores. |
|
| |
| Se implementó un clasificador basado en inteligencia artificial con modelos de aprendizaje supervisado como redes neuronales, máquinas de soporte vectorial y discriminante lineal y de aprendizaje no supervisado como k-means. | La solución propuesta en este proyecto ha demostrado que existe la posibilidad de que un algoritmo de Machine Learning pueda utilizarse para clasificar videos de movimientos alternantes como provenientes de una persona diagnosticada con Parkinson o de una persona sana. En este caso, el procesamiento y la extracción de características se concentró en la detección de bradicinesia a partir de características relacionadas con la amplitud, la velocidad y la periodicidad del movimiento. A pesar de la cantidad limitada de datos se obtuvo una exactitud (accuracy) del 95 %. |
|
| |
| En este trabajo, se aplica una red neuronal siamesa para diagnosticar la EP. Las redes siamesas predicen la clase de muestra estimando lo similar que es una muestra a otras. La idea que subyace a este trabajo es agrupar el conjunto de datos antes de entrenar la red, ya que los pares diferentes que pertenecen al mismo grupo son candidatos a ser confundidos por la red y se asume que son pares coincidentes. | La precisión alcanzada en la clasificación de pacientes con EP no agrupados fue del 76,75%, mientras que en los datos agrupados fue del 84,02%, superando a la misma técnica en los datos no agrupados |
|
| |
| El presente trabajo consiste en el desarrollo de un modelo de aprendizaje profundo para el reconocimiento de expresiones faciales asociadas a la enfermedad de Párkinson, con la finalidad de contar con una herramienta que aporte al análisis médico para un diagnóstico temprano y un tratamiento oportuno de la enfermedad | La precisión del modelo fue de aproximadamente un 70%, lo cual permite pueda ser utilizado como herramienta de apoyo para un diagnóstico temprano de la enfermedad |
|
| |
| Se evalúa la combinación de las señales usando un enfoque multicanal, donde se busca determinar si se obtiene un modelo más robusto al analizar todas o algunas de las señales de manera conjunta. La generalización de los modelos desarrollados fue verificada mediante una estrategia de validación cruzada donde los mejores resultados se obtienen usando la señal de altitud para el enfoque monocanal y combinando las señales x, z y altitud en el enfoque multicanal. | El modelo monocanal presenta un mejor balance en la clasificación de ambas clases. Finalmente, el multicanal presenta un desempeño inferior esto puede deberse a que algunas señales no aportan más información para detectar la enfermedad de Parkinson por medio del deterioro de las habilidades grafomotoras. |
Las investigaciones incluidas estuvieron relacionadas a modelos que analizan síntomas del habla/voz (Berrio-Zapata & Orozco-Arroyave, 2022); la bradicinesia (Steinke et al., 2020); trastornos de la marcha (Nguyen et al., 2019); y en menor medida sobre datos adquiridos a través de tomografía por emisión de positrones; reconocimiento y visualizaciones de imágenes por resonancia Magnética MRI (Huang et al., 2020); señales cardiovasculares (Mata et al., 2020); congelación de la marcha (Li et al., 2018); Clasificación de Expresión Facial (Figueroa Villacreses et al., 2022); Señales de escritura (Zapata Ortiz, 2023); Células dopaminérgicos de la sustancia nigra (Muddapu et al., 2019); y relacionados al tratamiento de la estimulación cerebral profunda.
Inteligencia artificial para el diagnóstico de la EP
La inteligencia artificial (IA) es un campo en crecimiento que cubre una amplia gama de tecnologías que tienen como objetivo imitar las funciones cognitivas y el comportamiento inteligente de los humanos. (Kazeminejad et al., 2017) Convencionalmente, la IA se basa en reglas y hace uso del conocimiento de expertos humanos.
Los algoritmos y técnicas de IA se pueden aplicar a los datos recopilados de sensores, integrados en dispositivos portátiles u otros objetos cotidianos. Hoy en día, estos datos son abundantes y fáciles de adquirir gracias al paradigma de Internet de las cosas (IoT), que permite que varios objetos físicos con sensores integrados e identificadores únicos se comuniquen entre sí y transfieran datos a través de una red. La mayoría de los sensores desplegados para el diagnóstico de la EP incluyen sensores inerciales o unidades de medición inercial (IMU), como acelerómetros, giroscopios y magnetómetros, así como sensores de presión y placas de fuerza de reacción del suelo (GRF) que miden características correspondientes a los síntomas del motor de EP.
También se han utilizado sensores de imagen y profundidad, así como sensores de sonido o audio para capturar manifestaciones de DP motoras y no motoras. Otros sensores desplegados que capturan diversas bioseñales incluyen sensores de electroencefalografía (EEG), electrocardiografía (ECG) y electromiografía (EMG), dispositivos de medición del dolor, dispositivos portátiles de medición del sueño y sensores de polisomnografía (PSG), sistemas de seguimiento ocular, sensores de frecuencia cardíaca y temperatura, entre otros.
El aprendizaje automático (ML) representa un subconjunto de la IA e incluye potentes algoritmos que brindan a los sistemas la capacidad de explorar y encontrar patrones dentro de los datos, clasificar y predecir resultados mediante el aprendizaje a través de la experiencia (Agarwal et al., 2016). El ML tiene importantes aplicaciones en el cuidado de la salud, contribuyendo al diagnóstico, manejo de enfermedades, monitoreo de progresión y predicción de resultados (Ahmadi et al., 2019).
Dentro de los métodos más empleados para el diagnóstico de la EP se encuentran la Máquina de Vectores de Soporte (SVM), árboles de decisión (DT), aleatorios (RF), árboles empaquetados, potenciados y finos, k-vecinos más cercanos (kNN), regresión logística (LR), análisis discriminante lineal (LDA) y clasificadores Naïve Bayes (NB), así como perceptrones multicapa (MLP) u otras redes neuronales (NN).
En la investigación “Efficient diagnosis system for Parkinson's disease using deep belief network” que fue desarrollada por Al-Fatlawi y colaboradores (Al-Fatlawi et al., 2016), los autores adoptaron una red de creencias profundas (DBN) para el diagnóstico de la EP. El sistema propuesto fue entrenado y probado con voces de varios pacientes y personas sanas. Se preparó un proceso de extracción de características para ingresar a la DBN que se utilizó para crear una plantilla de coincidencia de las voces. Con DBN se logró clasificar la enfermedad de Parkinson que se compone de dos máquinas de Boltzmann restringidas (RBM) apiladas y una capa de salida. Para ilustrar la efectividad del sistema propuesto, los autores describieron los resultados experimentales y los comparan con diferentes enfoques y trabajos relacionados. La precisión general de las pruebas del sistema propuesto es del 94 %.
El estudio “Classification of the Speech Signal of Parkinson's Patient using Optimized Ensemble Model” fue desarrollado por Mohapatra y colaboradores(Mohapatra et al., 2023), los autores se basaron también las señales del habla. Propusieron un clasificador de conjunto apilado para clasificar las señales del habla de los pacientes con EP. El conjunto de datos utilizado es del repositorio de aprendizaje automático de UCI que consta de las características de las señales de voz. Como clasificador base, se utilizan cuatro redes neuronales profundas (DNN) estándar. La salida de la primera etapa se entrega a la segunda etapa, que es el clasificador Meta. La máquina de vectores de soporte y los metaclasificadores de aumento de gradiente óptimo se utilizan para comparar el rendimiento del modelo entre sí. La precisión se encuentra mejor en el clasificador Meta optimizado como 98%.
El estudio “Recent Advances in Statistical Data and Signal Analysis: Application to Real World Diagnostics from Medical and Biological Signals” de Mahapatra y colaboradores, se implementa un sistema neuronal difuso (FNS) para el diagnóstico de la EP (Mahapatra et al., 2016). El estudio presenta el diseño del sistema de reconocimiento que discrimina entre personas sanas y personas con EP. Se realiza un diagnóstico mediante la fusión del sistema difuso y las redes neuronales. Se probó a través de la simulación del sistema que se ha realizado utilizando datos obtenidos del repositorio de aprendizaje automático de la UCI. Hasta este punto de validación, los resultados se consideraron muy favorables.
Discusiones
El diagnóstico de la EP es eminentemente clínico (Marín et al., 2018) y se basa en la identificación de alguna combinación de los signos motores cardinales de bradicinesia, rigidez, temblor e inestabilidad postural. Los criterios más ampliamente aceptados fueron introducidos por la UK Parkinson Disease Society - Brain Bank. Según (Súbita & de Referencia Rápida, 2013) Estos criterios aplicados por neurólogos especialistas en movimientos anormales presentan una sensibilidad y especificidad del 98.6% y 91.1% respectivamente.
Por medio del estudio de los datos de la enfermedad del Parkinson, extraídos de pacientes enfermos y no enfermos, los investigadores médicos pueden crear una tabla de evaluación con el fin de concienciar a los médicos y a la gente común sobre síntomas tempranos de la EP y hacer tratamientos más tempranos.
La minería de datos también se ha utilizado en las ciencias biomédicas y la investigación para predecir y analizar grandes volúmenes de datos médicos, como la enfermedad de Parkinson. Así lo plantean (Wu & Guo, 2011), quienes realizaron un estudio para examinar las mediciones de voz biomédicas por tres métodos de minería de datos para discriminar a los pacientes con EP de las personas sanas.
Según (Ríos Urrego, 2019), los correlatos acústicos de la EP tienen el potencial de proporcionar biomarcadores útiles y métodos sensibles para la detección temprana del inicio, la progresión de la enfermedad. Sobre este tema se han propuesto estudios por varios autores, uno de ellos en específico utiliza la técnica de aprendizaje por transferencia en redes neuronales convolucionales con el fin de mejorar la eficacia de los sistemas para el apoyo diagnóstico de la enfermedad de Parkinson en tres idiomas diferentes.
Para un enfoque más práctico (Amato et al., 2021) realizaron la implementación de un modelo k‑Nearest Neighbors optimizado para la clasificación binaria de pacientes con EP versus controles sanos, donde los resultados obtenidos lograron una precisión del 99,4 % en la validación cruzada de 10 veces y del 94,3 % en las pruebas en la base de datos PC-GITA (valor promedio de sujetos masculinos y femeninos). A modo de conclusión exponen que el modelo implementado confirma la viabilidad de la evaluación automática de la EP mediante grabaciones de voz. Además, un análisis post-hoc de las características más relevantes revela la opción de procesamiento de voz usando una aplicación de teléfono inteligente simple.
El análisis de la voz/habla ha permitido que podamos hallar una serie características vocales dentro de grabaciones controladas, lo que nos ayuda a poder diferenciar entre pacientes y sujetos sanos con una tasa de acierto aceptable, así lo afirma (Fernández Sanz, 2021), quien propone un proyecto que sea eficaz para la detección de la enfermedad de Parkinson de una manera alternativa, a través de la grabación de audios de los pacientes.
Los autores (Damota et al., 2021) aprovechan el uso del Machine Learning (ML) para la clasificación de pacientes con Parkinson con el empleo de aprendizaje automático. En su investigación, plantea que los algoritmos más utilizados del 2018 al 2021 son Random Forest, Support Vector Machine, K Nearest Neighborg, red Neuronal Convolucional y Gauss Process. Y los algoritmos que mejores resultados obtienen en su investigación resultan Random Forest (85%, 84%) y Support Vector Machine (85%, 83%).
Los autores (Olivares et al., 2020) evalúan su propuesta utilizando el conjunto de datos de audio de la enfermedad de Parkinson tomado del repositorio de aprendizaje automático de UCI. Sus resultados sugieren el uso del algoritmo de optimización bioinspirado para ajustar los parámetros de Extreme Learning Machine como una alternativa real para mejorar el rendimiento. Durante la fase de validación, el proceso de clasificación de la Enfermedad de Parkinson alcanza una precisión máxima del 96,74 % y una pérdida mínima del 3,27 %.
Conclusiones
La EP no tiene una forma efectiva de curar, pero el diagnóstico temprano de La EP y las intervenciones médicas, psicológicas y sociales tempranas pueden mejorar significativamente la calidad de vida relacionada con la salud, aliviar los síntomas y prolongar el tiempo de supervivencia de los pacientes. Por lo tanto, el diagnóstico temprano de la EP es muy importante.
Esta revisión sistemática presentó una descripción general de los estudios que investigan el uso de herramientas computacionales, la inteligencia artificial y los algoritmos de aprendizaje automático para el diagnóstico y evaluación del progreso de la EP. Se identificó evidencia significativa que demuestra que las herramientas computacionales y la IA son factibles para el diagnóstico de pacientes con la EP.