En los últimos años se ha informado acerca del gran potencial de microorganismos endófitos asociados a las plantas de cacao (organismos que colonizan los tejidos: hojas, frutos, tallos y raíces de plantas, sin causar enfermedad) como candidatos para el biocontrol de enfermedades (Eun y Mee, 2016; Villarreal-Delgado et al., 2017).
T. cacao es el hábitat de una comunidad microbiana diversa que todavía está parcialmente caracterizada, razón que justificó la identificación de los potenciales agentes de control biológico en este trabajo estuviera centrado sobre las bacterias endófitas formadoras de endosporas, ya que estas estructuras de resistencia son el principal ingrediente activo de los formulados comerciales, y les confiere como propiedad una mayor viabilidad en el tiempo (Ek-Ramos et al., 2019).
El objetivo del presente trabajo fue identificar morfológica, fisiológica y molecularmente cepas de bacterias endófitas asociadas a T. cacao en Quinindé, Esmeraldas, Ecuador.
El trabajo se realizó en el Laboratorio de Fitopatología del Departamento de Protección Vegetal de la Estación Experimental Tropical Pichilingue perteneciente al Instituto Nacional de Investigaciones Agropecuarias (INIAP), Ecuador.
Se emplearon 8 aislados de bacterias endófitas pertenecientes a la colección de cultivos microbianos del propio Centro. La descripción de los caracteres morfológicos (forma, agrupación y respuesta a la tinción) en tinciones simples y de Gram, se realizaron mediante observaciones al microscopio óptico Karl Zeiss (aumento 1000 x) de los aislados que resultaron ser bacilos Gram positivos se les realizó la prueba de la enzima catalasa en portaobjetos lisos con Peróxido de hidrógeno al 3 %. Para la identificación molecular, se realizó la extracción del Ácido Desoxirribonucleico (ADN) de las cepas de bacterias endófitas sembradas a 28±1°C por 24 h en medio de cultivo TSA. El proceso de extracción se hizo acorde a las normas de manufactura de PureLink® Genomic DNA Mini Kit (Invitrogen) con un volumen de elución de ADN final a 100 µL por muestra. El ADN total se amplificó para la región 16S rRNA mediante la Reacción en Cadena de la Polimerasa (PCR), usando los cebadores universales: 27F (5’-AGAGTTTGATCMTGGCTCAG-3’) (Hogg y Lehane, 1999) y 1492R (5’- GGTTACCTTGTTACGACTT-3’) (Turner et al., 1999), a una concentración de 25 pmol.
Las condiciones de la PCR fueron: 35 ciclos, con desnaturalización inicial a 94 °C por 3 min, seguido de los ciclos con desnaturalización a 94 °C por 30 s, temperaturas de anillamiento a 50 °C, por 30 s, con extensión a 72 °C por 2 min, seguido de una extensión final a 72 °C por 10 min. El volumen de reacción de la PCR fue de 25 µL: 2,5 µL de 10x Pfx tampón de amplificación, 17,4 µL de agua desionizada, destilada estéril, 0,8 µL de dNTPs (10nM), 0,5μL de mM MgSO4, de cada cebador 0,8 µL, 0,8 µL de dimetilsulfóxido (DMSO), 0,2 µL de Platinum Pfx® de Invitrogen y 2 µL de ADN.
Los productos de la PCR se comprobaron por electroforesis con geles de agarosa al 1 % más 1x GelRed® Safe Nuclied Acid Gel Stain (Biotium, Hayward, USA), las condiciones de corrida fueron; 128V, 3000mA por 20min. Se utilizó 2μL de marcador de peso molecular 1 Kb (Invitrogen), en el gel se cargó 2 µL del producto de PCR más 3 µL de bromo fenol azul. El tampón de corrida fue SB 1X. Los productos de PCR fueron purificados con el protocolo para PureLink™ PCR Purification Kit, obteniendo un volumen final de 60 µL. Los productos positivos fueron enviados a secuenciar en Macrogen (Seoul-Korea).
Los cromatogramas de las secuencias obtenidas se verificaron Sequencher 4.6 (Gene Codes, Ann Arbor, MI, USA). Las secuencias correctas fueron comparadas en la base de datos (GenBank; http://www.ncbi.nlm.nih.gov/).
Se observó que las colonias de bacterias aisladas en TSA a las 72 h, tenían características culturales y morfológicas macroscópicas semejantes a las del género Bacillus tales como tamaño de mediano-grande, borde irregular, elevación planoconvexa y color blanquecino (Figura A). Después de realizar la tinción de Gram, se constató a nivel microscópico, que todos los aislados resultaron ser bacilos Gram positivos (Figura B), formadores de endosporas (Figura C) y catalasas positivas (Figura D).
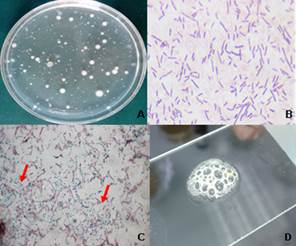 A) Morfología macroscópica; B) Células bacilares Gram positivas; C) endosporas (flechas rojas); D) prueba de la enzima catalasa (positiva)
A) Morfología macroscópica; B) Células bacilares Gram positivas; C) endosporas (flechas rojas); D) prueba de la enzima catalasa (positiva)Figura Características culturales, morfológicas y fisiológicas de Bacillus sp. (aislado 33), con aumento de 1000 X
En el estudio de Melnick et al. (2011), para la caracterización fenotípica de Bacillus en TSA tomó en cuenta el tamaño, forma, elevación margen y color, obteniendo como resultado colonias medianas a grandes, de borde irregular, elevación planoconvexa y color blanco/crema, corroborando estas características para el género Bacillus como las de la presente investigación.
La secuenciación del gen que codifica para el ADNr 16S mostró que la cepa 9-2, 24, 29-2, 45-1, 51-2 y 53-4 presentaron un grado de similitud del 99 % y se correspondieron con las especies B. subtilis, B. amyloliquefaciens, B. mycoides y B. cereus, respectivamente; mientras que, las cepas 33 y 72 no produjeron una secuencia consenso óptima, quedando como Bacillus sp. con un 98 % de similitud (Tabla).
Tabla Especies identificadas en cepas bacterianas endófitas obtenidos de mazorcas de Theobroma cacao L. colectadas en la provincia de Esmeraldas, Ecuador
| Código de cepa # | Fasta más cercana | No. Accesión | Homología % de identidad |
|---|---|---|---|
| 9-2 | KP165035.1 | 99 | |
| 24 | MF000350.1 | 99 | |
| 29-2 | KY352815 | 99 | |
| 33 | KT583479.1 | 98 | |
| 45-1 | EU266622.1 | 99 | |
| 51-2 | KX694390.1 | 99 | |
| 53-4 | KX694390.1 | 99 | |
| 72 | KR528492.1 | 98 |
La identificación basada en criterios morfológicos, coincidió con los criterios moleculares correspondientes a la secuenciación del gen que codifica para el ARNr 16S.
Los resultados de la presente investigación caracterizaron cepas endófitas de Bacillus spp. asociados a T. cacao. Las bacterias B. subtilis, B. amyloliquefaciens, B. mycoides y B. cereus pueden ser empleadas como agentes de control biológico de una de las principales enfermedades fúngicas que limitan la producción cacaotera en Ecuador














