INTRODUCCIÓN
La estomatitis aftosa recurrente (EAR) afecta aproximadamente al 60 % de las personas en edades comprendidas entre los 20 y 50 años y su presencia no guarda relación con la ubicación geográfica ni con la raza. 1,2,3) Si bien existe evidencia a favor de que las interacciones del sistema inmunitario (encargado de proteger y reparar al organismo) contribuyen principalmente a la magnitud del proceso patológico, 4,5 su etiología no está clara, ya que estas lesiones se asocian a un gran número de procesos locales y sistémicos muy diversos con rasgos histopatológicos similares. 6
Desde el punto de vista inmunopatogénico define como una enfermedad iniciada por un desorden de las células T y B del sistema inmune y de los factores de defensa no específicos. Esto conlleva a un incremento del contenido y la virulencia de la microflora bucal, lo que a su vez estimula la sensibilidad bacteriana de los pacientes con EAR. 7,8,9,10,11
Se sostiene que la eficacia de las propuestas de tratamiento de la EAR es cuestionable debido a las deficiencias metodológicas de los ensayos clínicos, en particular aquellos estudios que incluyen pacientes inmunocomprometidos, 12,13 razón por la cual el objetivo del presente estudio consiste en evaluar el efecto clínico de los tratamientos propuestos para la EAR en pacientes inmunocomprometidos.
METODOLOGÍA
Esta revisión se realizó en correspondencia con las directrices de la declaración PRISMA (Preferred Reporting Items for Systematic reviews and Meta-Analyses) para las revisiones sistemáticas. Se consideran solo ensayos clínicos que evalúen el efecto clínico de los tratamientos de la estomatitis aftosa recurrente en pacientes inmunocomprometidos. La pregunta clínica se estructura del modo siguiente:
Participantes: Pacientes inmunocomprometidos con estomatitis aftosa recurrente mayores de 18 años.
Intervención: Cualquier tratamiento preventivo o curativo administrado sistemáticamente por un periodo no inferior a 2 semanas.
Comparación: Incluye tratamiento con placebo o con otro fármaco. También ensayos clínicos que no incluyen grupo de comparación.
Variables de resultado
Las variables de resultado principales fueron cicatrización de la úlcera aftosa bucal, tiempo de cicatrización, tiempo de recurrencia, número de recurrencias, número de úlceras aftosas bucales e intensidad del dolor. Las variables secundarias: efectos adversos y síntomas.
Diseño del estudio: Ensayos clínicos
Se excluyen las series de casos, los reportes de casos, estudios observacionales, estudios en animales, editoriales, cartas al editor, artículos de revisión, comentarios y monografías.
Estrategia de búsqueda
La búsqueda de los estudios se desarrolló en las bases de datos PubMed/Medline y Cochrane de enero a abril de 2021 y se limitó a ensayos clínicos publicados entre 1995 y 2020. Los términos empleados fueron: estomatitis aftosa (stomatitis, aphthous), recurrencia de estomatitis aftosa (recurrent aphthous stomatitis), úlceras orales recurrentes (recurrent aphthous ulcers), trastornos inmunológicos (immunologic disorder), inmunodeficiencia (immunodeficiency). Los títulos y resúmenes de los artículos identificados se analizaron, excluyéndose los que no resultaron necesarios para esta investigación. El resto de los artículos se analizó en profundidad y en caso de desacuerdos, se resolvió mediante el consenso.
Extracción de datos
De cada uno de los estudios incluidos se obtuvo los siguientes datos: Autores, año de publicación, diseño del estudio, tipo y características de la intervención, descripción de los participantes (número, datos sobre edad y género), periodo de seguimiento y principales variables de resultado.
Calidad de los estudios
Tres de los autores evaluaron de modo independiente la calidad metodológica de los estudios con la herramienta propuesta por la colaboración Cochrane, la cual posibilita una evaluación del riesgo de sesgo basada en 6 dominios metodológicos: Generación de la secuencia, ocultamiento de la secuencia, cegamiento de los participantes y del personal, cegamiento de los evaluadores de los resultados, datos de resultados incompletos, comunicación selectiva de resultados y otras fuentes de sesgo. Cada dominio se evalúa en una escala de tres categorías: Bajo riesgo de sesgo, alto riesgo de sesgo, riesgo poco claro. En caso de discrepancias en las evaluaciones un cuarto autor evaluó el estudio, para debatir los resultados hasta obtener una evaluación y llegar a un consenso.
RESULTADOS
Información general de los estudios incluidos
En la figura 1 se muestra el proceso de selección de los estudios incluidos; inicialmente fueron identificados 113 registros de estudios (Figura 1), de los cuales 58 fueron irrelevantes. De los 55 restantes, 23 se excluyeron luego de leer el título y el resumen, quedaron 21 estudios potencialmente elegibles; de estos, no se consideraron 10 por presentar datos insuficientes, incluyéndose finalmente 11 estudios. 14,15,16,17,18,19,20,21,22,23,24
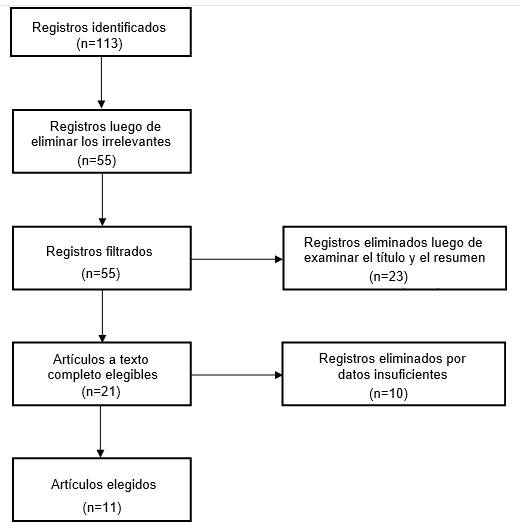
Fig 1 Diagrama de flujo del proceso de selección de los estudios incluidos en la revisión sistemática.
Se incluyeron 11 estudios que fueron publicados entre los años 1995 y 2020 y que aportan resultados sobre la eficacia de varias intervenciones terapéuticas: Talidomida (4), (14,15,16,17 irsogladine (2), rebamipida (1), láser de diodo (1), cápsulas de Omega-3 (1), vitamina B 12 (1), Complejo B (1). Ocho son ensayos controlados, (15,16,17,20,21,22,23,24 seis declaran que incluyeron pacientes que presentaban la forma menor de EAR. (15,17,21,22,23,24 El periodo de seguimiento fue desde los 14 hasta los 360 días y el tamaño de muestra entre 10 y 30 participantes. En tres estudios (16,19,23 no se aportan los datos del sexo y de estos en dos tampoco se informa sobre la edad de los participantes. 16,23) De los nueve estudios que aportan datos sobre la edad, uno informa el número de sujetos por debajo o encima de los 40 años (29 - 22), 21 tres describen el rango que va desde los 10 hasta los 78 años, tres estudios 15,22,24 reportan que en el grupo de estudio la edad promedio fue 36.2, 37.7, 36.76 y en el control 34.4, 37.71, 34.93 y dos que fueron de 48.5 y 59.6. 18,19) (Tabla 1)
Tabla 1 Características generales de los ensayos clínicos incluidos.
| Autor/es (año) | Intervención | Control | Tipo de EAR | Seguimiento (días) | Tamaño de muestra E/C | Sexo | Edad media (rango) |
|---|---|---|---|---|---|---|---|
| Paterson DL, et al. 14 (1995) | Talidomida 200 mg/d | No | ND | 14 | 20/0 | M | 26-53 |
| Jacobson JM, et al. 15) (1997) | Talidomida (200 mg /d) | Placebo | Menor | 28 | 29/28 | E: 26 M C: 24 M | E: 36.2 C: 34.4 |
| Jacobson JM, et al. 16) (2001) | Talidomida 100 mg 3 x semana | Placebo | ND | 180 | 23/26 | ND | ND |
| Mimura MA, et al. 17) (2009) 1 | Talidomida (100 mg/d) | Dapsona Colchicina Pentoxifilina | Menor:15 Mayor: 6 | 180-360 | Talidomina 7 Dapsona 8 Colchicina 5 Pentoxifilina 1 | 9 M | 35.5 (10-78) |
| Nanke Y, et al. (18) (2008) | Isogladine 2-4mg/ d | No | ND | 90 | 10/0 | 7 M | 48.5 |
| Hayashi N, et al. 19) (2013) | Melato de irsogladine 4mg/d | No | ND | 336 (48 s) | 10/0 | ND | 59.6 |
| Matsuda T, et al. 20) (2003) | Rebamipida 300 mg/d | Placebo | ND | 84-168 (12-24 s) | 19/16 | E: 9 M C: 5 M | E:46.7 (19-75) C: 44.3 (20-66) |
| Huo X, et al. 21) (2020) 2 | Láser de diodo | Acetato de triamcinolona 0.1% | Menor | 7 | 25/26 | E: 8 M C: 9 M | < 40 años E: 16 C: 13 |
| Hadian Z, et al.22 (2021) | 3 cápsulas diarias de Omega-3 (1000 mg) | Placebo | Menor | 180 | 20/20 | E: 11 M C: 10 M | E: 37.7 C: 37.71 |
| Golestannejad Z, et al. 23 (2017) 3 | Metilcobalamina | Triamcinolona | Menor | 9 | 20/20 | ND | ND |
| Rasi A, et al. 24 (2017) 4 | Inyectable | Oral | Menor | 56 | 30/30 | E: 17 M C: 13 M | E: 36.76 C: 34.93 |
1: Dapsona (25 mg/día por 3 días, 50 mg/día por 3 días, 75 mg/día por 3 días, 100 mg/día dosis mantenimiento), colchicina (0.5 mg/día por 7 días 1.0 mg/día por 7 días 1.5 mg/día dosis mantenimiento), pentoxifilina (400 mg 3 veces al día.
2: Láser de diodo (810 nm, 1.0 W, tiempo de irradiación 20 segundos para 3 aplicaciones) durante 3 días consecutivos y acetato de triamcinolona 0.1 % tres veces al día.
3: Metilcobalamina: una inyección diaria (0.1 cc/cm2) en la submucosa y triamcinolona: una inyección diaria (0.1 cc/cm2) en la submucosa.
4: Inyectable: Vitamina B (B1: 100 mg, B6: 100 mg, B12: 1000 μg) y oral: Complejo B (B1 + B2 + B6 + nicotinamide), una tableta de hierro, ácido fólico y vitamina C (250 mg).
Efectos de las intervenciones
Intervención terapéutica: Talidomida
Paterson DL, et al. 14 describe el uso de la talidomida (200 mg diarios por 14 días) en una serie de casos compuesta por 20 hombres con enfermedad ulcerativa dolorosa, portadores de VIH (edad 26-53 años) y que participaron en un ensayo clínico abierto entre julio de 1989 y marzo de 1993. El 80 % tiene un conteo de linfocitos T CD4+<200 μL.
Se observaron efectos adversos en 7 pacientes (35 %): erupción cutánea (5), neuropatía periférica (1) y fatiga excesiva (1). En 14 de los 16 pacientes con úlceras bucales se observó una cicatrización completa después de 14 días de tratamiento; los dos restantes necesitaron extender el tratamiento hasta los dos meses y solo se observó una mejoría en el proceso de cicatrización (alivio de los síntomas que no requiere terapia analgésica local). No se encontró diferencia estadísticamente significativa entre los conteos de linfocitos T CD4+ antes y después del tratamiento (p=0.06).
En 1997 Jacobson JM, et al. 15 publicaron los resultados de un ensayo clínico aleatorizado, a doble ciegas con grupo placebo como control para comparar la eficacia de la talidomida (200 mg 1 vez al día por cuatro semanas) en el tratamiento de la estomatitis aftosa recurrente en pacientes con VIH. Incluyó 57 pacientes mayores de 13 años (edad promedio cercana a los 35) con úlceras aftosas bucales de no más de 5 mm de diámetro y al menos 2 semanas de duración. De estos 29 en el grupo que recibió talidomida (26 M, 3 F; edad media: 36.2) y 28 en el grupo placebo (24 M, 4 F; edad media: 34.4).
El total de participantes se calculó asumiendo una potencia estadística del 80 % para detectar un cambio clínicamente importante en su variable de respuesta principal, cicatrización completa de úlceras aftosas después de 4 semanas de iniciado el tratamiento.
En este estudio, 16 de los 29 pacientes que recibieron talidomida experimentó una cicatrización completa de sus úlceras aftosas después de 4 semanas de tratamiento, en comparación con solo 2 en el grupo que recibió placebo (OR=15; IC 95 %: 1.8-499, p<0.001). El tiempo medio de cicatrización de las úlceras aftosas de estos 16 pacientes fue de 3.5 semanas (IC 95 %: 2-4).
Si este resultado se combina con el de los pacientes que experimentaron una cicatrización parcial, entonces el porcentaje de pacientes con cicatrización total o parcial pasadas 4 semanas de tratamiento con talidomida llega al 90 % (26) en comparación con el 25 % (7) observado en el grupo placebo (OR=24; IC 95 %: 5.2-162, p<0.001).
De los 29 pacientes tratados con talidomida, 12 presentaron efectos adversos. La somnolencia, la neuropatía sensorial periférica y la erupción cutánea fueron los más frecuentes (7 pacientes, 24 %), en 6 pacientes hubo que interrumpir el tratamiento debido a su toxicidad. Este tratamiento disminuye la intensidad del dolor y favorece la ingestión de alimentos.
En 2001 Jacobson JM, et al. 16 publicaron los resultados de un ensayo clínico multicéntrico, aleatorizado, a doble ciegas con grupo placebo como control para evaluar la seguridad y eficacia de las dosis reducidas e intermitentes de talidomida para prevenir la recurrencia de las lesiones aftosas en pacientes con VIH. Este estudio incluyó 49 pacientes (26 recibieron placebo y 23 talidomida) cuyas úlceras habían cicatrizado con un tratamiento previo de talidomida. El régimen de tratamiento consistió en 100 mg tres veces por semana durante 6 meses o hasta que se produzca la recidiva.
En el grupo tratado con talidomida el 61 % de los pacientes (14) experimentó recurrencia de sus úlceras bucales, mientras en el grupo placebo esto ocurrió en el 42 % de los pacientes (11). No hubo diferencias significativas entre los tiempos de recurrencia de las úlceras de ambos grupos (p=0.22). Entre los efectos adversos en los pacientes tratados con talidomida se encuentran la neutropenia (5 pacientes), la erupción cutánea (5) y neuropatía sensorial periférica (3).
Mimura MA, et al. 17 incluyeron 21 pacientes de entre 10 y 78 años [Hombres (10-58); mujeres (13-78)] con estomatitis aftosa recurrente grave en un ensayo clínico abierto cuyo propósito fue evaluar la eficacia de cuatro intervenciones terapéuticas [talidomida (0.5-1.5 mg/d), dapsona (25-100 mg/d), colchicina (0.5-1.5 mg/d), pentoxifilina (400 mg 3 veces al día)]. Seis presentan la forma mayor y 15 la forma menor.
La asignación se realizó sobre la base de que los cuatro grupos (talidomida, dapsona, colchicina, pentoxifilina) fuesen de similar tamaño. El tiempo de tratamiento fue de seis meses. Aquellos pacientes que presentaron efectos adversos o no respondieron al tratamiento asignado fueron reasignados a uno de los tres grupos restantes reiniciándose el umbral de tiempo de 6 meses. Una vez culminado el tratamiento, se siguió a los pacientes entre 6 y 12 meses.
La eficacia del tratamiento se evaluó sobre la base de su potencial para prevenir recidivas y reducir los síntomas, el número de úlceras y el tiempo de cicatrización. En este sentido, se utilizó una escala ordinal de 4 categorías: Excelente (paciente sin recidivas), Moderada (recidivas menos frecuentes, disminuyen las lesiones por ciclos y se alivian los síntomas), Ligera (solo se alivian los síntomas), No respuesta (sin mejoría observada). Los efectos adversos se agruparon en tres categorías: ligero (leve dolor gastrointestinal, nauseas), moderado (fatiga, diarreas, letargo, mareo, dolor de cabeza), severo (hemólisis, ictericia, hemoglobina baja).
De 8 los pacientes tratados con talidomida, 7 tuvieron una respuesta excelente y solo uno presentó efectos adversos ligeros. La colchicina también mostró buenos resultados pues 8 de los 10 pacientes tuvieron una respuesta excelente o moderada (4 excelente, 4 moderada) y solo 3 presentaron efectos adversos ligeros. En el caso de la dapsona, aún cuando la respuesta al tratamiento fue excelente o moderada en 8 de los 9 pacientes; 6 pacientes debieron abandonar el tratamiento debido a los efectos adversos (3 severos, 3 moderados). La pentoxifilina solo se administró en 5 pacientes, uno con una respuesta excelente, 2 con respuesta moderada y 2 sin respuesta. Solo un paciente presentó efectos adversos moderados. Durante el periodo de seguimiento todos los pacientes experimentaron recidivas entre las 2 semanas y los 9 meses.
Intervención terapéutica: Irsogladine
En 2003, Nanke Y, et al. 18 publicaron los resultados de un ensayo clínico abierto y no controlado que incluyó 10 pacientes con la enfermedad de Behçet (7 hombres y 3 mujeres), estomatitis aftosa recurrente y una edad promedio de edad de 48.5 años. El propósito fue evaluar la eficacia de la irsogladine (2-4 mg/día) sobre la base del hallazgo de lesiones macroscópicas de lesiones aftosas (número de úlceras). En todos los pacientes el promedio de úlceras aftosas disminuyó luego de 3 meses de tratamiento (p<0.0003). No se observaron efectos adversos.
Hayashi N, et al. 19) publicaron un ensayo clínico abierto y no controlado que incluyó 10 pacientes con virus de la hepatitis C que estando tratándose con interferón (durante 48 semanas) desarrollaron estomatitis aftosa, 3 de grado 3 y 7 de grado 2 según la escala de clasificación CTCAE (Common Terminology Criteria for Adverse Events). Fueron tratados por vía oral con melato de irsogladine (4 mg al día) observándose en 6 pacientes una respuesta eficaz (grado 0) durante la primera semana de tratamiento, en dos después de dos semanas y pasadas tres en los dos restantes. No se observó recurrencias en los 8 pacientes que mantuvieron dicho tratamiento durante todo el tiempo que estuvieron tratándose con interferón.
Intervención terapéutica: Rebamipida
Matsuda T, et al. 20 desarrolló entre agosto de 1994 y diciembre de 1996 un ensayo clínico multicéntrico, aleatorizado, a doble ciegas, con placebo como control, para evaluar la eficacia de un tratamiento con rebamipida (300 mg/día entre 12 y 24 semanas) en términos de intensidad del dolor (ninguno (0), ligero (1), moderado (2), fuerte (3)) y del número de aftas. El estudio incluyó 35 pacientes con la enfermedad de Behçet (16 recibieron placebo y 19 rebamipida) entre 19 y 75 años (placebo: 20-66; rebamipida: 19-75).
Los investigadores tomaron de cada paciente los datos diarios sobre el número de aftas e intensidad del dolor y propusieron una escala de 6 categorías (fuerte, moderada, ligera, sin cambios, empeoramiento, no juzgable) para evaluar la eficacia del tratamiento concluyendo que resultó eficaz en relación al placebo para disminuir el número de aftas pues en el 65 % de los pacientes tratados con rebamipida se observó una disminución moderada o fuerte del número de aftas contra un 36 % en los que recibieron placebo. Respecto a la intensidad del dolor, el 43 % de los pacientes del grupo placebo experimentó una disminución moderada o fuerte, mientras en el grupo tratado con rebamipida fue del 65 %.
Intervención terapéutica: Láser de diodo
Entre enero de 2018 y diciembre de 2019 Huo X, et al. 21 ejecutaron un ensayo clínico aleatorizado y controlado con el objetivo de evaluar el efecto clínico del láser de diodo y del tratamiento convencional (acetato de triamcinolona 0.1 %) en pacientes con estomatitis aftosa recurrente que poseen solo una lesión bucal (afta menor de diámetro<10 mm) de no más de 3 días de aparición. El número de participantes (56, 28 en cada grupo) se determinó asumiendo un nivel de significación del 5 %, una potencia del 80 % y una diferencia mínima en la intensidad del dolor entre los dos protocolos de tratamiento de 3.53.
El grupo asignado a la terapia láser (25 pacientes, 3 pérdidas) fue tratado con un láser de diodo (810 nm, 1.0 W, tiempo de irradiación 20 segundos para 3 aplicaciones) durante 3 días consecutivos; mientras el otro (26 pacientes, 2 pérdidas) con acetato de triamcinolona 0.1 % tres veces al día. Ambos grupos fueron similares en edad, sexo.
Al tercer día de tratamiento el dolor espontáneo (percepción de dolor sin realizar actividad alguna) y el dolor funcional (dolor al masticar, beber o hablar) fueron significativamente inferiores en el grupo tratado con láser de diodo (dolor espontáneo: 0.60 ± 0.25; dolor funcional: 1.36 ± 0.33) en relación con las cifras obtenidas en el grupo que recibió tratamiento con triamcinolona 0.1 % (dolor espontáneo: 3.00 ± 0.44; dolor funcional: 4.00 ± 0.46). En ambos casos la diferencia fue estadísticamente significativa (p=0.00). Respecto al tiempo de cicatrización (días), se observó una diferencia estadísticamente significativa (Láser: 6.60 ± 0.29; A triamcinolona 0.01 %: 7.77 ± 0.52; p=0-03) aunque no relevante desde el punto de vista clínico.
Intervención terapéutica: Omega 3
En febrero de 2021 Hadian Z, et al. 22 publicaron los resultados de un ensayo clínico aleatorizado, a doble ciegas controlado (placebo) cuyo propósito fue evaluar el efecto del suplemento Omega-3 en pacientes con estomatitis aftosa recurrente. Incluyó 40 sujetos mayores de 18 años con recurrencia de al menos una úlcera aftosa mensual y que presentan al momento de su reclutamiento entre 1 y 3 úlceras aftosas menores cuyo momento de aparición es de al menos 48 h. El grupo de estudio (20 sujetos; 11 hombres) recibió cápsulas de Omega-3 de 1000 mg tres veces al día durante un periodo de tiempo de 6 meses, el grupo placebo (20 sujetos; 10 hombres) recibió cápsulas de similar formato que contenían harina. Ambos grupos fueron similares en la edad promedio (Placebo: 37 años,75 años y Omega-3: 37 años,75 años) y el sexo (Placebo: 10 hombres y 10 mujeres, Omega-3: 11 hombres y 9 mujeres).
Antes de iniciar el tratamiento, a los 3 meses de iniciado y al culminar (6 meses) se aplicaron dos cuestionarios. El primero orientado a obtener evidencias sobre el grado de severidad de las úlceras (tamaño, cantidad, duración (semanas), intensidad del dolor, tiempo de recurrencia, sitio). El segundo, diseñado para valorar la calidad de vida de los pacientes con enfermedades crónicas de la mucosa que incluye 26 ítems evaluados en una escala Likert de 5 categorías que van desde Nunca (0) hasta muy frecuente (4).
A los 3 meses de iniciado el tratamiento se observó una diferencia estadísticamente significativa en el número de úlceras (Placebo: 2.45 y Omega-3: 1.9; p=0.018) y su duración (Placebo: 8.83 y Omega-3: 4.94; p<0.0001), así como en el puntaje total del grado de severidad de las úlceras (Placebo: 30.35 y Omega-3: 25.75; p<0.0001). No hubo diferencias significativas en el tamaño (Placebo: 4.65 y Omega-3: 4.37; p=0.08), intensidad del dolor (Placebo: 7.2 y Omega-3: 4.9; p=0.07) y en el tiempo libre de úlceras (Placebo: 3.1 y Omega-3: 3.2; p=0.65).
Sin embargo, a los 6 meses hubo diferencias estadísticamente significativas (p<0.0001) en todas las características de las úlceras aftosas. Asimismo, el puntaje medio del cuestionario sobre calidad de vida de los pacientes con enfermedades crónicas mejoró a los 3 y 6 meses en el grupo que recibió tratamiento con Omega-3.
Intervención terapéutica: Vitamina B 12
Golestannejad Z, et al. 23 incluyó en un ensayo clínico a simple ciega a 40 pacientes con lesiones aftosas (forma menor) de no más de 48 h de aparición, los cuales fueron asignados aleatoriamente a 2 grupos (20 sujetos) con el objetivo de evaluar el efecto de la metilcobalamina sobre la intensidad del dolor y el periodo de recuperación. Durante 9 días los pacientes del grupo de estudio recibieron una inyección de B12 (metilcobalamina 0.1 cc/cm2) en la submucosa; mientras los del control una de triamcinolona (0.1 cc/cm2).
La intensidad del dolor se midió a través de una escala ordinal (numérica) basada en la percepción del paciente y donde el valor cero (0) representa la ausencia de dolor. El periodo de recuperación se refiere al número de días requeridos para que el paciente refiera ausencia de dolor (valor cero).
Los resultados muestran que la inyección de metilcobalamina reduce significativamente el dolor en comparación con la inyección de triamcinolona (p<0.05) y disminuye el tiempo de recuperación (Metilcobalamina: 4.85 (1.4 y triamcinolona: 6.3(1.2; p<0.001).
Entre los años 2015 y 2017 Rasi A, et al. (24 desarrolló un ensayo clínico que incluyó 60 pacientes mayores de 18 años con estomatitis aftosa recurrente, sin enfermedades sistémicas asociadas, que en el último año habían presentado lesiones aftosas (forma menor) con intervalos de recurrencia no mayor de 2 meses y que al momento de su inclusión en el estudio exhibían lesiones con no más de 72 h de aparición.
Estos fueron asignados aleatoriamente a dos grupos de 30 pacientes. Uno de los grupos fue tratado con una forma inyectable de vitamina B (B1: 100 mg, B6: 100 mg, B12: 1000 μg) y el otro recibió un tratamiento oral que incluyó complejo B (B1 + B2 + B6 + nicotinamide), una tableta de hierro, ácido fólico y vitamina C (250 mg). El tiempo de seguimiento fue de 10 meses.
La eficacia de estas intervenciones se midió en una escala ordinal [Alta (sin recidivas), Moderada (algunas recidivas, alivio de síntomas y se reduce el tiempo de recuperación), Baja (solo alivio de síntomas), Sin respuesta] que refleja su potencial para prevenir las recurrencias, disminuir los síntomas, el número de lesiones y el tiempo de recuperación del paciente.
La forma inyectable mostró mejor eficacia que la forma oral (p<0.001) pues en el grupo inyectable fue alta en 14 pacientes, moderada en 12 y baja en 4; mientras en el grupo oral, fue moderada en 9 pacientes y baja en 12. En los restantes 9 no se observó respuesta.
Variables de resultado
Los cuatro estudios que emplean la talidomida 14,15,16,17 reportan efectos adversos y difieren en el periodo de seguimiento. Dos de ellos usan la cicatrización de la úlcera aftosa bucal como indicador de la eficacia del tratamiento, 14,15 pero con diferentes métodos de valoración (Visual y endoscopia). En tres de estos 14,15,17 se concluye que la talidomida es eficaz en el tratamiento de la EAR.
De los 7 estudios restantes, ninguno reporta efectos adversos, 18,19,20,21,22,23,24 dos usan la intensidad del dolor y el tiempo de cicatrización 21,23 para evaluar la eficacia del tratamiento (métodos de valoración distintos), uno las recurrencias, los síntomas y el tiempo de recuperación 24 y 4 emplean variables de resultado compuestas, 17,20,22,24 aunque difieren en los parámetros que incluyen. En todos se concluye que los tratamientos resultan eficaces. (Tabla 2)
Tabla 2 Principales resultados de los estudios incluidos.
| Autor/es (año) | Variables medidas | Efectos adversos | Resultados |
|---|---|---|---|
| Paterson DL, et al. 14 (1995) | Cicatrización de la úlcera aftosa bucal | Erupción cutánea, fatiga, neuropatía periférica | El tratamiento con talidomida es eficaz para lograr una cicatrización completa de las úlceras aftosas bucales. |
| Jacobson JM, et al. 15) (1997) | Cicatrización de la úlcera aftosa bucal, intensidad del dolor | Somnolencia y erupción cutánea | La talidomida es más eficaz que el placebo para lograr una cicatrización de las úlceras aftosas bucales, disminuye la intensidad del dolor. |
| Jacobson JM, et al. 16) (2001) | Tiempo de recurrencia, recurrencia | Neutropenia, erupción cutánea y neuropatía sensorial periférica | La talidomida en dosis reducidas e intermitentes no es eficaz para prevenir la recurrencia de las úlceras bucales. |
| Mimura MA, et al. 17) (2009) | Recurrencia, síntomas, número de úlceras, tiempo de cicatrización | Dolor gastrointestinal leve, náuseas | El tratamiento con talidomida es más eficaz en comparación con la dapsona, colchicina y la pentoxifilina. |
| Nanke Y, et al. 18) (2008) | Número de aftas bucales | No declara | El tratamiento con irsogladine es eficaz. |
| Hayashi N, et al. 19) (2013) | Grado de estomatitis aftosa | No declara | El tratamiento con irsogladine es eficaz. |
| Matsuda T, et al. 20) (2003) | Número de úlceras aftosas bucales, intensidad del dolor | No declara | El tratamiento con rebamipida es eficaz en relación al placebo. |
| Huo X, et al. 21) (2020) | Intensidad del dolor, tiempo de cicatrización | No declara | El láser de diodo es más eficaz en el alivio de la intensidad del dolor. |
| Hadian Z, et al. 22 (2021) | Severidad de la úlcera aftosa bucal | No declara | El suplemento oral Omega-3 disminuye la severidad de la úlcera aftosa bucal. |
| Golestannejad Z, et al. 23) (2017) | Intensidad del dolor, tiempo de recuperación | No declara | La metilcobalamina reduce significativamente el dolor y disminuye el tiempo de recuperación en comparación con la triamcinolona. |
| Rasi A, et al. 24 (2017) | Recurrencia, síntomas, tiempo de recuperación | No declara | La forma inyectable mostró mejor eficacia que la oral. |
Calidad de los estudios
De los 8 ensayos controlados (Tabla 3), solo 2 explican el método empleado para generar la secuencia aleatoria 21,24 y ninguno expone el método empleado para ocultar la secuencia aleatoria. Respecto al enmascaramiento de los participantes y del personal implicado, en 5 estudios existe un alto riesgo de sesgo, (14,17,18,19,23 en 5 un riesgo bajo 15,16,20,21,22 y en uno no se detalla. 24) Sobre el enmascaramiento de la medida de los resultados, 3 estudios tienen un riesgo alto. 14,18,19 El riesgo de una comunicación selectiva fue bajo en todos los estudios. Dos estudios presentan datos incompletos. 17,20
Tabla 3 Valoración de los autores sobre el riesgo de sesgo en los estudios incluidos
| Autor/es (año) | Generación de secuencia (Sesgo de selección) | Ocultación de la secuencia (Sesgo de selección) | Cegado de los participantes y el personal (sesgo de ejecución) | Cegado en la evaluación de los resultados (sesgo de detección) | Datos incompletos (sesgo de atrición) | Comunicación selectiva (sesgo de publicación) | Libre de otros sesgos |
|---|---|---|---|---|---|---|---|
| Paterson DL, et al. (14) (1995) | Alto | Alto | Alto | Alto | Bajo | Bajo | No claro |
| Jacobson JM, et al. (15) (1997) | No claro | No claro | Bajo | Bajo | Bajo | Bajo | No claro |
| Jacobson JM, et al. (16) (2001) | No claro | No claro | Bajo | Bajo | Bajo | Bajo | No claro |
| Mimura MA, et al. (17) (2009) | Alto | No claro | Alto | Bajo | Alto | Bajo | No claro |
| Nanke Y, et al. (18) (2008) | Alto | Alto | Alto | Alto | Bajo | Bajo | No claro |
| Hayashi N, et al. (19) (2013) | Alto | Alto | Alto | Alto | Bajo | Bajo | No claro |
| Matsuda T, et al. (20) (2003) | No claro | No claro | Bajo | Bajo | Alto | Bajo | No claro |
| Huo X, et al. (21) (2020) | Bajo | No claro | Bajo | Bajo | Bajo | Bajo | No claro |
| Hadian Z, et al. (22) (2021) | No claro | No claro | Bajo | Bajo | Bajo | Bajo | No claro |
| Golestannejad Z, et al. (23) (2017) | No claro | No claro | Alto | Bajo | Bajo | Bajo | No claro |
| Rasi A, et al. (24) (2018) | Bajo | No claro | No claro | Bajo | Bajo | Bajo | No claro |
DISCUSIÓN
Fueron analizados 11 estudios que evalúan la eficacia de 10 intervenciones terapéuticas diferentes para el tratamiento de la estomatitis aftosa recurrente, pero presentan una gran heterogeneidad con respecto a los desenlaces evaluados y a los métodos de valoración utilizados. En los que emplean la intensidad del dolor como variable de respuesta principal, 21,23 resulta complejo comparar sus resultados dado que utilizan diferentes métodos de valoración. Algo similar ocurren en los 4 estudios que utilizan variables compuestas 17,20,22,24 pues difieren los parámetros que incluyen.
Varios de los estudios no prestaron atención a la declaración de los efectos adversos 18,19,20,21,22,23,24 y ello puede limitar la generalización de las intervenciones a casos específicos. Aunque la mayoría de los estudios sobre la terapia de la talidomida para pacientes con VIH declararon la efectividad de la intervención, se identifica cierta inconsistencia entre los resultados de estas investigaciones. Por ejemplo, algunos autores 14 reconocieron que el mecanismo del efecto de la talidomida era incierto, ya que los síntomas reaparecen después de interrumpir el tratamiento y se registra la presencia de eventos adversos.
La talidomida en dosis intermitentes más bajas es ineficaz para prevenir la recurrencia de úlceras aftosas en personas infectadas por el VIH. 16 Sin embargo, otros autores 15,17) refieren que es eficaz para la curación completa de la úlcera y para el alivio del dolor, aunque el número de participantes en el ensayo es reducido y no hubo asignación aleatoria. La irsogladine 18,19 y la rebamipida (20 pueden ser útiles en el tratamiento de la EAR en pacientes con enfermedad de Behcet y EAR; sin embargo, sus resultados deben ser interpretados con cautela dado que incluyeron pocos pacientes.
El tratamiento con láser de diodo 21 muestra una disminución importante en la intensidad del dolor en comparación con el tratamiento de triamcinolona 0.1 %, aunque no muestra una diferencia importante respecto al tiempo de cicatrización, mientras un tratamiento con vitamina B12 23 produce una disminución tanto de la intensidad del dolor como del tiempo de recuperación resultado, similar al aportado por Taleb R, et al. 25 quienes afirman que el 77 % de los sujetos tratados con metilcobalamina (500 μg B12) experimentó una importante mejoría en el disco bucal y una reducción del dolor.
Los estudios revisados pudieran tomarse como fundamento para la elaboración de guías de prácticas clínicas en la atención a la estomatitis aftosa recurrente en pacientes inmunocomprometidos. No obstante, las investigaciones precedentes han destacado que se necesita de un mayor número de ensayos clínicos para evaluar la eficacia y seguridad de los agentes tópicos para el tratamiento de la EAR. 7
CONCLUSIONES
La evidencia disponible sugiere que, de los tratamientos incluidos en la revisión, la talidomida puede ser eficaz en el alivio de los síntomas, la cicatrización y remisión de las lesiones; mientras el diodo de láser y vitamina B12 en la disminución de la intensidad del dolor. Sin embargo, debido a la heterogeneidad de los estudios incluidos y a lo pequeña de sus muestras, se necesitan diseñar ensayos clínicos con tamaños de muestra adecuados para evaluar la eficacia de estas intervenciones.














