INTRODUCCIÓN
La enfermedad inflamatoria pélvica aguda (EIPA) es una de las enfermedades infecciosas más frecuentes e importantes en las mujeres no embarazadas en edad reproductiva, y constituye un problema de salud pública debido a sus manifestaciones clínicas y secuelas. Representa el 20 % de las consultas ginecológicas. En Estados Unidos se estima que cada año más de un millón de mujeres sufren un episodio de EIPA, más del 25 % tienen menos de 25 años y un 75 % son nulíparas. Esta entidad es responsable del 20 % de los casos de infertilidad.1-3 En la mayoría de los países latinoamericanos no se cuenta con cifras confiables sobre la incidencia de EIPA ni a nivel nacional ni regional, ya que las formas subclínicas son subdiagnosticadas y no es una enfermedad de declaración obligatoria, pero es sabido que se trata de una entidad frecuente.4 Se considera que en más del 90 % de todas las EIPA se encuentra presente un episodio reciente de ITS (infección transmisión sexual). En Cuba, según el Anuario estadístico de salud 2015, hubo un aumento de los casos de blenorragia en el sexo femenino con respecto al año 2014.5
El diagnóstico tradicional se ha basado en una tríada integrada por dolor pélvico, dolor a la movilización del cérvix y dolor anexial al tacto. El dolor pélvico de cualquier tipo tiene alta sensibilidad (> 95 %) para EIPA y constituye la causa más frecuente de consulta.6,7 La ecografía resulta un medio diagnóstico con respaldo científico para su evaluación, accesible, económico, con una alta efectividad y de gran utilidad para valorar la evolución de la enfermedad y la respuesta al tratamiento.8,9
Según su gravedad la entidad se clasifica en grado I (leve), grado II (moderada) y grado III (grave).10 Los casos leves y moderados pueden ser manejados de forma ambulatoria, pero los severos requieren hospitalización. La etiología polimicrobiana está claramente aceptada, por lo que debe instaurarse rápidamente tratamiento con antibióticos que ofrezcan cobertura contra un amplio espectro de patógenos.7
El tratamiento con antinflamatorios no esteroideos (aines) se utiliza tempranamente en la fase aguda de la enfermedad para el alivio de los síntomas y la prevención de las secuelas, ya que la inflamación se considera responsable del desarrollo de complicaciones reproductivas.11 El piroxicam supositorio se encuentra entre los de mayor prescripción, por su probada eficacia y las ventajas que ofrece la vía de administración empleada.
La estreptoquinasa recombinante (SKr) es una proteína de origen bacteriano con actividad trombolítico en el tratamiento del infarto agudo de miocardio y otras afecciones trombóticas. Tiene una acción antiinflamatoria, dada por el efecto trombolítico en sí mismo al activar el sistema del plasminógeno-plasmina, por despolimerización de las proteínas macromoleculares de prefibrina, la eliminación de coágulos de fibrina y activación de peptidasas que antagonizan citocinas que participan en la inflamación.12,13
En Cuba, desde 2012, se cuenta con una formulación de estreptoquinasa recombinante (SKr) en supositorio (Proctokinasa®) 200 000 UI, con acciones trombolítica y antiinflamatoria demostradas. Es un producto seguro y tolerable, con mínimos eventos adversos.14 A esto se suma la posibilidad de su aplicación a través de la vía rectal, no invasiva, y el breve tiempo de su administración que propicia la adherencia al tratamiento. El propósito de este trabajo es evaluar la eficacia y seguridad del tratamiento con Proctokinasa® en la EIPA grados I y II.
MATERIALES Y MÉTODOS
Se realizó un ensayo clínico experimental fase II, prospectivo, aleatorizado, controlado, con grupos paralelos, abierto, en pacientes mayores de 18 años con diagnóstico de EIPA grados I y II tributarias de tratamiento ambulatorio. Se evaluaron todas las pacientes con diagnóstico de EIPA recibidas en un servicio de ginecobstetricia del nivel de atención primaria en Matanzas, entre enero de 2017 y enero de 2018. Se incluyeron en el estudio 76 pacientes que firmaron el consentimiento informado y cumplieron los criterios de inclusión. Se excluyeron del estudio las pacientes con participación en otro ensayo clínico, las que estuvieran lactando, o aquellas con antecedentes de hipersensibilidad al producto o a cualquiera de los componentes de la formulación, con diagnóstico clínico y ecográfico de EIPA grave o con criterios de hospitalización, con cirugía de menos de siete días, sangramiento activo o desorden hemorrágico diagnosticado con anterioridad o con hipertensión descompensada.
Esta investigación se realizó de acuerdo a lo establecido en la declaración de Helsinki y su protocolo fue revisado y aprobado por el Comité de Ética para la Investigación de la Universidad de Ciencias Médicas de Matanzas.
El diagnóstico fue confirmado clínica y ecográficamente. La muestra de estudio se dividió en dos grupos de 38 pacientes cada uno. El grupo 1 fue tratado con supositorio de Proctokinasa® 200 000 UI -producido en el Centro de Ingeniería Genética y Biotecnología, de La Habana-, 1 supositorio cada 8 horas por 2 días, y el grupo 2 recibió supositorio de Piroxicam 20 mg, 1 supositorio cada 24 horas por 7 días. Las características organolépticas, presentación y regímenes terapéuticos fueron diferentes, lo cual determinó que el estudio no se pudiera enmascarar. La asignación a uno u otro grupo se realizó al azar, utilizando una lista creada por medios computarizados.
Adicionalmente, las pacientes recibieron tratamiento antimicrobiano con ciprofloxacino (250 mg): 2 tabletas en dosis única, azitromicina (500 mg): 2 g (1 g semanal), metronidazol (250 mg): 2 tabletas cada 12 horas por 10 días, y la recomendación de reposo físico y sexual.3,15
Se aplicó escala visual analógica del dolor en el momento del diagnóstico, evaluándose el dolor como leve cuando la puntuación estuvo entre 1-3; moderado, entre 4-6, y severo entre 7-10.16
Al tomar como punto base la intensidad del dolor antes de iniciar el tratamiento, se consideró respuesta clínica si se constató reducción de la misma de una medición a otra en al menos 20 mm al 3er, 5to, 10mo y 15to días. Una variable igualmente significativa para evaluar la respuesta al tratamiento, fue la evolución de los hallazgos ecográficos con la constatación de la remisión o persistencia de los mismos en la ecografía transvaginal evolutiva al 5to día de tratamiento.
Los eventos adversos relacionados con la medicación fueron identificados y cuantificados para cada grupo de tratamiento, y recogidos en la base de datos.
Estadística: Los datos correspondientes a las variables del estudio fueron introducidos en una base de datos creada al efecto en el paquete estadístico SPSS en su versión 22 para su posterior análisis. Se utilizaron frecuencias absolutas y relativas para variables cualitativas y la media y la desviación estándar para variables cuantitativas. Para evaluar la comparabilidad de los grupos de tratamiento y de los resultados obtenidos con la intervención se utilizó la prueba de chi cuadrado para variables cualitativas y la t-Student para variables cuantitativas.
RESULTADOS
Entre las características sociodemográficas y clínicoecográficas estuvieron edades predominantes entre los 20 a 39 años y una mayor representación de la raza blanca (> del 50 %), el dolor en el momento del diagnóstico era intenso en la mayoría de las pacientes (76,3 % grupo Proctokinasa® y 50 % grupo Piroxicam), asociado al dolor bajo vientre se detectó como síntoma más frecuente la leucorrea en el 100 % de los casos.
Para corroborar el diagnóstico se realizó ecografía que mostró anejos engrosados como hallazgo más frecuente en el 65,8 % y el 52,6 % de los grupos Proctokinasa® y Piroxicam respectivamente, no encontrando diferencias significativas entre ambos grupos.
Durante el seguimiento se perdieron 12 pacientes que abandonaron el estudio, 6 en cada grupo; por este motivo se excluyeron de la presentación de los resultados evolutivos.
En la tabla 1 se muestra la respuesta clínica obtenida según grupo de tratamiento y momentos de evaluación. A los tres días hubo respuesta en más de la mitad de las pacientes con independencia del tratamiento recibido; en el grupo Proctokinasa® en el 65,6 % de las pacientes hubo disminución de la intensidad del dolor mayor de 20 mm en la escala analógica, mientras que en el grupo Piroxicam esta respuesta fue de 56,2 %. A los cinco días los porcentajes de respuesta clínica superaron el 85 % y en las evaluaciones realizadas los días 10 y 15 en el grupo Proctokinasa® fue del 100 %.
Tabla 1 Distribución de pacientes según respuesta clínica, grupo de tratamiento y períodos de evaluación
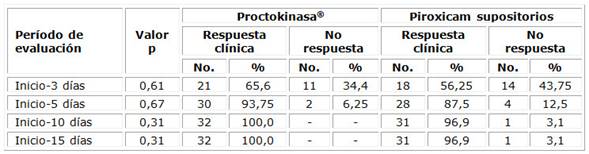
* Doce pacientes no asistieron a las consultas de seguimiento. n= 32
En cuanto a la intensidad del dolor, se apreció una reducción paulatina de los valores medios obtenidos en la escala visual analógica, en la medida que avanzó el tratamiento en ambos grupos, que sin que se encontraran diferencias significativas, resultó más evidente en el grupo Proctokinasa® donde a partir del 5to día se obtuvieron cifras medias inferiores a las reportadas en el grupo Piroxicam. (Gráfico)
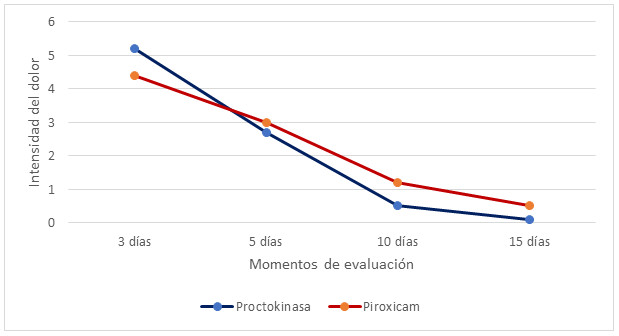
Gráf Valores medios de la intensidad del dolor (escala analógica del dolor) según grupo de tratamiento.
Los resultados del estudio ecográfico evolutivo al 5to día de iniciadas las terapias se muestran en la tabla 2. En 31 de las pacientes del grupo Proctokinasa® (96,9 %), el estudio resultó negativo, en el grupo Piroxicam la negativización de la ecografía se corroboró en 28 pacientes para un 87,5 %, las diferencias antes comentadas no fueron estadísticamente significativas.
Tabla 2 Distribución de pacientes según hallazgos ecográficos evolutivos y grupo de tratamiento
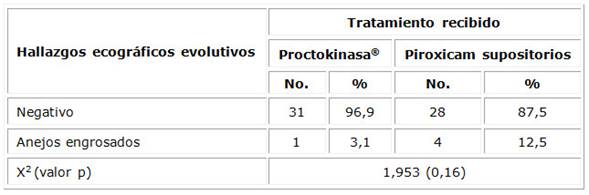
* Doce pacientes no asistieron a las consultas de seguimiento. n= 32
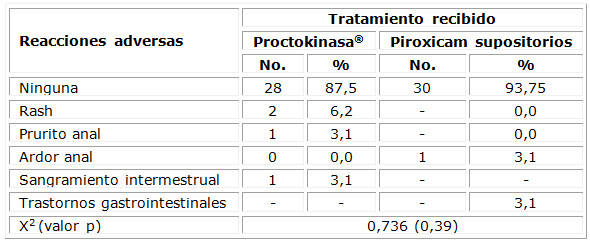
Ambos tratamientos se consideraron seguros, fueron reportados 4 eventos adversos en el grupo Proctokinasa® y 2 en el grupo Piroxicam, que se presentan en la tabla 3. No se encontraron diferencias significativas entre los grupos de tratamiento respecto a esta variable.
DISCUSIÓN
Las características clínico-ecográficas de las pacientes que formaron parte de este estudio son coincidentes con lo reportado en la literatura, en la que se hace referencia a la significación del dolor como síntoma asociado al diagnóstico clínico de EIPA, junto a síntomas y signos acompañantes tales como leucorrea y fiebre,17,18 así como la importancia de los hallazgos ecográficos y su relevancia para la confirmación del diagnóstico y clasificación del grado o estadio de la EIPA.1,8
Los objetivos terapéuticos en la EIPA incluyen la supresión de la infección aguda, de los síntomas y la prevención de las secuelas, su etiología poli microbiana está claramente aceptada, por lo que debe ser tratada con antibióticos que ofrezcan amplia cobertura. Asimismo, se recomienda tratamiento con antinflamatorios no esteroideos para el alivio de los síntomas inflamatorios incluido el dolor y para prevenir secuelas, ya que la inflamación se considera responsable del desarrollo de complicaciones reproductivas.4,8,11
En este estudio la respuesta clínica en ambos grupos de tratamiento fue evidente, ocurrió desde el tercer día en más de la mitad de las pacientes y en las dos últimas evaluaciones (días 10 y 15) en el grupo Proctokinasa® estuvo presente en el total de los casos, mientras que en el grupo Piroxicam se mantuvo una paciente con dolor. Así mismo, pudo apreciarse una reducción paulatina de los valores medios de dolor en la medida que avanzó el tratamiento en ambos grupos, lo que puso de manifiesto la contribución de la Proctokinasa® en el grupo de estudio para el control de los síntomas inflamatorios y el dolor, acción previamente confirmada en estudios clínicos realizados con este producto.12-16
En cuanto a la evolución de los hallazgos ecográficos pudo apreciarse que habían desaparecido en casi la totalidad de los casos al 5to día de tratamiento; siendo más evidente en el grupo Proctokinasa® en el que en solo un paciente persistió el engrosamiento de los anejos. Estos resultados son reflejo de la evolución satisfactoria de la EIPA en las pacientes incluidas en el presente estudio, reforzando la importancia de la ecografía evolutiva en la evaluación objetiva de la respuesta a los tratamientos indicados, a través de un procedimiento seguro y no invasivo.1,8
Los eventos adversos que aparecieron en las pacientes tratadas con Proctokinasa® fueron escasos y resolvieron de forma espontánea, de manera similar a lo ocurrido en el control piloto realizado.12
Los resultados del presente ensayo clínico mostraron la eficacia del supositorio Proctokinasa® en el control de síntomas inflamatorios y el dolor en la EIPA grados I y II con un perfil de seguridad adecuado.
Código del Registro Público de Ensayos Clínicos: RPCEC00000416.