Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Anestesiología y Reanimación
versión On-line ISSN 1726-6718
Rev cuba anestesiol reanim vol.16 no.2 Ciudad de la Habana may.-ago. 2017
ARTÍCULO ORIGINAL
Administración de lidocaína en infusión continua en pacientes sometidos a procedimientos quirúrgicos abdominales oncológicos
Administration of lidocaine by continuous infusion in patients undergoing oncological adnominal surgical procedures
Dr. Guillermo Capote Guerrero,I Dr. C. Yurisnel Ortiz Sánchez,II Dr. Domingo Angel Labrada Tapia,I Dra. Yacnira Martínez Bazán,I Dr. Ramón Fernández LeyvaII
I Hospital General docente "Carlos Manuel de Céspedes". Cuba.
II Universidad de Ciencias Médicas Bayamo. Cuba.
RESUMEN
Introducción: La administración de lidocaína intravenosa para el control del dolor posoperatorio ha ganado interés. Su aplicación en el periodo perioperatorio a dosis baja reduce el dolor y el consumo de opioides en el posoperatorio.
Objetivo: Evaluar la eficacia de la administración de lidocaína en infusión continua en el tratamiento del dolor posoperatorio en pacientes intervenidos quirúrgicamente por enfermedad abdominal oncológica.
Métodos: Se realizó un estudio cuasi experimental en pacientes intervenidos por procedimiento quirúrgico abdominal oncológico a quienes se les administró infusión continua de lidocaína. Seguidamente se les evaluó la intensidad del dolor con la escala visual análoga. Esta se aplicó a los 30 min, 2, 6, 12 y 24 h después de la operación. Se determinó la presencia o no de complicaciones intra- y posoperatorias.
Resultados: Los pacientes entre 31 y 50 años de edad prevalecieron en ambos grupos. El sexo masculino predominó en el grupo estudio y el femenino en el control. En el grupo estudio la respuesta no fue satisfactoria solo en dos pacientes, en 11 pacientes fue satisfactoria, en el testigo en cinco pacientes fue no satisfactoria. En el grupo estudio tres pacientes tuvieron dolor por menos de 2 h y fue catalogado entre ligero y moderado. En el control 12 presentaron dolor por más de 4 h catalogado entre moderado y grave. En dos pacientes aparecieron efectos adversos.
Conclusiones: Con la administración de lidocaína se logra una disminución del dolor y del consumo de opioides.
Palabras clave: Procedimiento quirúrgico oncológico; lidocaína; infusión continua; cáncer.
ABSTRACT
Introduction: The intravenous administration of lidocaine for postoperative pain control has gained interest. Its administration in the perioperative period and at a low dose reduces postoperative pain and opioid use.
Objective: To evaluate the effectiveness of continuous infusion of lidocaine in the treatment of postoperative pain in surgically intervened patients with oncologic abdominal disease.
Methods: A quasiexperimental study was performed in patients undergoing oncologic abdominal surgical procedures and who were given continuous infusion of lidocaine. The pain intensity was then evaluated with the analogue visual scale. This was applied after 30 minutes, two, six, twelve and twenty-four hours after the operation. The presence or absence of intraoperative and postoperative complications was determined.
Results: Patients aged 31-50 prevailed in both groups. The male gender predominated in the study group and the female gender, in the control group. In the study group, the response was not satisfactory only in two patients, while it was satisfactory in 11 patients; in the control group, it was not satisfactory in 5 patients. In the study group, three patients had pain for less than 2 hours and this was classified as mild to moderate. In the control group 12 of them presented pain for more than 4 hours, which was classified as moderate and severe. Adverse effects appeared in two patients.
Conclusions: The administration of lidocaine leads to a decrease in pain and opioid consumption.
Key words: Oncological surgical procedure; lidocaine; continuous infusion; cancer.
INTRODUCCIÓN
Uno de los principales retos de los anestesiólogos es lograr una recuperación temprana de los pacientes durante el periodo posoperatorio.1 Por lo tanto, resulta esencial resolver de forma precoz los síntomas que, con mayor frecuencia se presentan en esta etapa, entre los cuales se encuentran dolor, náuseas y vómitos. La terapéutica habitual para resolverlos consiste en la administración parenteral de analgésicos y antieméticos. En la práctica médica se observa que estos medicamentos constituyen un factor desencadenante de reacciones alérgicas en pacientes susceptibles.2,3
El dolor agudo posoperatorio fue señalado por la American Association of Anesthesiologists (ASA) en 1995, como la sensación que está presente en el paciente quirúrgico debido a la enfermedad, al procedimiento quirúrgico y sus complicaciones, o a una combinación de ambos.4
El dolor posoperatorio, llamado el quinto signo vital, es usualmente grave e incapacitante; además, es infravalorado y tratado de forma insuficiente, por estar influenciado por diversos factores, entre los que se encuentran la dificultad para su valoración y el miedo a las medicaciones (causa más común de efectos adversos e interacciones).4-7
Existe consenso en que el dolor intraoperatorio está condicionado por una serie de factores epidemiológicos como son la intervención quirúrgica, el paciente, la preparación quirúrgica, las complicaciones que pueden surgir en el perioperatorio, la técnica anestésica empleada y los cuidados posquirúrgicos. Es predecible, por cuanto resulta de una agresión planificada y deliberada, que aparece al inicio del procedimiento quirúrgico y que finaliza con la curación de la enfermedad quirúrgica que lo ha generado. Por lo común, resulta intenso inmediatamente después del procedimiento quirúrgico y autolimitado. Se asocia con frecuencia a complicaciones cardiopulmonares, tromboembólicas, gastrointestinales, así como a disfunción cerebral, todo lo cual determina una convalecencia prolongada.1,2,8
En la actualidad, en el tratamiento de este tipo de dolor se recomienda la analgesia preventiva que es el bloqueo farmacológico de las vías nociceptivas antes de que ocurra una estimulación, disminuya o se eviten los cambios que se producen a este nivel.7,8
Hoy, en el mundo existen varios medicamentos analgésicos como los analgésicos antiinflamatorios no esteroides (AINES) y los narcóticos que se utilizan en el posoperatorio, pero ninguno llega a ser eficaz en su totalidad, por lo que es necesario el empleo de más de uno, lo que se conoce como analgesia multimodal. Estos analgésicos en su mayoría presentan reacciones adversas y cuando fracasan es necesaria la administración de narcóticos que son analgésicos más potentes pero entre cuyas reacciones adversas puede encontrarse la somnolencia, los vómitos y la depresión respiratoria, lo cual implica una mayor vigilancia posoperatoria con mayor estadía en la sala de recuperación y hospitalaria en general.9-12
El uso de lidocaína intravenosa para el control del dolor posoperatorio ha ganado interés en los últimos años. Estudios clínicos plantean que su aplicación en el periodo perioperatorio a dosis bajas y similares a las usadas para la profilaxis de arritmias, reduce el dolor y el consumo de opioides en el posoperatorio, pero su beneficio clínico no es aún concluyente y no se aplica de rutina en la práctica clínica. Las publicaciones hacen referencia a diversos modos de administración en diferentes tipos de procedimientos quirúrgicos que incluyen periodos variables del posoperatorio.13
La dosis y la duración de la infusión intravenosa de lidocaína permanecen como aspectos controvertidos. Además de eso, todavía no se ha determinado su eficacia. El trauma quirúrgico causa liberación de citocinas que son las responsables de las respuestas inflamatorias locales y generan la cicatrización hística. La interleucina-6 (IL-6) es una citocina que se detecta precozmente en respuesta al trauma y su aumento está correlacionado con el grado de lesión hística. Algunos autores14 han mostrado que la lidocaína intravenosa promueve la reducción de citocinas, del consumo de anestésicos inhalatorios y de los opioides, así como la disminución de la intensidad del dolor posoperatorio. Además, bajas dosis de lidocaína intravenosa (concentraciones plasmáticas menores que 5 µg/mL) no interfieren en la conducción nerviosa normal, y están asociadas a una menor incidencia de efectos adversos de los opioides.
Los pacientes oncológicos constituyen un grupo muy particular de individuos que se benefician notablemente con el adecuado control del dolor posoperatorio. Las medidas encaminadas a disminuir el estrés quirúrgico pueden tener un efecto benéfico no solo a corto plazo, sino también sobre el pronóstico de la enfermedad oncológica, así como en el control del dolor, el estrés psicológico, la normotermia y la transfusión sanguínea juiciosa.15-17
El paciente con cáncer está expuesto continuamente a factores que modifican negativamente su inmunidad y facilitan la diseminación de las células tumorales. Uno de los elementos que atenta en contra de estos individuos lo constituye el consumo de opioides en el periodo intra- y posoperatorio, además del dolor posquirúrgico. Una de las maneras con las que se puede contribuir positivamente en el tratamiento sería buscar estrategias encaminadas a disminuir no solo el consumo de opioides en este periodo, sino también a disminuir la incidencia del dolor; por tales razones se decidió realizar este estudio con el objetivo de responder al siguiente problema científico: ¿Será eficaz y segura la utilización de la lidocaína en infusión continua intraoperatoria para la prevención del dolor posoperatorio de pacientes sometidos a procedimiento quirúrgico abdominal oncológico?
El objetivo de esta investigación consiste en evaluar la eficacia de la utilización de lidocaína en infusión continua intraoperatoria en el tratamiento del dolor posoperatorio en pacientes intervenidos quirúrgicamente de enfermedad abdominal oncológica e identificar la aparición de eventos adversos con el empleo de esta alternativa de tratamiento.
MÉTODOS
Se realizó un estudio cuasi experimental, en pacientes sometidos a procedimiento quirúrgico abdominal oncológico en el Hospital Carlos Manuel de Céspedes de Bayamo, provincia Granma, en el último semestre del año 2015.
El universo Estuvo constituido por todos los pacientes intervenidos quirúrgicamente por enfermedad oncológica a nivel abdominal en el Hospital Carlos Manuel de Céspedes de Bayamo durante el periodo de estudio.
Para seleccionar el tamaño de la muestra, se tuvo en cuenta el error tipo I de un 5 % (α = 5 %) con una desviación estándar que no excedió del 25 %. Se empleó el paquete estadístico EpiInfo versión 6.1 para el cálculo de la muestra, y esta fue de 34 pacientes.
La selección de pacientes se realizó durante la evaluación anestésica el día antes de la intervención quirúrgica, por medio de interrogatorio y exploración física, revisión de exámenes complementarios con la finalidad de evaluar la función de órganos y sistemas, así como detectar cualquier anormalidad en ellos; se les explicó a los pacientes en qué consistía la investigación y se solicitó el consentimiento informado, además se les dio una breve explicación sobre el concepto de la escala análoga visual.
Los pacientes fueron distribuidos en dos grupos: el grupo I (experimental o estudio), formado por los primeros 17 pacientes que acudieron al servicio y que recibieron lidocaína en infusión continua intraoperatoria, y el grupo II (control), los últimos 17 pacientes en los que se empleó placebo.
Criterios de inclusión: Pacientes mayores de 20 años de edad, de cualquier sexo, con estado físico ASA II al III, anunciados para procedimiento quirúrgico electivo abdominal oncológico, y que expresaron su consentimiento de participar en la investigación.
Criterios de exclusión: Pacientes en los que esté contraindicado el uso de los fármacos que se iban a evaluar, en quienes esté contraindicado el procedimiento anestésico y quienes no comprendieron la Escala Visual Análoga (EVA).
Criterios de salida: La solicitud del paciente de abandonar el estudio y con aquellas complicaciones intraoperatorias y posoperatorias que impidan una adecuada evaluación de la EVA.
Tratamiento: Desde el periodo preoperatorio inmediato de todos los pacientes se administró por vía intravenosa: metamizol sódico a 1,8 g, tramadol a 100 mg, dexametasona a 8 mg y ondansertron a 4 mg diluido en 500 cc de solución salina al 0,9 % en infusión que debe durar de 30-40 min; de esta manera se garantiza no solo la analgesia preventiva sino también la analgesia multimodal intraoperatoria en estos individuos.
Inducción anestésica: En el quirófano después de haber realizado la monitorización no invasiva del paciente (frecuencia cardiaca, presión arterial no invasiva, electrocardiografía y oximetría de pulso), se procedió a la inducción anestésica de esta forma: previa oxigenación con FiO2 al 100 % durante 3 min por máscara facial, se realizó hipnosis con propofol a 2 mg/kg y fentanilo a 3 µg/kg. Luego se administró de 60-90 s antes de la intubación lidocaína al 2 % a razón de 1,5 mg/kg. Se provocó bloqueo neuromuscular para la laringoscopia con vecuronio a 0,08 mg/kg.
El mantenimiento anestésico se realizó con propofol en infusión continua, a 6 mg/kg/h. Se empleó como bloqueante neuromuscular no despolarizante el vecuronio a 0,04 mg/kg cada 30 min según las necesidades. El fentanilo se administró a razón de 1-2 µg/kg cada 30 min, según los requerimientos hemodinámicos.
De 30-40 min antes de terminar la operación se les administró a los pacientes por vía parenteral diclofenaco sódico 75 mg diluido en 100 cc de solución salina al 0,9 %.
Inmediatamente después de la intubación, en el grupo estudio se administró en infusión intravenosa, lidocaína a 1,5 mg/kg/h durante todo el periodo intraoperatorio.
Se mantuvo vigilancia estricta durante el intraoperatorio para detectar y tratar tempranamente la presencia de alteraciones hemodinámicas u otras complicaciones durante la intervención quirúrgica y al terminar esta. Todos los datos fueron recogidos además en la planilla de recolección de datos confeccionada para el estudio.
En la Unidad de Cuidados Posoperatorios, 30 min después de la llegada del paciente y una vez que recobró completamente la conciencia, se evaluó en ellos la intensidad del dolor y los requerimientos de analgesia de rescate con la Escala Visual Análoga. Esta se aplicó a los 30 min, 2 h, 6 h, 12 h y a las 24 h del posoperatorio. Esto requirió la visita del anestesiólogo a la sala de hospitalización. Además, se evaluó durante estas visitas la aparición de alguna complicación.
Las dosis de rescate fueron pautadas de la manera siguiente:
Dolor leve: Cuando la escala análoga visual (EVA) osciló entre 0 y 3 ptos., se administró diclofenaco a 1 mg/kg por vía i.m. o i.v. siempre y cuando hubiesen pasado más de 12 h después de la última dosis de este fármaco. En caso contrario se administró tramadol.
Dolor moderado: Cuando la EVA se valoró entre 4 y 7 ptos. En este caso se administró tramadol 1 mg/kg intravenoso.
Dolor intenso: Cuando la EVA se valoró entre 7 y 10 ptos. Se administró petidina a 1 mg/kg intravenoso.
Grupo II (control). No se le administró la infusión de lidocaína.
Se determinó el tiempo de aparición del dolor en el posoperatorio, el cual se determinó a las 4, 6, 8 y 12 h. Se operacionalizó de la forma siguiente:
- No satisfactorio: Cuando el paciente manifestó dolor en las primeras 4 h después de la intervención quirúrgica y fue necesario administrar analgésico.
- Satisfactorio: Cuando refirió dolor entre 5-6 h después de la operación.
- Muy satisfactorio: Cuando no refirió dolor hasta después de 6 h de operado y no se administró analgésico.
Duración del dolor (cuantitativa continua): Se reportó el tiempo en que duró el dolor en el paciente. Se expresará en dolor con duración de 2 o 4 h.
Intensidad del dolor (cualitativa ordinal): Se utilizó la (EVA) modificada para nuestro estudio, lo cual representó una línea graduada con centímetros de 1 al 10. El punto 0 significó la ausencia del dolor y el punto 10 el máximo de dolor, el propio paciente debió marcar en la escala el grado de intensidad que representaba su dolor en el posoperatorio.
El criterio se evaluó como: ausencia de dolor 0 cm, dolor ligero de 1,0 cm a 3,0 cm. Dolor moderado de 3,1 cm a 6,0 cm y dolor grave de 6,1 cm a 10 cm.
Criterios de evaluación de la eficacia
1. Respuesta satisfactoria: Cuando al realizar la valoración en el posoperatorio (6 h) el paciente no refirió dolor o presente dolor ligero y cuando no aparecieron eventos adversos.
2. Respuesta no satisfactoria: Cuando al realizar la valoración en el posoperatorio el paciente refirió dolor moderado o grave y cuando apareció algún efecto adverso.
Análisis estadístico. Se aplicó desde el punto de vista estadístico la prueba chi cuadrado de independencia para determinar la existencia de asociación entre las variables que participan en el estudio, a través del programa STATISTICA 6.0, soportado en Windows XP, con un nivel de confianza de 0,05.
Los resultados obtenidos se reflejaron en tablas de contingencias R x C; y están realizados sobre la base de relaciones porcentuales.
Se utilizaron los programas computacionales de Microsoft Office: Microsoft Word y Excel, para el procesamiento de la información.
RESULTADOS
En este estudio se constató que prevalecieron los pacientes en ambos grupos de tratamiento en las edades comprendidas entre los 31-50 años de edad: 14 pacientes en el grupo estudio (14,18 %) y 16 en el grupo control (47,06 %). Hubo resultados no significativos desde el punto de vista estadístico al aplicar la prueba chi cuadrado (X2), lo que muestra la homogeneidad de los grupos en estudio.
Prevaleció el sexo masculino en el grupo de estudio con 10 pacientes (29,41 %), mientras que en el grupo control fueron las féminas (26,47 %). Hubo resultados no significativos desde el punto de vista estadístico al aplicar la prueba chi cuadrado (X2), lo que muestra la homogeneidad de los grupos en estudio.
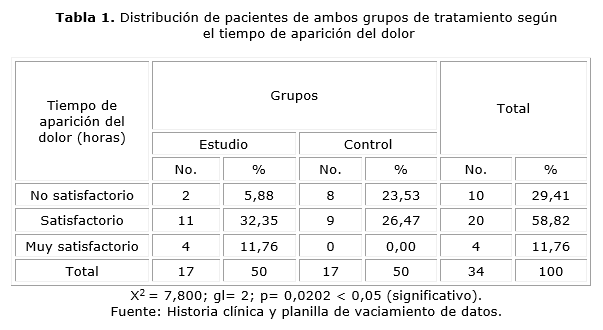
La distribución de los pacientes por grupos de tratamiento según el tiempo de aparición del dolor se muestra en la tabla 1. Resultó notorio destacar que en el grupo estudio solo en dos pacientes la respuesta fue no satisfactoria; sin embargo, en 11 pacientes esto ocurrió entre las 5-6 h (respuesta satisfactoria), en el resto (4 pacientes, 11,76 %) la aparición del dolor aconteció 12 h después del procedimiento quirúrgico (respuesta muy satisfactoria); no ocurrió así en el grupo control que desde las 2 h se reportaban 5 pacientes con dolor. Además, la prueba chi cuadrado (X2) de independencia arrojó diferencias significativas, por lo que concluye que las variables están relacionadas.
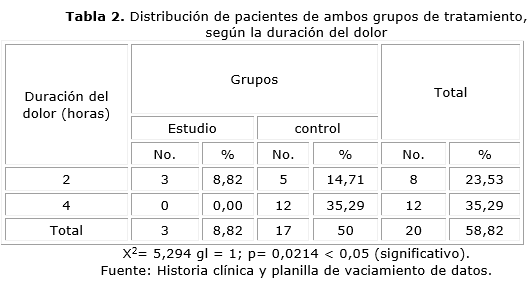
En la tabla 2 se constató la distribución de pacientes de ambos grupos de tratamiento según la duración del dolor; en el grupo estudio los tres pacientes tuvieron aproximadamente 2 h de duración del dolor; el resto no mostró dolor; mientras que en el grupo control 5 pacientes refirieron 2 h de duración de dolor y 12 pacientes refirieron 4 h. También se arrojaron resultados significativos desde el punto de vista estadístico al aplicar la prueba chi cuadrado (X 2).
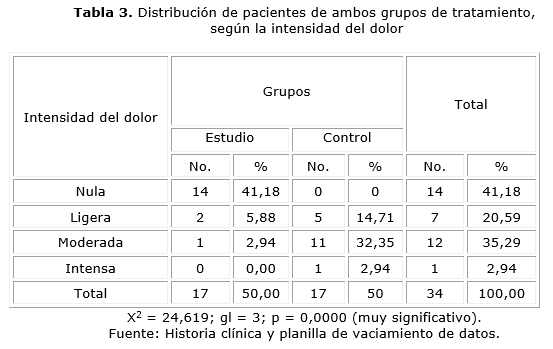
En la tabla 3 se muestra que en el grupo estudio de los tres pacientes que refirieron dolor, dos de ellos lo catalogaron de intensidad ligera y uno de moderada; mientras que en el grupo control 12 pacientes refirieron dolor de intensidad moderada y grave. También se arrojó resultados significativos desde el punto de vista estadístico al aplicar la prueba chi cuadrado (X2).
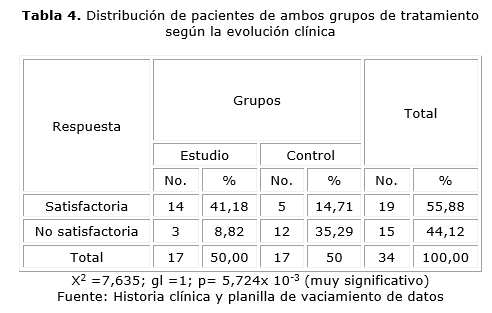
Se comprobó la hipótesis planteada al inicio de la investigación. Se evidenció la eficacia de la aplicación de lidocaína en infusión continua intraoperatoria de pacientes intervenidos quirúrgicamente de procedimientos abdominales oncológicos. Se logró una mejor calidad analgésica y menor administración de analgésicos posoperatorios en comparación con la administración de placebo, pues en el grupo estudio 49 pacientes (98 %) mostraron respuesta satisfactoria y en el grupo control 14 pacientes (41,18 %) mostraron respuesta satisfactoria. Desde el punto de vista estadístico también se arrojaron resultados significativos al aplicar la prueba chi cuadrado (X2) (tabla 4).
En relación con la aparición de eventos adversos, solo dos pacientes del grupo que recibió infusión intravenosa de lidocaína presentaron visión borrosa, arritmia, náuseas, ansiedad y prurito. Para el grupo control el evento adverso más frecuente fue la náusea.
DISCUSIÓN
El dolor es uno de los problemas de salud que causa mayor preocupación en la población, pues compromete su calidad de vida. En la literatura científica se observa una tendencia creciente en la prevalencia del dolor en los últimos años.18
Diversos estudios han evaluado la epidemiologia del dolor agudo posoperatorio y muestran porcentajes muy variables que dependen de múltiples factores; Apfelbaum y otros.19 indicaron que aproximadamente el 80 % de los pacientes experimentan dolor después de la procedimiento quirúrgico, de los cuales un 86 % de los casos es moderado, grave o dolor extremo.
Según Niraj Gl y otros,8 en una revisión sobre la situación actual del dolor posoperatorio, dicha incidencia presenta un valor oscilante: 20-50 % en mastectomía, 5-30 % histerectomía, entre otros. Por tanto, no se disponen de datos específicos de prevalencia del dolor agudo posoperatorio en ortopedia, pero sí se dispone de estudios que muestran una prevalencia elevada del dolor a pesar de los esfuerzos y las herramientas disponibles al alcance. Este estudio demostró que la administración de lidocaína intravenosa en el intraoperatorio a dosis de 1,5 mg/kg/h no fue superior al placebo para prevenir el dolor posoperatorio en pacientes mastectomizadas.
Otros autores20 mostraron un beneficio con el uso de la lidocaína intravenosa en el alivio del dolor posoperatorio. En pacientes intervenidos de colectomía laparoscópica, al utilizar una dosis inicial de 1,5 mg/kg seguida de infusión continua de 2 mg/kg, que se prolongó durante 24 h del posoperatorio, los autores encontraron una mejoría de la analgesia.
Mientras, de Oliveira et al.21 al evaluar el dolor en mujeres intervenidas por procedimientos quirúrgicos laparoscópicos, en régimen ambulatorio que recibieron la lidocaína a dosis de 1,5 mg/kg, 20 min antes de la incisión quirúrgica, seguida de una infusión de 2 mg/kg/h hasta el final de la intervención quirúrgica, observaron un alivio del dolor en el grupo lidocaína.
El beneficio de la lidocaína evidenciado por esos autores puede estar relacionado con los regímenes distintos de infusión que fueron utilizados. La infusión de la lidocaína durante 24 h en el posoperatorio puede haber dado como resultado la supresión de la sensibilización central y así haber contribuido a la obtención del efecto analgésico positivo cuando se la comparó con esta investigación. La utilización de bolos antes del inicio del procedimiento quirúrgico puede hacernos pensar que la administración de la lidocaína antes de la incisión quirúrgica puede promover mejores resultados en lo que se refiere al dolor posoperatorio, por disminuir la liberación de sustancias inflamatorias.22
Un estudio realizado en seres humanos23 demostró que existe una acción excitatoria del anestésico local en la musculatura lisa del intestino y, por ende, una disminución de la distensión colónica y de la incomodidad posoperatoria. Esa acción justifica la capacidad de la lidocaína de aliviar el dolor visceral como quedó demostrado en modelos animales24,25 y comprobado a partir de los resultados relatados en las intervenciones quirúrgicas abdominales.
Ese hallazgo contribuye a enfatizar la hipótesis de que la lidocaína intravenosa tiene un efecto analgésico preferencial en el dolor visceral y neuropático. Sin embargo, estudios recientes han demostrado que la lidocaína intravenosa tiene acciones analgésicas y antihiperálgicas en razón del bloqueo periférico de los impulsos ectópicos involucrados en la nocicepción y también de su acción en los canales de potasio, canales de calcio y en los receptores acoplados a las proteínas. También presenta una acción antiinflamatoria, efecto proveniente de la disminución de la acumulación de neutrófilos en la región de la lesión y de la reducida liberación de mediadores inflamatorios. Esas acciones justifican su uso en el abordaje multimodal de la analgesia posoperatoria.22
Se concluye que la hipótesis planteada al inicio de la investigación se comprobó, y se evidenció la eficacia de la aplicación de lidocaína en infusión continua intraoperatoria en pacientes intervenciones quirúrgicamente por enfermedad oncológica abdominal, se logra una mejor calidad analgésica y menor administración de analgésicos posoperatorios en comparación con la administración de placebo.
REFERENCIAS BIBLIOGRÁFICAS
1. Salazar Diez MC, Barranco Pedraza L, Díaz Rivadeneira MO, Baute Vilardell L.Eficacia de la acupuntura en el tratamiento de los síntomas postoperatorio en procedimiento quirúrgico pediátrica ambulatoria. Archivo Médico de Camagüey 2011;15(2):214-24
2. White PF, Kehlet H, Neal JM, Schricker T, Carr DB, Carli F. The role of the anesthesiologist in fast-track surgery: from multimodal analgesia to perioperative medical care. Anesth Analg [Internet]. 2007 Jun [citado 18 de Agosto de 2015];104(6):1380-96. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/17513630
3. Raja SN, Jensen TS. Predicting postoperative pain based on preoperative pain perception: are we doing better than the weatherman? Anesthesiology [Internet]. 2010 Jun [citado 17 de septiembre de 2013];112(6):1311-2. Disponible en: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=2884220&tool=pmcentrez&rendertype=abstract
4. Force TAS of AT. Practice Guidelines for Acute Pain Management in the perioperative setting. Anesthesiology. 2012;116(2):248-73.
5. Ruiz Martín de la Torre R; Heredia Benito, M; Sánchez Ruiz de Gordoa, M; Tenias Burillo, JM; Valenzuela Gámez, JC. Factors influencing on acute postoperative pain:review. Eur J Clin Pharmacy. 2013;15(6).
6. Muñoz JM. Manual del dolor agudo postoperatorio. Comisión Hospital sin Dolor. Hospital Universitario La Paz. Madrid: Ergon; 2010. p. 57.
7. Cho S-H, Kim Y-R, Lee J-H, Kim S-H, Chae W-S, Jin H-C, et al. A questionnaire study investigating the prevalence of chronic postoperative pain. Korean J Anesthesiol [Internet]. 2012 Jan;62(1):40-6. Disponible en: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3272528&tool=pmcentrez&rendertype=abstract
8. Niraj G, Rowbotham DJ. Persistent postoperative pain: where are we now? Br J Anaesth [Internet]. 2011 Jul [citado 2 de septiembre de 2013];107(1):25-9. Dsiponible en: http://www.ncbi.nlm.nih.gov/pubmed/21610014
9. Ng B, Dimsdale JE, Shragg GP, Deutsch R. Ethnic differences in analgesic consumption for postoperative pain. Psychosom Med [Internet]. 2013 [citado 5 de septiembre de 2013];58(2):125-9. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/8849628
10. Ong CK-S, Lirk P, Seymour R a, Jenkins BJ. The efficacy of preemptive analgesia for acute postoperative pain management: a meta-analysis. AnesthAnalg [Internet]. 2005 Mar [citado 3 de septiebre de 2015];100(3):757-73, table of contents. Deisponible en: http://www.ncbi.nlm.nih.gov/pubmed/15728066
11. Møiniche S, Kehlet H, Dahl JB. A qualitative and quantitative systematic review of preemptive analgesia for postoperative pain relief: the role of timing of analgesia. Anesthesiology [Internet]. 2002 Mar [cited 2015 Sep 6];96(3):725-41. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11873051
12. Macintyre P, SA S, Scott D, Visser E, SM W. AMP: SE Working group of the Australian and New Zealand College of Anaesthetists and Faculty of Pain Medicine, Acute Pain Management: Scientific Evidence. 2010. 3rd edition, ANZCA&FPM, Melbourne.
13. Ayala S, Castromán P. Efecto de la lidocaína intravesona sobre el control del dolor y el Consumo de opioides en el postoperatorio. Rev Anestesia Analgesia Reanimación. 2012;25(1):1-16.
14. Barros de Oliveira CM, Kimiko R, Slullitel A, Salomao R, Lanchote VL, Machado A. Efectos de la lidocaína venosa intraoperatoria sobre el dolor e interlucina-6 plasmática en pacientes sometidas a histerectomía. Rev Bras Anestesiol. 2015; 65(2):42-98.
15. Sánchez-Pedrosa G, Garutti I, Moraga FG. Orozco HD. Diseminación tumoral perioperatoria. 1. Influencia de los factores perioperatorios. Rev Esp Anestesiol Reanim. 2012;59(5):259-66.
16. Sánchez-Pedrosa G, Garutti I, Moraga FG, Orozco HD. Diseminación tumoral perioperatoria. 2. Efectos de la anestesia y analgesia. Rev Esp Anestesiol Reanim. 2012;59(5):267-75.
17. Mille-Loera JE. La transfusión sanguínea como factor pronóstico en el paciente con cáncer. Rev Mex de Anestesiol. 2006;29(1):221-5.
18. Ministerio de sanidad política social e igualdad. Unidad de Tratamiento del Dolor. Estándares y recomendaciones de calidad; 2011. p. 161.
19. Apfelbaum JL, Chen C, Mehta SS, Gan and TJ. Postoperative Pain Experience: Results from a National Survey Suggest Postoperative Pain Continues to Be Undermanaged. Anesth Analg. 2003 Aug;97(2):534-40.
20. Kaba A, Laurent SR, Detroz BJ. Intravenous lido-caine infusion facilitates acute rehabilitation after laparoscopic colectomy. Anesthesiology. 2007; 106:11-8.
21. De Oliveira GS, Fitzgerald P, Streicher LF. Systemic lidocaine to improve postoperative quality of recovery after ambulatory laparoscopic surgery. Anesth Analg. 2012;115:262-7.
22. Couceiro TC. Lidocaína intravenosa en el tratamiento del dolor posmastectomía: ensayo clínico aleatorizado, encubierto, placebo controlado. Rev Bras Anestesiol. 2015;65(3):207-212.
23. McKay A, Gottschalk A, Ploppa A. Systemic lidocaine decreased the perioperative opioid analgesic requirements but failed to reduce discharge time after ambulatory surgery. Anesth Analg. 2009;109:1805-8.
24. Maggi CA, Manzini S, Meli A. Contribution of neurogenic and myogenic factors in the response of rat proximal colon to dis-tention. Am J Phisiol. 1987;252:G447-57.
25. Ness TJ. Intravenous lidocaine inhibits visceral nocicep-tive reflexes and spinal neurons in the rat. Anesthesiol. 2000;92:1685-91.
Recibido: 3 de abril de 2017.
Aprobado: 23 de abril de 2017.
Guillermo Capote Guerrero. Hospital General docente "Carlos Manuel de Céspedes". Cuba.