Introducción
El síndrome de Morquio (SM) es una enfermedad hereditaria autosómica recesiva con distintos grados de afectación al metabolismo de los glúcidos, genera incapacidad para romper los enlaces de las cadenas largas de glucosamiglicanos, lo que provoca acumulación de mucopolisacáridos en distintos tejidos del cuerpo humano.1
Los pacientes con mucopolisacaridosis (MPS) muestran un desarrollo inicial normal, con anomalías que aparecen en la infancia o más tarde en la niñez. Los síntomas se caracterizan por tener un amplio espectro de gravedad en la expresión de las manifestaciones musculoesqueléticas y neurológicas las cuales preceden al diagnóstico. En consecuencia, muchos procedimientos se realizan antes de que este pueda realizarse.2
En pacientes con MPS IVA, el sistema esquelético es el más afectado. Múltiples anomalías someten al paciente a un alto riesgo anestésico.3Tomatsu y otros comunicaron una serie de casos en los que el 67 % de los pacientes presentaban estrechamiento traqueal que empeora con la edad.4 En una revisión retrospectiva, solo uno de cada seis pacientes con MPS IVA presentó mala visibilidad laringoscópica, probablemente debido a la movilidad limitada del cuello causada por una fusión cervical previa.2 En el estudio de Frawley y otros, el único paciente con MPS IVA incluido no presentó complicaciones anestésicas.5 El estudio más grande sobre pacientes con MPS IVA es un estudio retrospectivo y descriptivo de 28 niños; ocho pacientes (siete de ellos con la columna cervical fusionada quirúrgicamente) fueron difíciles de intubar. Parte de las intubaciones realizadas fueron laringoscopias convencionales mediante estabilización en línea con posición neutra de cabeza y cuello o con videolaringoscopio en cuanto estuvo disponible. Cuatro niños tuvieron complicaciones perioperatorias, principalmente debido a la inestabilidad de la columna cervical y depósitos de GAG en la tráquea.7
Entre los desafíos anestésicos que se manifiestan en este síndrome se encuentran los problemas respiratorios, debido a un defecto restrictivo en caja torácica, la obstrucción de la vía aérea superior con la cabeza en flexión, la inestabilidad atlantoaxial y la compresión de la médula espinal cervical debido a la hipoplasia del canal medular.6 Los tres últimos con frecuencia crean dificultades y requieren extrema precaución con el manejo de la vía aérea (VA).6
La mayoría de los pacientes con mucopolisacaridosis requieren anestesia por múltiples intervenciones quirúrgicas, ya sea como tratamiento paliativo en el manejo de la misma enfermedad o por padecimientos agregados. Atendiendo a que las MPS son enfermedades raras, con una escasa casuística, esta es la primera paciente de este tipo que se atiende en el Hospital General Provincial Docente “Roberto Rodríguez” de Morón. El objetivo fue describir el manejo anestésico de una gestante con síndrome de Morquio.
Presentación del caso
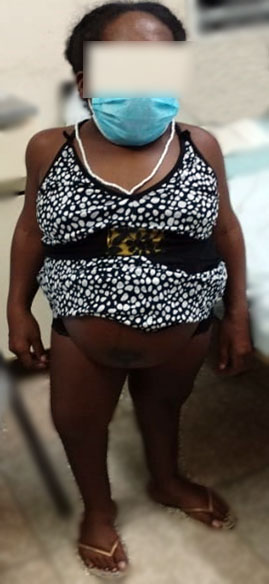
Gestante primigesta de 30 años de edad, de raza negra, de 103 cm de estatura y 33 Kg de peso. Acude a consulta preoperatoria por presentar embarazo a término, baja talla y se realizó interrupción por cesárea. En la valoración preanestésica se recogen antecedentes de MPS IV diagnosticada en la infancia, antecedentes de intervención quirúrgica previa con anestesia general para corrección de paladar hendido y cirugía correctora de deformidad en los pies. Además, presentó ingreso previo por cifras elevadas de tensión arterial y alergia a la dipirona (Fig. 1).
Examen físico y complementario
Aparato cardiovascular: Ruidos cardíacos rítmicos de buen tono e intensidad. No se ausculta soplo. TA: 100/60 mmHg. FC: 78 lpm.
Aparato Respiratorio: Murmullo vesicular conservado. No se auscultan estertores. FR: 18 rpm.
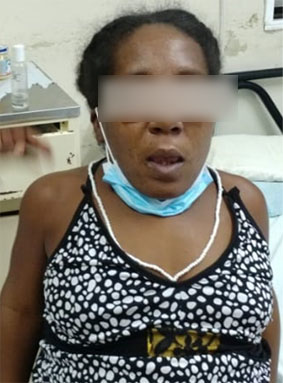
Boca: Apertura bucal menor de 3 cm con macroglosia. Test de Mallampati: grado IV (Fig. 2).
Tráquea: Medial. Distancia tiromentoneana 2,5 cm (Fig. 2).
Columna vertebral: Escoliosis dorsolumbar.
Este examen físico arrojó signos de vía aérea difícil (VAD).
Técnica anestésica
En la Unidad Quirúrgica, se realizó monitorización estándar de ECG (DII), tensión arterial no invasiva (TANI), frecuencia cardíaca, ritmo cardíaco, saturación parcial de oxígeno por pulsioximetría (SpO2). Los signos vitales fueron: TANI: 100/60 mmHg, FC: 98 lpm, SpO2: 98 %, FR: 20 rpm.). Previa instilación de Xilocaína 10 % en la vía aérea y con espátula Macintosh perfil americano. Se realiza laringoscopia directa con la paciente despierta, se obtuvo clasificación de Cormack y Lehane grado I.
Una vez realizada asepsia y antisepsia de la zona quirúrgica y colocados los paños de campo y borde, se procede a realizar la inducción anestésica con Ketamina 2 mg/kg (66 mg), Midazolam 0,07 mg/kg (2 mg), paciente que ventiló sin ninguna complicación con máscara facial, bloqueo neuromuscular con succinilcolina 2 mg/kg (66 mg) por vía EV. Se realiza laringoscopia y se introduce tubo endotraqueal 7 sin complicaciones. Se utilizó ventilación protectora con volumen tidal a 6 mL/Kg (200 mL), FR: 12 rpm, I/E: 1:2, VM: 2.4, Presión pico: 13 mbar, Presión meseta: 11 mbar y PEEP: 3 mbar. Se mantuvo hidratación por vía parenteral a razón de 10 mL/kg/h. El mantenimiento anestésico fue con fentanilo 2 mcg/kg EV, atracurio a 0,4 mg/kg (13,2 mg) y una combinación de oxígeno, aire comprimido y sevoflurano a una concentración de 0.8 Vol %.
La intervención duró 30 min, se realizó incisión media infraumbilical, apertura por planos hasta la cavidad abdominal, histerotomía segmento arciforme, amniotomia y extracción fetal sin complicaciones, se pinza el cordón umbilical, se obtuvo recién nacido vivo, del sexo femenino, Apgar 9/9, peso 2000 g. Se administran 10 U de oxitocina para la contracción uterina. Se realiza alumbramiento manual y revisión de la cavidad uterina, hiterorrafia en un plano a sutura continua, y se cierra por planos hasta la piel.
Durante el acto quirúrgico la paciente se mantuvo con estabilidad hemodinámica y eléctrica. Concluyó la cirugía sin complicaciones, sangrado estimado de 400 mL y se administraron 850 mL de soluciones cristaloides. Diuresis de 200 mL, aproximadamente. Se revirtió efecto de las benzodiacepinas y se realiza extubación orotraqueal en salón de operaciones, sin ninguna complicación, fue trasladada a sala de cuidados pos anestésicos con ventilación espontánea y analgesia multimodal por vía EV.
Discusión
Las MPS constituyen un reto para todo anestesiólogo sobre todo en el abordaje la vía aérea, donde se encuentra una VAD esperada y las demás comorbilidades, por lo que un plan anestesiológico adecuado nos permite llevar un perioperatorio sin complicaciones.
La evaluación preoperatoria debe realizarse de manera minuciosa y con un enfoque multidisciplinario y durante esta el anestesiólogo debe examinar todas las pruebas diagnósticas realizadas. El examen físico es vital para determinar la posibilidad de una vía aérea anatómica difícil (sistema de clasificación de Mallampati, basado en la visibilidad de las amígdalas, los pilares, la úvula y el paladar blando; evaluar el estrechamiento de las fosas nasales, la hipertrofia y macroglosia adenoamigdalar, la obstrucción nasofaríngea y el estrechamiento supraglótico).8 Los pacientes pueden desarrollar una oclusión de las vías respiratorias al flexionar el cuello y adoptar una “posición de olfateo” para preservar la permeabilidad de las vías respiratorias. La función respiratoria comprometida debido a enfermedad restrictiva con volúmenes pulmonares disminuidos y desajuste de ventilación-perfusión es una posible complicación.
Una evaluación cardíaca de rutina completa (electrocardiografía, lectura de la presión arterial y ecocardiografía) es obligatoria antes de la cirugía.
La premedicación con narcóticos debe evitarse si se anticipan problemas de las vías respiratorias, como suele ser en el caso que se presenta.2 Si se administra una benzodiazepina como premedicación, los pacientes deben ser controlados estrictamente con un oxímetro de pulso.2 En estos casos resulta muy útil el uso de agentes secantes orales disponibles.
Para favorecer la inducción, la primera consideración es identificar la posición correcta del paciente. La ketamina debería ser el fármaco ideal, pero puede aumentar la cantidad de secreciones. No se deben administrar dosis apneicas completas de narcóticos antes de la intubación traqueal.2
En la intubación orotraqueal, los pacientes con MPS tienen múltiples comorbilidades, de las cuales muchas requieren intervenciones quirúrgicas. Debido a que esta afección se asocia con características fenotípicas específicas de las vías respiratorias y faciales, se pueden esperar desafíos sustanciales para el manejo perioperatorio de las vías respiratorias. En dos series de casos, la dificultad con la ventilación con mascarilla ha oscilado entre el 7 % y el 14 % de los pacientes con MPS,9 La incidencia global de intubación traqueal difícil, en series de casos de varios tipos de MPS, oscila entre el 28 %.9
La extubación de la tráquea al final de la anestesia general puede representar otro riesgo importante. Esta debe realizarse con el paciente despierto y posterior vigilancia estricta para detectar a tiempo signos de obstrucción de la vía aérea. Si no se consigue su extubación precoz, se preconiza su traslado para una sala de Cuidados Intensivos para permitir el destete seguro de la ventilación mecánica, la fisioterapia torácica agresiva, la detección precoz y el tratamiento de las complicaciones respiratorias infecciosas.2
Theroux y otros en un estudio retrospectivo sobre niños con MPS IVA, describen seis casos de catéteres epidurales colocados con éxito para analgesia posoperatoria. Se prefirió un abordaje caudal al lumbar en uno de cada cuatro niños debido a las irregularidades de los cuerpos vertebrales y la cifosis frecuente.7 Por otro lado, también se reporta un caso de falla, donde los autores hipotetizan el depósito de mucopolisacáridos ya sea en el espacio epidural general o en la vaina de las fibras nerviosas lo que impidió el acceso directo del anestésico local al nervio.2 Por lo que su uso aún es controversial.
Los pacientes con MPS tienen una alta incidencia de dificultad para la ventilación y la intubación endotraqueal asociada con insuficiencia cardiopulmonar. La afectación de la columna presenta dificultades adicionales para los anestesiólogos. Cualquier cirugía electiva requiere una evaluación preoperatoria de los factores de riesgo anestesiológicos y la disponibilidad de un espectro de equipos para el manejo de las vías respiratorias. La anestesia debe ser realizada por un equipo con experiencia en el manejo de la vía aérea.