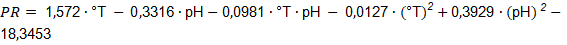INTRODUCCIÓN
En la industria alimentaria existe un aumento progresivo del uso de edulcorantes sintéticos en una gran variedad de alimentos (Durán y col., 2013). Pese al bajo nivel calórico que presentan, no dejan de ser asociados con el desarrollo de distintas enfermedades como el sobrepeso, la obesidad, la diabetes y enfermedades cardiovasculares (Swithers, 2013; Lara y col., 2017), además de la condición de intolerancia a la glucosa causada por alteraciones de la microbiota intestinal (Suez y col., 2014), ingesta con alteraciones metabólicas, hígado graso, entre otras (Riveros y col., 2014). El uso de la fructosa como edulcorante se ha ido incrementado en los últimos años en la industria alimentaria, su producción de forma industrial se limita a la extracción netamente de almidón de maíz genéticamente modificado, con la intervención de catalizadores y enzimas que permite hidrolizar el almidón de maíz en fructosa (Serna-Saldivar, 2016).
La problemática principal en la producción de jarabe de maíz de alta fructosa radica en el efecto negativo en la salud debido a su fuente de obtención, además de la contaminación producida por el mercurio de muestras de Jarabe de maíz de alta fructosa (JMAF) durante su proceso de producción, por otra parte el método empleado para su extracción representa alta toxicidad induciendo a la muerte de insectos como las abejas (Parker y col., 2010). Uno de los métodos de hidrólisis se basa en la inmovilización enzimática en diferentes materiales de soporte, esta técnica es una alternativa promisoria para la producción de fructosa, ya que este método permite mejorar los procesos biocatalíticos industriales y además proporciona la producción de biocatalizadores estables y eficientes, posibilidad de reutilización y fácil purificación de los productos, en comparación con las enzimas libres en el medio de reacción (Giraldo y Díaz, 2013). Las enzimas al ser producidas a partir de materias primas renovables son completamente biodegradables y pueden operar en equipos relativamente simples y totalmente controlados, disminuyendo el consumo de energía, productos químicos y la generación constante de desechos (Homaei y col., 2013). Para todas las enzimas, la posibilidad de ser inmovilizadas y utilizadas repetitivamente representa importantes ventajas industriales y medioambientales (Andler y Goddard, 2018).
Investigaciones previas han estudiado las condiciones de inmovilización basadas en diferentes formulaciones de polímeros, el uso de estas permiten la retención máxima de la enzima (Datta y col., 2013; Liu y col., 2018). La presente investigación tiene como objetivo determinar las condiciones de pH y temperatura para la hidrólisis, utilizando inulinasa inmovilizada en alginato de sodio. Mediante la Metodología de Superficie de Respuesta se evaluaron las mejores condiciones de pH y temperatura para maximizar la productividad total de fructosa.
MATERIALES Y MÉTODOS
Los reactivos utilizados son de grado analítico provenientes de Sigma-Aldrich, USA, al igual que la enzima.
2.1 Preparación del sustrato de inulina
Para preparar la solución del sustrato de inulina se disolvió 1 g de inulina de achicoria (Inulin from chicory®, Sigma-Aldrich, USA) en 1 L de agua destilada (Álvarez y col., 2015), con base en la concentración del indicador de fructosa de la curva de calibración para azúcares reductores, según el método DNS (Miller, 1959).
2.2 Inmovilización enzimática
La enzima utilizada fue inulinasa de Aspergillus niger (Inulinase from Aspergillus niger®, Sigma-Aldrich, USA) y alginato de sodio (GRINDSTED® Alginate FD/PH 120). Para la encapsulación de las enzimas se utilizó una solución de alginato de sodio al 2% m/v, con una temperatura de 35°C y pH de 9,6 de acuerdo con investigaciones previas (Aviles y col., 2018; Lara y col., 2019). La enzima, previamente diluida en agua destilada relación 1:1, se vertió en la solución de alginato de sodio agitando a 120 rpm para su total homogeneización. La mezcla con la enzima se dejó gotear en una solución de cloruro de calcio al 10%, utilizando una pipeta Pasteur de 3 mL, las perlas se dejaron reposar durante 30 min en la solución cálcica. Finalmente, las perlas fueron lavadas con agua destilada para eliminar restos de cloruro de calcio adherido en la superficie.
2.3 Reacción enzimática
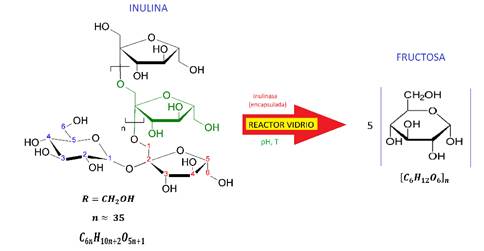
Para el proceso de hidrólisis se considera los valores óptimos teóricos de pH y temperatura para la activación de la enzima (Nakamura y col., 1995; Aziz y col., 2015). La reacción experimental se llevó a cabo durante tres horas utilizando inulina de achicoria (Inulin from chicory®, Sigma-Aldrich, USA) como sustrato, tal como se muestra en la Fig. 1.
Cada unidad experimental constó de 25 mL de sustrato y 12,5 mL de solución enzimática gelificada en cloruro de calcio al 10%. Al finalizar el proceso se realizó un choque térmico con agua helada a 4°C para frenar la reacción. Finalmente, se separaron las cápsulas de alginato del producto final mediante un proceso de filtración en un tamiz de lavado número 8 (2,38 mm), serie U.S. STD. Sieve. A continuación se cuantificaron los azúcares reductores aplicando el método del ácido 3,5-dinitrosalicílico (Miller, 1959) y utilizando un espectrofotómetro 6705 UV-Vis JENWAY a una longitud de onda de 540 nm.
2.4 Diseño del experimento
Se ejecutó un Diseño Compuesto Central de la Metodología de Superficie de Respuesta para encontrar la combinación de temperatura (°C) y pH (-) que maximicen la productividad de fructosa (Myers y col., 2016). Todos los experimentos se planificaron y analizaron empleando el software DOE Design-Expert 11.0.3.0 (Stat-Ease, Inc., Minneapolis, Estados Unidos), los cuales se muestran en la Tabla 1.
Tabla 1 Valores reales y codificados de las variables independientes: temperatura (°C) y pH con los cinco niveles sugeridos (-1,41;-1; 0; +1; +1,41)
| R1 | 0 | 0 | 50,0 | 5,0 |
| R2 | 0 | 0 | 50,0 | 5,0 |
| R3 | 0 | 0 | 50,0 | 5,0 |
| R4 | 1 | 1 | 60,0 | 6,0 |
| R5 | 1 | -1 | 60,0 | 4,0 |
| R6 | 1,414 | 0 | 64,1 | 5,0 |
| R7 | 1,414 | 0 | 64,1 | 5,0 |
| R8 | 0 | -1,414 | 50,0 | 3,6 |
| R9 | 0 | + 1,414 | 50,0 | 6,4 |
| R10 | -1,414 | 0 | 35,9 | 5,0 |
| R11 | -1,414 | 0 | 35,9 | 5,0 |
| R12 | 0 | 0 | 50,0 | 5,0 |
| R13 | 0 | 0 | 50,0 | 5,0 |
| R14 | 0 | 0 | 50,0 | 5,0 |
| R15 | -1 | -1 | 40,0 | 4,0 |
| R16 | -1 | 1 | 40,0 | 6,0 |
| R17 | 0 | 0 | 50,0 | 5,0 |
| R18 | 0 | 0 | 50,0 | 5,0 |
| R19 | 0 | 0 | 50,0 | 5,0 |
RESULTADOS Y DISCUSIÓN
En la Fig. 2 se muestra la variabilidad de la productividad total de fructosa (mg/h), en función de las condiciones de temperatura y pH señaladas anteriormente. El comportamiento de los datos demuestra que la temperatura (°C) tiene una influencia directa sobre la productividad, ocasionando que esta disminuya considerablemente si se sobrepasan los 50 °C. Por otra parte, al alcalinizar el medio de reacción también se produce una disminución de la productividad.
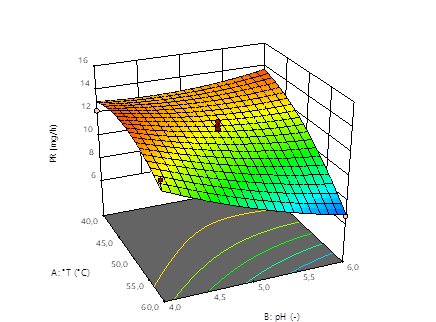
Fig. 2 Gráfico en 3D de la superficie de respuesta que muestran el efecto combinado de la temperatura (° C) y el pH (-) sobre la productividad de fructosa (mg/h)
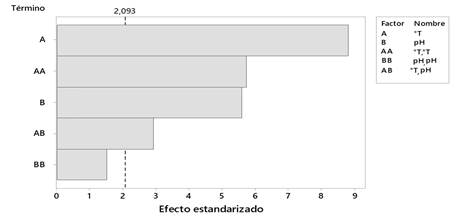
De acuerdo con el experimento realizado (confiabilidad del 90%) existe evidencia que tanto la temperatura y el pH como la interacción de ambos factores inciden en la conversión de inulina a fructosa, y por consiguiente en la productividad de la reacción. A continuación se presenta la Fig. 3, en la cual se muestra que la temperatura (A) influye de manera más significativa que el valor de pH (B), así como las distintas interacciones de estas variables en todo el proceso de hidrólisis, lo que infiere directamente en su productividad.
El modelo en términos de factores reales del diseño experimental se muestra en la ecuación 1:
Donde:
PR= Productividad expresada (mg/h).
°T= Temperatura del medio de reacción (°C).
pH= pH del medio de reacción.
En la Tabla 2 se muestran los resultados del análisis del efecto de cada una de las variables operacionales sobre la productividad de fructosa dentro del espacio del diseño experimental. Se evidencia la influencia positiva de la temperatura y el cuadrado del pH sobre el modelo cuadrático obtenido, a diferencia del resto de factores que aportan de forma negativa a la variable dependiente, esto concuerda con lo presentado en el diagrama de Pareto (Fig. 3), que especifica el mayor efecto estandarizado sobre el elemento A, debido a los cambios abruptos que pueden producirse en la temperatura de la reacción inactivando la enzima, lo que perjudicaría el proceso de hidrólisis e influyendo directamente sobre la productividad, a diferencia de cambios de pH que son mas fáciles de regular experimentalmente con la adición de soluciones de control.
Tabla 2 ANOVA para el modelo de segundo orden relacionado con la productividad de fructosa en función de la temperatura y pH
| Modelo | 86,29 | 5 | 17,26 | 24,66 | < 0,0001 |
|---|---|---|---|---|---|
| A-T | 49,26 | 1 | 49,26 | 70,39 | < 0,001 |
| B-pH | 8,73 | 1 | 8,73 | 12,48 | 0,0037 |
| AB | 7,75 | 1 | 7,75 | 11,07 | 0,0055 |
| A² | 17,42 | 1 | 17,42 | 24,89 | 0,0002 |
| B² | 1,85 | 1 | 1,85 | 2,64 | 0,1282 |
| Residual | 9,10 | 13 | 0,6997 | - | - |
| Falta de ajuste | 7,35 | 3 | 2,45 | 14,01 | 0,0007 |
| Error puro | 1,75 | 10 | 0,1748 | - | - |
| Correlación Total | 95,39 | 18 | - | - | - |
La adecuación del modelo cuadrático para la determinación de la productividad en función de la temperatura y el pH se puede evaluar a través de gráficos de diagnóstico de la distribución normal de los residuos (Fig. 4A), que expresa un patrón de residuos al azar en relación a la tendencia del modelo, lo que muestra la validación de la expresión matemática y la gráfica de los valores de respuesta pronosticados frente a los valores de respuesta reales (Fig. 4B), que no presenta ningún tipo de sesgo, tendencia o algún tipo de dispersión no constante entre los residuos (González y col., 2012), lo que indica la correcta relación entre las variables estudiadas para la construcción del modelo, dichas gráficas se muestran en la Fig. 4 A y B:
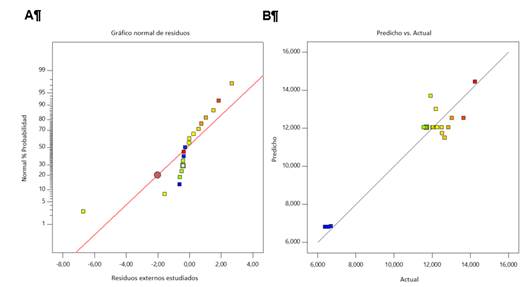
Fig. 4 Gráficos de diagnóstico. A: gráficos de probabilidad normal de residuos externamente estudiados; B: valores predichos versus valores reales de la productividad de fructosa (mg/h)
Los valores sugeridos tras la optimización numérica del modelo fueron validados, obteniendo como resultado (P1= °T:40 °C y pH:6), cuyo punto alcanzó valores de 12,27 mg/h. Otros autores reportaron temperaturas óptimas de actividad de la inulinasa de A. Niger alrededor a 50 °C (Nakamura y col., 1995), mientras que otros informaron valores mayores, alcanzando los 60°C (D'Arcadia y col., 1998).
El pH óptimo de activación de la inulinasa en otros reportes indica valores de 4 a 6 (Aziz y col., 2015; Derycke y Vandamme, 1984). Los rendimientos de conversión máximos alcanzados en investigaciones similares son del 82% (Yun y col., 2000), similar al reportado en el presente trabajo del 82,1%. La variación de los resultados se debe a la carga enzimática y la concentración del sustrato, además de los valores de los factores de pH y temperatura utilizados en cada caso.
CONCLUSIONES
La inmovilización de las enzimas de inulinasa en alginato de sodio demostró que la productividad de fructosa obtenida no se ve afectada al utilizar este tipo de material y los valores obtenidos son similares a otros tipos de material, que están alrededor de los 12,27 mg/h.
Los valores de pH y de temperatura en el rango estudiado (pH: 4-6; T: 40-60 °C) demostraron que afectan la productividad del proceso de hidrolisis enzimática y no así a la conformación de las cápsulas del alginato de sodio. El valor máximo productividad obtenido fue a pH =6 y de temperatura 40 °C.