INTRODUCCIÓN
Según la Organización Mundial de la Salud (OMS) la depresión y la ansiedad son las principales causas de enfermedades no fatales que han conducido al consumo masivo de antidepresivos. Entre los antidepresivos más consumidos se encuentran los inhibidores selectivos de la recaptación de serotonina (ISRS), tales como la fluoxetina (FLU), citalopram (CIT), paroxetina (PAR), sertralina (SER), y fluvoxamina (FLX) (Silva y col., 2012). Estas moléculas integran el grupo de los antidepresivos de segunda generación, denominación que permitió hacer una distinción frente a los inhibidores de la monoamino oxidasa (IMAO) y a los antidepresivos tricíclicos (ATC) (Korman y Sarudiansky, 2011). Sin embargo, uno de los problemas que generan estos fármacos desde el punto de vista ambiental, son su presencia omnipresente en el medio ambiente, principalmente en matrices acuosas superficiales (Schultz y Furlong, 2008), provenientes de la excreción por las personas en vía doméstica, y principalmente, por la descarga de efluentes de la industria farmacéutica.
Los antidepresivos se introducen en el ambiente debido a varias actividades antropogénicas como la excreción del paciente, ya sea como compuesto original o metabolitos a través del sistema de alcantarillado, la liberación directa al sistema de aguas residuales de la fabricación, los hospitales o la eliminación a través de inodoros/lavabos o deposiciones terrestres (Castillo-Zacarías y col., 2021). Sin embargo, se plantea que la excreción de productos farmacéuticos después del uso terapéutico humano y veterinario domina la entrada global de estas sustancias al medio ambiente.
En la literatura se reporta la presencia de ISRS y sus metabolitos en aguas urbanas como naturales a nivel mundial (Quadra y col., 2016; Sarker y col., 2018; Silva y col., 2015; Souza y col., 2021). Así como, su potencial bioacumulación en diferentes organismos acuáticos, principalmente peces, plantas acuáticas, moluscos y caracoles, representando un riesgo debido a su toxicidad (Fernandes y col., 2020; Gould y col., 2021; Salahinejad y col., 2022). Desafortunadamente las plantas de tratamientos de aguas residuales (PTARs) convencionales no cuentan con los métodos de remoción necesarios para eliminar estos productos farmacéuticos (Gornik y col., 2021), lo cual es motivo de preocupación para los organismos reguladores de todo el mundo. En consecuencia, se han realizado varios estudios que evalúan diferentes tecnologías y métodos de tratamiento de aguas residuales y naturales, que tienen la finalidad de eliminar estos contaminantes ambientales emergentes. Por todo lo mencionado anteriormente, el objetivo del presente artículo es brindar una actualización sobre las tecnologías de tratamiento de aguas utilizadas para remover los antidepresivos inhibidores selectivos de la recaptación de serotonina de los cuerpos de aguas y su eficiencia.
MATERIALES Y MÉTODOS
La selección de la literatura consultada se realizó principalmente a través de las bases de datos Science Direct, Elsevier, PubMed y Google Scholar. La presente revisión de la literatura se enfocó en artículos centrados en medicamentos antidepresivos inhibidores selectivos de la recaptación de serotonina (ISRS), su metabolismo, propiedades físico-químicas y tratamientos. La selección de medicamentos se elaboró a partir de información difundida por la OMS, sobre los principales antidepresivos recetados para la depresión antes y durante la pandemia del SARS-CoV-2. En consecuencia, la búsqueda incluyó las palabras clave: COVID-19, SARS-CoV-2, antidepresivos, fluvoxamina, fluoxetina, sertralina, citalopram, paroxetina, Agua, Aguas Residuales, Ocurrencia, Degradación, Eliminación, Remoción, Metabolismo, Propiedades Físico-Químicas y Tratamiento. Se realizaron búsquedas individuales para cada fármaco seleccionado. Finalmente, se excluyeron todos los artículos que no estaban relacionados con el enfoque y los objetivos de la revisión. Para ello se revisaron los títulos, resúmenes y palabras clave. Esto permitió verificar si los trabajos obtenidos cubrían la presencia de las drogas en ambientes acuáticos o su eliminación por técnicas de tratamiento de aguas superficiales y aguas residuales. En total, se citaron 67 artículos científicos.
RESULTADOS Y DISCUSIÓN
Metabolismo y excreción de los fármacos antidepresivos
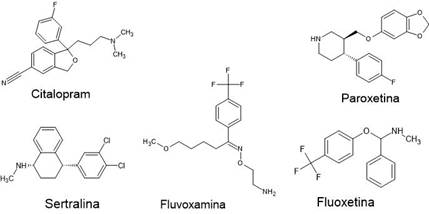
Los ISRS tienen diferentes estructuras moleculares (figura 1), sin embargo, todos presentan una elevada liposolubilidad, lo que determina su rápida y amplia distribución en el organismo, difundiéndose a través de la barrera hematoencefálica, para llegar a su sitio de acción específico (receptores presinápticos 5HT-1A, 5HT-2C y 5HT-3C) y producir el efecto antidepresivo (Chávez-León y col., 2008).
Por lo general los fármacos no se metabolizan por completo en el organismo, lo que resulta en la excreción de porcentajes variables del compuesto original junto con varios metabolitos y conjugados en orina y heces (Carlsson y col., 2006). Se considera que la excreción es la vía principal de entrada de productos farmacéuticos en las matrices ambientales, por tanto, la comprensión del metabolismo y las tasas de excreción de los ISRS, resulta importante para la evaluación de las concentraciones ambientales de estas sustancias. Al igual que otros fármacos lipofílicos, los ISRS después de su administración experimentan un metabolismo hepático para formar compuestos más hidrofílicos, que son excretados con mayor facilidad, donde el grado de metabolismo es relativamente alto. Los datos farmacocinéticos muestran que la mayoría de los ISRS se excretan como metabolitos, no como compuestos originales (Hiemke y Härtter, 2000).
Las reacciones metabólicas de primera fase en los ISRS dan como resultado la N-desmetilación de CIT, FLU y SER, es decir, desmetilcitalopram (DCIT), didesmetilcitalopram (DDCIT), (S)-(-)-norfluoxetina (nor-FLU) y desmetilsertralina (DSER), que presentan actividad farmacológica, pero son, con excepción de la norfluoxetina, menos potentes que los compuestos originales (Barclay y col., 2011; Silva y col., 2015). La FLX sufre eliminación oxidativa de un grupo metoxilo para formar el desmetilfluvoxamina (ácido carboxílico inactivo), mientras que PAR se transforma en un intermedio de catecol inactivo (Hiemke y Härtter, 2000). Durante la segunda fase del metabolismo, estos compuestos se conjugan, principalmente con glucurónido o sulfato, y luego se eliminan por la orina o las heces (Kosjek y Heath, 2010).
En la literatura existen grandes discrepancias entre las tasas de excreción de los ISRS, y las cantidades excretadas en formas modificadas o conjugadas varían considerablemente. La excreción del CIT como compuesto inalterado oscila entre 12 y 20%, mientras que, para su enantiómero activo (escitalopram) fluctúa entre un 8 y 10% (Rao, 2007). La FLU se excreta principalmente en la orina, un 20 % como nor-FLU y su glucurónido, y un 10 % como FLU y FLU-glucurónido (Nałecz-Jawecki, 2007). Con respecto a la FLX casi el 100 % de una dosis oral se recupera en la orina, pero solo cantidades insignificantes se excretan sin cambios (< 4 %) (van Harten, 1995), se han identificado al menos 11 metabolitos de este fármaco en la orina (Vaswani y col., 2003). La SER se excreta en las heces (50%) (Hiemke y Härtter, 2000) y solo el 0,2% de la dosis oral se excreta sin cambios en la orina (De Vane y col., 2002). La PAR también experimenta excreción urinaria y biliar, el 62% se excreta en orina y el 36% en heces, en forma de metabolitos inactivos, mientras que, alrededor del 2% se excreta como compuesto original en orina y el 1% en las heces (Calisto y Esteves, 2009).
A pesar de la inactividad farmacológica de los conjugados de glucurónidos, se cree que estos metabolitos se descomponen fácilmente por acción bacteriana y se reconvierten en el compuesto activo original (Alfonso-Muniozguren y col., 2021). Parece muy probable que los conjugados de glucurónidos se desconjuguen fácilmente en aguas residuales domésticas y PTAR debido a la presencia generalizada de la bacteria fecal Escherichia coli, responsable de la producción de grandes cantidades de la enzima β-glucuridasa (Jones y col., 2005). El proceso de desconjugación da como resultado un aumento de la cantidad del compuesto original en aguas residuales (Calisto y Esteves, 2009).
Propiedades fisicoquímicas y destino ambiental
Las propiedades fisicoquímicas de los ISRS reportadas en la literatura consultada se muestran en la tabla 1. Los ISRS presentan solubilidades en agua relativamente altas y coeficientes de partición octanol-agua relativamente bajos (Kow: 1,12-1,39), indicando que estos compuestos tendrán una baja persistencia en el medio acuático, ocasionada por una mayor probabilidad de degradarse por procesos microbianos, debido a su solubilidad (Us EPA, 2007). Sin embargo, los pka de los ISRS oscilan entre 9,05 y 10,5, en consecuencia, estarán presentes en el agua principalmente en forma neutra a pH alto y en forma iónica a pH bajo (Metcalfe y col., 2003).
Si bien la solubilidad en agua y la hidrofobicidad son parámetros cruciales para predecir la persistencia y destino ambiental de los ISRS, la absorción en suelos o sedimentos también es un factor importante a tener en cuenta. Los ISRS presentan altos coeficientes de sorción (log Koc o coeficiente de sorción normalizado de carbono orgánico) con suelos y sedimentos, con valores de log Koc que van desde 3,82 a 5,63 para fluvoxamina (menor grado de sorción) y citalopram (mayor grado de sorción) respectivamente, lo que significa que estos compuestos tienen tendencia a incorporarse a sedimentos, lodos y suelos (Kwon y Armbrust, 2008). Las interacciones electrostáticas, los enlaces químicos y las fuerzas no específicas entre las moléculas ionizadas y la materia orgánica disuelta (DOM) se desprecian mediante enfoques exclusivos de log Kow y Koc (Silva y col., 2012).
Baker y Kasprzyk-Hordern, (2011), reportaron que la fluoxetina, y otros ISRS, exhiben una unión apreciable (hasta 50 %) a las partículas en suspensión, por lo que, la vida media activa de estos fármacos en ambientes acuáticos puede verse incrementada.
Tabla 1 Propiedades físico-químicas de los ISSRs (adaptado de Silva y col., 2015)
| Compuesto | Número CAS | Fórmula molecular | Peso molecular | pKa | Log kowx | Log kocy | Solubilidad (mgL-1) |
|---|---|---|---|---|---|---|---|
| Citalopram | 59729-33-8 | ( C 20 H 21 FN 2 O) | 324,16 | 9,59 | 1,39 | 5,63 | 31,1 |
| Fluoxetina | 54910-89-3 | (C 17 H 18 F 3 NO) | 309,13 | 10,05 | 1,22 | 4,65 | 60,3 |
| Fluvoxamina | 54739-18-3 | (C 15 H 21 F 3 N 2 O 2 ) | 318,16 | 9,39 | 1,21 | 3,82 | - |
| Paroxetina | 61869-08-7 | (C 19 H 20 FNO 3 ) | 329,14 | 10,32 | 1,37 | 4,47 | 35,3 |
| Sertralina | 79617-96-2 | (C 17 H 17 Cl 2 N) | 305,07 | 9,47 | 1,37 | 4,17 | 3,52 |
- Datos no disponibles.
x Medido en forma de sal (HCl) en cada ISRS.
y Promedio calculado a partir de experimentos con cinco suelos y sedimentos diferentes a pH 5,0 - 7,8.
Inhibidores selectivos de la recaptación de serotonina en el medio ambiente
De manera general las propiedades fisicoquímicas de los ISRS y su elevada absorción en los sedimentos, indican una alta tendencia a persistir y acumularse en el ambiente acuático. En las últimas décadas, se ha descrito en la bibliografía la presencia constante de estos fármacos, así como de sus metabolitos, en matrices acuosas de diferentes regiones geográficas, en concentraciones de hasta varios ng L−1 (Mole y Brooks, 2019). Después del 2019, varias investigaciones reportan un aumento de la concentración de ISRS, particularmente en el ciclo urbano del agua (tabla 2), lo cual puede relacionarse con el incremento de la prescripción y uso de ISRS, como consecuencia de los problemas de salud mental que ha ocasionado la pandemia de COVID-19 (Teymoorian y col., 2021).
Tabla 2 Presencia de ISRS en matrices acuosas antes y después del 2019
| Fármacos antidepresivos ISRS | Antes del 2019 | Después del 2019 | ||||||
|---|---|---|---|---|---|---|---|---|
| Concentración (ng L-1) | Tipo de agua | País | Referencia | Concentración (ng L-1) | Tipo de agua | País | Referencia | |
| Fluoxetina | 9,22 | Afluente de PTAR | Portugal | (Paíga y col., 2016) | 212,5 | Afluente de PTAR | Grecia | (Kosma y col., 2020) |
| 16,4 | Efluente de PTAR | Portugal | (Paíga y col., 2016) | 20,9 - 124,4 | agua de PTAR | Grecia | (Christoforidis, 2021) | |
| 10 | aguas residuales | Eslovenia | (Trontelj y Zakšek, 2016) | <600 | Afluente de PTAR - | Costa Rica | (Ramírez-Morales y col., 2020) | |
| 42,9 | agua residual de PTAR - | Shanghai | (Wu y col., 2017) | 1200 | Afluente de PTAR | Túnez | (Afsa y col., 2020) | |
| Citalopram | 205 - 414 | efluente de Petar | Estados Unidos | (Subedi & Kannan, 2015) | 211,5 | Afluente de PTAR | Grecia | (Kosma y col., 2020) |
| 259 | efluente de petar - | Eslovaquia | (Ivanová y col., 2017) | |||||
| 5,82 - 21,26 | efluente de PTAR - | Shanghái | (Ma y col., 2018) | |||||
| Sertralina | 27,9 - 88,3 | efluente de Petar - | Estados Unidos | (Subedi y Kannan, 2015) | 549 | agua residual de hospital - | Eslovenia | (Gornik y col., 2020) |
| 50 | aguas residuales | Eslovenia | (Trontelj y Zakšek, 2016) | 119 | agua de PTAR | Eslovenia | (Gornik y col., 2020) | |
| 5 | agua residual de PTAR - | Shanghái | (Wu y col., 2017) | |||||
| 4,26 - 11,53 | efluente de PTAR - | Shanghái | (Ma y col., 2018) | |||||
| Paroxetina | 23,6 | Afluente de PTAR | Portugal | (Paíga y col., 2016) | 89,3 | Afluente de PTAR | Grecia | (Kosma y col., 2020) |
| 25,5 | Efluente de PTAR | Portugal | (Paíga y col., 2016) | 40,5 | Efluente de PTAR | Grecia | (Kosma y col., 2020) | |
| 2,1 | agua residual de PTAR - | Shanghai | (Wu y col., 2017) | |||||
| Fluvoxamina | 5,21-17,8 | Afluente de PTAR | Portugal | (Paíga y col., 2016) | 203 | Afluente de PTAR | Grecia | (Kosma y col., 2020) |
| 11,3-34 | Efluente de PTAR | Portugal | (Paíga y col., 2016) | 324,9 | Efluente de PTAR | Grecia | (Kosma y col., 2020) | |
Técnicas de tratamientos de agua
La eliminación de los ISRS de las aguas residuales no se realiza ni está regulada por normas internacionales. Sin embargo, existen estudios actuales en los que se evalúan técnicas y métodos efectivos para este objetivo.
Fotodegradación
La fotodegradación es la transformación fotoquímica de una molécula en otras de menor peso molecular que se produce bajo la influencia de la luz (absorción de radiación UV, VIS o IR), generalmente es un proceso combinado de oxidación e hidrólisis, el cual puede producirse en la atmósfera, en la superficie del suelo y del agua (Sánchez, 2007). Debido a la fotosensibilidad que presentan los ISRS, se han estudiado diferentes sistemas fotoquímicos en la degradación de estos contaminantes emergentes en distintas matrices de agua (Tabla 3).
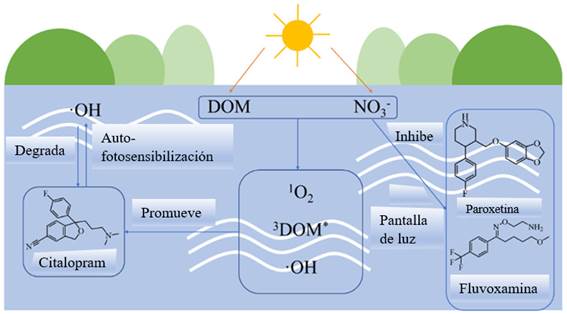
Los estudios han demostrado que la materia orgánica disuelta (DOM), debido a que contiene fracciones antioxidantes como compuestos fenólicos, puede promover o inhibir la fotólisis de contaminantes orgánicos (Vione y col., 2014). El mecanismo de remoción es principalmente a través de procesos de fotólisis indirecta, como la reacción de oxidación fotosensibilizada. Este comportamiento ha sido reportado para varios ISRS. Calza y col., (2021), estudiaron el comportamiento fotolítico de la SER (1 mg • L • −1 • ), bajo radiación solar artificial (Lámpara de arco de xenón de 1500 W a 25 °C), en diferentes matrices acuosas tales como agua ultrapura, efluentes de aguas residuales, así como en presencia de materia orgánica disuelta (ácidos húmicos), iones bicarbonato y nitrato, concluyendo que la fotólisis de este fármaco, sigue una cinética de primer orden y que fue más rápida en aguas de efluentes de EDAR (t½ 34h) en comparación con el agua ultrapura (t½ 57h), atribuyéndolo a reacciones autocatalíticas. En otro estudio similar, Jiménez-Holgado y col., (2021), investigaron el comportamiento fotolítico del CIT en diferentes matrices de aguas, reportando que las tasas de fotodegradación del CIT en las aguas naturales (residuales y de lago) fueron más rápida en comparación con el agua ultrapura, tanto bajo irradiación solar natural como simulada, indicando que los constituyentes de las aguas naturales, contribuyen al incremento de la descomposición de CIT y que la fotólisis indirecta puede ser un proceso de degradación importante en el medio ambiente acuático. También, Guo y col., (2022) reportaron que CIT se transforma principalmente por fotólisis indirecta en agua de lago, mientras que PAR y FLX se degradan por fotólisis directa, señalando que la DOM y NO3 - fueron los principales factores que afectaron la fotodegradación de los antidepresivos (figura 2). La fotodegradación de PAR y FLX fue inhibida por NO3 - o DOM, debido al efecto de pantalla de luz y/o especies reactivas depuradoras, mientras que se observaron efectos de remoción para CIT a través de la reacción con -OH y el estado de triplete excitado de DOM. Otro estudio encontró que la fotodegradación de PAR en el agua de un río se retrasó significativamente, planteando que el efecto de fotoprotección de los contaminantes orgánicos que absorben la luz y/o el efecto de extinción de DOM en el estado excitado, fueron los responsables de esta inhibición (Santoke y Cooper, 2017).
Los datos de la literatura muestran que se han estudiado diferentes sistemas fotoquímicos en la degradación de ISRS. Moreira y col., (2019) investigaron la fotodegradación de la fluoxetina (FLU) empleando dos sistemas: un reactor UV y un reactor integrado de microondas-ultravioleta (UV/MW), obteniendo una degradación del 99,2% en 5 min mediante el uso del reactor UV/MW y del 98,9 % en 120 min cuando se empleó el reactor UV, siendo el primer proceso 95,8% más eficiente en relación al tiempo de degradación. Además, identificaron 9 productos de transformación (TPs) y comprobaron que el reactor UV/MW tiene el potencial de degradar FLU y sus TPs en cortos intervalos de tiempo.
Cabe señalar que, numerosos procesos fotoquímicos, se aplican en combinación con peróxido, hierro, ozono y semiconductores, para aumentar la eficiencia en la degradación de los productos farmacéuticos, al favorecer la formación de oxidantes fuertes, especialmente radicales hidroxilos (Moreira y col., 2019). No obstante, su aplicación en plantas de tratamientos no se ha dado a gran escala debido a la falta de estudios experimentales que confirmen su efectividad y determinen los parámetros operacionales, termodinámicos y cinéticos.
Fotocatálisis UV/TiO2
Entre los diversos fotocatalizadores semiconductores que existen, el dióxido de titanio (TiO2) ha llamado especialmente la atención en la comunidad científica, debido a su alta eficacia oxidante y mineralizadora hacia una amplia variedad de contaminantes orgánicos, su estabilidad química, no toxicidad y bajo costo (Tang y col., 2022).
Varias investigaciones realizadas a escala de laboratorio han confirmado que la fotocatálisis TiO2/UV es altamente efectiva para la eliminación de ISRS en matrices acuosas (tabla 3). Por ejemplo, Calza y col., (2021) usaron TiO2 (400
Fotocatálisis UV/H2O2
En el proceso UV/H2O2, el H2O2 se agrega al agua que se trata y se irradia con luz ultravioleta, lo que conduce a la producción de radicales hidroxilos. El proceso no es selectivo, sino que depende de la absorbancia UV del agua. Para una eliminación eficiente de los productos farmacéuticos con el empleo UV/H2O2, el agua tratada biológicamente y relativamente libre de partículas es una ventaja. Además, es recomendable que el contenido de secuestrantes de hidroxilo (p. ej., nitrito, iones inorgánicos) sea bajo. Por lo tanto, el uso de UV/H2O2 a menudo se limita a pasos de tratamiento terciario o aguas residuales específicas. Sin embargo, los sistemas UV/H2O2 tienen la ventaja adicional en comparación con otros sistemas POA, debido a que tienen un diseño flexible y utilizan productos químicos de menor costo y fácil disponibilidad. En consecuencia, Spina y col., (2021), estudiaron la degradación de fluoxetina y escitalopram (ESC) (tabla 3), en diferentes matrices (agua ultrapura, agua potable del grifo, aguas residuales recuperadas y aguas superficiales), mediante la fotoperoxidación (UV/H2O2). Reportando un 99% de degradación de FLU independientemente de la matriz de agua. Sin embargo, para eliminar completamente el ESC del agua potable del grifo y de las matrices de agua PTAR, fueron necesarios más de 60 min de reacción y se requirió una radiación UVC diez veces mayor, mientras que, en aguas superficiales el 10% del ESC permaneció en la solución incluso después de 60 min de radiación. Los metabolitos primarios de ambos antidepresivos fueron identificados como los principales subproductos generados por el proceso UV/H2O2 y persistieron en la solución incluso cuando se degradó el compuesto original. En un estudio similar, Hollman y col., (2020), lograron remover el 33% de FLU durante 5 min de radiación UVC (3,5 kW/m3) en presencia de H2O2 (100 mg L-1), el experimento se realizó con diferentes concentraciones de H2O2, donde se determinó que con el incremento de concentración de H2O2 se incremente el porcentaje de remoción. A su vez, se llevaron a cabo experimentos de control de H2O2 en condiciones de oscuridad en donde no se detectó degradación por parte de ningún fármaco durante 24 horas, atribuyendo así toda la degradación mediante UVC/ H2O2 al POA.
Tabla 3 Método de fotodegradación
| Fármaco antidepresivo ISRS | Tratamiento usado | Concentración del fármaco | Matriz acuosa agua | Características del proceso | Resultados obtenidos | Referencias |
|---|---|---|---|---|---|---|
| Sertralina | Fotodegradación por radiación solar simulada | 1 mg L-1 | Agua ultra pura y agua de PTAR | Escala: pruebas a escala de laboratorio. • Lámpara de arco de xenón: 1500 W. • Longitud de onda: 300 a 800 nm. • Temperatura óptima 25 °C | Eficiencia de eliminación: agua ultra pura t1/2= 57 h. • agua de PTAR t1/2= 34 h. | (Calza y col., 2021) |
| Citalopram | Fotodegradación por irradiación solar natural | 10 mg L-1 | Agua Ultra pura, agua superficial (NOM = 11,7 mgL- 1), agua de PTAR (NOM = 23,2 mgL- 1) | Escala: pruebas a escala de laboratorio. • Irradiación de luz natural: radiación media diaria total de onda corta fue de 286 y 273 W/m2 para julio y agosto. | Eficiencia de eliminación: • Agua ultra pura t1/2= 3456,74 h, agua superficial t1/2=693h, agua de PTAR t1/2= 462,1 h. | (Jiménez-Holgado y col., 2021) |
| Citalopram | Fotodegradación por radiación solar simulada | 10 mg L-1 | Agua Ultra pura, agua superficial (NOM = 11,7 mgL- 1), agua de PTAR (NOM = 23,2 mgL- 1) | Escala: pruebas a escala de laboratorio • Simulador de luz solar equipado con una lámpara de xenón (1500 W) • Longitud de onda: 295-400 nm • Poterncia UV: 18 Wm- 2 | Eficiencia de eliminación: • Agua ultra pura t1/2= 61,89 h, agua superficial t1/2=25,77 h, agua de PTAR t1/2= 23,42 h. | (Jiménez-Holgado y col., 2021) |
| Citalopram | Fotodegradación | 10 μM | Agua de lago | Escala: pruebas a escala de laboratorio. • Lámpara de mercurio: 500 W. • Longitud de onda: 290 nm. • Rango de pH: 6-9 | Eficiencia de eliminación: • pH 6: t1/2= 8,11 h • pH 7: t1/2=8,33 h • pH 8: t1/2= 35,98 h | (Guo y col., 2022) |
| Paroxetina | Fotodegradación | 10 μM | Agua de lago | Escala: pruebas a escala de laboratorio. • Lámpara de mercurio: 500 W. • Longitud de onda: 290 nm. • Rango de pH: 6-9 | Eficiencia de eliminación: • pH 6: t1/2= 0,09 h • pH 7: t1/2=0,08 h • pH 8: t1/2= 0,07 h • pH 9: t1/2= 0,08 h | (Guo y col., 2022) |
| Fluvoxamina | Fotodegradación | 10 μM | Agua de lago | Escala: pruebas a escala de laboratorio. • Lámpara de mercurio: 500 W. • Longitud de onda: 290 nm. • Rango de pH: 6-9 | Eficiencia de eliminación: • pH 6: t1/2= 0,49 h • pH 7: t1/2=0,5 h • pH 8: t1/2= 0,38 h • pH 9: t1/2= 0,32 h | (Guo y col., 2022) |
| Paroxetina | Fotodegradación por radiación solar simulada | No reporta | Agua ultrapura • Agua superficial (río Suwannee.) | Escala: pruebas a escala de laboratorio. • Lámpara de xenon: 300 W. • Longitud de onda: 300-900 nm. • Rango de pH: 7 | Eficiencia de eliminación: • Agua ultrapura: t1/2= 13,30h. • Agua superficial:t1/2= 38,5h. | (Santoke y Cooper, 2017) |
| Sertralina | Fotodegradación UV/TiO2 | 20 mg L-1 | Agua ultra pura | Concentración inicial óptima de TiO 2: 400 mg L-1 • Longitud de onda: 290 a 400 nm | Eficiencia de eliminación: 100 % a los 60 min | (Calza y col., 2021) |
| Citalopram | Fotodegradación UV/TiO2 | 20 mg L-1 | Agua ultra pura | Escala: pruebas a escala de laboratorio (modo por lotes). • TiO2 concentración: 400 mg L-1 • Longitud de onda: 290-400 nm • Potencia UV: 90 Wm- 2 | Eficiencia de eliminación: • 100 % a los 30 min • 90 % TOC reducción a las 5 h | (Jiménez-Holgado y col., 2021) |
| Fluoxetina | Fotodegradación UV/TiO2 | 500 µg L-1 | Agua ultra pura | Escala: pruebas a escala de laboratorio (modo por lotes). • TiO2 concentración: 0,5 g L-1 • Longitud de onda: 365 nm • Potencia UV: 0,39 mW/cm2 | Eficiencia de eliminación: • > 80 % a los 120 min | (de Wilt y col., 2020) |
| Escitalopram | Fotoperoxidación con UV/ H2O2 | 25 µg L-1 | Agua ultra pura, agua de grifo, agua de PTAR y agua superficial | Escala: pruebas a escala de laboratorio (modo por lotes). • H2O2 concentración: 0,42 mmol L-1 • Temperatura óptima 20 °C • Radiación: Lámpara UV-C (λmax = 254 nm, 8 W) • Intensidad de radiación UV-C: 1,9 kJ. | Eficiencia de eliminación: • Agua ultrapura, agua potable del grifo y PTAR: 100% a los 60 min • Agua superficial: 90 % a los 60 min. | (Spina y col., 2021) |
| Escitalopram | Fotodegradación | 25 µg L-1 | Agua ultrapura | Escala: pruebas a escala de laboratorio, • Temperatura óptima 20 °C • Radiación: Lámpara UV-C (λmax = 254 nm, 8 W) | Eficiencia de eliminación: 60% a los 30 min | (Spina y col., 2021) |
| aNOM materia orgánica natural | TOC carbono orgánico total |
Ozonización
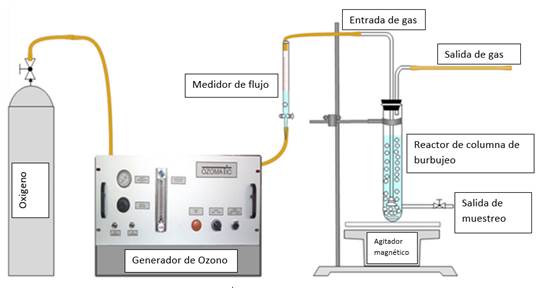
Actualmente, la ozonización es un proceso de oxidación avanzada que se ha revelado como una solución factible para la degradación de contaminantes orgánicos recalcitrantes en matrices acuosas (figura 4), aunque en muchos casos implica el uso de altas dosis de ozono (O3) y el encarecimiento del proceso (Amaral-Silva y col., 2016).
Este proceso consiste en que, una vez disuelto en el agua a tratar, el O3 molecular reacciona con las moléculas orgánicas directamente a través de una reacción de ciclo adición dipolar 1-3 en enlaces insaturados y una reacción electrofílica en compuestos aromáticos que tiene grupos donantes de electrones como OH, NH2 o reacciona indirectamente, por descomposición, a través de la formación de radicales libres, incluido el radical hidroxilo (Snyder y col., 2007). Dado que los ISRS presentan en su estructura aminas secundarias o terciarias y anillos conjugados, la ozonización, se ha estudiado como método alternativo para la degradación de estos fármacos en distintas matrices acuosas (Tabla 4).
Rosal y col., (2010) observaron altas eficiencias de eliminación de CIT (93 %) y FLU (100 %) en muestras de aguas residuales expuestas a 2,4 - 6,1 mg • L • −1 • de O3 durante menos de 5 min. Mientras que, Snyder y col., (2007) informaron una eficiencia de eliminación similar para FLU (> 93 %) en muestras de efluentes tratadas con 3,6 mg • L • −1 • de O3.
En otro estudio Lajeunesse y col., (2013), reportaron que la efectividad de la ozonización para la remoción de ISRS (FLU, SER, PAR, CIT) en aguas residuales urbanas, tiende a aumentar con el incremento de la concentración de O3. En el tratamiento con la mayor concentración de ozono probada (13 mg • L • −1 • ), todos los ISRS se oxidaron y degradaron, sin embargo, a concentraciones de 5 mg • L • −1 • y 9 mg • L • −1 • de O3, la eficiencia de remoción para el CIT fue menor, 34 % y 62 % respectivamente, mientras que para el resto de ISRS fue 100 %. La menor remoción presentada por el CIT, puede estar relacionada con su estructura química, dado que presenta una larga cadena alifática de amina terciaria, pudiendo existir impedimento estérico que dificulte la reacción del ozono sobre sitios específicos de la molécula (Moreira y col., 2019). Además, la materia orgánica disuelta, presente en el efluente pudo haber frenado la descomposición del O3, al inhibir la cadena de reacción de radicales libres y, en consecuencia, la formación de radicales hidroxilos (OH·) necesarios para degradar los carbonos alifáticos saturados presentes en la estructura del CIT (Badii y col., 2018).
Cabe mencionar que la asociación de dos o más oxidantes permite aprovechar los posibles efectos sinérgicos entre ellos, por ejemplo, al combinar O3 con peróxido de hidrógeno (O3/H2O2), los compuestos orgánicos pueden ser oxidados tanto por el O3 molecular (directamente) como por los radicales HO• (indirectamente). Méndez-Arriaga y col., (2011), estudiaron la fotooxidación de FLU en medio acuoso mediante el método híbrido O3/H2O2, observando que, en condiciones de oscuridad, la degradación de FLU a pH 3 por ozonización fue más rápida que por el proceso de O3/H2O2 (k = 0,65 min-1 frente a k = 0,39 min-1). De manera similar, FLU se degradó más rápido por UV/ozonización que por el proceso de UV/O3/H2O2. Evidenciándose que, en estas condiciones, la presencia de H2O2 (0,12 mM) tiene un efecto inhibidor sobre la dinámica de degradación de FLU. Por otro lado, Aghaeinejad-Meybodi y col., (2015), reportaron una eficiencia de eliminación del 86,14 % para la fluoxetina (50
En trabajos posteriores Aghaeinejad-Meybodi y col., (2019), investigaron la ozonización catalítica de FLU en presencia de nanocatalizadores de boehmita y γ-alúmina, en un medio acuoso en un reactor de columna de burbujeo semicontinuo, reportando que la eficiencia de eliminación de FLU aumentó notablemente para la ozonización catalítica en comparación con el proceso de ozonización en un reactor discontinuo. En condiciones óptimas, obtuvieron una eficiencia máxima de eliminación de FLU del 96,14 % con una concentración de 1gL⁻¹ de γ-alúmina. A pesar de la alta efectividad que presentan otros métodos de degradación sobre el CIT, se observó que al parecer este contaminante es resistente a la ozonización como mecanismo de degradación (Aghaeinejad-Meybodi y col., 2021). Sin embargo, la ozonización demostró una alta eficiencia en la remoción del resto de los fármacos ISRS, donde se obtuvieron aún mejores resultados al combinar el ozono con otros grupos oxidantes.
(Aghaeinejad-Meybodi y col., 2015)
Tabla 4 Método de degradación ozonización
| Fármaco antidepresivo ISRS | Tratamiento usado | Concentración del fármaco | Matriz acuosa agua | Características del proceso | Resultados obtenido/s | Referencias |
|---|---|---|---|---|---|---|
| Fluoxetina | Ozonización | No reporta | aguas residuales urbanas | Escala: pruebas a escala de laboratorio (por lotes).Concentración de O3: 2,4 - 6,1 |
Eficiencia de eliminación: 100%. | () |
| Citalopram | Ozonización | No reporta | Aguas residuales urbanas | Escala: pruebas a escala de laboratorio (por lotes).Concentración de O3: 2,4 - 6,1 |
Eficiencia de eliminación: 93%. | (Rosal y col., 2010) |
| Citalopram | Ozonización | 186 ng L-1 • 148 ng L-1 | Aguas residuales urbanas | Escala: pruebas a escala de laboratorio (por lotes). • Concentración de O3: 5 a 9 mg L-1. | Eficiencia de eliminación: 34% y 62% (5 - 9 mg L-1) | (Lajeunesse y col., 2013) |
| Fluoxetina | Ozonización | No reporta | Agua superficial urbana (PTAR) | Escala: pruebas a escala de laboratorio. • Concentración de O3: 5 a 9 mg L-1. | Eficiencia de eliminación: 100%. | (Lajeunesse y col., 2013) |
| Sertralina | Ozonización | 14 ng L-1 9,4 ng L-1 | Agua superficial urbana | Escala: pruebas a escala de laboratorio (por lotes). • Concentración de O3: 5 a 9 mg L-1. | Eficiencia de eliminación: 100% a 5 y 9 mg L-1 de O3 | (Lajeunesse y col., 2013) |
| Paroxetina | Ozonización | 9 ng L-1 • 13 ng L-1 | Agua superficial urbana | Escala: pruebas a escala de laboratorio (por lotes). • Concentración de O3: 5 a 9 mg L-1. | Eficiencia de eliminación: 100% a 5 y 9 mg L-1 de O3 | (Lajeunesse y col., 2013) |
| Fluoxetina | Ozonización /H2O2 | 34 mg L-1 | Solución acuosa | Escala: pruebas a escala de laboratorio • Concentraciones: O3: 25 mg L-1; H2O2: 0,12 mM • Temperatura: 25°C; pH: 3, 11 | Eficiencia de eliminación: 70%. | (Méndez-Arriaga y col., 2011) |
| Fluoxetina | Ozonización /H2O2/UV | 34 mg L-1 | Solución acuosa | Escala: pruebas a escala de laboratorio • Concentración de O3: 25 mg L-1. • Lámpara de Hg, Longitud de onda: 360 nm • Concentración de H2O2: 0,12 mM • Temperatura: 25°C. | Eficiencia de eliminación: 97%. | (Méndez-Arriaga y col., 2011) |
| Fluoxetina | Ozonización /H2O2 | 50 mg L-1 | Solución acuosa | Escala: pruebas a escala de laboratorio (por lotes). • Concentraciones: O3: 30 mg L-1; H2O2: 0,02 mM • Temperatura: 25°C; pH: 7 | Eficiencia de eliminación: 86,14% | (Aghaeinejad-Meybodi y col., 2015) |
| Fluoxetina | Ozonización/ Nano-γ-Al2O3 | 28,56 mgL-1 | Solución acuosa | Masa del catalizador =1 g L-1 • Concentración de Ozono: 30m g L-1 • Temperatura: 25 °C; pH: 7 | Eficiencia de eliminación: 96,14% | (Aghaeinejad-Meybodi y col., 2019) |
Otros métodos de degradación
Los datos de la literatura muestran que se han realizado varias investigaciones de la degradación de ISRS en matrices acuosa empleando métodos diferentes a los ya mencionados (Tabla 5). Dentro de estos métodos se encuentran los procesos de oxidación avanzada con hipoclorito de sodio, dióxido de cloro y ferrato de potasio, y método de radiación gamma, el cual es un método utilizado para la esterilización de equipos médicos y alimentos con un tipo de radiación ionizante con una alta capacidad de penetración la cual es capaz de causar graves daños al núcleo de las células (Fuchs y col., 2002).
La radiación gamma es otro proceso de oxidación avanzada que se ha estudiado para la degradación de sertralina y citalopram. Bojanowska-Czajka y col., (2021), realizaron pruebas en diferentes matrices acuosas con SER y CIT, obteniendo diferencias significativas en la eficiencia de degradación en función de la matriz acuosa y entre la SER y el CIT para las mismas matrices. Sin embargo, cuando se aplicaron dosis de radiación ionizante de 500 Gray (Gy), se obtuvo una degradación prácticamente completa tanto en soluciones acuosas puras como en aguas superficiales, demostrando que, a mayor radiación gamma se obtiene una mayor degradación de los ISRS. Cabe destacar que la ventaja de utilizar tecnología de radiación gamma en comparación con otros POA, es que el tiempo se reduce significativamente.
A escala de laboratorio se ha estudiado la degradación ISRS empleando agentes oxidantes diferentes a los comentados anteriormente. Drzewicz y col., 2018, investigaron la degradación de 10
Tabla 5 Otros métodos
| Fármaco antidepresivo ISRS | Tratamiento usado | Concentración del fármaco | Matriz acuosa agua | Características del proceso | Resultados obtenidos | Referencias |
|---|---|---|---|---|---|---|
| Sertralina | Fotodegradación con radiación gamma | 1 mg L-1 | Agua ultra pura, agua de PTAR y agua superficial de río | Escala: pruebas a escala de laboratorio (modo por lotes). • Radiación: fuente de60Co Gamma Chamber 5000 con una tasa de dosis absorbida de 2,15 kGy h−h. Dosis de radiación máxima: 200Gy. Dosis de radiación mínima: 10 Gy. | Eficiencia de eliminación: • Agua ultra pura: 90% (10 Gy). • Agua de PTAR: 30 % (200Gy). • Agua superficial: 60% a 80% (200Gy). | (Bojanowska-Czajka y col., 2021) |
| Citalopram | Fotodegradación con radiación gamma | 1 mg L-1 | Agua ultra pura, y agua superficial de río | Escala: pruebas a escala de laboratorio (modo por lotes). • Radiación: fuente de60Co Gamma Chamber 5000 con una tasa de dosis absorbida de 2,15 kGy h−h. Dosis de radiación máxima: 200Gy. | Eficiencia de eliminación: • Agua ultrapura: 90% (100 Gy). • Efluyente de PTAR: 80% (10Gy) • Agua superficial, 50% a 80% (200Gy). | (Bojanowska-Czajka y col., 2021) |
| Fluoxetina | Oxidación con ferrato de potasio | 10 mg L-1 | Solución acuosa | Escala: pruebas a escala de laboratorio. Concentraciones de ferrato de potasio: 50 - 100 - 200 - 400 mg L-1; pH: 4 | Eficiencia de eliminación: 88% (1 h de reacción con 400 mg L-1). | (Drzewicz y col., 2018) |
| Fluvoxamina | Oxidación con ferrato de potasio | 10 mg L-1 | Solución acuosa | Escala: pruebas a escala de laboratorio. Concentraciones de ferrato de potasio: 50 - 100 - 200 - 400 mg L-1; pH: 4 | Eficiencia de eliminación: 90% (1 h de reacción con 400 mg L-1). | (Drzewicz y col., 2018) |
| Citalopram | Oxidación con hipoclorito de sodio y dióxido de cloro | 0,8 μM - 32 μM | Agua superficial y residual | Escala: pruebas a escala de laboratorio (modo por lotes). • Concentración de hipoclorito de sodio y dióxido de cloro: 1 mM. pH: 7 | Eficiencia de eliminación: 100% (0,67 h). • La eliminación con NaOCl demostró ser más eficiente, sin embargo, provocó una mayor formación de NDMA. | (Lv y col., 2019) |
CONCLUSIONES
Los estudios han demostrado que los coeficientes de partición de los ISRS favorecen la adsorción de sedimentos y que tienen un alto potencial de bioacumulación. Por lo tanto, puede representar un problema ambiental, ya que, estos compuestos como sus metabolitos, al ser excretados por los humanos ingresan a los cuerpos de agua, debido a que existe una baja o nula tasa de remoción en las plantas de tratamiento de agua, existiendo una necesidad urgente de desarrollar mejores técnicas de tratamiento de aguas. De acuerdo con esta revisión de la literatura, se ha descrito en una amplia variedad de tecnologías de tratamiento de aguas utilizadas para eliminar los ISRS de las aguas residuales. A escala de laboratorio, las técnicas de fotodegradación y ozonización se presentan como métodos muy eficientes, ya que eliminan más del 85% de estos fármacos e incluso en algunos casos llegando a alcanzar el 100% de su eliminación. Además, otros métodos como la radiación gamma y la oxidación con hipoclorito de sodio, dióxido de cloro y ferrato de potasio se presentan como una alternativa interesante, ya que eliminan entre un 60% y 100% de estos mismos fármacos en diversas condiciones. Sin embargo, está bajo investigación la factibilidad para aplicarse a gran escala, debido a la falta de información sobre los problemas de diseño de sus reactores, datos adecuados sobre sus mecanismos y los impactos de las variables operativas. Como perspectiva se propone continuar con el estudio de nuevas técnicas que permitan eliminar del agua este tipo de contaminantes de manera eficiente, sin generar compuestos que puedan volverse más tóxicos. Finalmente, la combinación de diversas tecnologías se presenta como un campo de estudio en auge, debido a que pueden generar ventajas operativas, técnicas y económicas, gracias al comportamiento sinérgico de los procesos individuales.