Introducción
Los desórdenes temporomandibulares (DTM) son trastornos que afectan la articulación temporomandibular (ATM), y los tejidos musculoesqueléticos asociados o ambos.1,2,3,4,5,6,7) Los signos y síntomas, que se presentan entre el 6-12 % de la población adulta, son: dolor crónico, dolor muscular, ruido articular, rango de movimiento limitado, función de la mandíbula alterada, desviación o deflexión al abrir y cerrar la boca o bloqueo abierto.2,3,4,6,7,8,9) Otros signos y síntomas incluyen: asimetría del movimiento de la mandíbula (comúnmente descritos erróneamente como chasquidos), chasquidos propiamente, rejillas o crepitación,4,6,10 hipertrofia de músculos masticatorios sin dolor, fatiga muscular,4,5,6 dolor de cabeza, bruxismo, sensibilidad a la palpación y dificultad para abrir la boca.4,6,11 Los DTM tienen una amplia variedad de causas, las más comunes son: hábitos parafuncionales, desarmonía oclusal, estrés, ansiedad, traumatismo y microtrauma, inestabilidad mandibular, desequilibrio postural y condiciones fisiológicas anormales.4,6,7,11 Varios factores, incluidos los trastornos del sueño, así como el estrés físico, emocional y oclusal, pueden inhibir la capacidad adaptativa del sistema estomatognático y hacer que la aparición de los DTM sea más probable.4,6
Los DTM incluyen condiciones degenerativas de las superficies articulares de la ATM, de estas condiciones, la osteoartritis (OA) es la más prevalente; aunque también predominan otras, como el desplazamiento del disco de la ATM (con o sin reducción), el cual se refiere a la interrupción de la relación fisiológica entre las superficies articuladas y el disco de la ATM.1,2,7 Los estudios epidemiológicos han demostrado que el 8,9 % de la población general sufre de osteoartritis de la ATM y, en pacientes con DTM, hasta el 55,6 %.1) Los DTM son más comunes en mujeres que en hombres. El 44,2 % de los pacientes presentan desplazamiento del disco de la ATM, aunque esto no siempre se acompaña de cambios articulares degenerativos.1,2,3,4,7,9,12
La osteoartritis de la ATM es un trastorno crónico degenerativo progresivo que incluye cambios erosivos en las capas de cartílago, pérdida de hueso subcondral y sinovitis. 1,2,13) Prevalece con el aumento de la edad y las mujeres se ven afectadas con el doble de frecuencia que los hombres.13) A diferencia de la osteoartritis de la rodilla, que se atribuye principalmente a la obesidad, el envejecimiento y el trauma, las causas de la osteoartritis de la ATM siguen sin estar claras; sin embargo, la carga mecánica excesiva, acompañada por una capacidad de adaptación del huésped disminuida, es la hipótesis principal.1,13,14,15) Existen otros factores biológicos como: la genética, la inflamación, el estrógeno, la remodelación del hueso y la apoptosis de los condrocitos; que también se han propuesto como mecanismos asociados con el desarrollo de la osteoartritis de la ATM.13,15) En casos de desplazamiento del disco de la ATM, se establece un contacto patológico entre las superficies articuladas. En algunos pacientes, esto conduce a la alteración de la homeostasis del cartílago y los cambios artrósicos, debido a la sobrecarga, el desgaste excesivo y la capacidad de adaptación inferior.1,2 A pesar del hecho de que aún no se ha establecido una clara correlación entre los dos trastornos, parece que existe una relación y algunos pacientes presentan un desplazamiento del disco que precede a la osteoartritis de la ATM.1
Actualmente, el tratamiento terapéutico de los DTM se enfoca en aliviar el dolor funcional y establecer un rango normal de movimiento mandibular. Las modalidades no invasivas son el tratamiento inicial, que incluye fisioterapia, el uso de una férula de estabilización y medicamentos para aliviar los síntomas. Para los pacientes en los que los síntomas persisten y la gravedad de la degeneración es mayor, se pueden aplicar tratamientos mínimamente invasivos, como el lavado, el ácido hialurónico y las inyecciones de corticosteroides, la artrocentesis y la artroscopia.1,2,3,6,13,16
El ácido hialurónico (AH) o también conocido como hialuronano, es un glicosaminoglicano natural de alto peso molecular producido por las células sinoviales que están presentes de manera natural en el líquido sinovial.1,2,7,13) El AH es considerado como un componente esencial del líquido sinovial y participa en la lubricación de las articulaciones. La degradación del AH fue observada generalmente en casos de degeneración de la ATM.1,2,13 Las inyecciones de AH intraarticulares en la ATM han sido indicados para el tratamiento de los DTM durante muchos años, mostrando resultados positivos con respecto a la apertura de la boca y una disminución en la intensidad del dolor.1,2,7,8,13 A pesar de la extensa bibliografía sobre el tema, el mecanismo de acción exacto del AH sigue sin estar claro, aunque posiblemente los efectos positivos son el resultado del aumento de la viscosidad del líquido sinovial, la restauración de la nutrición y la reducción de los mediadores inflamatorios.1,13
Los concentrados de plaquetas (CP) (plasma rico en plaquetas [PRP] o plasma rico en factores de crecimiento [PRFC] y fibrina rica en plaquetas [FRP]) se usan con frecuencia para procedimientos quirúrgicos en muchos campos médicos, particularmente en cirugía oral y maxilofacial, cirugía plástica y medicina deportiva.17,18 El objetivo de todas estas tecnologías es extraer (mediante centrifugación) todos los elementos de una muestra de sangre, en particular: las plaquetas (ricas en factores de crecimiento), fibrina (matriz de soporte) y, en algunos casos, el contenido celular (principalmente leucocitos), los que podrían ser útiles para mejorar la cicatrización y promover la regeneración del tejido.17
El plasma rico en plaquetas y la fibrina rica en plaquetas son terapias biológicas que comprenden un concentrado de plaquetas de la sangre del paciente.1,2,7,13,17,19,20,21,22) Ambas terapias se obtienen a través de la extracción de sangre y su centrifugación para adquirir una alta concentración de plaquetas (de tres a ocho veces mayor que la concentración basal), que en algunos casos puede superar los 2 000 000 plaquetas/mL.1,2,13,17,19,20,21,22 Estos concentrados han mostrado un gran potencial como modalidad terapéutica, debido a contiene una abundancia de factores de crecimiento.1,7,13,17,20,21,22,23
A pesar de que el mecanismo de acción exacto del PRP aún es desconocido por muchas profesiones de la salud, se ha hecho popular en ortopedia y medicina deportiva. Actualmente resulta un tratamiento prometedor para los defectos degenerativos del cartílago y la osteoartritis. 1,18 Esto es atribuido principalmente a sus propiedades antiinflamatorias y analgésicas, así como a los resultados positivos obtenidos en estudios clínicos cuando fue administrado de forma intraarticular en articulaciones con una patología de cartílago, como la osteoartritis de rodilla.1,2,7,18,23 Más específicamente, existe evidencia científica sustancial para respaldar los efectos potenciales del PRP sobre los defectos del cartílago.1,2,13,18 Además, el PRP tiene varias ventajas como tratamiento, porque es obtenido fácilmente y se asocia con pocas complicaciones posoperatorias.1,13,17,18
Recientemente, las inyecciones de PRP se han aplicado de forma intraarticular en la articulación temporomandibular en pacientes con osteoartritis y desplazamiento del disco. A pesar de la extensa literatura sobre la aplicación de PRP en otras articulaciones, especialmente en la rodilla, su aplicación como tratamiento en la ATM es relativamente nueva1,2,13 y, además, no existe evidencia de inyecciones de fibrina rica en plaquetas para el tratamiento de los DTM. Por lo tanto, esta revisión sistemática fue realizada para determinar la efectividad de los concentrados de plaquetas en el tratamiento de los DTM.
Métodos
El desarrollo de la presente revisión fue realizado según un protocolo de investigación previamente confeccionado siguiendo las directrices de las normas PRISMA.24
Se realizó una estrategia de búsqueda amplia en las bases de datos biomédicas PubMed, Embase, SciELO, Science Direct, Scopus, SIGLE (System of Information on Grey Literature in Europe), LILACS, Google Scholar y en el Registro Central de Ensayos clínicos Cochrane. El periodo analizado fue desde el 2 de enero del 2014 hasta el 30 de abril del 2019. Fue utilizada una combinación de encabezados temáticos mediante las siguientes palabras clave y conectores boleanos:
((((((temporomandibular joint disorder) OR temporomandibular joint disorders) OR temporomandibular joint dysfunction) OR temporomandibular disorder) OR temporomandibular disorders) OR temporomandibular dysfunction) AND (((((platelet rich plasma) OR PRP) OR platelet rich fibrin) OR PRF) OR plasma rich in growth factor).
Todo este proceso fue realizado por dos autores (Heber Arbildo Vega y Hernán Vásquez Rodrigo) de forma independiente.
Se incluyeron en el estudio aquellos artículos que reportaran:
el uso de CP (PRP o PRF, PRGF);
la efectividad de los CP (reducción del dolor y aumento de apertura máxima) en el tratamiento de los DTM;
como máximo una antigüedad de 5 años de publicación; y
ensayos clínicos sin restricción de idioma y de tiempo de seguimiento;
Se excluyeron los artículos que hubiesen sido publicados en revistas no indexadas.
Se revisaron los títulos y los resúmenes de cada uno de los estudios obtenidos con los criterios de inclusión y exclusión anteriormente descritos; y se obtuvieron los textos completos de los estudios que cumplían con estos parámetros para poder determinar su riesgo de sesgo.
Para valorar los estudios se realizó una lista de chequeo por duplicado, con el fin de extraer la información de interés y de conmutar los datos. Dos revisores (Víctor Alay-Baca y Gustavo Giribaldi-Ugáz) realizaron de forma independiente la evaluación de los artículos respecto a nombre, autor, año de publicación, tipo de estudio, número de pacientes (proporción entre hombres y mujeres), edad media y rango de edad de los pacientes, tiempo de seguimiento, país en donde fue realizado el estudio, grupos de estudio, número de pacientes por grupo de estudio (proporción entre hombres y mujeres), edad media por grupo de estudio, lugar de administración de los CP, tipo de CP, criterios de inclusión y exclusión, reducción del dolor, aumento de apertura máxima, cantidad de sangre extraída, tipo de anticoagulante usado, protocolo de obtención del CP, centrifugación, temperatura, tipo de activador usado, volumen de la inyección, número de inyecciones y riesgo de sesgo. Para la resolución de cualquier discrepancia entre los revisores estos se reunieron y discutieron junto a un tercer revisor (Hernán Vásquez-Rodrigo) para llegar a un acuerdo.
Para la evaluación del riesgo de sesgo, cada estudio fue analizado según el Manual Cochrane de revisiones sistemáticas de intervenciones.25) Los datos de cada estudio fueron colocados y analizados en el programa RevMan 5.3 (Grupo Cochrane, UK).
Resultados
Selección de los estudios
La búsqueda inicial en las bases de datos biomédicas determinó un total de 134 títulos, de los cuales 39 eran títulos repetidos, por lo que quedaron solamente 95. Luego de leer los títulos se excluyeron 59. De los documentos restantes, se examinaron los resúmenes y fueron descartados aquellos que no cumplieron con los criterios de inclusión. Se seleccionaron 9 artículos para una revisión exhaustiva de su contenido y su metodología, procedimiento a través del cual se descartaron dos artículos más. Finalmente, la muestra para el metaanálisis quedó conformada por siete documentos (Fig. 1).
Característica y resultados de los estudios
En todos los estudios incluidos 26,27,28,29,30,31,32,33,34 el número de pacientes osciló entre 20 y 100, con un tiempo de seguimiento entre 14 días y 24 meses. Ocho investigaciones26,27,28,29,30,31,32,34) reportaron que la media de edad de los pacientes osciló entre 26,3 y 38,6 años. Coincidentemente, esas mismas investigaciones informaron que el número total de pacientes con relación a su género fue de 83 hombres y 359 mujeres. Seis investigaciones28,26,30,31,32,34) precisaron que los pacientes eran de entre 16 y 80 años. Los países donde se realizaron los estudios fueron: Turquía,26,28,30 Egipto,27 España,(29, 31) Polonia32,34 e India33) (Tabla 1).
El número total de pacientes tratados fue de 462. En todas las investigaciones hubo un grupo control y PRP o PRFC como tratamiento de los DTM. Solamente en el estudio de Nitecka-Buchta y otros34 el lugar de administración del CP fue el músculo masetero, el resto de los autores describieron que fue en la ATM. Excepto Hegab y otros27 y Pihut y otros,32) los artículos mencionaron que la cantidad de sangre extraída por persona osciló de entre 20 y 40 mL. Ocho investigaciones27,28,29,30,31,32,33,34) reportaron que el anticoagulante usado fue el citrato de sodio al 3,2 % o al 3,8 % y el citrato trisódico. Cuatro estudios28,30,31,34) refirieron que el protocolo usado para la obtención del CP fue el de Ehrenfest, Anitua y Andia (2001) y Anitua (1999). Cuatro investigaciones26,32,33,34 realizaron una doble centrifugación y cinco,27,28,29,30,31) una sola. Tres investigaciones26,29,31) refirieron que el activador utilizado fue el cloruro de calcio y el Aid Light. En el 100 % de los cosos la temperatura usada para la obtención del CP fue la de ambiente, el volumen de la inyección del CP osciló de entre 0,4 y 5,0 mLy el número de inyecciones estuvo entre 1 y 4. Dentro de los parámetros clínicos evaluados, todos los autores, excepto Gupta y otros33) reportaron la reducción del dolor cuando aplicaron la escala visual análoga; mientras que otro grupo26,27,28,29,30,31) reportó el aumento de apertura máxima (Tabla 1).
Análisis del riesgo de sesgo de los estudios
Solamente la investigación publicada por Nitecka-Buchta y otros34 mostró un bajo riesgo de sesgo (Fig. 2).
Síntesis de resultados (metaanálisis)
Análisis de la reducción del dolor de los CP en el tratamiento de los DTM
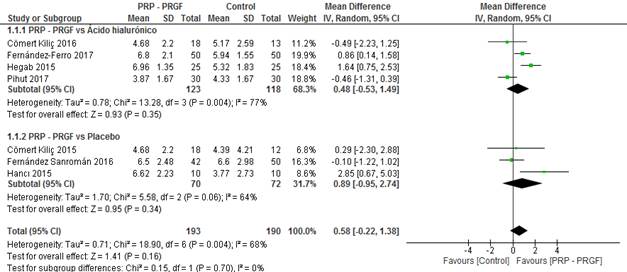
La reducción del dolor analizado para determinar la efectividad de los CP en el tratamiento de los DTM, fue determinado en varios trabajos26,27,28,29,30,31,32 los cuales demostraron que no había una diferencia significativa. Sin embargo, en la gráfica se observó que existe una tendencia al uso de los CP (PRP o PRFC) (Fig. 3).
Análisis de subgrupos
La reducción del dolor entre el PRP o PRFC y el AH fue determinada en 4 estudios27,30,31,32) los que demostraron que no había una diferencia significativa, pero en la gráfica se observó que existe una tendencia al uso de los CP (PRP o PRFC) en el tratamiento de los DTM. La reducción del dolor entre el PRP o PRFC y el placebo fue determinada en 3 investigaciones26,28,29 los que demostraron que no había una diferencia significativa, pero en la gráfica se observó que también existe una tendencia al uso de los CP (PRP o PRFC) en el tratamiento de los DTM.
Análisis del aumento de la apertura máxima de los CP en el tratamiento de los DTM
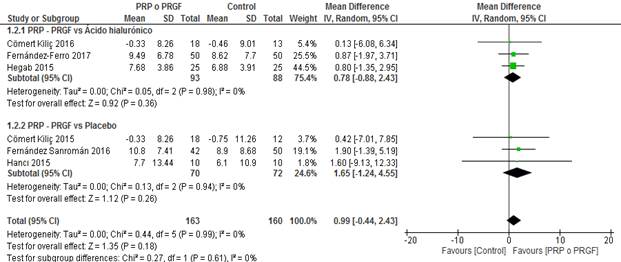
El aumento de la apertura máxima evaluada para determinar la efectividad de los CP en el tratamiento de los DTM fue determinada en 6 estudios,26,27,28,29,30,31) los cuales demostraron que no había una diferencia significativa. En el gráfico se observó que existe una tendencia al uso de los CP (PRP o PRFC) (Fig. 4).
Análisis de subgrupos
El aumento de la apertura máxima entre el PRP o PRFC y el AH fue determinada en tres estudios,27,30,31) los que demostraron que no había una diferencia significativa, pero en el gráfico se observó que existe una tendencia al uso de los CP (PRP o PRFC) en el tratamiento de los DTM.
El aumento de la apertura máxima entre el PRP o PRFC y el placebo fue determinada en tres investigaciones26,28,29) las que demostraron que no había una diferencia significativa, pero en el gráfico se observó que existe una tendencia al uso de los CP (PRP o PRFC) en el tratamiento de los DTM.
Discusión
Los resultados de la presente revisión sistemática demostraron que el uso de los CP provocó una reducción en el dolor y el aumento de la apertura máxima. Estos resultados encontrados pueden deberse posiblemente a que los CP presentan propiedades antiinflamatorias y analgésicas. Su abundancia en factores de crecimiento podría ser útil para mejorar la cicatrización y promover la regeneración del tejido.1,2,7,13,17,18,20,21,22,23
En este estudio fue utilizado un modelo de efectos aleatorios para el metaanálisis debido a la heterogeneidad entre los estudios, la misma que pudo deberse a la diferencia que había, tanto en sus criterios de inclusión y exclusión, como en el protocolo de obtención de los CP.
En la revisión sistemática fue excluido un estudio cuyo CP fue la FRP,7) ya que no cumplía los criterios de selección del presente estudio (no grupo control). A pesar de ello, es interesante observar el inicio de estudios que determinen la efectividad del FRP en el tratamiento de los DTM. Además, para el metaanálisis no fue tomado en cuenta el estudio de Nitecka-Buchta y otros34) debido a que el lugar de administración del CP fue el músculo masetero.
La fortaleza de esta revisión sistemática radica en la selección de los estudios, porque se utilizaron criterios estrictos de inclusión y se realizó una exhaustiva búsqueda en las más importantes bases de datos. Sin embargo, la revisión también presenta limitaciones, que la mayoría de los ECA incorporados exhibían un alto riesgo de sesgo, por ejemplo.
A partir de todo lo mencionado anteriormente, creemos que estos resultados no pueden generalizarse aún, por cuanto los ensayos clínico aleatorizados presentan una alta heterogeneidad y los evaluados en este estudio son de solamente 3 continentes (Europa, África y Asia) con muy pocos países que representaban a estos continentes. Por ende, pudiera provocarse una disyuntiva, ya que cada continente y país tiene su propia cultura, etnia y tipo de alimentación. Tales factores podrían influir en los resultados, sobre todo al tratarse de los CP. Es por ello que se recomienda en este estudio la realización de ECA bien diseñados, que traten sobre este tema en los demás países del resto de los continentes para así poder comparar los resultados y llegar a una conclusión más clara y general.
Conclusiones
En general y en base a los resultados obtenidos, la literatura revisada sugiere que existe una ligera evidencia de los beneficios potenciales de las inyecciones intraarticulares de los concentrados plaquetarios en pacientes con DTM. Sin embargo, es necesario establecer un protocolo estandarizado para la preparación y aplicación de estos concentrados.