Introducción
Los agentes antifibrinolíticos constituyen una de las estrategias farmacológicas para reducir el sangrado quirúrgico y el segundo pilar del manejo de sangre del paciente; aunque no suplen la hemostasia del cirujano. Actualmente se utilizan los antifibrinolíticos sintéticos, análogos de la lisina: el ácido tranexámico (ATX) y el ácido épsilon-aminocaproico (AEAC); cuyo mecanismo de acción se basa en la inhibición competitiva de la unión del plasminógeno, para que este no se convierta en plasmina, a los residuos de lisina.1,2
El control prehospitalario de la hemorragia y la reanimación desempeñan un importante papel en el paciente politraumatizado, teniendo en cuenta que la pérdida de sangre se considera la primera causa de muerte prevenible.1,2,3) La medicina militar ha incorporado el ATX a las guías clínicas del tratamiento del herido (baja) de combate porque el control del flujo sanguíneo resulta vital. Junto con los torniquetes de material hemostático tópico, la administración de hemoderivados y la monitorización de la coagulopatía, el ATX supone una terapia novedosa que aumenta la supervivencia de la baja en la guerra.4
Los resultados de las publicaciones de ortopedia, relativos a la cirugía de artroplastia de cadera, de rodilla o sobre programas “de manejo de sangre de paciente”, indican que la aplicación del ATX disminuye significativamente las pérdidas hemáticas y los pacientes transfundidos.5) El empleo de este fármaco se prefiere en la fractura de huesos largos como el fémur6 y en los traumas de cadera.7,8
Dado el interés en las últimas décadas por la aplicación del ATX, se consideró pertinaz buscar diferentes artículos sobre su aplicación en la cirugía ortopédica y traumatológica, con vista a orientar la dosis más efectiva. Por consiguiente, el objetivo del presente trabajo fue demostrar la importancia del ácido tranexámico en la cirugía electiva y de urgencia en ortopedia y traumatología.
Empleo del ATX en las acciones combativas
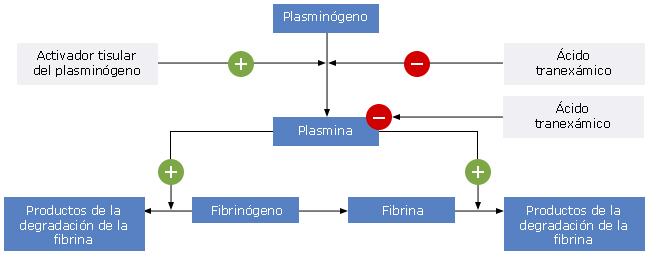
El ácido tranexámico (ATX) constituye un derivado sintético del aminoácido lisina y, en bajas dosis, se une competitivamente a los cinco sitios de la lisina en el plasminógeno. Inhibe la actividad de la plasmina, serina proteasa que diluye la fibrina en los coágulos (fig. 1). También se considera que mejora la función plaquetaria al impedir la activación de los monocitos, neutrófilos y complementos.
 Fuente: Singh y otros7
Fuente: Singh y otros7
Fig. 1 Muestra la acción del ácido tranexámico en la inhibición de la fibrinólisis.
La Administración de Drogas y Alimentos de EE.UU (FDA) aprobó el uso del ATX, vía intravenosa, en pacientes con hemofilia para prevenir hemorragias durante la extracción dental y evitar el reemplazo del factor de coagulación; y, por vía oral, para reducir la menorragia.9 Aunque no se recomienda en el sangrado de origen traumático, el ATX se ha generalizado en las últimas dos décadas, basado en los beneficios que reporta en escenarios no convencionales y el nivel de supervivencia que garantiza.
Controlar el flujo sanguíneo en lesiones de cabeza, cuello, tronco, abdomen y extremidades constituye uno de los problemas más acuciantes en los conflictos militares. Los servicios médicos de las diferentes fuerzas armadas siempre han buscado diversos procederes para contener la hemorragia y evacuar adecuadamente a los lesionados desde los campos de batalla. Belbry,10) en su análisis de las bajas potencialmente recuperables en la guerra de Vietnam, planteó que muchos de los que mueren por heridas en el cráneo y traumatismos severos podrían salvarse con un mejor manejo quirúrgico y anestésico. Se deben desarrollar regímenes de tratamiento mejorados para disminuir las víctimas de sepsis y falla multiorgánica por el sangramiento mal controlado.
En la guerra de Vietnam la mayoría de las muertes ocurrieron antes de la evacuación a las instalaciones sanitarias.10 Por ello, en conflagraciones más recientes, se han aplicado diferentes métodos, desde el mismo campo de batalla, para cortar el flujo sanguíneo.
Eastridge y otros,11 en un estudio entre octubre de 2001 y junio de 2011, analizaron 4596 cadáveres de las acciones militares de Estados Unidos en Afganistán e Irak. El 87,3 % de las muertes se produjo por lesiones antes del tratamiento médico, y el 90,9 % se asoció con hemorragia. Igualmente, Kelly y otros,12 en un análisis de la gravedad de las lesiones en las autopsias a soldados de Irak y Afganistán, demostraron que la primera causa de los decesos resultó la pérdida de sangre, que en el caso de las extremidades, la axila, el cuello o la ingle se controla con torniquetes y agentes hemostáticos tópicos como los vendajes; en cambio, la hemorragia no comprimible o del torso necesita de complementos cauterizantes intravenosos y la reanimación para el control de daños.
Morrison y otros4 realizaron el estudio “Aplicación militar de ácido tranexámico en trauma Estudio de Resucitación de Emergencia” (MATTERs), basado en la experiencia del ensayo “Clinical Randomisation of an Antifibrinolytic in Significant Haemorrhage 2” (CRASH-2).13 De un total de 896 heridos, a 293 se les administró ATX dentro de la primera hora de la lesión; estos lograron mejores resultados en cuanto a la coagulopatía y la supervivencia en comparación con los pacientes que recibieron al menos una unidad de concentrado de glóbulos rojos sin ATX. Se destacó el beneficio de este medicamento para los casos que requieren una transfusión masiva solamente y se recomendó aplicarlo en la práctica clínica como parte de una estrategia de reanimación después de una hemorragia grave.
Johnston y otros14 examinaron 455 bajas militares de la guerra de Afganistán y señalaron que se debían proponer guías de aplicación del ATX porque su uso excesivo, en bajas dosis, había provocado trombosis venosa profunda o pulmonar. Por su parte, Fisher y otros15 evaluaron una aplicación más adecuada a nivel prehospitalario y propusieron usarlo vía endovenosa de forma lenta en 10 minutos, en la primera hora de la lesión; además consideraron incluirlo en el botiquín de auxilio para que el combatiente se aplique una dosis intramuscular dentro de las primeras tres horas herido. Robert y otros16 realizaron una investigación multicéntrica en más de 20 000 pacientes con traumatismos. El ATX versus placebo redujo la mortalidad, especialmente la asociada a exanguinación (4,9 % frente a 5,7 %). El análisis post-hoc exploratorio identificó un efecto dependiente del tiempo: el riesgo de hemorragia disminuyó cuando se administró el ATX durante la primera hora de la lesión (5,3 % frente a 7,7 %); en cambio, después de 60 minutos (4,8 % frente a 6,1 %) tuvo un efecto menor y pasadas tres horas aumentó el riesgo de exanguinación (4,4 % frente a 3,1 %). No informaron diferencias con respecto al tromboembolismo venoso entre los grupos, aunque este trastorno no incidió significativamente.
Chang y otros17 apoyan el empleo del ATX en escenarios complejos como zonas de combate y de difícil acceso. Asimismo, Jamal y otros18 demostraron que la administración intravenosa de este medicamento bajó la mortalidad de un 23,9 a un 17,4 % en el campo de batalla. En concordancia con esto, las pautas de la Atención de Víctimas de Combate Táctico (TCCC) recomiendan aplicar 1 g de ATX, seguido de 1 g en infusión durante 8 horas, dentro de un período de ventana de 180 minutos, en cualquier paciente con hemorragia significativa, o con riesgo de ella, en fracturas pélvicas, lesiones severas de las extremidades o evidencia de sangrado intraabdominal. Sin embargo, señalan que después de tres horas merma la efectividad del ATX y puede causar un daño potencial, ya que la eficacia se relaciona directamente con el tiempo de administración.
Aedo y otros19 evaluaron 745 pacientes durante la guerra de Afganistán, atendidos por lesiones complejas de armas de fuego y explosivos. Todos recibieron ATX antes de las tres primeras horas. La dosis más empleada fue 1 g intravenoso. La hemorragia se controló en el 100 % de los casos y no se lamentaron muertes ni se observaron efectos secundarios. Estos datos coinciden con lo recomendado en las guías de atención a la baja de combate seguidas por las sanidades militares de países como Noruega, Canadá, Israel, entre otros.
Empleo del ATX en traumatología ortopédica
La atención al paciente politraumatizado resulta un problema de salud para el sistema sanitario de cualquier país por los cuidados que requiere; especialmente, los casos que acuden con un evento importante de sangrado. Durante las últimas décadas, con los avances tecnológicos y el control fisiológico del flujo sanguíneo, se ha disminuido la mortalidad, y el paciente se restablece más rápidamente. El ATX se ha investigado y se aplica pese a la controversia entre los diferentes especialistas.
En 2005 comenzó el estudio Clinical Randomization of an Antifi brinolytic in Significant Haemorrhage 2 (CRAHS-2). El ensayo se llevó a cabo en 274 hospitales de 40 países. Se asignaron aleatoriamente 20 211 pacientes adultos con traumatismos y sangrado significativo, o con riesgo de este, dentro de las 8 horas posteriores a la lesión: 10 096 recibieron ATX y 10 115 placebo (dosis de carga de 1 g durante 10 minutos y luego infusión de 1 g durante 8 horas o placebo equivalente). La mortalidad se redujo significativamente, con un riesgo relativo de 0,91, IC del 95 % 0,85-0,97; p = 0,0035; también disminuyeron los decesos por hemorragia, riesgo relativo 0,85, IC 95 % 0,76-0,96; p = 0,0077.
Este estudio demuestra que el ATX atenúa el riesgo de muerte en pacientes con traumatismos hemorrágicos y podría administrarse en una amplia gama de entornos de la atención médica; en consecuencia, debería incluirse en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud (OMS) y estar disponible para los médicos que tratan a pacientes traumatizados en todos los países. El precio de este fármaco oscila entre 55 y 60 dólares el bulbo, que sería otra ventaja a considerar.13 El manejo a los pacientes politraumatizados resulta un problema complejo en los escenarios de urgencia.20 El cuadro clínico de inestabilidad hemodinámica en los casos de sangrado severo puede llevar al fallecimiento en las primeras horas; por tanto, desde su llegada al centro, se aplica el esquema del Soporte Vital Avanzado para Traumatismos (ATLS).
Quintero y otros21 plantean que la hemorragia externa puede contenerse con el empaquetamiento, la compresión, el torniquete para las extremidades y el cinturón pélvico en las fracturas de pelvis; sin embargo, el sangramiento no compresible del torso requiere de manejo quirúrgico o endovascular urgente. Estos autores aplican un protocolo que consiste en 1 g de ATX en bolo y 20 ml de gluconato de calcio al 10 %, junto a cuatro unidades de glóbulos rojos, cuatro unidades de plasma sin pruebas cruzadas y una reserva de aféresis de plaquetas, con el objetivo de lograr una hipotensión permisiva, y cifras de presión arterial sistólica entre 80 y 90 mm Hg. Con ello se contiene la pérdida de sangre y se maneja mejor al paciente; además, se facilitan los estudios para diagnosticar las lesiones y la toma de decisiones quirúrgicas. Salamea y otros22 coinciden con los criterios anteriores a partir de sus experiencias en el manejo de los politraumatizados.
Gausden y otros23 explican la efectividad del ATX en las cirugías de trauma ortopédico, teniendo en cuenta que la administración profiláctica de esta droga reduce la hemorragia, los índices de transfusión y el nivel de la hemoglobina, sin aumentar el riesgo de tromboembolismo venoso, unido a una adecuada hemostasia por parte de los cirujanos. Pfeifer y Pape24 afirman que los objetivos de la Reanimación de Control de Daños en los pacientes politraumatizados se centran en los trastornos fisiológicos (tríada de la muerte) con hemorragia severa. Incluye hipotensión permisiva, recalentamiento del paciente, uso limitado de cristaloides y uso de fármacos hemostáticos como el ATX.
Otros estudios demuestran que el fármaco tiene mayor beneficio en los pacientes con una presión sistólica menor de 75 mmHg, tratados inmediatamente después de sufrir las lesiones; especialmente, cuando lo reciben dentro de la primera hora. En cambio, si se administra después de tres horas aumenta la mortalidad.2
Para Ramírez y otros25 la aplicación del ATX disminuye la mortalidad en casos con traumatismos hemorrágicos cuando se suministra dentro de las tres horas posteriores a la lesión; sin embargo, no se reducen las transfusiones de hemoderivados. Otros autores afirman que 1 g atenúa el sangrado en pacientes quirúrgicos, sin incrementar la dosis; no obstante, en los traumas, cantidades mayores inciden más en el tratamiento. Estos resultados divergentes llevan a la conclusión de que la farmacocinética y la dosificación óptima aún se desconocen. Se necesitan ensayos futuros para comprender los mecanismos de acción de ATX y optimizar su empleo.
En los últimos 20 años varias publicaciones se han referido al empleo del ATX en las fracturas de cadera, tanto en las hemiartroplastia en las fracturas subcapitales como en la osteosíntesis. Ekinci y otros26 evaluaron 102 pacientes con fracturas intertrocantéricas de cadera. La mitad se consideró el grupo control y al resto se le aplicó una sola dosis de 15 mg/kg endovenoso preoperatorio. Se determinaron los siguientes hallazgos: la merma de flujo sanguíneo intraoperatorio no tuvo diferencias; la pérdida de sangre oculta bajó significativamente en el grupo ATX; al igual que la tasa de transfusión posoperatoria y la unidad de transfusión; y las complicaciones médicas se asemejaron en ambos grupos. Se concluyó que el ATX restringe las transfusiones de sangre en la osteosíntesis intramedular proximal y no aumenta el riesgo de trombosis venosa pulmonar o eventos tromboembólicos.
Ashkenazi y otros27 analizaron las fichas electrónicas de 1722 pacientes sometidos a hemiartroplastia de cadera, de ellos 504 utilizaron ATX intraoperatorio y redujeron la mortalidad a los 30 días, así como el sangrado y las transfusiones alogénicas, sin aumentar la readmisión posoperatoria. Por su parte, Qi y otros28 examinaron la aplicación del ATX endovenoso y señalaron su capacidad de reducir los requisitos de transfusión de sangre alogénica de forma segura, sin aumentar la incidencia de eventos tromboembólicos en cirugías de cadera.
Ma y otros29 efectuaron un estudio prospectivo, aleatorizado y controlado de fractura intertrocantérea, para evaluar la pérdida de sangre oculta postraumática. Con la aplicación de ATX intravenoso 15 minutos antes de la operación, disminuyó significativamente la tasa de transfusión preoperatoria. Asimismo, Huynh y otros30 evaluaron 505 pacientes tratados quirúrgicamente por fracturas de cadera. De manera no aleatorizada, 307 recibieron ATX y en promedio perdieron 235 ml de sangre menos que el resto. No aumentaron los eventos de tromboembolismo venoso en ninguno de los grupos durante la hospitalización.
Powell y otros31 realizaron osteosíntesis intramedular en fracturas femorales por fragilidad en 360 casos y emplearon en 178 el ATX, estos últimos requirieron menos transfusiones de sangre y las tasas de complicaciones resultaron semejantes. Por su parte, Gaspar y Lassam6 seleccionaron cinco ensayos controlados aleatorios, con un total de 295 participantes, y concluyeron que el uso de ATX durante cirugías de fracturas de huesos largos reduce la hemorragia y evita la transfusión. Asimismo, Shu y otros32 determinaron que este medicamento se asocia con tasas más bajas de transfusión de sangre en la intervención quirúrgica de fractura pélvica o acetabular.
Peyman y otros33 explicaron los posibles efectos terapéuticos ATX y su seguridad en los procederes de pie y tobillo. Los resultados demostraron que reduce el sangramiento de manera efectiva, tanto en la fractura como en la cirugía electiva. Las dosis empleadas fueron de 15 mg/kg, por vía tópica y endovenosa.
Grassin y otros34 aplicaron 1 g, vía endovenosa, en las primeras tres horas de sangrado de origen traumático y, posteriormente, dos dosis intramuscular de 0,5 g. Midieron las concentraciones de ATX mediante cromatografía líquida acoplada a espectrometría de masas, y entre 4 u 11 minutos se produjo la concentración terapéutica (5 o 10 mg) después de una inyección intramuscular de 1 g de ATX, o sea, en pacientes con traumatismos hemorrágicos, el ATX intramuscular se tolera bien y se absorbe rápidamente.
Empleo del ATX en la cirugía electiva en ortopedia
Zhang y otros35 evaluaron el efecto combinado del ATX con torniquete en la artroplastia total de rodilla primaria. Incluyeron ensayos controlados aleatorios de nueve métodos de tratamiento: placebo, ATX intravenoso, ATX tópico, ATX tópico combinado intravenoso, ATX oral, placebo + torniquete, ATX intravenoso + torniquete, ATX tópico + torniquete y ATX intravenoso - tópico combinado + torniquete. Los pacientes se dividieron en ocho grupos según las estrategias de tratamiento. Se compararon las diferencias en el volumen de sangre, el número de pacientes transfundidos, la hemoglobina antes y después de la operación, y las complicaciones. Los grupos de ATX tópico combinado por vía intravenosa y ATX tópico combinado por vía intravenosa + torniquete atenuaron la hemorragia y el riesgo de transfusión. El ATX tópico combinado intravenoso resultó más eficaz.
Gómez y otros,36 en un estudio prospectivo, controlado y aleatorizado en 2 brazos, aplicaron 15 mg/kg intravenoso en el grupo A y 2 g intraarticular en el B. En el primer grupo se perdió una media de 1505 ml de sangre frente a 1280 ml en el otro grupo. Se necesitaron 5,1 % de transfusiones; pero no hubo complicaciones secundarias. Las vías de administración del ATX en la artroplastia total de cadera demostraron un efecto similar en la reducción del sangrado posoperatorio, sin incrementar las complicaciones. También Ma y otros37 indicaron que el ATX reduce la hemorragia; disminuye la hemoglobina, la producción de drenaje y las complicaciones de la herida, sin aumentar los eventos tromboembólicos en la osteotomía tibial alta. Pero no hay evidencias de que pueda reducir las tasas de transfusión.
Grzelecki y otros38 evaluaron 145 pacientes sometidos a artroplastias de cadera de revisión. Con dos dosis de 1 g de ATX intravenoso, se minimizaron la pérdida de sangre perioperatoria y las transfusiones. No se observaron casos de tromboembolismo venoso o pulmonar, gracias también al uso estándar de heparina de bajo peso molecular. A pesar de los beneficios registrados, Sukeik y otros39 apuntan que este fármaco tiene efectos secundarios, sin diferencias significativas en la trombosis venosa profunda, las embolias pulmonares u otras complicaciones.
Suhail y otros40 compararon los efectos de la administración intraarticular e intravenosa de ATX en la artroplastia total de rodilla primaria. El grupo A recibió 2 g en la articulación después de cementada la prótesis y el B una dosis intravenosa de 1 g, 5-10 minutos antes de que se inflara el torniquete neumático. La administración intraarticular de ATX se consideró tan efectiva y segura como la intravenosa, para reducir el sangrado.
Wu y otros41 analizaron casos de artroplastia total de cadera y artroplastia total de rodilla primarias unilaterales. En el curso de tres días de dosis múltiples de ATX se constató su efectividad para moderar las caídas de hemoglobina posoperatorias, la pérdida de sangre total estimada, y las respuestas inflamatorias y fibrinolíticas; sin embargo, estos hallazgos deben confirmarse por estudios prospectivos.
Zhang y otros42 investigaron si la administración intravenosa cambiaba la coagulación después de la artroplastia total de cadera primaria, mediante el análisis de trombomastografía y las pruebas de laboratorio convencionales. El ATX intravenoso redujo significativamente la hemorragia, las transfusiones y las complicaciones tromboembólicas. Además, se confirmó, a través del análisis de trombomastografía, que no modifica la coagulación. Tavares y otros43 evaluaron 124 pacientes con artroplastia total de cadera. La mitad utilizó 1,5 g de ATX, de forma tópica, diluido en 45 ml de suero fisiológico, durante la cirugía de reemplazo articular de cadera con prótesis total no cementada. Se restringieron el sangrado y los requerimientos de transfusión, sin aumento de complicaciones en el grupo de ATX.
Otro grupo de autores hizo un estudio prospectivo de 285 artroplastias primarias de cadera divididas en 4 grupos. El grupo A recibió 2,5 g de ATX tópico, el B no usó ATX, el C utilizó 1 g intravenoso y el D tuvo la administración combinada. La reducción de la hemoglobina a las 48 horas fue mayor en el grupo B con una estancia hospitalaria más larga. Un paciente del grupo A presentó tromboembolismo pulmonar a las 72 h de la cirugía y resolvió sin complicaciones. En sus conclusiones señalan que el ATX por vía tópica, intravenosa o combinada proporciona el mismo efecto en el flujo sanguíneo y la hemoglobina, tras la artroplastia total primaria de cadera, que la no administración.44
Godoy y otros45 implementaron un protocolo en las artroplastias de cadera y rodilla que disminuyó la cantidad de transfusiones, la caída de hemoglobina y la estadía hospitalaria, sin aumentar el número de complicaciones. Se administró el ATX en el perioperatorio: 1g endovenoso 15 minutos antes de la cirugía y la misma dosis tres horas después de la intervención. Hui y otros,46 sobre el uso tópico del ATX en la cirugía espinal, coinciden con el resultado anterior. Afirman que este fármaco reduce significativamente el drenaje posoperatorio, la pérdida de sangre oculta y la estancia hospitalaria.
Los estudios sobre el empleo del ATX en Cuba resultan escasos. Solo se encontraron tres artículos de autores cubanos en la Revista Cubana de Cirugía: una revisión bibliográfica47 y dos sobre el sangrado digestivo alto.48,49 Se considera que este medicamento aporta más beneficios que complicaciones. Todas las formas de aplicación resultan efectivas, pero la combinada detiene mejor el sangrado. En cuanto a la dosis de aplicación en pacientes con hemorragias de origen traumático, se requieren más estudios.














