INTRODUCCIÓN
Las plantas muestran varias reacciones defensivas cuando perciben patrones moleculares asociados a microorganismos (MAMP) que pueden ser reconocidas por receptores de la membrana plasmática 1-3. Las leguminosas son capaces de detectar los MAMP y así reconocer y discriminar entre rizobios y patógenos para desencadenar el proceso de simbiosis o la respuesta de defensa, respectivamente. Los factores de nodulación (Nod) producidos por los diferentes rizobios son los encargados de iniciar el proceso de formación del nódulo en las raíces y, en su estructura básica, poseen oligosacáridos de quitina que son reconocidos inductores de respuestas defensivas en plantas 3, mientras que otros compuestos específicos derivados de los rizobios modulan la inducción defensiva en las plantas hospederas y benefician la infección simbiótica 4-6.
La quitina, un polisacárido presente en la pared celular de los hongos y sus derivados (quitosanos y quitooligosacáridos parcialmente N-acetilados) son liberados mediante la degradación de la pared celular fúngica por enzimas β 1-3 glucanasas y quitinasas. Estas enzimas se secretan por la planta como respuesta al ataque del patógeno en el proceso de patogénesis 7,8.Los quitosanos han sido implicados en la inducción de una gran variedad de respuestas vinculadas a la defensa en varios sistemas de plantas, como son la expresión de genes defensivos, la inducción de fitoalexinas y proteínas de resistencia, la lignificación de las paredes celulares, entre otros 9,10. Esta respuesta inducida en plantas depende de numerosos factores, tales como la especie vegetal, el microorganismo patógeno, las características físico-químicas del quitosano y la forma en que se aplican 11.
Estudios previos en soya cv INCAsoy-27 demostraron el efecto negativo de altas concentraciones de polímeros y oligosacáridos de quitosano adicionados al medio de cultivo vegetal en la respuesta de variables de nodulación y de crecimiento in vitro de las plántulas inoculadas con Bradyrhizobium elkanii12. El efecto negativo encontrado en la nodulación de soya con el polímero de quitosano, pudiera relacionarse con la acción inhibitoria a las concentraciones de 500 y 1000 mg L-1 en la viabilidad del simbionte. Esta afectación podría, además, estar relacionada con la estimulación de respuestas defensivas en la plántula por el quitosano, lo cual afectaría directamente la entrada del microsimbionte a las raíces y comprometería el balance energético requerido para otras funciones de crecimiento en la planta.
Por lo anterior, la hipótesis de este trabajo fue conocer si la presencia de un polímero de quitosano en el medio de cultivo de crecimiento de soya inoculada con Bradyrhizobium causa la inducción de indicadores defensivos (actividad β 1-3 glucanasa, quitinasa y fenilalanina amoniaco-liasa, PAL) en las hojas y raíces de las plántulas.
MATERIALES Y MÉTODOS
Compuesto de quitosano
Un polímero de quitosano con masa molecular de 130,000 g mol-1 y 12 % de desacetilación se obtuvo de quitina del exoesqueleto de langosta (Panulinus argus) por desacetilación básica (NaOH), que se caracterizó según lo descrito por Costales et al. 12. Se tomaron alícuotas de una solución patrón de quitosano disuelta en ácido acético (1 %), que se adicionaron al medio de cultivo vegetal Norris & Date 13, hasta una concentración final de 0, 10, 50, 100, 500 y 1000 mg L-1.
Bioensayo de crecimiento de las plántulas de soya
Las semillas de soya del cultivar INCAsoy-27 se desinfectaron previamente con etanol (70 %) e hipoclorito de sodio (0,25 %, v/v) durante cinco minutos y se enjuagaron seis veces con agua destilada estéril antes de colocarlas en placas Petri que contenían medio de agar- agua (0,75 %) para su germinación a 30 °C durante tres días en la oscuridad. Luego, las semillas pregerminadas (15-20 mm de raíz emergente) se colocaron en tubos de ensayo que contenían 40 mL de medio semisólido 13 y las diferentes concentraciones del polímero, a razón de una semilla por tubo. Las raíces de las plántulas se inocularon siete días después, descargando con micropipeta 1 mL de inóculo obtenido con la cepa ICA 8001 de B. elkanii (109 UFC mL-1), en medio líquido de extracto de levadura-manitol (YEM). Las plántulas se cultivaron en una cámara de crecimiento en condiciones controladas de luz/oscuridad de 16/8 horas, a 25 °C y 70 % de humedad relativa, con luz artificial de 1 x 104 moles m-2 s-1 durante 35 días. Durante este tiempo, a todos los tubos de ensayo se les añadió semanalmente, el medio líquido Norris & Date estéril, para garantizar el buen desarrollo de las plántulas. Se seleccionaron seis plántulas por tratamiento para la conformación de tres muestras homogéneas de hojas y raíces frescas, para la cuantificación de las proteínas solubles totales y las determinaciones de las actividades enzimáticas, a los 7 y 21 días después de la inoculación con la bacteria (ddi). En las raíces, se eliminaron los nódulos, se lavaron con agua destilada y se escurrieron sobre papel de filtro antes de su conservación en nitrógeno líquido, hasta el momento de las extracciones vegetales.
Extracción de proteínas en hojas y raíces de soya
Para las extracciones de proteínas totales se pesó un gramo de las muestras de ambos órganos, que se maceraron con nitrógeno líquido en mortero de porcelana y se homogenizaron en solución de acetato de sodio (0,05 mol L-1, pH 5,2) + cloruro de sodio (1 mol L-1) + EDTA (0,005 mol L-1) + Mercapto-etanol (0,005 mol L-1), a razón de 1,5 mL g-1 por muestra. El extracto se centrifugó a 12 000 g durante 15 minutos a 5 °C en una centrífuga refrigerada, se descartó su precipitado y se centrifugó nuevamente durante cinco minutos. El sobrenadante se colectó y se congeló por debajo de 0 °C hasta realizar las determinaciones enzimáticas. La cuantificación de proteínas se realizó en el sobrenadante, siguiendo la metodología de Micro Lowry descrita por Falcón et al. 14. La absorbancia se leyó a 750 nm y se utilizó 0,5 mg mL-1 de albúmina de suero bovino (BSA) como estándar de la curva de calibración con un rango de concentraciones desde 5 hasta 100 µg. El contenido de proteína se expresó como mg de proteína g-1 de hojas y raíces frescas.
Determinación de actividades enzimáticas
La actividad enzimática β 1-3 glucanasa (EC 3.2.1.6) se determinó mediante la metodología descrita por Falcón et al. 14. Los componentes del ensayo se ajustaron proporcionalmente para obtener un volumen final de 0,5 mL. Se cuantificaron los azúcares reductores liberados de la laminarina (Sigma, 5 mg L-1) por acción de las enzimas del extracto (0,025 mL). La mezcla de reacción se incubó durante una hora a 50 °C. Los azúcares reductores totales liberados en el ensayo se determinaron mediante el método colorimétrico Somogyi 15 y sus resultados se expresaron como actividad específica (mg de glucosamina-1 min-1 por mg de proteína-1), con base en la ecuación de la recta de la curva de azúcares reductores para un patrón de glucosa, a 520 nm.
La actividad quitinasa (EC 3.2.1.15) se estimó a través de los azúcares reductores liberados por la quitina coloidal. El ensayo estándar (0,5 mL) contenía extracto enzimático (0,03 mL), 0,25 mL de quitina coloidal en tampón de acetato de sodio 50 mM (pH 5,2) y 0,21 mL del mismo tampón. Después de incubar durante cuatro horas a 37 °C bajo agitación lineal continua (250 rpm), se añadió hidróxido de potasio (0,01 mL, 5N) a la mezcla para detener la reacción. La solución de prueba se centrifugó durante cinco minutos (12 000 g) para precipitar el sustrato sin reaccionar y determinar el contenido de azúcares reductores en el sobrenadante 14. El cálculo de la quitinasa (mg N-acetil glucosamina min-1 por mg proteína-1) se realizó a partir de la ecuación de la recta de la curva de azúcares reductores para un patrón de N-acetil glucosamina a 520 nm.
La actividad fenilalanina amonio-liasa (PAL, EC 4.3.1.5) se determinó de acuerdo con la metodología descrita por Falcón et al.14. El ensayo se incubó durante dos horas. El ácido trans-cinámico formado por la acción de las enzimas PAL presentes en el extracto (0,1 mL) se cuantificó usando L-fenilalanina (Sigma, 0,1 mol L-1, pH=8,8) como sustrato. Esta enzima se expresó como actividad específica (mg de ácido trans-cinámico min-1 por mg de proteína-1), después de determinar previamente la ecuación de la recta de la curva del ácido trans-cinámico a 290 nm.
Análisis estadístico
En el experimento se utilizó un Diseño Completamente Aleatorizado con 9 repeticiones por tratamiento para los indicadores: proteínas solubles y enzimas defensivas de los órganos de la planta (hojas y raíces). Los datos obtenidos de cada indicador se les realizó un análisis de ANOVA de Clasificación Simple. Las medias resultantes se compararon mediante la Prueba Tukey HSD para p<0,05 en el programa Statgraphics, versión 5.1 (Statistical Graphics Corporation, 2001). Las correlaciones de Pearson se realizaron en los dos momentos evaluados (7 y 21 ddi) y entre órganos (hojas y raíces) de soya, utilizando las medias resultantes por tratamiento en todas las variables.
RESULTADOS
En la Figura 1, aparece el contenido de proteínas en hojas y raíces durante el crecimiento in vitro de plantas de soya tratadas con quitosano e inoculadas con Bradyrhizobium.
 Proteínas solubles totales en hojas (7 ddi (ESx = 0,40*), 21 ddi (ESx = 0,44*) y raíces (7 ddi (ESx = 0,40*), 21 ddi (ESx = 0,50*) de plantas de soya inoculada. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSD
Proteínas solubles totales en hojas (7 ddi (ESx = 0,40*), 21 ddi (ESx = 0,44*) y raíces (7 ddi (ESx = 0,40*), 21 ddi (ESx = 0,50*) de plantas de soya inoculada. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSDFigura 1 Efecto de un polímero de quitosano adicionado al medio de cultivo vegetal en el contenido de proteínas solubles totales
El contenido de proteínas solubles totales en las hojas fue menor a los 7 ddi en comparación con los 21 ddi, excepto la concentración más alta de polímero (1000 mg L-1), que excedió notablemente al resto de las concentraciones en esta variable, a los 7 ddi (Figura 1A). Además, las concentraciones de 50 y 500 mg L-1, con diferencias entre ellas, acumularon mayor contenido de proteínas totales con valores superiores a las plantas inoculadas (0 mg L-1).
Se observó un comportamiento similar a los 21 ddi, ya que los valores más altos se registraron con concentraciones de 50 y 1000 mg L-1. En ambos momentos evaluados, la concentración 10 mg L-1 del polímero disminuyó el contenido de proteínas totales (Figura 1A). Sin embargo, el contenido de proteínas solubles en las raíces mostró una respuesta diferente (Figura 1B). Los niveles disminuyeron significativamente en cada tratamiento a los 21 ddi, excepto la concentración más baja de polímero (10 mg L-1), respecto al tratamiento control. En contraste con la respuesta de proteínas en hojas a los 7 ddi, la concentración de 10 mg L-1 mejoró la síntesis de proteínas en las raíces, sin diferencias con la concentración más alta de quitosano evaluada y seguida por 500 mg L-1. Las concentraciones restantes no difirieron del tratamiento control (Figura 1B).
Concerniente a las hojas, las concentraciones de 50 a 1000 mg L-1 del polímero redujeron los niveles de actividad de β 1-3 glucanasa hasta alcanzar cinco veces menos el valor de control, a los siete días. La respuesta de esta enzima fue variable a los 21 ddi. Las concentraciones 10 y 100 mg L-1 de quitosano incrementaron la actividad enzimática por encima del control, mientras que esta fue reducida por las concentraciones 500 y 1000 mg L-1 (Figura 2A).
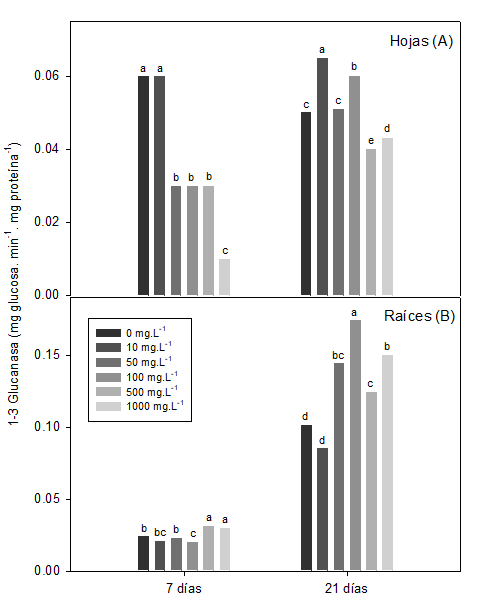 β 1-3 glucanasa en hojas (7 ddi (ESx = 0,006*), 21 ddi (ESx = 0,006*) y raíces (7 ddi (ESx = 0,007*), 21 ddi (ESx =0,012*) de plantas de soya inoculadas. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSD
β 1-3 glucanasa en hojas (7 ddi (ESx = 0,006*), 21 ddi (ESx = 0,006*) y raíces (7 ddi (ESx = 0,007*), 21 ddi (ESx =0,012*) de plantas de soya inoculadas. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSDFigura 2 Efecto de un polímero de quitosano adicionado al medio de cultivo vegetal en la actividad enzimática β 1-3 glucanasa
Sin embargo, en las raíces, la actividad β 1-3 glucanasa aumentó a los 7 ddi con las concentraciones altas (500 y 1000 mg L-1) a diferencia de 100 mg L-1 del polímero (Figura 2B). Por otro parte, a los 21 ddi, concentraciones mayores de 50 mg L-1, principalmente 100 mg L-1, aumentaron esta actividad (Figura 2B).
La concentración inferior (10 mg L-1) de quitosano redujo la β 1-3 glucanasa en raíces, pero sin diferencias con el control (Figura 2B). Curiosamente, los valores absolutos de la actividad enzimática fueron casi cinco veces mayores a los 21 ddi que a los siete días después de efectuada la inoculación de las plantas.
A los 7 ddi, la actividad quitinasa en hojas disminuyó al aumentar la concentración de quitosano por encima de 100 mg L-1, mientras que a los 21 ddi las plantas, los niveles de la actividad de la enzima se redujeron con 1000 mg L-1. El resto de las otras concentraciones no difirieron del control en ambos momentos evaluados (Figura 3A).
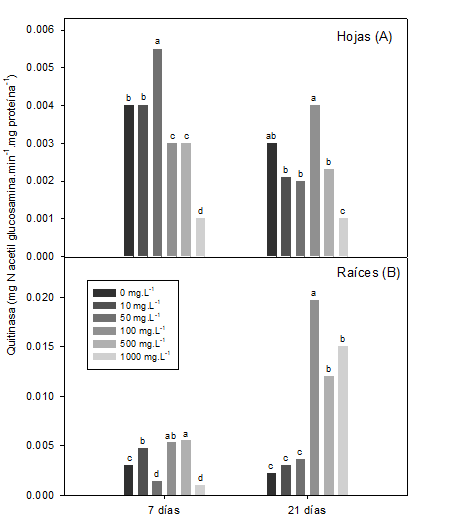 Quitinasa en hojas (7 ddi (ESx = 0,0002*), 21 ddi (ESx = 0,0002*) y raíces (7 ddi (ESx = 0,0002*), 21 ddi (ESx = 0,0007*) de plantas de soya inoculada. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSD
Quitinasa en hojas (7 ddi (ESx = 0,0002*), 21 ddi (ESx = 0,0002*) y raíces (7 ddi (ESx = 0,0002*), 21 ddi (ESx = 0,0007*) de plantas de soya inoculada. Medias con letras comunes no difieren estadísticamente para p <0,05, según la Prueba de Rango Múltiple Tukey HSDFigura 3 Efecto de un polímero de quitosano adicionado al medio de cultivo vegetal en la actividad enzimática quitinasa
En contraste, la mayor actividad de quitinasa en raíces de soya, a los 7 ddi, se observó con la concentración 500 mg L-1 del polímero, seguido de 100 y 10 mg L-1 (Figura 3B).
Las concentraciones 50 y 1000 mg L-1 de quitosano redujeron la enzima con relación al control. Sin embargo, a los 21 ddi, las plantas tratadas con la concentración de 100 mg L-1 de quitosano aumentó significativamente la actividad de quitinasa, seguida de las concentraciones más altas (500 y 1000 mg L-1), que aumentaron la actividad enzimática de cuatro a seis veces más, que las restantes concentraciones y las plantas controles (Figura 3B).
Los niveles de fenilalanina amonio-liasa (PAL) en hojas de soya fueron más altos en el primer tiempo de muestreo evaluado, que en el segundo (Figura 4A). Las concentraciones 10 y 50 mg L-1 del polímero incrementaron la enzima PAL a los 7 y 21 ddi, respectivamente.
En hojas, el quitosano aumentó la actividad PAL hasta un 75 % con la concentración de 10 mg L-1 a los 7 ddi, respecto al control inoculado. Por otro lado, las concentraciones más altas del polímero redujeron estos niveles enzimáticos en las hojas a los 7 ddi, mientras que a los 21 ddi este efecto solo se observó en plantas tratadas con 1000 mg L-1 de quitosano (Figura 4A).
La actividad PAL en raíces fue similar a la respuesta encontrada a los 21 ddi con la actividad β 1-3 glucanasa (Figura 4B).
La concentración 50 mg L-1 causó los mayores niveles de actividad PAL, seguida de las concentraciones más altas a los 7 ddi, mientras que 10 mg L-1 y el control mostraron los niveles más bajos de actividad. Sin embargo, a los 21 ddi, las concentraciones 100 y 1000 mg L-1 de quitosano incrementaron la actividad de esta enzima (Figura 4B).
 Fenilalanina amonio-liasa (PAL) en hojas (7 ddi (ESx = 0,006 *), 21 ddi (ESx = 0,003 *) y raíces (7 ddi (ESx = 0,0006 *), 21 ddi (ESx = 0,003 *) de plantas de soja inoculada Las medias con letras comunes no difieren estadísticamente para p <0,05, de acuerdo con la prueba de rango múltiple Tukey HSD
Fenilalanina amonio-liasa (PAL) en hojas (7 ddi (ESx = 0,006 *), 21 ddi (ESx = 0,003 *) y raíces (7 ddi (ESx = 0,0006 *), 21 ddi (ESx = 0,003 *) de plantas de soja inoculada Las medias con letras comunes no difieren estadísticamente para p <0,05, de acuerdo con la prueba de rango múltiple Tukey HSDFigura 4 Efecto de un polímero de quitosano adicionado al medio de cultivo vegetal en la actividad de fenilalanina amonio-liasa (PAL)
Las determinaciones de los coeficientes de correlación de las proteínas solubles totales y las tres actividades enzimáticas, entre ambos órganos de la planta, mostraron correlaciones positivas y negativas, tanto a los siete días como los veintiún días de efectuada la inoculación en soya, en presencia de quitosano (Tabla 1).
Tabla 1 Determinación de los coeficientes de correlación de Pearson del contenido de proteínas y las actividades enzimáticas en órganos de soya
| Variables comparadas variables | Coeficientes de correlación de Pearson | ||||
|---|---|---|---|---|---|
| Días | Raíces | Hojas | |||
| Proteínas | β 1-3 Glucanasa | PAL | Quitinasa | ||
| 7 | Proteínas | -0,603* | ---- | ---- | ---- |
| β 1-3 Glucanasa | ---- | 0,412 | ---- | ---- | |
| Quitinasa | ---- | ---- | -0,021 | ||
| PAL | ---- | ---- | 0,769* | ---- | |
| 21 | Proteínas | 0,958* | ---- | ---- | ---- |
| β 1-3 Glucanasa | ---- | -0,87* | ---- | ---- | |
| Quitinasa | ---- | ---- | ---- | -0,581 | |
| PAL | ---- | ---- | 0,673* | ---- | |
(β 1-3 Glucanasa, PAL y quitinasa) en hojas y raíces de plantas de soya, a los 7 y 21 días después de la inoculación con B. elkanii
* Nivel de significación del coeficiente de determinación de la correlación de Pearson para p< 0,05
La aplicación de quitosano en el medio de cultivo vegetal aumentó los niveles de las proteínas totales tanto en raíces como en hojas (Tabla 1). Se encontró una correlación positiva y de mayor significación (R2= 92) en los niveles de concentración del indicador en ambos órganos a los 21 ddi, que a los 7 ddi. Similar comportamiento se encontró en la actividad enzimática PAL, donde ambos órganos correlacionaron de forma positiva y significativa a los 7 ddi (R2= 76) y 21 ddi (R2= 59) (Tabla 1). Sin embargo, la actividad β 1-3 glucanasa correlacionó inversamente y significativamente (R2= 76) entre ambos órganos, por lo que los aumentos de actividad de esta enzima en las hojas se corresponden con reducciones significativas de actividad en las raíces a los 21 ddi, mientras que no fue significativa la correlación a los 7 ddi. A su vez, la actividad quitinasa aumentó en raíces, pero se redujo en hojas, por lo que la correlación entre órganos fue negativa y de baja significación en los dos momentos de crecimiento de las plantas evaluados (Tabla 1)..
DISCUSIÓN
Las actividades β1-3 glucanasa, quitinasa y fenilalanina amonio-liasa (PAL) son consideradas indicadores de resistencia basal contra fitopatógenos 16. Asimismo, estas enzimas han sido evaluadas previamente en plantas tratadas con quitosano 17,18. Es conocido que el quitosano y sus derivados son potentes inductores de respuestas defensivas y de resistencia contra patógenos y, aumentan la síntesis de metabolitos secundarios en las plantas 8,17. Este trabajo demostró que el quitosano moduló los niveles enzimáticos de las respuestas defensivas en hojas y raíces de soya inoculada con B. elkanii, en dependencia del órgano de la planta y del momento evaluado. Además, estos aumentos están en el rango de los niveles informados en plantas tratadas con quitosano 18.
En general, en ambos momentos en que se evaluaron los indicadores defensivos, las tres concentraciones mayores causaron disminuciones y aumentos significativos de los niveles enzimáticos en las hojas y raíces, respectivamente, comparadas con el control (Figuras 2, 3 y 4). En consecuencia, los aumentos enzimáticos encontrados constatan una inducción defensiva estimulada por el polímero de quitosano en las raíces de soya, lo que podría permitir elevar el estado de resistencia en la planta contra posibles infecciones por patógenos.
Entre las proteínas PR, las enzimas quitinasas y β 1-3 glucanasas han sido las más estudiadas e informadas en respuesta a patógenos y elicitores bióticos 16,17. Los resultados de este trabajo demostraron aumentos de actividad de ambas enzimas con 10 mg L-1 de quitosano en las hojas, de manera diferente en las raíces, donde se destacaron las concentraciones entre 100 y 1000 mg L-1, en ambos momentos. A los 21 días, en el caso de la β 1-3 glucanasa, se lograron aumentos de hasta dos veces, mientras que, en el caso de la quitinasa, entre tres y cuatro veces en las raíces, con respecto a las plantas controles (Figuras 2 y 3).
De manera similar, las mismas concentraciones que indujeron los mayores incrementos de las enzimas en este trabajo, se han informado como inductoras de actividad quitinasa en hojas de soya mediante imbibición de semillas previo a la siembra 19. Otros resultados en este cultivo demostraron aumentos de la actividad quitinasa, en dependencia de la concentración de quitosano utilizada 20.
Otros autores demostraron mayor acumulación de actividad quitinasa en raíces cultivadas en soluciones que contenían oligómero de quitosano o factores Nod; sin afectar la nodulación de plantas de soya 21. Lo anterior sugiere que la estimulación de esta actividad enzimática puede deberse tanto a una respuesta defensiva como a la asociación simbiótica de rizobios con la planta hospedero. Sin embargo, en varias especies de leguminosas se ha informado, que las enzimas quitinasas hidrolizan los factores Nod excretados por las bacterias y, por tanto, reducen el reconocimiento de estas señales por la planta 22,23. Esto puede ser respaldado por la disminución en el número y la masa seca de los nódulos observada en plantas de soya cultivadas in vitro tratadas con concentraciones elevadas de quitosano incluido en el medio de cultivo 12. Lo anterior concuerda con el incremento en la actividad β 1-3 glucanasa y quitinasa observado en el presente estudio en plantas tratadas con las concentraciones más altas del polímero.
La actividad de PAL en las hojas aumentó en concentraciones de 10 y 50 mg L-1 del polímero a los 21 ddi, mientras que, con las concentraciones intermedias a altas, disminuyeron los niveles enzimáticos en ambos momentos del crecimiento de la soya (Figura 4A). Sin embargo, en las raíces a los 7 ddi, se indujo actividad PAL con las concentraciones más altas, principalmente 50 mg L-1, que duplicó el valor de control (Figura 3B). Se informaron respuestas similares en la inducción de esta actividad por quitosano en raíces de plantas de tabaco (Nicotiana tabacum L) y de pino (Pinus koraiensis) con esta concentración 19,24, además de encontrarse incrementos de esta actividad enzimática en soya y otras leguminosas cuando se aplican otras formas del inductor 18,25-27.
Algunos compuestos formados en la vía de los Fenilpropanoides, como por ejemplo flavonoides e isoflavonoides, están involucrados en el proceso de reconocimiento simbiótico entre rizobios y plantas hospederas 28,29. Es bien conocido que el quitosano activa la formación de compuestos secundarios por la vía de los fenilpropanoides, reforzando la resistencia en las plantas ante estreses bióticos 18,30, pero también pudiendo contribuir positivamente en el proceso simbiótico mencionado 31. El aumento de la actividad PAL encontrado en las raíces de soya en este estudio podría contribuir en ambos procesos. Por ejemplo, se ha informado del aumento de flavonoides en soya como resultado de la aplicación previa de quitosano 8,22 o de factores Nod a las plantas 28,32.
Sin embargo, se ha informado que la inducción de respuestas defensivas en plantas contra patógenos inhibe el proceso simbiótico en las leguminosas 33. Las actividades enzimáticas en este trabajo fueron determinadas en dos momentos importantes del proceso simbiótico de la soya: a los 7 ddi, cuando la planta está en plena formación de nódulos, luego de la colonización de los pelos radicales por la bacteria y su conversión a bacteroide y a los 21 ddi, cuando los nódulos están formados y los bacteroides dentro de ellos en forma activa, ejerciendo una intensa actividad de fijación del nitrógeno. Además, se ha demostrado que las leguminosas autorregulan la magnitud de la simbiosis mediante la inducción de respuestas defensivas 4 que limitan la entrada del microsimbionte y causan, entonces, la formación de nódulos menos desarrollados o disfuncionales 33. En este sentido, el quitosano podría inducir mecanismos defensivos en la planta que afectarían directamente la entrada del microsimbionte a las raíces de la planta.
Los resultados del trabajo también demostraron una relación de activación de las variables evaluadas en los dos órganos, dependiente del momento evaluado. A los 7 ddi correlacionaron negativamente las proteínas y positivamente la actividad PAL, mientras que a los 21 ddi las cuatro variables correlacionaron entre raíces y hojas (Tabla 1).
La concentración de proteínas aumentó en ambos órganos con la aplicación de quitosano a 1000 mg L-1 y en las raíces a los 21 ddi cuando solamente se inocularon las plántulas. Ambos comportamientos coinciden con resultados previos informados en plantas de caupí 34,35.
A los 21 ddi, las concentraciones mayores de quitosano elevaron las actividades β 1-3 glucanasas y quitinasas en raíces, en la medida que se redujeron en las hojas. Aunque este comportamiento puede estar vinculado a un balance energético en la propia planta, son necesarias investigaciones adicionales para dilucidar el significado biológico de los comportamientos observados. Por tanto, es necesario evaluar el efecto inductor del quitosano en la regulación de otras respuestas defensivas que pudieran estar implicadas en mejorar o impedir el proceso simbiótico de la soya con Bradyrhizobium, en bioensayos ex vitro, más allá del aumento de resistencia basal de la planta contra patógenos.
CONCLUSIONES
Los resultados del trabajo demostraron que el quitosano induce la acumulación de proteínas y modula los indicadores enzimáticos defensivos relacionados con la protección de las plantas contra el ataque de patógenos, en dependencia de la concentración, el órgano vegetal y la etapa de crecimiento in vitro de soya inoculada con Bradyrhizobium.
En el futuro se debe profundizar en la inducción elicitora del quitosano mediante otras formas de aplicación y momentos del desarrollo de soya inoculada y en condiciones ex vitro.











 texto en
texto en 


