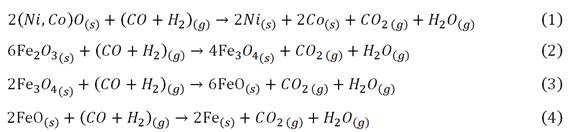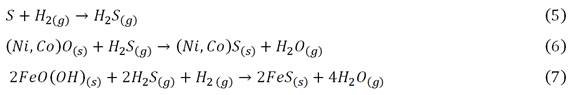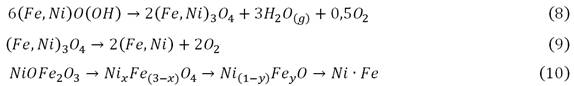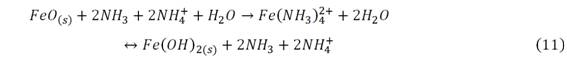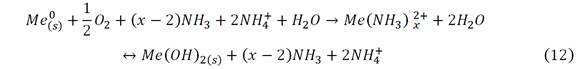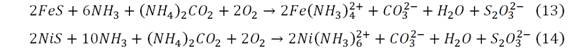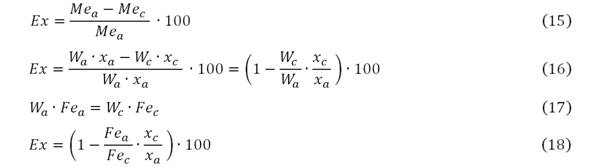Introducción
La tecnología de lixiviación carbonato amoniacal para la extracción selectiva del níquel y cobalto de minerales lateríticos, también conocida como proceso Caron, ha sido utilizada en Cuba desde 1944. El mineral se alimenta a los hornos de reducción con una humedad no mayor que un 4% y tamaño de partícula con un 83 a 85 % fracción inferior que 0,074 mm. La reducción se realiza en hornos cilíndricos verticales de hogares múltiples, disponen de un eje central rotatorio que contiene 4 barras fijas horizontales por hogar, dichas barras sostienen paletas en disposición adecuada que remueven el mineral en cada hogar y lo hacen descender en zigzag por soleras a contracorriente con los gases reductores.
Cada horno presenta 10 cámaras donde se alimenta petróleo aditivo, ya sea mezclado con el mineral o a través de una lanza automatizada, ocurre la combustión incompleta del petróleo, se generan los gases calientes que determinan el perfil térmico; y a su vez, favorecen las reacciones endotérmicas de reducción, ecs. (1) a (4). (1,2,3
Parte del azufre alimentado con el petróleo aditivo, forma sulfuro de metales, ecs. (5) a (7).
Las problemáticas fundamentales del área que afectan los índices de eficiencia de recuperación de níquel y cobalto, son: 2,3,4,5
Formación de aleaciones (Fe,Ni/Co), ecs. (8), (9).
Encapsulado del NiO libre en espinelas complejas, ec. (10).
Baja descomposición térmica de la serpentina y espinelas.
Se han reportado numerosos estudios del proceso de reducción, a escala de banco e industrial, de las variables de operación y sus interacciones para lograr la mayor extracción potencial de níquel y cobalto, donde se consideran: la composición química del mineral, expresada fundamentalmente por la relación número de mineral Nm=(Ni∙Fe)/(SiO2·MgO)6; distribución granulométrica; perfil térmico; dosis de aditivos como: petróleo, carbón bituminoso, petcoke7,8; el tiempo de retención9; la composición de la atmósfera reductora en cuanto a la relación CO2/CO, H2O/H2 y la presión.3,5,10,11
El mineral reducido pasa a lixiviación mezclándose con el licor carbonato amoniacal hasta alcanzar una densidad entre 1140 y 1150 kg/m3 y temperatura de 38 a 44ºC, e inicia la lixiviación del óxido de hierro (II), ec. (11).
La lixiviación de los metales (y los sulfuros de metales), ocurre en reactores continuos con agitación aireados; y se completa en los sedimentadores por reacciones de oxihidrolisis y formación de aminos complejos; pero el hierro precipita resultando un residuo del proceso denominado colas negras 1,2, ecs. (12)-(14).
donde:
x para Fe
Cu es 2, 3 y 4;
para Ni y Co es 2, 3, 4, 5 y 6.
Las causas fundamentales de pérdidas níquel y cobalto en lixiviación son:12,13,14,15
Co-precipitación con el hierro (II) y el manganeso.
Pasivación de las aleaciones metálicas (Fe,Ni/Co) con el oxígeno y en presencia de los iones de azufre SxOy z-, debido a la co-precipitación de sulfuros de metales en la superficie de las partículas de hierro.
Para reducir las pérdidas, se ha recomendado operar la lixiviación a concentración de amoníaco entre 85 y 90 g/L, cobalto menor que 0,2 g/L, relación NH3/CO2 entre 1,5 y 1,7 y controlar la aireación considerando el potencial redox. 6,16,17,18,19
La extracción máxima de níquel y cobalto del mineral reducido que es posible obtener en el proceso de lixiviación, se denomina extracción potencial o extractable de hornos y se determina experimentalmente por la prueba QT (siglas en idioma inglés, de tanque de contacto). Estudios previos demostraron que la deficiencia fundamental de la QT consiste en el elevado flujo específico (K) de aire que se aplica (3,5 m3·t-1·min-1) en la lixiviación, sin tener en cuenta el contenido de hierro soluble en el mineral reducido (MR). Tal intensidad de aireación provoca pérdidas de níquel y cobalto, por ello propusieron suministrar el flujo específico de aire diferenciado según el potencial redox inicial de la pulpa de MR. 16,17
La prueba del extractable de hornos de reducción, se utiliza en estudios geológicos de reservas minerales, para la obtención de modelos de pronóstico, la optimización de los parámetros de operación y para calcular índices de eficiencia del procesamiento industrial. Es un indicador de la calidad del proceso de reducción y lixiviación. Otros autores utilizan el grado de reducción, el cual se obtiene por determinación analítica del Ni, Co y Fe metálicos, por lixiviación con Br2-CH3OH o con Cu2SO4 en baño María. Estas variables se contrastan con los cambios en las fases minerales, la morfología y la composición química utilizando técnicas como ICP-OES, XRD, SEM/EDS. 5,6,7,8,9,11 Sin embargo, las variables flujo específico de aire diferenciado para el método del extractable potencial y el potencial redox, han sido poco aplicadas en las investigaciones.
El propósito de este trabajo fue comprobar los flujos de aire para determinar experimentalmente el extractable de níquel y cobalto con mineral del frente de minería Pinares de Mayarí; y determinar las interacciones entre las características del mineral reducido, los extractables y el potencial redox.
Métodos y materiales
Se utilizó un horno selas para reducir el mineral laterítico y comprobar los flujos de aire que se proponen para la prueba QT de la extracción potencial de níquel y cobalto.
El horno selas consiste en una cámara de combustión revestida de ladrillos refractarios donde se insertan quemadores de combustión de LPG, garantizándose con estos la temperatura de trabajo deseada. Cuenta con recipientes herméticos (6 botellas) donde se coloca el mineral con el petróleo, unidos a un sistema de transmisión que les imprime movimiento rotatorio. En el interior de cada recipiente y en la cámara, se coloca un termopar, (figura 1a). 9
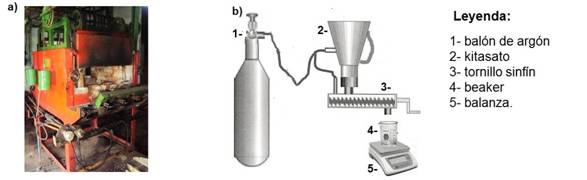
Fig. 1 Equipos y accesorios, a) Horno Selas, b) Implementos para operar el mineral reducido y preparar la suspensión
La operación del horno selas consistió en alimentar 700 g del mineral en cada botella mezclado con un 3 % de petróleo, la temperatura se incrementó linealmente durante 60 min y se retuvo 15 min a 700ºC; luego, el mineral reducido se dejó enfriar hasta 100ºC y se extrajo hacia kitasatos en atmósfera inerte de argón.
El mineral reducido se descargó de las botellas hacia kitasatos metálicos previamente purgados con argón.
La suspensión de mineral reducido y licor carbonato amoniacal, se preparó bajo campana de laboratorio y atmósfera inerte de gas argón (ver figura 1 b). Una masa de 100 g de mineral reducido se pesó directamente en 1,4 L de licor, para un 6,6 % en peso de sólidos.
La lixiviación se realizó a una temperatura entre 25 y 28ºC, tiempo de retención 180 min, concentración de amoníaco (NH3) 90 g/L y relación amoníaco - dióxido de carbono (NH3/CO2) 1,8. Se utilizó un banco de reactores, modelo mezclado perfecto, cada uno con capacidad de 2,5 L. 8,20
Las corridas experimentales se realizaron suministrando el flujo de aire (Qa) tradicional de 350 mL/min, para un flujo específico (K) 3,5 m3·t-1·min-1, y a modo comparativo, se varió Qa según el potencial redox (Eh) de la suspensión.
Si Eh ≤ -455 mV, K: 1,3 m3·t-1·min-1, Qa: 130 mL/min.
Si Eh > -455 mV, K: 1,8 m3·t-1·min-1, Qa: 180 mL/min.
Posteriormente, la suspensión lixiviada se filtró con un embudo Büchner conectado a un kitasato y a una bomba de vacío, la cola (o cake) se lavó con solución amoniacal de concentración 30 g/L para despojar el licor embebido en el sólido hasta que el color azul del filtrado se tornara transparente.
Para medir el potencial redox (Eh), se pesaron entre 5 y 6 g de mineral reducido en atmósfera inerte directamente en un beaker de 100 mL, enrazado a 80 mL de licor carbonato amoniacal, con 90 g/L de amoníaco y relación NH3/CO2 igual a 1,8. Luego de agitar con una varilla de vidrio se leyó el potencial con un pHmetro/mV Crison PH25, L-429, electrodo 5055 combinado Platino-Calomel. El punto de lectura de Eh fue análogo al punto crítico de la velocidad de sedimentación.
Los análisis químicos se realizaron en el laboratorio de la Unidad de Proyecto Nicaro del Centro de Investigaciones del Níquel, Cuba, aplicando los métodos: volumétrico, gravimétrico, potenciométrico y Espectrofotometría de Absorción Atómica.
Las extracciones (Ex) de los metales níquel y cobalto se determinan a partir de la masa del metal (Me) antes (a) y después de la lixiviación (c), Ec (15). Por su parte, la masa (Me), se calcula como el producto de la masa de mineral (W) por la concentración del compuesto químico (Ni, Co), en fracción masa (x), determinada por análisis químico, ec. (16). Finalmente, se plantea un balance de masa del componente hierro, ec. (17), y sustituyendo en (16), se deduce la ecuación para determinar las extracciones de los metales, ec. (18).
Fe: Concentración (%) de hierro en el mineral alimentado (a) y la cola lixiviada (c).
x: Concentración (%) de los metales níquel y cobalto.
Ex: Extracción potencial o extractable de los metales níquel y cobalto (%).
Resultados y discusión
El mineral reducido procesado en el horno selas, del frente de minería Pinares de Mayarí, tuvo la siguiente composición, expresada en promedio (+/- desviación estándar): níquel (Ni) 1,03 % (+/-0,135); cobalto (Co) 0,124 % (+/- 0,03); hierro (Fe) 55,93 % (+/-2,45); hierro ferroso (Fe2+) 23,36 % (+/- 3,18); y hierro metálico (Feº) 3,30 % (+/- 0,372).
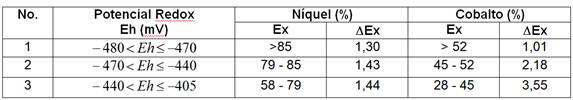
Los extractables (Ex) obtenidos mediante la prueba QT con aire diferenciado, se dividieron en tres rangos según el potencial redox (Eh), alcanzándose para el níquel entre 58,5% y 87,7%; y para el cobalto, entre 27,9% y 59,8%, (tabla 1).
Puede apreciarse en la tabla 1 que al considerar el potencial redox para determinar el flujo específico de aire (K: 1,3 o 1,8), hubo un incremento del extractable con respecto al método tradicional (K: 3,5) entre un 1,3 % y 1,4 % para el níquel, mientras que para el cobalto fue entre 1,0 y 3,6 %. Estos incrementos se obtuvieron utilizando el software Statgraphic 5.1, en el procedimiento contraste de múltiple rango, para un 95% de nivel de confianza, (figura 2).
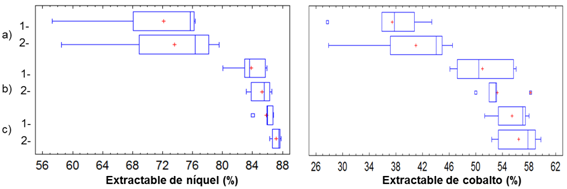
Fig. 2 Diagramas de bigote de los rangos de extractable de níquel y cobalto. Mineral de Pinares de Mayarí reducido en horno selas, a) -440<Eh≤-405 mV b) -470<Eh≤-440 mV c) -480<Eh≤-470 mV. 1-K: 3,5 2-K=f(Eh)
Luego, es recomendable considerar el potencial inicial, para determinar el flujo de aire a suministrar en el procedimiento experimental de la máxima extracción.
Se obtuvo una relación entre la concentración de hierro ferroso, los extractables de níquel y cobalto y el potencial redox de la pulpa de mineral reducido. El incremento de la concentración de níquel en el mineral reducido del rango 0,90 ≤ Ni ≤ 1,06 (%) a 1,15 ≤ Ni ≤ 1,25 (%), no tuvo una incidencia significativa sobre el extractable potencial, y los datos se colocaron sobre la misma línea de tendencia, con un coeficiente de determinación, R2, 97,4%, (figura 3a); en cambio, el incremento de la concentración de cobalto, del rango 0,098 ≤ Co ≤ 0,105 (%) a 0,153 ≤ Co ≤ 0,171 (%), propició un incremento del extractable hasta un 10% con R2 de 96,8% y 99,0% respectivamente, (figura 3b), por lo que debe considerarse esta variable en la construcción de nuevas interacciones.
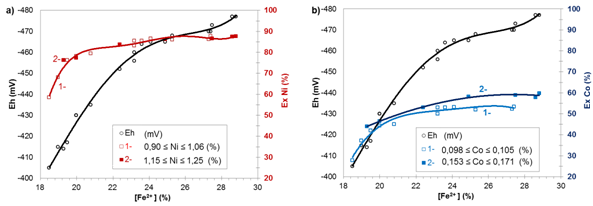
Fig. 3 Interacción del hierro (II) (Fe2+, %) en el mineral reducido con el potencial redox (Eh) y los extractables (Ex) de: a) níquel (Ni) b) cobalto (Co). Mineral de mina Pinares de Mayarí. Reducción en horno selas
Luego, una vez medido el potencial redox en la pulpa de la prueba QT, sería posible determinar las interacciones (figura 3) y estimar la calidad del mineral reducido que se entrega al proceso de lixiviación, en cuanto a la extracción potencial de los metales Ni y Co, asumiéndolo como un ensayo físico.
Conclusiones
Se comprobó que al considerar el potencial redox para determinar el flujo específico de aire para la prueba QT con mineral de Pinares de Mayarí, hubo un incremento del extractable con respecto al método tradicional de un 1,4 % de níquel, mientras que para el cobalto fue entre 1,0 y 3,6 %.
Se obtuvo una relación entre la concentración de hierro ferroso en el mineral reducido, con el potencial redox y el extractable, lo cual sugirió asumir la medición de potencial como un ensayo físico para estimar el extractable que se entrega a lixiviación.