Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd v.22 n.4 Ciudad de la Habana sep.-dic. 2003
Trabajos originales
Instituto de Ciencias Básicas y Preclínicas “Victoria de Girón”
Participación tubular renal en la génesis de la hipertensión arterial primaria
Dr. Manuel Chaple La Hoz, Dr. Ernesto Barber Gutiérrez, Dra. María Ofelia Fox Pascual, Dr. José Castillo Herrera, Dra. María Ofelia Barber Fox y Dr. Antonio Raúl Chauvín Roche
Resumen
Se utilizó una muestra compuesta por 45 pacientes hipertensos esenciales, 40 hipertensos y 40 sujetos sanos, de edades comprendidas entre 18 y 30 años, todos del sexo masculino, clasificados según los criterios establecidos por la Organización Mundial de la Salud, con el propósito de estudiar el papel tubular en la hipertensión arterial primaria. A todos se les realizaron pruebas de función renal y ultrasonido, entre otras. De acuerdo con los resultados, los jóvenes prehipertensos presentaron un cuadro de desbalance glomérulo tubular de preponderancia glomerular que justifica la sobrecarga reabsortiva encontrada, con aumento del volumen renal evaluado. En los jóvenes hipertensos estudiados los valores bajos de aclaramiento plasmático de creatinina, suponiendo que transitaron previamente por estado de prehipertensos, determinaron un desbalance glomérulo tubular, ahora de preponderancia tubular si se tiene en cuenta el aumento de la reabsorción tubular de sodio y litio, la disminución de la excreción de Na+ y el mayor volumen renal que presentaron.
DeCS: HIPERTENSION; TEST DE FUNCION RENAL; RIÑON, HIPERTROFIA; SODIO; LITIO.
Hasta el presente ha sido imposible establecer las causas de la hipertensión arterial (HTA) en la mayor parte de los pacientes, considerándose que alrededor de 90 % padecen de hipertensión arterial denominada primaria, idiopática o “esencial”, asimismo es conocido que solo 5 a 10 % de la enfermedad hipertensiva está constituida por hipertensiones secundarias,1,2 lo cual lógicamente, convierte la hipertensión primaria en el elemento más importante para el tratamiento y la prevención de esta enfermedad.
Desde la década de los años 60 se ha venido planteando el carácter multifactorial del agente causante de la HTA primaria, compuesto así por factores genéticos, hormonales, nerviosos, renales, ambientales, dietéticos, etc.1,3 Sin embargo, el análisis de cada uno de estos factores conduce de una manera u otra, al riñón, como órgano que resulta afectado en el manejo de la excreción renal del sodio y agua, lo cual ha sido enfatizado por Guyton y otros.3,4
Así la relación del riñón con la enfermedad hipertensiva ha sido corroborada por múltiples observaciones clínicas y experimentales (hipertensión renal parenqui-matosa, hipertensión por aldosteronismo primario, hipertensión renovascular, modelos de hipertensión renal de Goldblatt, Page y Grollman, entre otros (Galvizu Díaz, K; Barber, E. Estudio evolutivo de la administración del propranolol a ratas normotensas. Tesis para la terminación de la Especialidad, 1998; 10-12.)( Barber MO, Barber, E. Efectos renales y hemodinámicos en ratas de la Saralasina y su posterior supresión. Tesis para la terminación de Especialidad, 1992; 20-24.)
En algunas enfermedades renales, como las antes señaladas, el papel patogénico del riñón en la elevación de la presión arterial no se discute. No ocurre igual con otros tipos de hipertensiones y particularmente con la esencial o primaria. La fácil producción de hipertensión arterial mediante los modelos experimentales señalados, son argumentos de fuerte apoyo a la hipótesis que sostiene el papel patogénico del riñón en la hipertensión arterial primaria.5-6
Así, últimamente se ha venido haciendo énfasis en el posible papel a desempeñar por el túbulo renal en su trabajo reabsortivo, que de incrementarse sería un factor de hipertensión aún no bien estudiado. Esto ha sido planteado por Guyton y otros como una posibilidad más de generarse glomérulo-tubular que determine la hipertensión. En tal sentido se ha generado en ratas normotensas, hipertensión arterial provocando hipertrofia tubular7-9 y se ha encontrado aumento del trabajo reabsortivo tubular en la rata MHS.10
Indudablemente que la generación de una hipertrofia tubular en el humano, pudiera ser causa también de hipertensión y tal cambio morfológico no es valorado a la hora de estudiar una biopsia renal, no describiéndose como alteración, que puede estar presente, con el lógico riñón agrandado y no ser detectado. Así, el propósito de este trabajo fue estudiar el papel tubular en la hipertensión arterial primaria en el humano.
Métodos
Se utilizó una muestra compuesta por 45 pacientes hipertensos esenciales, 40 prehipertensos y 40 sujetos sanos, de edades comprendidas entre 18 y 30 años; todos del sexo masculino. Para la selección de los pacientes hipertensos se tomaron en cuenta:
1. Los criterios señalados por el Report of Joint National Comittee que plantea cifras de 140/90 o más en mayores de 18 años, detectados en 3 ocasiones distintas.11
2. Que fueran hipertensos leves, grado I, jóvenes, sin tratamiento medicamentoso o si lo tenían, que fuera suprimido 3 semanas antes de ser estudiados.
Los sujetos prehipertensos fueron aquellos que cumplían criterios de la Organización Mundial de la Salud (OMS) para los llamados border line, es decir, aquellas personas jóvenes con antecedentes familiares de HTA y que en algunas ocasiones hubiesen tenido cifras ligeramente elevadas de presión arterial y en otros, valores normales.11
Con el propósito de establecer el carácter primario de la HTA en los pacientes hipertensos, así como en los prehipertensos y el estado de salud en los sujetos sanos, todos los miembros de los 3 grupos fueron sometidos al estudio siguiente: hemograma, leucograma con diferencial, examen parcial de orina, eritrosedimentación, pruebas funcionales hepáticas, ionograma en 3 ocasiones, ácido vanilil-mandélico en orina, proteinuria de 24 h, glicemia, urea, colesterol, lipoproteínas de alta densidad, ácido úrico y calcio en sangre, aclaramiento plasmático renal de creatinina, electrocardiograma y ecografía renal y suprarrenal.
Adicionalmente, a los pacientes hipertensos se les realizó la pielografía minutada y arteriografía renal, lo cual por razones éticas no se les practicó a los otros grupos.
Todos los sujetos fueron sometidos a minucioso examen clínico y anamnesis que contribuyó a su clasificación, seleccionán-dose los que tuvieron normales los resultados de las pruebas anteriores.
A todos los sujetos tanto hipertensos como prehipertensos y normales se les practicó aclaramiento plasmático renal de paraminohipurato, de creatinina endógena (ApCr) y de litio (ApLi) para valorar el flujo plasmático renal efectivo, la intensidad de filtración glomerular y la capacidad reabsortiva de los túbulos proximales respectivamente. Asimismo se determinaron los aclaramientos plasmáticos renales de sodio y potasio, derivándose sus fracciones de reabsorción y excreción respectivamente. Adicionalmente se obtuvo por ultrasonido el volumen renal de ambos riñones.
Las presiones arteriales fueron registradas por el método clásico de Riva Rocci, en la mañana y después de tener al sujeto de 30 min en reposo. El registro se obtuvo en 3 ocasiones, tomándose los valores promedio tanto de las presiones sistólicas como diastólicas (PAS y PAD). De los valores anteriores se calculó la presión arterial media (PAM) utilizando la expresión siguiente:12
PAM = PAD + 1/3 (PAS – PAD)
Para la determinación de los aclaramientos plasmáticos de creatinina, sodio y potasio, se les recogió la orina de 24 h y a la mañana siguiente en ayunas, se tomó la muestra de sangre. En estas orinas y muestras de sangre se determinaron las concentraciones respectivas de creatinina, sodio y potasio, con lo que se calcularon los aclaramientos respectivos.
El aclaramiento plasmático de paraminohipurato fue determinado por el procedimiento de una perfusión continua de PAH con muestra de orina. Los aclaramientos plasmáticos de litio se determinaron luego de administrar por vía oral 16,2 mmol de carbamato de litio 14 h antes de los períodos de aclaramiento; al día siguiente, en la mañana, durante la hidratación oral, se recolectó la orina de períodos de 2 h en 3 ocasiones sucesivas, tomando muestras de sangre respectivas, de donde se calcularon los ApLi. La media de los 3 aclaramientos fue utilizada para calcular la fracción de reabsorción de litio (FRLi), según la fórmula siguiente:13
FRLi = 1 – ApLi/ApCr
El PAH se determinó por el método del sulfato de cadmio,14 utilizando la técnica fotocolorimétrica de Bratton y Marshall15 modificada por Homer W. Smith.16
La creatinina se determinó por el método de Jaffé sin desproteinización en medición cinética a los 2 min.17
Los electrolitos litio, sodio y potasio se determinaron por fotometría de llama.18
Se realizaron exámenes de ultrasonido a todos los pacientes y sujetos sanos, explorando ambos riñones con un equipo de tiempo real Sonolayer Sal 30A, midiéndoles a cada uno la longitud (diámetro vertical), el ancho, diámetro transversal y el grosor (diámetro anteroposterior). Las 3 mediciones obtenidas se marcaron en el digital para determinar el volumen de cada riñón según el método del elipsoide19 mediante la fórmula: V = L.A.G. (p/6), ya programada en el equipo. Para el procesamiento y análisis estadístico de los datos se utilizaron la media (X), y la desviación estándar (DE); calculados para cada grupo y cada variable. La comparación entre las medias de los distintos grupos para cada variable, se realizó mediante un análisis de varianza de clasificación simple y como test complementario el de Duncan.20
Resultados
En primer lugar la uniformidad de la muestra seleccionada se demuestra en que la edad promedio de todos los grupos: hipertensos, prehipertensos y normales fue de 22 años, no habiendo diferencias significativas entre los grupos (tabla 1); similar característica se logró para toda la muestra con respecto a la tabla corporal, no resultando así con el peso y la superficie corporal, donde los sujetos hipertensos presentaron valores de 13 y 8 % superiores en las variables respectivas, con respecto a los otros 2 grupos, en ambos casos (tabla 1).
Tabla 1. Comportamiento de la edad y talla física en sujetos normales, prehipertensos e hipertensos
| | Edad | Peso | Talla (cm) | Superficie corporal (m) | |||||||||
| | n |
| DE | p |
| DE | p |
| DE | p |
| DE | p |
| Normales | 40 | 22,68 | 4,4 | NS | 65,03 | 10,32 | NS | 170,65 | 8,58 | NS | 1,75 | 0,15 | NS |
| Prehipertensos | 40 | 22,10 | 3,15 | | 65,73 | 9,94 | | 170,50 | 7,62 | | 1,72 | 0,23 | |
| Hipertensos | 45 | 22,29 | 3,96 | NS | 74,39 | 8,38 | < 0,01 | 172,93 | 8,13 | NS | 1,88 | 0,15 | < 0.01 |
Por otra parte las concentraciones plasmáticas de creatinina y urea fueron más bajas en los prehipertensos, tanto con respecto a los normales como con los hipertensos, estos últimos presentaron siempre las cifras más elevadas (tabla 2).
Tabla 2. Comportamientos de las concentraciones plasmáticas de creatinina y urea en sujetos normales prehipertensos e hipertensos tomados para estudio
| Grupo | N | P c r mg / 100 mL | | | Pu mg / 100 mL | | |
| | |
| DE | p |
| DE | p |
| Normales | 40 | 0,99 | 0,16 | NS | 24,29 | 3,50 | NS |
| Prehipertensos | 40 | 0,91 | 0,26 | | 22,20 | 4,28 | |
| Hipertensos | 45 | 1,11 | 0,39 | < 0,01 | 25,15 | 8,39 | NS |
Pc r: concentración plasmática de creatinina, Pu: concentración plasmática de urea.
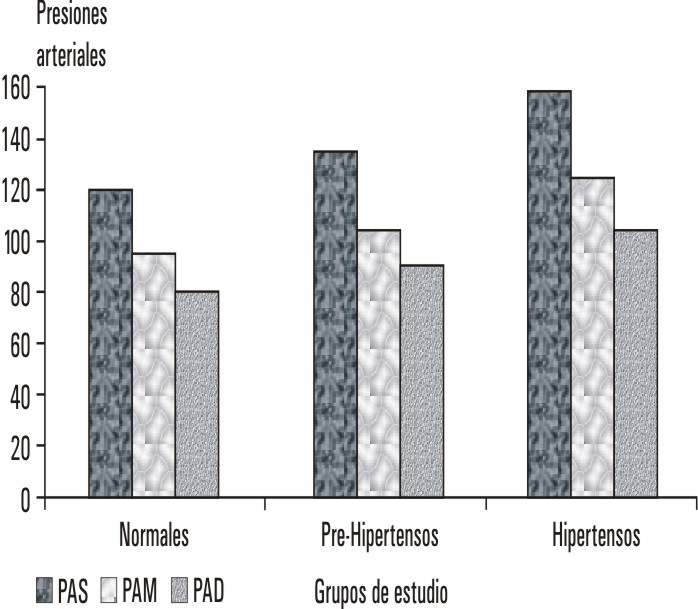
El registro de las presiones arteriales sistólicas y diastólicas y el cálculo de la presión arterial media de todos los sujetos estudiados reflejó la característica de los grupos seleccionados; existiendo para todas las presiones una escala de valores según se desplazara desde los normales hasta los hipertensos, pasando por los prehipertensos (fig.). Los flujos plasmáticos renales en los prehipertensos fueron superiores a los normales en 22 %; mientras que en los hipertensos fue 33 % menor que los normales (tabla 3).
PAD: presión arterial diastólica, PAM: presión arterial media, PAS: presión arterial sistólica.
Fig. Comportamiento de las presiones arteriales sistólicas medias y diastólicas en sujetos normales, prehipertensos e hipertensos tomados para estudio.
Tabla 3. Comportamientos del flujo plasmático renal efectivo, aclaramiento plasmático de creatinina, fracción de filtración y aclaramiento plasmático de urea en sujetos normales, prehipertensos e hipertensos tomados para estudio
| | | FPRE mL/min/1,73 m2 | ApCr mL/min/1,73 m2 | FF | ApU | ||||||||
| Grupo | n | ||||||||||||
| |
| DE | p |
| DE | p |
| DE | p |
| DE | p | |
| Normales | 40 | 527,80 | 77,99 | < 0,01 | 102,97 | | < 0,01 | 0,20 | 0,055 | < 0,05 | 59,90 | 15,23 | NS |
| Prehipertensos | 40 | 646,24 | 107,13 | | 142,51 | 22,54 | | 0,22 | 0,049 | | 64,42 | 18,32 | |
| Hipertensos | 45 | 395,57 | 161,30 | < 0,01 | 96,11 | 29,71 | < 0,01 | 0,26 | 0,072 | < 0,05 | 59,30 | 25,97 | NS |
ApCr: aclaramiento plasmático de creatinina, ApU: aclaramiento plasmático de urea, FF: fracción de filtración, FPRE: flujo plasmático renal efectivo.
Los ApCr mostraron también cifras elevadas en los prehipertensos, de 38 % superior a los normales y 48 % con respecto a los hipertensos; no habiendo diferencias significativas entre normales e hipertensos (tabla 3).
Las fracciones de filtración mostraron valores cada vez mayores a partir de los normales hasta los hipertensos, pasando por los prehipertensos (tabla 3).
Los aclaramientos plasmáticos de urea no fueron diferentes en los grupos estudiados (tabla 3).
El manejo renal del sodio se manifestó de la forma siguiente:
La concentración plasmática de este ion fue significativamente superior en los sujetos hipertensos comparados con normales y prehipertensos, mientras que la excreción renal de sodio fue contraria, es decir, significativamente menor en los hipertensos (tabla 4).
Tabla 4. Comportamientos de la concentración plasmática, la excreción urinaria, la reabsorción tubular y el aclaramiento plasmático de sodio en sujetos normales, prehipertensos e hipertensos, tomados para estudio
| Grupo | | PNa mEq /L | ENa mEq /L/1,73 m2
| CRNa mEq /L/1,73 m2 | ApNa mL /min/1,73 m2 | ||||||||
| | DE | p | | DE | p | | DE | p | | DE | p | ||
| Normales | 40 | 141,15 | 6,05 | NS | 0,13 | 0,027 | NS | 14,32 | 2,73 | NS | 0,91 | 0,20 | < 0,01 |
| Prehipertensos | 40 | 138,70 | 4,75 | 0,15 | 0,020 | 14,40 | 3,76 | 1,22 | 0,70 | ||||
| Hipertensos | 45 | 147,43 | 9,96 | < 0,01 | 0,08 | 0,049 | < 0,05 | 17,06 | 3,52 | < 0,01 | 0,53 | 0,32 | < 0,01 |
ApNa: aclaramiento plasmático de sodio, CRNa: cantidad reabsorbida de sodio, Ena: excreción urinaria de sodio, Pna: concentración de sodio.
La cantidad reabsorbida de sodio fue significativamente mayor en los hipertensos (tabla 4) quienes mostraron elementos indicativos de retención de sodio y los aclaramientos plasmáticos de sodio significativamente menores que en normales y prehipertensos, siendo estos últimos los que mostraron valores mayores (tabla 4).
En relación con el potasio no hubo diferencias en las concentraciones plasmáticas del ion entre los sujetos de los distintos grupos de estudio, presentando los prehipertensos una excreción renal de potasio significativamente superior a normales e hipertensos, a la par que los prehipertensos presentaron una cantidad reab-sorbida de potasio superior sin diferencia en el volumen de plasma aclarado de este ion con normales e hipertensos (tabla 5).
Tabla 5. Comportamientos de la concentración plasmática, la excreción urinaria , la reabsorción tubular y el aclaramiento plasmático de potasio en sujetos normales, prehipertensos e hipertensos tomados para estudio
| Grupo | | PNa mEq /L | ENa mEq /L/1,73 m2
| CRNa mEq /L/1,73 m2 | ApNa mL /min/1,73 m2 | ||||||||
| | DE | p | | DE | p | | DE | p | | DE | p | ||
| Normales | 40 | 4,03 | 0,43 | NS | 0,02 | 0,0085 | < 0,01 | 0,38 | 0,10 | < 0,01 | 5,47 | 2,14 | NS |
| Prehipertensos | 40 | 4,12 | 0,40 | 0,05 | 0,0047 | 0,58 | 0,29 | 4,61 | 3,60 | ||||
| Hipertensos | 45 | 4,09 | 0,57 | NS | 0,02 | 0,0012 | < 0,01 | 0,35 | 0,11 | < 0,01 | 5,85 | 3,78 | NS |
Adicionalmente el estudio de litio arrojó un aclaramiento plasmático del ion (ApLi) menor en los hipertensos, contrastando con los valores mayores por encima de los normales que presentaron los prehipertensos, mientras que la fracción de reabsorción de litio fue significativamente mayor en los hipertensos (tabla 6).
Tabla 6. Comportamientos del aclaramiento plasmático y la fracción reabsorbida de litio en sujetos normales, prehipertensos e hipertensos tomados para estudio
| Grupo | | ApK mL /min/1,73 m2 | FR Li
| ||||
| | DE | p | | DE | p | ||
| Normales | 40 | 33,35 | 3,01 | < 0,01 | 0,67 | 0,07 | NS |
| Prehipertensos | 40 | 37,50 | 2,85 | 0,69 | 0,08 | ||
| Hipertensos | 45 | 22,93 | 4,02 | < 0,01 | 0,75 | 0,07 | < 0,01 |
Finalmente, el estudio morfométrico ultrasonográfico de los riñones de los sujetos normales, prehipertensos e hipertensos seleccionados para este trabajo arrojó que el volumen integral de los riñones derecho e izquierdo, calculados a partir de las medidas de los 3 ejes vertical, transversal y anteroposterior de cada órgano presentó un valor significativamente mayor en los riñones de los hipertensos, y existía una escala ascendente de valores de volumen renal según se iba desde los sujetos normales a los hipertensos pasando por los prehipertensos, lo cual se manifestó con cifras mayores en los riñones izquierdos (tabla 7).
Tabla 7. Comportamiento de los volúmenes de los riñones derecho e izquierdo en sujetos normales, prehipertensos e hipertensos, tomados para estudio
| Grupo | | VRD mL |
| ||||
| | DE | p | | DE | p | ||
| Normales | 40 | 120,20 | 20,61 | < 0,01 | 123,10 | 22,89 | < 0,01 |
| Prehipertensos | 40 | 128,23 | 13,10 | 130,80 | 14,22 | ||
| Hipertensos | 45 | 151,62 | 15,41 | < 0,01 | 154,88 | 16,69 | < 0,01 |
VRD: volumen del riñón derecho, VRI: volumen del riñón izquierdo.
Discusión
En este estudio renal humano, en tiempos prematuros de la enfermedad hipertensiva, que justificó la uniformidad de la muestra en jóvenes de tallas similares, sin embargo, fue característico que los hipertensos superaran en peso y superficie corporal a los demás grupos, un elemento que podrá tener significación importante más adelante.
Es llamativo que los sujetos prehipertensos mostraron flujos plasmáticos 22 % superiores a los normales, así como 38 % mayor los ApCr, tomados como valoración de las intensidades de filtración glomerular a pesar de sus imprecisiones, mientras que los hipertensos presentaron flujos plasmáticos renales inferiores a los normales; estos hechos recuerdan el comportamiento de estas variables en las ratas bajo la administración de propranolol y su posterior supresión respectivamente (Chaple MH. Estudio de la participación tubular renal en la génesis de la hipertensión arterial renal. Tesis de Doctorado, 1998; 30-32.).
Debe señalarse que los riñones de todos los sujetos estudiados cumplieron sus misiones de depuración, porque aclararon la urea de forma similar; pero los hipertensos presentaron un marcado incremento de la fracción de filtración a pesar de tener disminuidos los FPRE, lo cual da indicios de la participación de otro factor determinante de este incremento y que la intensidad de filtración glomerular no está siguiendo la flujo-dependencia y más bien es posible sea resultado del incremento de la presión arterial.
En estas circunstancias, la revisión de los volúmenes renales determinados por ultrasonografía, que fueron mayores en los hipertensos, pero estando elevados en los prehipertensos, da signos de que pudiera plantearse un crecimiento renal según se entra en el estado prehipertensivo y se pasa al hipertensivo.
No se sabe tal aumento de volumen de qué depende, lógicamente, no se hicieron biopsias renales, pero sí se realizó un estudio del manejo renal del litio, que como se conoce es reabsorbido solo por el túbulo proximal. Sus resultados indican una fracción de reabsorción de litio superior al normal en los prehipertensos, que se hizo mayor en los hipertensos.
Un resultado similar se presentó en el estudio, en estos grupos, del procesamiento renal del sodio, donde la cantidad reabsorbida se mostró aumentada en los hipertensos, con menor excreción, todo a favor de una mayor retención hidrosalina.
Es decir, que los incrementos de flujo plasmático renal efectivo y ApCr de forma marcada en los prehipertensos sugiere que los riñones de tales sujetos están sometidos a un desbalance glomérulo-tubular de preponderancia glomerular, el cual habría que determinar si produce una hipertrofia tubular como pudiera esperarse y justificaría los aumentos de volumen renal encontrados, pues, de ser así, la disminución posterior que se observa en los ApCr en los pacientes hipertensos pudieran convertir el desbalance glomérulo-tubular en uno de preponderancia tubular que afectaría la curva de excreción de sodio, determinando una retención hidrosalina en sujeto que, como se dijo al comienzo, con iguales tallas y edad presentaron mayor peso, que pudiera justificar la HTA, o sea que al parecer podría existir una significativa justificación tubular en el desarrollo del estado hipertensivo.
Luego, a pesar de los múltiples estudios de la hipertensión arterial primaria o esencial humana, no está completamente caracterizada desde el punto de vista renal y hemodinámico, pues, al no ser factible determinadas investigaciones, se mantienen innumerables interrogantes, lo cual se reflejó en este diseño, donde no se incluyó la biopsia renal, la determinación del máximo tubular de paraminohipurato, etc.; sin embargo, con los resultados obtenidos se puede plantear que hay muchas similitudes entre la hipertensión esencial humana y el modelo experimental de hipertensión al inducirse una hipertrofia tubular (Chaple MH. Estudio de la participación tubular renal en la génesis de la hipertensión arterial renal. Tesis de Doctorado, 1998; 30-32.).
La posible participación tubular en la génesis de la HTA primaria, ya ha sido sugerida por Guyton y otros3,4 a partir de un análisis teórico. Bianchi y otros7 han establecido comparación entre la rata MHS que se desarrolla genéticamente y la hipertensión esencial humana y suponen los autores que la participación tubular es teóricamente posible, se encontró aumento del transporte tubular de sodio en las ratas MHS.7
Es válido señalar aquí, como refiere Barber y otros en su trabajo generando ratas hipertensas a partir de desarrollar hipertrofia tubular, que en la misma proporción en que se incrementan las investigaciones sobre la génesis de la hipertensión arterial primaria, los estudios del papel del riñón en esta aumentan, en particular aquellos relacionados con la participación tubular,3,4,7 su manejo del sodio4,21 tomando gran interés la intervención del balance glomérulo-tubular y su regulación,22 lo cual da relevancia al significado de los resultados que se discuten.
Se concluye que:
- Los jóvenes hipertensos presentan un cuadro de desbalance glomérulo-tubular de preponderancia glomerular, el cual justifica la sobrecarga reabsortiva encontrada y puede derivar sin que se haya determinado, en una hipertrofia tubular que explicaría el aumento de volumen renal evaluado.
- En los jóvenes hipertensos estudiados, los valores bajos de ApCr, suponiendo que hayan transitado previamente por estado de prehipertensos, determinan un desbalance glomérulo-tubular, ahora de preponderancia tubular, si se tiene en cuenta el aumento de la reabsorción tubular de sodio y litio, la disminución de la excreción de sodio y el mayor volumen renal que presentan.
- La afectación de la curva de excreción renal de sodio en estos pacientes puede conducir a una HTA.
Summary
A sample of 45 essential hypertensive patients, 40 hypertensives and 40 healthy subjects aged 18-30 years, all males and classified according to the WHO criteria, was used to study the tubular role in primary blood hypertension. All of them were applied renal function tests and ultrasound among others. According to the results achieved, the pre-hypertensive young males showed a picture of tubular glomerular imbalance of glomerular predominance that explains the re-absorptive overload found, with rise in the evaluated renal volume. The low values of plasmatic creatinine clearing in the studied hypertensive young males, assuming that they were previously pre-hypertensive, determined a tubular glomerular imbalance with tubular predominance at present if the increase of tubular reabsorption of sodium and lithium, the decrease of Na+ excretion and the higher renal volume present in these persons are taken into consideration.
Subject headings: HIPERTENSION; KIDNEY FUNCTION TEST; KIDNEY; HYPERTROPHY; SODIUM; LITHIUM.
Referencias bibliográficas
- Cecil Russel La Fayette. Arterial hypertension. En: Textbook of Medicine. New York: WB Saunders; 2000. p. 224-30.
- Pickering TG, Laragh JM. Renovascular hypertension. En: The Kidney. New York: W.B. Saunders; 2000. p. 1940-67.
- Guyton AC. Salt balance and long-term blood pressure control. Am Rev Med 1999; 31:15-19.
- Coleman TG. Renal abnormalities that do and do not cause hypertension. Proc Int Cong Nephrol 1976;6:266-70.
- Kaplan NM. New aspects in pathophysiology and management of hypertension. J Hum Hyperten 1992;2:51-60.
- Duddley CR. Identifying genetic determinants in human essential hypertension. J Am Soc Nephrol 1996;3:2-8.
- Bianchi C. The kidney in essential hypertension. Contr Nephrol 1998;49:173-8.
- Muldoon MF. Family history studies in hypertension. Am J Hyperten 1993;6:76-80.
- Schieken RM. Genetic factors that predispose the child to develop hypertension. Pediatr Clin North Am 2000;40:1-11.
- Weihprecht H, Lorenz JN. Vasoconstrictor effect of angiotensin an vasopressin in isolated rabbit afferent arterioles. Am J Physiol 1998;261:273-82.
- Macías Castro I, Álvarez GG, Suárez E. Evaluación y tratamiento del paciente hipertenso. Rev Cubana Med Gen Integr 1998;7: 83-93.
- Berne RM, Levy MN. The arterial system. Cardiovascular Physiology, St Louis.The CV Mosby, 1998. p.98-9.
- Semplicini A. Red blood cell Na+/H+ and Li+/Na+ exchange in patients with essential hypertension. AJH 1999;2:903-8.
- Smith HW. Técnicas de aclaramiento plasmático. Madrid: Ateneo; 1963.p.43-8.
- Bratton AC, Marshall EK Jr. A new coupling component for sulfanilamide determination. J Biol Chem 1939;128:537.
- Smith HW. The renal clearance of susstituted hipuric acid derivatives and other aromatic acids in dog and man. J Clin Invest 1945;24:388-92.
- Bartels H. Test-combination creatinine. Clin Chem Acta 1971;32:81.
- Oser BL. Blood analysis. En: Physiological Chemistry. New York: McGraw-Hill Book, 1965. p. 1040.
- Jones TB. Ultrasonographic determination of renal mass and renal volumen. J Ultrasound Med 1993;2:151-4.
- Martínez HY. Pruebas de hipótesis. En: Manual de procedimientos estadísticos. La Habana: Editorial Ciencias Médicas, 1998. p. 80-5.
- Eiskjaer M. Abnormal tubular handling of sodium and water induced by atrial natriuretic peptide in essential hypertension. J Intern Med 1991;320:37-48.
- Kill FG. Glomerulotubular balance. Proc Int Union Physiol Sci 1990;14:161-2 .
Recibido: 20 de junio de 2003. Aprobado: 28 de agosto de 2003.
Dr. Manuel Chaple La Hoz. Oeste # 1773 / Perla y Avenida de los Pinos. Reparto Los Pinos. Habana 18. Municipio Arroyo Naranjo. Ciudad de La Habana. Cuba. Teléf: 209 90 36. Correo electrónico: chaple@giron.sld.cu