Introducción
La contaminación de los suelos constituye un problema provocado por la industrialización, que ha traído consigo el vertimiento de residuos industriales, ya sea como aguas residuales o residuos sólidos. La acumulación de sustancias tóxicas en el suelo afecta su capacidad de auto regeneración, además de poner en peligro recursos como el agua superficial, convirtiéndose el suelo contaminado en un elemento tóxico para los organismos que lo habitan y para la vegetación.
Entre las fuentes que más contribuyen a la contaminación del suelo se encuentran los metales pesados, presentes en el mismo como componentes naturales, o como consecuencia de la actividad del hombre; su impacto es valorado como uno de los más alarmantes problemas ambientales del presente siglo debido a su lenta y difícil restauración.1 Estos metales pesados presentan diferentes características fisicoquímicas y biológicas, y se encuentran formando complejos como iones libres o participando en reacciones redox que resultan potencialmente tóxicas para los organismos.2 La acumulación de metales pesados en las plantas inhibe o activa algunos procesos enzimáticos que afectan su productividad.
En suelos, los metales pesados constituyen uno de los contaminantes inorgánicos más importantes debido a su movilidad y toxicidad para las formas superiores de vida, y a las afectaciones que pueden causar en ecosistemas.3) El Cd y Pb se encuentran entre los elementos potencialmente tóxicos de mayor importancia ambiental, presentes en sitios contaminados, los cuales una vez movilizados al ambiente, tienden a persistir indefinidamente en el suelo, resultando en algunos casos altamente tóxicos y acumulativos.3) Estos metales han sido la causa de efectos negativos sobre la salud humana y de animales, así como de la perturbación de los ecosistemas naturales y los agroecosistemas.
Para remediar suelos contaminados con metales pesados, se han diseñado técnicas físicas de tratamiento como la excavación, fijación y lixiviación, pero presentan costos elevados y, además, contribuyen con el deterioro del sitio tratado. En contraste, existen plantas que naturalmente pueden establecerse en medios contaminados con metales pesados y acumularlos en sus tejidos; propiedad que es aprovechada en la fitorremediación, la cual consiste en el empleo de plantas y sus microorganismos asociados para remover, transferir, estabilizar y/o degradar contaminantes en suelo, sedimentos y agua. Además, es considerada una técnica amigable con el medio ambiente y de bajo costo para el tratamiento de suelos contaminados insitu.4
La fitorremediación comprende tanto los procesos dirigidos a liberar el contaminante de la matriz del suelo (descontaminación), como los encargados de retenerlos en dicha matriz (estabilización). Esta técnica ha ganado una elevada aceptación desde la última década, como un tipo de tecnología limpia que utiliza los organismos naturales, y preserva su medio ambiente.5,6,7,8
Diferentes investigaciones evidencian el potencial de la fitoremediación para remover, reducir, transformar, mineralizar, degradar, volatilizar o estabilizar diferentes tipos de contaminantes presentes en suelo, aire, agua o sedimentos tales como metales pesados, metales radioactivos, compuestos orgánicos y compuestos derivados del petróleo.6,7,9) La determinación de los coeficientes biológicos de fitorremediación de especies de plantas que asimilan los metales presentes en suelos contaminados, brinda información sobre su potencial, coincidiendo la mayoría de los autores en que valores mayores a uno de dichos coeficientes, son favorables para que la planta pueda ser empleada como fitorremediadora.10,11,12
En suelos contaminados con cadmio y plomo, crece Romerillo americano (HeleniumquadridentatumLabill), con una elevada densidad poblacional, lo que evidencia la resistencia de esta planta en condiciones adversas, y la tolerancia a las altas concentraciones de metales en el suelo, pudiendo ser empleado como un agente fitorremediador. La presente investigación tiene como objetivo, determinar los coeficientes de remediación de cadmio y plomo del Romerillo americano en suelos contaminados con estos metales.
Materiales y métodos
Determinación del contenido de cadmio y plomo
Selección y toma de muestra
Para la toma de muestras de los suelos contaminado, se tuvo en cuenta los resultados de la caracterización de dichos suelos realizada por Quero y colaboradores.13 Se definió una red de muestreo de 5 x 5 m para cada suelo (oscuro plástico gleysoso y pardo con carbonato), tomando muestras compuestas de la parte superficial de ambos suelos (0-20 cm). Posteriormente, las muestras fueron llevadas al laboratorio, secadas a 60°C en estufa Binder, Alemania, y finalmente se procedió a prepararlas en función de los ensayos por efectuar.
Las plantas sembradas en ambos experimentos realizados se recolectaron en el reparto “Los Moros”, municipio Santa Clara, sitio no contaminado con los metales evaluados. Después de seis meses de sembradas, fueron recolectadas las de cada sistema en su totalidad, se le realizó un lavado con agua destilada y luego con agua desionizada. Se separaron en sus órganos: flores, hojas, tallos y raíces (rizomas); los que se trituraron y secaron a peso contante en estufa a 60 ºC.
Digestión de las muestras
Se pesaron las muestras en una balanza analítico Denver Instrument, Alemania, y se trasvasaron a un tubo Kjeldahl; se le adicionaron 2 mL de agua desionizada y 10 mL de agua regia, luego se taparon con vidrio reloj, realizando la digestión en frío por 24 h bajo campana de extracción. Finalizada la digestión en frío, se conectó el tubo de reflujo en el bloque calefactor a 150 ºC durante 2 h (digestión en caliente). Se dejó enfriar progresivamente a temperatura ambiente, enjuagándose la columna refrigerante con un máximo de 30 mL de agua desionizada y recuperando el agua de enjuague en el vaso de digestión. Se filtró el extracto con un filtro resistente a ácidos y se enrazó en un matraz aforado. El recipiente de digestión y el residuo en el filtro se enjuagó varias veces con pequeñas cantidades de ácido nítrico caliente (50 °C) de concentración 2 mol/L.
Determinación de cadmio y plomo
Para el análisis del contenido de cadmio y plomo en las muestras se empleó un espectrómetro de absorción atómica marca PG-990. Las longitudes de onda utilizadas fueron 228,8 y 283,3 nm, respectivamente, para cada metal. Las condiciones de operación establecidas fueron 30 min de calentamiento; corriente de las lámparas de 5 mA; paso de banda de 0,4 y 0,2 nm; altura del quemador 6 mm (ángulo de inclinación de 45°); tipo de llama oxidante aire/acetileno; flujo de aire igual a 6 L/min, y de acetileno igual a 1,2 L/min; precisión tres mediciones, y tiempo de integración 3 s.
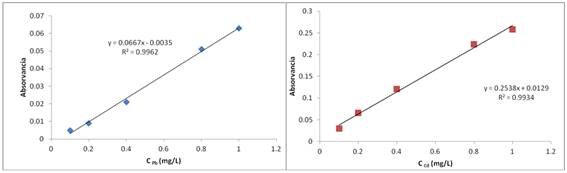
La curva de calibración instrumental se realizó con los estándares de 0,10; 0,20; 0,40; 0,80 y 1,00 mg.L-1, preparados a partir de la disolución patrón de Cd y Pb de concentración de 10 mg.L-1,la cual se preparó de la disolución madre de 1000 mg.L-1. En la figuras 1 se muestran las curvas de calibración del plomo (a) y el cadmio (b).
Implementación de los sistemas experimentales
Se montaron dos sistemas experimentales a escala de laboratorio de 0,45 m de largo; 0,33 m de ancho, y 0,20 m de profundidad, colocando como sustrato en uno de los sistemas experimentales el suelo oscuro plástico gleysoso, y en el otro el suelo pardo con carbonatos, ambos suelos procedentes de la zona contaminada (figura 2). Se sembró la planta Romerillo americano (Helenium quadridentatum Labill), extraída de un suelo no contaminado. Se realizó la determinación de cadmio y plomo en el suelo y en la planta antes de montar el experimento y al cabo de los seis meses de sembrada la planta.
Evaluación en el sitio contaminado
La evaluación de la asimilación de metales en el sitio contaminado se realizó en el suelo pardo con carbonato, más contaminado. Se sembró la planta Romerillo americano, extraída de un suelo no contaminado. A los seis meses de sembrada, cuando las plantas alcanzaron una madurez total, estas fueron cosechadas y se les realizaron los mismos análisis que para el sistema fitorremediador experimental.
Coeficientes biológicos de fitorremediación
La evaluación del potencial de fitorremediación en suelos expuestos a metales, utilizando especies de plantas que asimilan los mismos, se puede estimar determinando los coeficientes biológicos de fitorremediación en suelos.
Factor de bioconcentración, el cual relaciona la concentración del metal en la raíz entre la concentración del metal en el suelo.10-11
El coeficiente de absorción biológico, el cual relaciona la concentración del metal en la raíz entre la concentración del metal en el suelo.11-12
El factor de translocación biológico o de transferencia biológica (BT), el cual asocia la concentración de metal en la raíz entre la concentración del metal en las hojas 12,14-16
El factor de remediación (RC), que es la proporción del elemento contenido en la parte aérea de la planta con respecto a la superficie del suelo.17
Resultados y discusión
Evaluación de la remoción de cadmio y plomo en los suelos de los sistemas fitorremediadores experimentales
Al cabo de los seis meses de sembradas las plantas en los suelos contaminados, se obtuvieroin eficiencias de remoción superiores al 80 % (tabla 1), observándose una mayor concentración de plomo que de cadmio en ambos suelos, y una mayor contaminación por estos metales en el suelo pardo.
Tabla 1 Concentración total de cadmio y plomo en los suelos
| Antes | Después | Eliminado | % Remoción | |
|---|---|---|---|---|
| Cadmio (mg/kg de suelo) | ||||
| Suelo pardo | 30,64 | 5,08 | 25,56 | 83,4 |
| Suelo oscuro | 24,35 | 3,96 | 20,39 | 83,7 |
| Plomo (mg/kg de suelo) | ||||
| Suelo pardo | 165,36 | 21,2 | 144,16 | 87,2 |
| Suelo oscuro | 102,2 | 12,3 | 89,9 | 88,0 |
En el análisis realizado a las plantas de Romerillo americano antes de ser sembradas en el sistema fitorremediador experimental, no se detectaron concentraciones de los dos metales evaluados. Sin embargo, al cabo de los seis meses de sembradas, se observó que presentan concentraciones de Cd y Pb en todos sus órganos. En la tabla 2 se muestran las concentraciones totales de metales en las plantas. La planta sembrada en el suelo pardo con carbonato presentó una mayor concentración de los dos metales evaluados, resultado esperado por la mayor contaminación de este suelo con respecto al oscuro.
Tabla 2 Concentración total de metales asimilados por la planta
| C Total metales | Concentración asimilada por la planta (suelo pardo) | Concentración asimilada por la planta (suelo oscuro) |
|---|---|---|
| Cd (mg/kg) | 25,38 | 18,67 |
| Pb (mg/kg) | 139,00 | 90,25 |
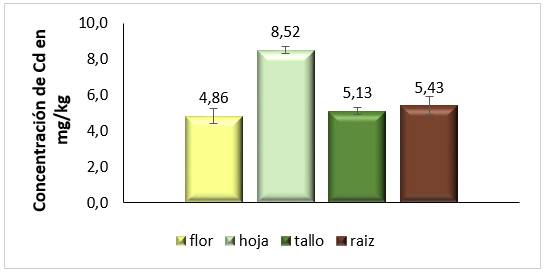
Como se observa en la figura 3, el contenido de Cd en la planta sembrada en el suelo pardo, se encuentra de forma equitativa en todos los órganos, siendo menor en la flor. Estos resultados evidencian la ocurrencia simultánea de los diferentes mecanismos de fitorremediación.

Fig. 3 Concentraciones promedio de Cd en los diferentes órganos de la planta sembrada en el suelo pardo con carbonato
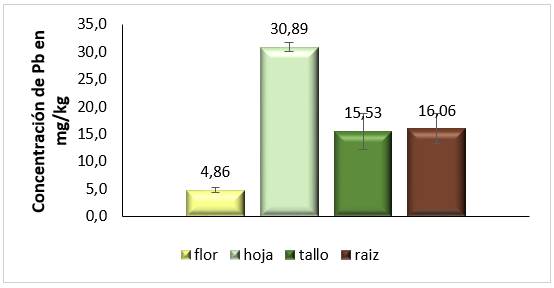
La concentración de plomo en las plantas sembradas en el suelo pardo fue superior en las hojas y las raíces (figura 4), evidenciando una asimilación del metal por la planta, al ser estos órganos los que mayor influencia tienen en la fitorremediación, ya que se reporta que el tallo funciona como transporte del metal hacia las zonas aéreas de la planta.18,19
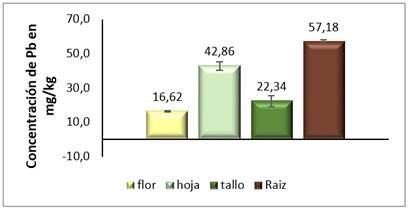
Fig. 4 Concentraciones promedio de Pb en los diferentes órganos de la planta sembrada en el suelo pardo con carbonato
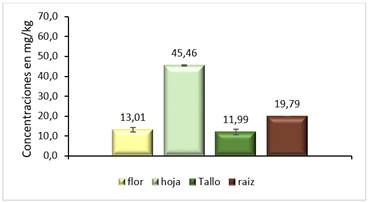
Al analizar los resultados obtenidos en las plantas sembradas en el suelo oscuro, se observa que la concentración de Cd es similar en todos los órganos de la planta, aunque en las hojas el contenido de este metal es ligeramente superior (figura 5). El contenido de Pb en la planta se comporta de forma similar al del Cd (figura 6), aunque en mayor proporción,lo que evidencia que esta planta asimila dicho metal.
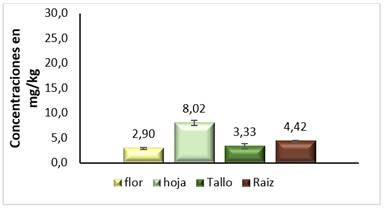
Fig. 5 Concentraciones promedio de Cd en los diferentes órganos de la planta sembrada en el suelo oscuro plástico gleysoso
Evaluación de la remoción de cadmio y plomo en el sitio contaminado
Como se muestra en la tabla 3, las concentraciones de cadmio y plomo obtenidas en el suelo pardo en la experimentación in situ, antes de la siembra del Romerillo americano, fueron similares a las obtenidas en el sistema fitorremediador experimental, con eficiencias de remoción de cadmio superiores al 80 %, y de plomo superior al 60 %, lo que coincide con lo obtenido anteriormente en el sistema experimental. Se obtuvo una menor remoción de plomo en la experimentación in situ, aunque se logró una concentración final por debajo de la concentración de fondo para suelos cubanos.19
Tabla 3 Concentración total de metales en el suelo pardo en el experimento in situ
| Metales (mg/kg de suelo) | Antes | Después | Eliminado | % Remoción |
|---|---|---|---|---|
| Cadmio | 28,97 | 4,75 | 24,22 | 83,6 |
| Plomo | 125,36 | 45,24 | 80,12 | 63,9 |
Después de seis meses de sembradas en el sitio contaminado, se detectaron concentraciones de Cd y Pb en todos los órganos de las plantas, lo que está en correspondencia con la presencia de dichos metales en el suelo (tabla 4). La concentración de cadmio fue similar a la obtenida en el sistema fitorremediador, pudiendo ser esta la concentración de este metal asimilable por la planta. Sin embargo, se obtuvo menores concentraciones de plomo que en el sistema fitorremediador.
Tabla 4 Concentración total de metales en el romerillo americano
| Metal | Cadmio | Plomo |
|---|---|---|
| CTotal(mg/kg) | 23,94 ± 5,64 | 67,34 ± 9,53 |
En la figura 7 se muestran las concentraciones promedio de Cd en los diferentes órganos de la planta. Se observa una mayor concentración de este metal en las hojas, comportamiento diferente al obtenido en el sistema fitorremediador, donde la mayor concentración de cadmio se acumula en la raíz.
El plomo asimilado en los diferentes órganos del Romerillo americano presentó un comportamiento similar al cadmio (figura 8), obteniéndose una mayor concentración en las hojas. La mayor concentración de este metal en el suelo condiciona una mayor concentración en los diferentes órganos de la planta que la obtenida para el cadmio, sin embargo, se obtuvo una menor concentración de este metal en todos los órganos de la planta con respecto a las obtenidas en el sistema fitorremediador experimental.
Coeficientes biológicos de fitorremediación
Los coeficientes biológicos de fitorremediación determinados en los sistemas experimentales (tabla 5) muestran que el Romerillo americano (HeleniumquadridentatumLabill) presenta capacidad de biacumular el cadmio y el plomo existentes en ambos suelos, con todos los coeficientes biológicos mayores a uno, excepto en el coeficiente de absorción biológica en la raíz para el plomo, que presenta valores muy cercanos a uno. Estos resultados se corresponden con los obtenidos por Bolaños y colaboradores 20 en otras especies de plantas estudiadas.
Tabla 5 Coeficientes de fitorremediación paraHeleniumquadridentatumLabillen los sistemas fitorremediadores experimentales
| Coeficientes biológicos | Suelo pardo | Suelo oscuro | |||
|---|---|---|---|---|---|
| Cd | Pb | Cd | Pb | ||
| Factor de bioconcentración(planta/suelo) | 5,17 | 6,56 | 13,24 | 5,28 | |
| Factor de translocación biológico (aérea/raíz) | 2,17 | 1,43 | 3,22 | 2,74 | |
| Factor de remediación (aérea/suelo) | 3,42 | 3,86 | 3,60 | 4,41 | |
| Coeficiente de absorción biológica en la raíz (raíz/suelo) | 1,75 | 2,70 | 1,12 | 0,87 | |
El comportamiento de los coeficientes de fitorremediación obtenidos en los experimentos desarrollados en el sitio contaminado (tabla 6) es similar a los obtenidos en el sistema fitorremediador para el suelo pardo, en correspondencia con las concentraciones de metales existentes en este suelo. Se observa un coeficiente de absorción biológica en la raíz menor a uno para el plomo, lo que está en correspondencia con las mayores concentraciones de plomo obtenidas en las hojas con respecto a la raíz, mostrando la capacidad de la planta para asimilar este metal.
Tabla 6 Coeficientes de fitorremediación para HeleniumquadridentatumLabill en el sitio contaminado
| Coeficientes biológicos | Cadmio | Plomo |
|---|---|---|
| Factor de bioconcentración(planta/suelo) | 5,04 | 1,56 |
| Factor de translocación biológico (aérea/raíz) | 3,41 | 3,19 |
| Factor de remediación (aérea/suelo) | 3,90 | 1,19 |
| Coeficiente de absorción biológica en la raíz(raíz/suelo) | 1,14 | 0,37 |
Conclusiones
El Romerillo americano, a los seis meses de sembrado enlos sistemas experimentales, asimiló una elevada concentración de cadmio y plomo en sus diferentes órganos, disminuyendo la concentración de estos metales en los suelos contaminados. La concentración total de cadmio asimilada por la planta fue similar en el sistema fitorremediador (23,39 mg/kg), y en el sitio contaminado (23,94 mg/kg), indicando lo que puede ser asimilado por la planta.Los coeficientes biológicos de fitorremediación determinados muestran que el Romerillo americano presenta capacidad de biacumular el cadmio y el plomo existentes en ambos suelos.