Introducción
En las últimas décadas, el empleo de hongos superiores con propiedades terapéuticas, ha sido de interés por parte de la comunidad científica a nivel mundial. Esto se debe a que los mismos presentan propiedades nutricionales y medicinales con potencialidades en la industria médico-farmacéutica, biotecnológica y alimentaria.
En cuanto a la composición micoquímica, las setas comestibles son ricas en vitaminas, como, tiamina, riboflavinas, niacina, biotina, ácido ascórbico; presentan lípidos (mono, di y triglicéridos, esteroles y fosfolípidos; proteínas y glicoproteínas; fibra dietética y polisacáridos.1
Diversos estudios muestran que los hongos comestibles medicinales, poseen varias propiedades bioactivas, principalmente como antioxidante, antinflamatorio, anticancerígeno, inmunomodulador, antimicrobiano, hepatoprotector y antidiabético.2 En este sentido, los mismos son considerados como alimentos funcionales y pueden ser consumidos para prevenir y tratar muchas enfermedades crónicas, como el cáncer, diabetes mellitus y desórdenes neurodegenerativos.3
Dichas propiedades se deben a que los hongos comestibles medicinales, pueden producir abundantes metabolitos funcionales, como polisacáridos, terpenos, esteroides y compuestos fenólicos 4, con importantes beneficios para la salud, por lo que constituyen una fuente promisoria para el descubrimiento de nuevos compuestos de interés farmacológico.5
De manera general, los compuestos de hongos comestibles medicinales, actúan sinérgicamente con los receptores de las membranas celulares para activar diversos eventos de señalización que conducen a una alta eficiencia y especificidad farmacológica.6 Por otro lado, los metabolitos bioactivos de hongos comestibles medicinales se pueden obtener de diferentes fuentes, ya sea en estado silvestre o cultivados comercialmente, a partir de cuerpos fructíferos o de la biomasa micelial.7,8
Uno de los compuestos que en la actualidad resultan más atractivos para el tratamiento de diferentes patologías relacionadas con el estrés oxidativo, son los fenoles. Los mismos son compuestos aromáticos con uno o más anillos a los que se une directamente uno o más grupos hidróxilos. Ellos presentan un largo número de subclases, entre las cuales se encuentran flavonoides, ácidos fenólicos, incluyendo ácidos hidrobenzoico e hydroxicinámico, lignanos, taninos, polifenoles oxidados, entre otros, desplegando una gran diversidad de estructuras y funciones.9,10
Los fenoles, además de sus acciones protectoras en los sistemas biológicos, muestran actividad antioxidante, pudiendo interactuar con diferentes proteínas involucradas en la cascada redox.
En particular los compuestos fenólicos provenientes de hongos comestibles medicinales, muestran excelente capacidad antioxidante.11
Resulta importante evaluar las interacciones de los fenoles con los centros activos de determinadas proteínas involucradas en procesos biológicos de interés farmacológico, a través de enfoques que permitan ahorrar tiempo y recursos materiales, con resultados efectivos y seguros.
Para ello, se presenta el docking molecular, el que es utilizado frecuentemente para predecir la orientación de los enlaces de fármacos o sustancias candidatas con sus proteínas blancos, en aras de pronosticar la afinidad y actividad de la pequeña molécula. De ahí que el docking molecular juegue un rol importante en el diseño de fármacos.12
Dentro del grupo de setas comestibles- medicinales, figura el género Pleurotus sp. con alto valor nutricional y propiedades terapéuticas, además de presentar aplicaciones biotecnológicas y ambientales.
Al respecto, el Centro de Estudios de Biotecnología Industrial (CEBI), de la Universidad de Oriente ha desarrollado estudios in vitro e in vivo sobre la actividad inmunomoduladora y antitumoral de la especie Pleurotus ostreatus, sin embargo, no se han confirmado aún las estructuras químicas de los compuestos presentes en esta seta, ni se han completado los estudios de su potencial actividad biológica.
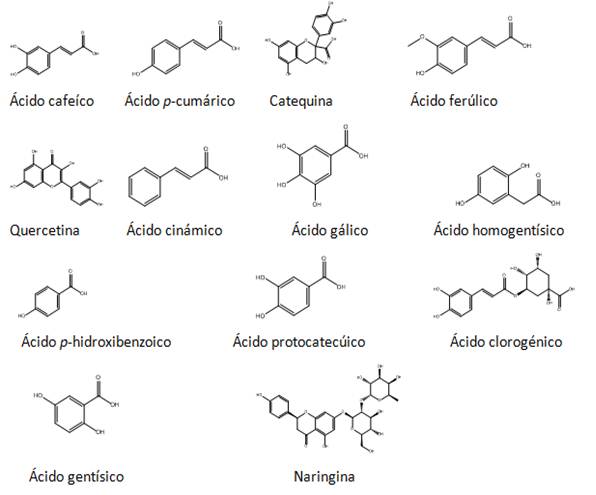
Diversos autores refieren que Pleurotus ostreatus, presenta diversidad de compuestos fenólicos, los cuales varían teniendo cuenta los factores ambientales de sus condiciones de cultivo.13 Dentro de los compuestos fenólicos más destacados se encuentran, el ácido p- cumárico, ácido felúrico, ácido gálico, ácido gentísico, ácido p- hidroxibenzoico, ácido homogentísico, mirecitina y ácido protocatecuico.13
Otros autores, sin embargo, reportan para dicha especie, la presencia de ácido cafeíco 14; ácido cinámico 15 y ácido vanílico.16
En general se plantea que los principales compuestos fenólicos encontrados en hongos son los ácidos fenólicos.17
En la actualidad, en nuestro grupo de investigación se necesitan evidencias experimentales que fundamenten, la potencial actividad antioxidante de esta seta. Es conocido la presencia de compuestos fenólicos en Pleurotus ostreatus, por lo que estos compuestos podrían interactuar directamente con proteínas del balance redox como: NFKB, NADPH-oxidasa y COX-2.
Tomando en consideración estos elementos, el objetivo del presente trabajo es realizar un estudio in silico a través de un docking molecular, sobre el potencial antioxidante de compuestos fenólicos de Pleurotus ostreatus con proteínas del balance redox.
Materiales y métodos
Recursos computacionales
Los cálculos fueron realizados basados en los recursos computacionales del Cluster del Departamento de Química de la Facultad de Ciencias Naturales y Exactas. Se utilizó el sistema operativo Linux distribución Debian 7.0.
Modelación molecular de proteínas y ligandos para el acoplamiento molecular
Para la representación de las estructuras de los fenoles (Figura 1), se empleó el programa Chem Draw Professional 15.0. El programa Chem3D 15.0, permitió la optimización de la geometría de los mismos, utilizando el método de mecánica molecular MM2 y MMFF94 (en inglés Merck Molecular Force Field).
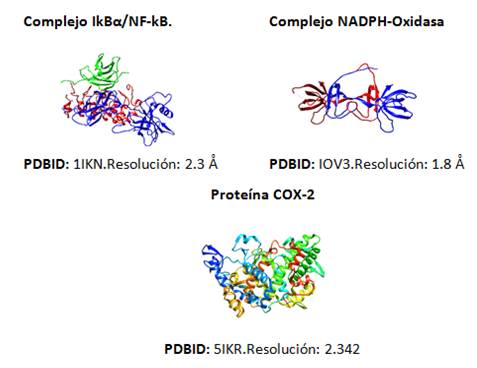
Por su parte, para la modelación molecular de las proteínas se obtuvieron sus estructuras tridimensionales en formato .pdb (figura 2), provenientes de la Base de Datos de Proteínas (en inglés Protein Data Bank), la cual es de acceso gratuito.18 El programa UCSF Chimera versión 1.10.227 19 se utilizó para identificar todos los residuos que no pertenecían a las proteínas y podían interferir con sus centros activos.
El estudio de acoplamiento molecular se llevó a cabo a través de los programas AutoDock 4.2 y AutoDockTools 1.5.6, los cuales son de libre y gratuito acceso. La visualización de las interacciones hidrofóbicas y por puente de hidrógeno de los complejos, se efectuó por el programa Ligplot 20 (figuras 3, 4, 5).
Las proteínas seleccionadas participan en algunos de los mecanismos generadores de especies reactivas de oxígeno o desencadenando procesos que tienen relación directa con el funcionamiento del balance redox.
La proteína NFKB es un complejo proteico, denominado factor nuclear potenciador de las cadenas ligeras Kappa de las células B activadas, el cual controla la transcripción del ADN. Esta proteína está implicada en la respuesta celular frente a estímulos como el estrés; su regulación defectuosa se relaciona con el cáncer, enfermedades inflamatorias y autoinmunes. Presenta un principal inhibidor a nivel de citoplasma, denominado IKBα.
La ciclooxigenasa 2 o COX-2 es una proteína de membrana periférica, situada en la membrana de microsomas y retículo endoplasmático. Participa en la síntesis de los prostanoides. En los humanos se expresa en un número limitado de tipos celulares y se regula por estímulos específicos. Dicha proteína es inducible a determinadas citocinas proinflamatorias, promotores tumorales o factores de crecimiento.
La NADPH-oxidasa está constituida por un complejo enzimático multiproteíco de cinco subunidades, distribuidas en el citoplasma, las membranas citoplasmáticas y las vesículas fagocíticas. La activación de la misma se caracteriza por un aumento en el consumo de oxígeno molecular y tiene como objetivo la liberación del radical anión superóxido dentro de la vacuola fagocítica o al medio extracelular.
Preparación del centro Grid y Acoplamiento molecular
El programa AutoDock requiere de la realización de un pre-cálculo de los mapas grid para cada tipo de elemento presente en la macromolécula, ubicando el ligando alrededor de la región de interés (sitio activo) en la macromolécula. En la tabla 1 se muestran las coordenadas y tamaño de la caja grid del sitio activo para las proteínas de estudio.
Tabla 1 Coordenadas y tamaño de la caja grid para las proteínas de estudio
| Proteínas | Coordenadas | Espaciado | Tamaño (puntos) | ||
|---|---|---|---|---|---|
| X | Y | Z | |||
| 1IKN (CYS215) | 33,414 | 34,35 | 21,325 | 0,375 | 60 x 60 x 60 |
| 1IKN (THR247) | 43,871 | 31,76 | 22,269 | 0,375 | 60 x 60 x 60 |
| IOV3(TRP193) | 56,003 | 46,427 | 29,035 | 0,375 | 60 x 60 x 60 |
| 5IKR(SER530) | 37,47 | 8,659 | 62,383 | 0,375 | 60 x 60 x 60 |
El Algoritmo Genético Lamarckiano (LGA) fue utilizado para explorar el mejor espacio conformacional para el ligando, con 50 corridas para cada uno de los acoplamientos.
Resultados y discusión
Análisis del acoplamiento molecular de los fenoles con las proteínas de estudio
Los compuestos fenólicos son antioxidantes, lo cual les permite actuar como agentes reductores, donadores de hidrógeno, captadores de radicales libres y quelantes del oxígeno singlete.21
En el presente trabajo se evaluó la proteína NFKB, frente a los trece fenoles seleccionados. En la tabla 2, aparecen los valores de las energías libres de unión (ΔG en kcal/mol) y los valores de la constante de inhibición (Ki en μM) del complejo proteína- fenol. El Complejo IkBα/NF-kB presenta dos sitios activos (1IKN Cisteína 215 y 1IKN THR247).
Tabla 2 Resultados del acoplamiento molecular entre los fenoles y el Complejo IkBα/NF-kB
| Ligando | 1IKN (CYS215) | 1IKN (THR247) | |||
|---|---|---|---|---|---|
| ΔG (Kcal/mol) | Ki (µM) | ΔG (Kcal/mol) | Ki (μM) | ||
| Ácido cafeíco | -5,30 | 131,29 | -5,72 | 64,33 | |
| Ácido |
-5,34 | 121,84 | -5,58 | 81,48 | |
| Ácido ferúlico | -5,44 | 103,69 | -5,83 | 53,62 | |
| Quercetina | -6,68 | 12,62 | -5,96 | 43,13 | |
| Catequina | -6,02 | 38,93 | -6,27 | 25,38 | |
| Ácido cinámico | -5,04 | 203,37 | -5,42 | 106,14 | |
| Ácido gálico | -4,47 | 530,21 | -5,29 | 133,28 | |
| Ácido homogentísico | -5,25 | 141,5 | -5,13 | 173,53 | |
| Ácido |
-4,66 | 385,89 | -5,18 | 159,16 | |
| Ácido protocatecúico | -4,78 | 311,84 | -5,64 | 74,00 | |
| Ácido clorogénico | -5,57 | 82,53 | -5,86 | 50,98 | |
| Ácido gentísico | -4,56 | 456,47 | -4,81 | 297,51 | |
| Naringina | -6,76 | 11,13 | -5,34 | 120,92 | |
En la tabla 2, se observa como los fenoles presentan una selectividad moderada frente al Complejo IkBa/NF-kB, atendiendo a que los valores de las energías de unión y de las constantes de inhibición calculadas están en los rangos medios. Los valores más adecuados de las interacciones de los fenoles con la proteína, muestran una mayor afinidad por el sitio activo 1IKN Cisteína 215, con un rango de energía de unión entre -4,47 y -6,76 kcal/mol y una constante de inhibición en el rango entre 11,13 y 530,21 μM, no siendo así para el caso de1IKN Treonina 247, donde el rango de energía de unión esta entre -5,34 y -6,27 kcal/mol y el de la constante de inhibición entre 25,38 y 297,51 μM. La naringina es la que presenta mayor selectividad frente al sitio activo 1IKN Cisteína 215, mientras que la quercetina y catequina poseen una buena selectividad en ambos sitos activos.
Algunos autores como 22, demostraron que diferentes extractos de hongos ejercen sus efectos en la ruta de activación del NFKB, mediante tres mecanismos: por inhibición de la fosforilación del IKBα, por inhibición de la degradación del IKBα o por ambos.
Otros autores 23, mostraron que tres compuestos derivados de la seta Phellinus baumii inhibieron la fosforilación de Ikk α y IKBα.
De manera general los polifenoles pueden modular la actividad de la NFkB, mostrando efectos neuroprotectores.24
En este caso, las sustancias de bajo peso molecular de origen fúngico, pueden penetrar la membrana celular e interferir en particular, en rutas celulares relacionadas con procesos como inflamación, carcinogénesis, diferenciación y supervivencia celular, metástasis, etc. Los hongos medicinales se han establecido como una nueva y promisoria fuente de terapéuticos naturales que pueden ser aplicados en el tratamiento de diferentes enfermedades, incluido el cáncer.25
Otra de las proteínas de interés en esta investigación es la NADPH-oxidasa. En el estudio, los fenoles evaluados con la proteína NADPH-oxidasa tienen una fortaleza de unión de débil a moderada, con un rango de energía de unión entre -3,73 y -6,31 kcal/mol y una constante de inhibición entre 1,19 y 674,38 μM (tabla 3).
Tabla 3 Resultados del acoplamiento molecular entre los fenoles y el Complejo NADPH-oxidasa
| Ligando | IOV3(TRP193) | ||
|---|---|---|---|
| ΔG (Kcal/mol) | Ki (µM) | ||
| Ácido cafeíco | -5,09 | 185,48 | |
| Ácido |
-4,58 | 437,01 | |
| Ácido ferúlico | -4,98 | 222,59 | |
| Quercetina | -6,31 | 23,52 | |
| Catequina | -6,15 | 30,83 | |
| Ácido cinámico | -4,64 | 399,42 | |
| Ácido gálico | -3,99 | 1,19 | |
| Ácido homogentísico | -4,61 | 415,49 | |
| Ácido p-hidroxibenzoico | -3,73 | 1,85 | |
| Ácido protocatecúico | -4,31 | 694,57 | |
| Ácido clorogénico | -5,01 | 213,69 | |
| Ácido gentísico | -4,33 | 674,38 | |
| Naringina | -5,32 | 125,86 | |
La quercetina y catequina, mostraron mayor selectividad frente a IOV3 Triptófano 193.
Es conocido que uno de los mecanismos a través de los cuales los flavonoides ejercen su acción antioxidante es a través de la inhibición de actividades de las oxidasas, tal es el caso de la quercetina con la NADPH oxidasa, evitando la generación de especies reactivas de oxígeno (EROs) in vivo y la acción sobre enzimas que están involucradas indirectamente en los procesos oxidativos.26
Para el caso de la proteína COX-2, los resultados refieren una mejor afinidad entre los fenoles y la proteína. En este sentido, los fenoles mantienen su fortaleza de unión de débil a moderada, con un rango de energía de unión entre -1,34 y -6,99 kcal/mol y una constante de inhibición entre 7,47 y 155,72 μM (tabla 4).
En estudios de acoplamiento molecular realizados por 27, se utilizaron diferentes compuestos de bajo peso molecular de hongos comestibles frente a seis proteínas relacionadas con procesos de inflamación, entre las que se encontraba la COX-2. Los resultados fueron adecuados para el caso del ácido iludacético derivado de Omphalotus olearius. El ácido iludacético interactuó con la proteína COX-2 en un enlace de por puente de hidrógeno en el residuo Ser 530, con un valor de ΔG de -8,42 Kcal/mol. En el presente estudio los fenoles que mostraron mayor selectividad frente a 5IKRSerina 530 de la proteína COX-2, fueron la quercetina, catequina y ácido cinámico.
La proteína COX-2 se ve incrementada en ciertos tipos de tumores sólidos como cáncer gástrico pancrático y esofagal. Al respecto, los flavonoides han mostrado actividad antiproliferativa y anticarcinogénica, así como efecto quimiopreventivo.28
En experimentos in vitro se ha confirmado el papel protector de la quercetina, la cual ejerce efectos de inhibición frente a células cancerígenas en humanos: en colon 29 y región gastrointestinal.30
En otros estudios, por ejemplo, se ha demostrado como la quercetina puede inhibir la enzima aromatasa que está relacionada con el cáncer de cuello uterino.31
Tabla 4 Resultados del acoplamiento molecular entre los fenoles y la Proteína COX-2
| Ligando | 5IKR(SER530) | ||
|---|---|---|---|
| ΔG (Kcal/mol) | Ki (µM) | ||
| Ácido cafeíco | -5,97 | 42,34 | |
| Ácido |
-6,07 | 35,33 | |
| Ácido ferúlico | -6,20 | 28,54 | |
| Quercetina | -6,99 | 7,47 | |
| Catequina | -6,31 | 23,56 | |
| Ácido cinámico | -6,42 | 19,65 | |
| Ácido gálico | -5,19 | 155,72 | |
| Ácido homogentísico | -5,72 | 63,94 | |
| Ácido p-hidroxibenzoico | -5,40 | 110,87 | |
| Ácido protocatecúico | -5,60 | 78,74 | |
| Ácido clorogénico | -6,05 | 36,64 | |
| Ácido gentísico | -5,82 | 54,47 | |
| Naringina | -1,34 | 104,83 | |
Análisis de las interacciones de las proteínas estudiadas con los mejores ligandos
Al analizar la proteína 1IKN - Complejo IkBa/NF-kB,se observan valores semejantes de energía y constante de inhibición entre la quercetina y naringina, debido a que las interacciones por puentes de hidrógeno son muy similares. El ligando naringina presenta cinco interacciones por puente de hidrógeno y doce interacciones hidrofóbicas, lo cual justifica que presente valores adecuados de Ki de los tres fenoles seleccionados (tabla 5).
Tabla 5 Interacciones del Complejo IkBa/NF-kB con los mejores ligandos
| Complejo IkBa/NF-kB | ||||
| Ligandos | PDBID | ΔG (kcal/mol) | Ki (µM) | Interacciones (Cys215) |
| Quercetina | 1IKN | -6,68 | 12,62 | GLU265; ASN200; ARG201; GLU211; ARG253 ILE266;ARG255;ASP254;ASP210 |
| Catequina | 1IKN | -6,02 | 38,93 | PRO344; THR256; SER326; LEU346; THR179 PRO214;LYS343;PHE345;ASN180;TYR181 |
| Naringina | 1IKN | -6,76 | 11,13 | THR256; LYS343; PRO342; THR179;GLN212 GLY183;ASN180;LEU346;SER326;ASN182; TYR181;ALA257;PRO214;PRO344;TRY248; GLU213;ALA211 |
Con respecto a la proteína IOV3 - Complejo NADPH-oxidasa, los valores de energía y constante de inhibición entre la quercetina y catequina resultaron semejantes, sin embargo, el ligando catequina presenta seis interacciones por puente de hidrógeno, con una menor energía de unión. La quercetina presenta mayor número de grupos funcionales, con puentes de hidrógenos más cercanos al sitio activo de la proteína. Esto provoca una mayor fortaleza en la unión entre el ligando y la proteína (tabla 6).
Tabla 6 Interacciones del Complejo NADH-oxidasa con los mejores ligandos
| Complejo NADPH-oxidasa | ||||
| Ligandos | PDBID | ΔG (kcal/mol) | Ki (µM) | Interacciones |
| Quercetina | IOV3 | -6,31 | 23,52 | SER208; GLY192; SER191; TYR279 PHE209;PRO206;ASP261;TRP263;PRO276; MET278 |
| Catequina | IOV3 | -6,15 | 30,83 | ASP261;TRP263;GLY262;SER277;MET278; TRP193 PHE209;PRO206;GLY192;SER208;PRO276; SER191 |
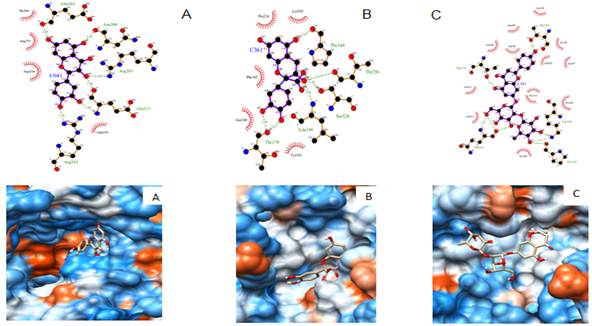
Fig. 3 Principales interacciones 2D y 3D entre el Complejo IkBa/NF-kB y los fenoles: I . A. Quercetina, B. Catequina, C. Naringina
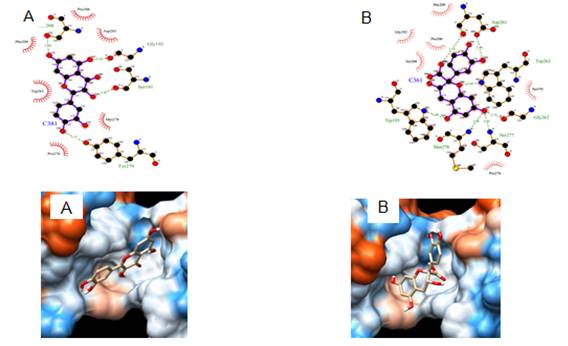
Fig. 4 Principales interacciones 2D y 3D entre el Complejo NADH-oxidasa y los fenoles: A. Quercetina, B. Catequina
En el caso de la proteína 5IKR - Proteína COX-2, se obtuvieron los valores semejantes de energía y constante de inhibición entre la quercetina y catequina. Al respecto, la quercetina muestra cuatro interacciones por puente de hidrógeno, la misma cantidad que el ligando quercetina, sin embargo, los puentes de hidrógeno que forma la quercetina se encuentran más cerca del sitio activo de la proteína, lo que provoca una mayor fortaleza en la unión (tabla 7).
Tabla 7 Interacciones de la Proteína COX-2 con los mejores ligandos
| ProteínaCOX-2 | ||||
| Ligandos | PDBID | ΔG (kcal/mol) | Ki (µM) | Interacciones |
| Quercetina | 5IKR | -6,99 | 7,47 | MET522; TYR385; SER530; TYR355 LEU384;GLY526;ALA527;ARG120;VAL116; LEU531;VAL349;TRP387 |
| Catequina | 5IKR | -6,31 | 23,56 | TYR385; VAL349; SER530; TYR355 TRP387;PHE381;MET522;VAL523;SER533; ARG120; VAL116;LEU531;ALA527;LEU352 |
| Ácido cinámico | 5IKR | -6,42 | 19,65 | GLN374 ASN375;PRO128;SER126;THR149;ASP125; ARG150; ALA151;ALA378;PHE529;ILE124; LYS 532 |
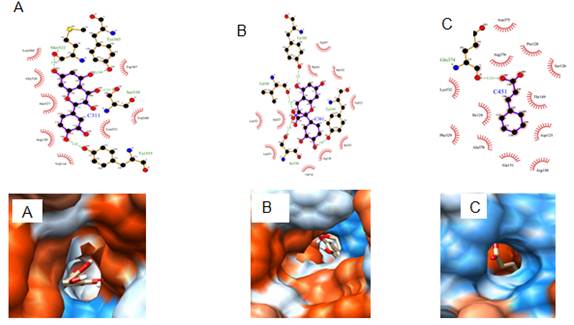
Fig. 5 Principales interacciones 2D y 3D entre 5IKR COX-2 y los fenoles: A. Quercetina, B. Catequina, C. Ácido cinámico
Algunos de los mecanismos celulares involucrados en la producción de estrés oxidativo, incluyen respuesta inflamatoria, generación de radicales libres a partir de mitocondrias y actividades prooxidantes de compuestos tóxicos.
En este sentido, las sustancias de bajo peso molecular de origen fúngico, pueden penetrar la membrana celular e interferir en particular, en rutas celulares relacionadas con procesos como inflamación, carcinogénesis, diferenciación y supervivencia celular, metástasis, entre otros. Los hongos comestibles medicinales se han establecido como una nueva y promisoria fuente de terapéuticos naturales que pueden ser aplicados en el tratamiento de diferentes enfermedades, consideradas como crónicas no trasmisibles y cuya base se sustenta por desbalances en los mecanismos que regulan el equilibrio redox en el organismo.
Conclusiones
Las magnitudes químico- físicas evaluadas en el complejo fenol-proteína, permitieron establecer que las interacciones estuvieron en el rango de aceptable a moderada, con valores de ΔG y Ki de -6 kcal/mol y 10-5M respectivamente.
Dentro de las interacciones evaluadas, dos de los ligandos, quercetina y catequina, mostraron resultados promisorios, con una energía de unión y una constante de inhibición aceptable