INTRODUCCIÓN
Según De la Cruz (2019) las cuencas hidrográficas son grandes unidades naturales donde se plasma el ciclo hidrológico en los continentes, siendo el agua el elemento central. Teniendo en cuenta el criterio natural del drenaje, la cuenca hidrográfica está estructurada por una red de corrientes o cauces y a su vez se pueden clasificar u ordenar. En ese sentido, una cuenca hidrográfica se estructura en una determinada cantidad de subcuencas que serían sus contribuyentes o afluentes. Es decir, en una cuenca o subcuenca existirá solo un curso de agua de mayor nivel que recibe aportes de otras corrientes.
Una cuenca hidrográfica alto andina normalmente consta de tres partes. Las partes altas comprenden altitudes superiores a los 3000 metros sobre el nivel del mar (msnm), llegando en algunos casos hasta los 6500 msnm. Las partes medias son las comprendidas entre los 800 y 3000 msnm. Por su parte las partes bajas abarcan desde el nivel del mar hasta los 800 msnm. En estas zonas se ubican los grandes proyectos de irrigación con importantes sistemas de embalse. El potencial de aguas subterráneas de estas zonas es alto (Vásquez y col., 2016).
Dentro de una cuenca hidrográfica se desarrolla las principales actividades económicas y productivas como la agricultura, ganadería, minería, entre otras industrias que utilizan las aguas de los ríos en sus diferentes procesos, siendo el agua fundamental en la obtención de la materia prima o en la transformación de esta. Sin embargo, en algunos casos no hay tratamientos adecuados para devolver estas aguas residuales de forma óptima a los cuerpos naturales, ocasionando una contaminación en los ríos que va a ser caracterizada por las diferentes actividades socioeconómicas que las generan, así como de otras condiciones propias del medio.
Entre los principales vectores de impactos ambientales causados por las actividades económicas se encuentran los cambios en la cantidad y calidad de los flujos continentales de agua, sedimentos y sus constituyentes químicos hacia el océano a través de los ríos. Asimismo, los ríos representan el principal vínculo entre el continente y el mar en la mayoría de los ciclos biogeoquímicos. Por otro lado, los ríos también son la principal vía de contaminación de las zonas costeras y estuarinas por los contaminantes generados en el continente (De Oliveira y Marins, 2011).
Esta situación podría complejizar la fragilidad ambiental de este ecosistema y los servicios que los ríos podrían brindar en las comunidades en el uso del agua y/o también como fuente de recursos hidrobiológicos como algas, peces, crustáceos, entre otros, que son aprovechables por las personas en muchos casos para consumo directo.
Ante este contexto, es importante realizar monitoreos de agua superficial en los ríos conjuntamente con el monitoreo de los sedimentos, para tener una visión completa de la calidad de este cuerpo natural, y plantear las estrategias integrales para la toma de decisiones en pos de lograr una conservación y/o recuperación del medio.
En esa línea es importante distinguir que, en el caso de los metales, especialmente los metales traza, estos se encuentran entre los contaminantes ambientales más comunes y su comportamiento en varios compartimentos ambientales merece atención, principalmente porque no son degradables, permaneciendo por largos períodos en el ambiente, principalmente en sedimentos y, por lo tanto, representan una amenaza potencial para la biodiversidad, así como para los ecosistemas (De Oliveira y Marins, 2011).
Un metal contaminante importante a mencionar es el arsénico, el cual es un elemento químico que tanto en su estado elemental como sus compuestos son extremadamente tóxicos, especialmente el arsénico inorgánico, que resulta de la combinación del arsénico con el oxígeno, cloro y azufre. Está en la naturaleza en distintas formas (en la tierra y en las rocas); muy pocas veces se lo encuentra en forma sólida. Se puede dispersar en el medio ambiente a través de acción volcánica, erosión de rocas y a través de actividades humanas como la minería o fundición de minerales que contengan arsénico o el desecho de pesticidas (Cabrera y col., 2013).
La norma de la Organización Mundial de la Salud (OMS) permite una concentración máxima de arsénico en aguas destinadas para el consumo humano de 10 µg/L. En Latinoamérica, se estima que por lo menos 4,5 millones de personas beben en forma permanente agua con niveles de arsénico que ponen en riesgo su salud. La cantidad de arsénico en el agua, especialmente en el agua subterránea, llega en algunos casos a superar la concentración de 1 000 µg/L. En Perú, su presencia en las fuentes de agua para consumo humano se puede deber a factores naturales de origen geológico, a la explotación minera y a la refinación de metales por fundición (Medina-Pizzali y col., 2018).
Las concentraciones de arsénico en el agua, sobre todo en el agua subterránea, presentan niveles que llegan en algunos casos hasta 1000 µg/L. En otras regiones del mundo como India, China y a la información obtenida, en India existen alrededor de 6 millones de personas expuestas, de las cuales más de 2 millones son niños. En Estados Unidos más de 350000 personas beben agua cuyo contenido es mayor que. 0,5 mg/L de arsénico, y más de 2,5 millones de personas están siendo abastecidas con agua con tenores de arsénico mayores a 25 µg/L (Cabrera y col., 2013).
Asimismo, el arsénico (As) es un elemento muy común en la atmósfera, en rocas y suelos, en la hidrosfera y la biosfera. Es movilizado al ambiente a través de una combinación de reacciones que incluyen tanto procesos naturales (meteorización, actividad biológica, emisiones volcánicas), así como procesos antropogénicos (actividad minera, uso de combustibles fósiles, pesticidas, herbicidas, desecantes, conservadores de la madera, aditivos de alimento de ganado, semiconductores, pigmentos, entre muchos otros) (Alarcón y col., 2014).
Se han identificado cinco mecanismos naturales de contaminación de fuentes naturales debido al arsénico: actividad volcánica o hidrotermal; meteorización oxidativa de sulfuros arsénicos, típicamente pirita y arseno-pirita; desorción de As desde superficies minerales a pH alto; reducción de oxi-hidróxidos de hierro sedimentario y concentración evaporativa. La presencia de As en aguas de consumo humano en ciertos ríos de México, Nicaragua, Perú, Argentina y Chile e incluso Ecuador se atribuye a factores geológicos (Aveiga y col., 2020).
La presencia de altos niveles de As en el agua es un tema prioritario de preocupación ambiental, que limita el uso del recurso para agua potable y otros propósitos e impide el crecimiento socioeconómico, la sostenibilidad del uso racional de los suelos y el desarrollo sostenible de la agricultura (Falchi y col, 2018).
En ese sentido, se hace necesario estudiar cual es el grado de correlación entre la concentración de metales en los sedimentos y su causalidad en la concentración en aguas superficiales, con el objetivo de determinar si existe algún metal pesado que presente una alta causalidad en la zona. De esta manera se determinara si en un área en específico la concentración del metal en agua se debe mayormente a la presencia de sedimentos que obedecería principalmente a factores geológicos propios de la zona en estudio, sin desconocer que el aporte de concentración de los metales pesados también se pueden originar por otros factores como las fuentes antrópicas.
Es preciso indicar que el presente estudio, no tiene la finalidad de averiguar cuáles son las causas de la presencia de metales pesados en los sedimentos o en las aguas superficiales, solo se limita a identificar si existe correlación y causalidad entre la concentración de sedimentos y el agua superficial de cada metal pesado de relevancia ambiental.
En ese sentido es importante realizar mayores estudios en el área con la finalidad de corroborar que la concentración del arsénico presente en los sedimentos influye en la concentración de arsénico de las aguas en los ríos estudiados.
Por lo tanto, el objetivo del presente estudio es evaluar la concentración de metales en sedimentos y advertir si existe causalidad en la concentración de metales en aguas superficiales, respecto de algún metal de relevancia ambiental.
MATERIALES Y MÉTODOS
Para el presente estudio se utilizó los seis monitoreos de calidad de agua y sedimentos realizados por la Autoridad Nacional del Agua de Perú (en adelante ANA), entre los años 2013 y 2014, cuyos informes son de acceso abierto a través del internet (Política de repositorio ANA, 2019).
Es preciso indicar que los informes de monitoreo de libre acceso del ANA respecto solo a la calidad de las aguas de los ríos se publican periódicamente, sin embargo, los informes que realizaron en calidad de agua y sedimentos en conjunto no se volvieron a publicar desde el año 2014 a la actualidad. La población estará conformada por los sedimentos de seis cuencas hidrográficas de los ríos; Huarmey, Huamansaña, Chicama, Moche, Santa y Virú.
La selección de las muestras para el presente trabajo de investigación ha sido de la forma no probabilística y por conveniencia. Para el criterio de selección de datos, los parámetros a considerar serán 31 metales monitoreados por la ANA, los cuales son: plata, aluminio, arsénico, boro, bario, berilio, calcio, cadmio, cerio, cobalto, cromo, cobre, hierro, mercurio, potasio, litio, magnesio, manganeso, molibdeno, selenio, sodio, níquel, fosforo, plomo, antimonio, estaño, estroncio, titanio, talio, vanadio y zinc.
Para verificar la existencia de correlación entre la calidad del agua superficial y la calidad de sedimento, se utilizó una prueba estadística, determinando en primera instancia si los datos tienen una distribución normal, para elegir una prueba paramétrica o no paramétrica. Para el desarrollo de las pruebas estadísticas mencionadas se hará uso del software IBM SPSS Statistics V.29.
Para las pruebas de correlación bivariadas se utilizó la prueba de Pearson en caso las variables cumplan las condiciones paramétricas, o la prueba de Spearman en caso las variables cumplan las condiciones de no paramétricas. Los resultados se pueden clasificar en correlación débil, media y buena conforme se aprecia a continuación en la tabla 1 (Roy-García y col., 2019).
Es preciso indicar que la correlación entre concentración de metales en sedimentos y agua o viceversa, no indica una causalidad.
Tabla 1 Rangos de correlación
| Valor | Descripción |
|---|---|
| 0 | Sin correlación |
| ± 0,20 | Correlación débil |
| ± 0,50 | Correlación moderada |
| ± 0,80 | Correlación buena |
| 1 | Correlación perfecta |
Para determinar la existencia o no de causalidad de los metales que presentaron un factor de correlación mayor a la correlación moderada de +- 0,50, se les aplicó la regresión polinomial por ser los datos no paramétricos. Se procedió a evaluar el R2 y el p valor. El indicador del R2 brindó el porcentaje de los puntos de muestreo en donde la concentración del metal en agua es influenciada por la concentración del metal presente en los sedimentos, entendiéndose que mientras el valor de R2 se acerque más a uno (100%) la causalidad será mayor. Para realizar las pruebas estadísticas se usó del software IBM SPSS Statistics V.29.
RESULTADOS Y DISCUSIÓN
Se obtuvieron 113 resultados tanto en calidad de agua superficial como de calidad sedimentos para los 31 metales evaluados. Estos datos se consiguieron de los seis Informe de monitoreos del ANA; cuenca del rio Aija- Huarmey (Villegas y col., 2014), cuenca del rio Chao (Malpica y col., 2014), cuenca del rio Chicama (Polo y Serpa., 2014), cuenca del rio Moche (Salbatier y col., 2014), cuenca del rio Santa (Alfaro y col., 2014), y cuenca del rio Viru (Verastegui y col., 2014). En los cuales se consignaron los puntos establecidos con coordenadas de los cuales se obtuvieron muestras de agua superficial y a su vez de sedimentos en el mismo punto o ubicación.
Esta base de datos se obtuvo consignando los valores de concentración en ppm de los 31 parámetros de metales en sedimento (mg/kg) y agua superficial (mg/l), a partir de los seis informes de monitoreo publicados por el ANA, a modo de ejemplo se muestra la base de datos elaborada para el Arsénico en la Tabla 2. De los cuales, se observa que los sedimentos presentan una concentración promedio de arsénico en ppm (mg/l o mg/kg) mucho más elevada que la del agua, siendo la concentración en sedimentos el 610466,667% de concentración del agua, por lo que en la presente investigación se delimitará en la concentración de arsénico en los sedimentos y su influencia en la concentración de arsénico en el agua.
Tabla 2 Concentración de arsénico en sedimentos y agua en ppm (mg/l o mg/kg)
| Metal As | Cuenca del río Aija-Huarmey | Cuenca del río Chao | Cuenca del río Chicama | Cuenca del río Moche | Cuenca del río Santa | Cuenca del río Viru | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Puntos de monitoreo | Agua (mg/l) | Sedimento (mg/kg) | Agua (mg/l) | Sedimen to (mg/kg) | Agua (mg/l) | Sedimento (mg/kg) | Agua (mg/l) | Sedimento (mg/kg) | Agua (mg/l) | Sedimento (mg/kg) | Agua (mg/l) | Sedimento (mg/kg) |
| 1 | 0,001 | 148,1 | 0,001 | 36,2 | 0,001 | 6,2 | 0,001 | 182,4 | 0,002 | 176 | 0,001 | 36,2 |
| 2 | 0,026 | 647,8 | 0,001 | 11,8 | 0,005 | 8 | 0,001 | 24,3 | 0,005 | 279,5 | 0,001 | 11,8 |
| 3 | 0,001 | 290,1 | 0,001 | 6,1 | 0,001 | 5,5 | 0,042 | 756,6 | 0,001 | 38,7 | 0,001 | 6,1 |
| 4 | 0,001 | 52,5 | 0,001 | 20,7 | 0,007 | 26,4 | 0,055 | 281,9 | 0,0204 | 982 | 0,001 | 20,7 |
| 5 | 0,011 | 119 | 0,001 | 2,1 | 0,009 | 40,6 | 0,152 | 366,4 | 0,037 | 28,3 | 0,001 | 2,1 |
| 6 | 0,024 | 221,8 | 0,001 | 1,4 | 0,01 | 39,3 | 0,001 | 14,1 | 0,022 | 85,1 | 0,001 | 1,4 |
| 7 | 0,103 | 806,9 | 0,049 | 17,9 | 0,009 | 38,7 | 0,017 | 22,1 | 0,0477 | 31,8 | 0,049 | 17,9 |
| 8 | 0,08 | 306,6 | 0,035 | 17,8 | 0,009 | 30,2 | 0,02 | 317,4 | 0,0195 | 70,4 | 0,035 | 17,8 |
| 9 | 0,036 | 2732,1 | 0,025 | 15 | - | - | 0,001 | 16,7 | 0,001 | 16,9 | 0,002 | 14,8 |
| 10 | 0,748 | 1486,4 | 0,001 | 8 | - | - | 0,001 | 24,603 | 0,058 | 52,1 | 0,002 | 6,4 |
| 11 | 1,427 | 18927,4 | 0,002 | 7,4 | - | - | 0,002 | 18,5 | 0,0537 | 81,1 | 0,002 | 9,3 |
| 12 | 0,01 | 231,2 | 0,001 | 14,8 | - | - | 0,001 | 17 | 0,0493 | 95,8 | 0,001 | 8 |
| 13 | 0,397 | 3055,3 | 0,002 | 9,3 | - | - | 0,003 | 5,1 | 0,015 | 48,2 | 0,002 | 7,4 |
| 14 | 0,21 | 991,9 | 0,002 | 6,4 | - | - | 0,007 | 8,8 | 0,01 | 41,7 | 0,001 | 11 |
| 15 | 0,001 | 10,3 | 0,001 | 11 | - | - | 0,02 | 193,9 | 0,0333 | 33,5 | 0,054 | 30,8 |
| 16 | 0,001 | 10,3 | 0,054 | 30,8 | - | - | 0,02 | 80,4 | 0,0103 | 74,2 | 0,001 | 6,7 |
| 17 | 0,235 | 282,3 | 0,001 | 6,7 | - | - | 0,001 | 4,2 | - | - | 0,001 | 6,6 |
| 18 | 0,001 | 210 | 0,001 | 6,6 | - | - | 0,002 | 18,3 | - | - | 0,002 | 5,9 |
| 19 | 0,002 | 133 | 0,002 | 5,9 | - | - | 0,001 | 48,9 | - | - | 0,001 | 3,6 |
| 20 | 0,043 | 168,3 | 0,001 | 3,6 | - | - | 0,006 | 21,4 | - | - | - | - |
| 21 | 0,025 | 169,4 | - | - | - | - | 0,025 | 47,5 | - | - | - | - |
| 22 | 0,0001 | 11,2 | - | - | - | - | 0,001 | 14 | - | - | - | - |
| 23 | 0,004 | 23,2 | - | - | - | - | 0,001 | 111,7 | - | - | - | - |
| 24 | 0,0001 | 13,2 | - | - | - | - | - | - | - | - | - | - |
| 25 | 0,487 | 110,8 | - | - | - | - | - | - | - | - | - | - |
| 26 | 0,281 | 51,2 | - | - | - | - | - | - | - | - | - | - |
| 27 | 0,211 | 27,5 | - | - | - | - | - | - | - | - | - | - |
Una vez que se contó con esta base de datos, se procedió en aplicar la prueba no paramétrica de Kolmogorov, para verificar si los datos cumplen con la característica de normalidad, obteniendo como resultado que todos los metales evaluados tienen un p valor menor a 0,05, por lo que se confirma la no normalidad y las condiciones no paramétricas en los datos de los 31 metales evaluados. A continuación, se procedió a aplicar la prueba de correlación de Spearman para estadística no paramétrica a los 31 metales evaluados respecto a las variables calidad de sedimentos y calidad de agua superficial, siendo que de los 31 metales solo dieron resultado superior a una correlación moderada cuatro metales: As, Na, Ni y Zn, tal como se aprecia en la tabla 3.
Tabla 3 Metales que presentan correlación mayor a 0,5
| Metal | Coeficiente de Correlación |
|---|---|
| As | 0,605 |
| Na | 0,545 |
| Ni | 0,591 |
| Zn | 0,637 |
Por lo tanto, considerando como una de las maneras de definir el término “metal pesado”, como un elemento químico comprendido entre 63,55 (Cu) y 200,59 (Hg) (Duffus, 2002), se tiene que de los cuatro metales que están correlacionados, dos son metales pesados siendo estos el arsénico y el zinc con pesos atómicos de 74,92 y 65,38 respectivamente. En el caso del sodio y del níquel estos no podrían ser considerados metales pesados bajo esta clasificación dado que tienen pesos atómicos de 22,99 y 58,69 respectivamente.
Posteriormente, se procedió a calcular la causalidad para lo cual se utilizó una prueba de regresión no paramétrica polinomial, mediante la estimación curvilínea en los 4 metales, para visualizar el porcentaje de causalidad a través del R2 que tiene la variable dependiente (calidad de agua) con la variable independiente (calidad de sedimentos), para este análisis se utilizó el software IBM SPSS Statistics V.29. En la estimación curvilínea se consideró la ecuación cubica por ser regresión polinómica, la cual mostró los mejores resultados para el R2 y p valor, tal como se verifica en las tablas 4 y 5.
Para el arsénico:
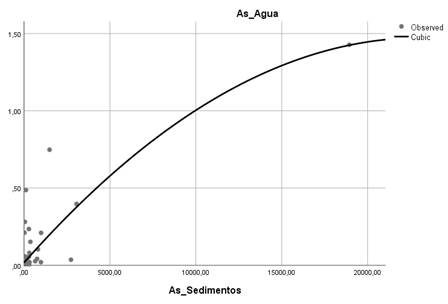
Tabla 4 Valor de R2 para el arsénico
| R | R cuadrado | R cuadrado ajustado | Error estándar de la estimación |
|---|---|---|---|
| 0,854 | 0,729 | 0,724 | 0,086 |
| La variable independiente es As_Sedimentos |
Tabla 5 Tabla ANOVA con p valor (Sig.) para el arsénico
| Suma de cuadrados | gl | Media cuadrática | F | Sig. | |
|---|---|---|---|---|---|
| Regresión | 2,205 | 2 | 1,103 | 147,932 | 0,000 |
| Residuo | 0,820 | 110 | 0,007 | ||
| Total | 3,025 | 112 | |||
| La variable independiente es As_Sedimentos |
De los resultados se obtiene un p valor de 0,000 que confirma la causalidad, asimismo se obtuvo un valor de R2 de 0,729 con tendencia alta, lo que indica que el 72,9% de la concentración de arsénico en agua es causada por la concentración de arsénico presente en los sedimentos. Lo cual se puede advertir en la figura 1.
Para el sodio:
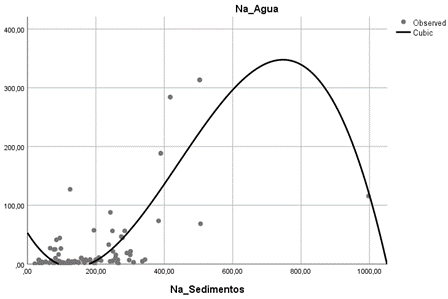
De la tabla 6, se obtuvo un p valor de 0,000 que confirma la causalidad, asimismo se obtiene un valor de R2 de 0,600 con tendencia media, lo que indica que el 60,0% de la concentración de sodio en agua es causada por la concentración de sodio presente en los sedimentos. Tal como se advierte en la figura 2.
Tabla 6 Valor de R2 y p valor (Sig.) para el sodio
| Variable dependiente: Na_Agua | ||||
| Ecuación | R cuadrado | F | gl | Sig. |
| Cúbica | 0,600 | 53,911 | 3 | 0,000 |
| La variable independiente es Na_Sedimentos | ||||
Para el níquel:
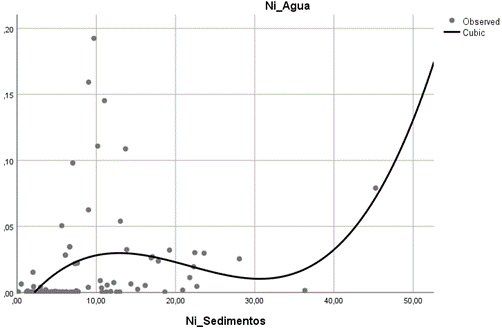
De la tabla 7, se obtuvo un p valor de 0,000 que confirma la causalidad, asimismo se obtiene un valor de R2 de 0,166 con tendencia muy baja, lo que indica que el 16,6% de la concentración de níquel en agua es causada por la concentración de níquel presente en los sedimentos. Lo mencionado se advierte de la figura 3 .
Tabla 7 Valor de R2 y p valor (Sig.) para el níquel
| Variable dependiente : Ni_Agua | ||||
| Ecuación | R cuadrado | F | gl | Sig. |
| Cúbica | 0,166 | 7,228 | 3 | 0,000 |
| La variable independiente es Ni_Sedimentos | ||||
Para el zinc:
Para el zinc, de la tabla 8, se obtuvo un p valor de 0,218 y 0,209 para la ecuación cuadrática y cúbica respectivamente por lo que no se confirma la causalidad.
CONCLUSIONES
De los 31 metales evaluados se advierte que, para las 6 cuencas hidrográficas los valores de calidad en sedimentos y agua superficial cumplen la estadística no paramétrica.
De los 31 parámetros solo cuatro (As, Na, Ni y Zn) muestran una correlación moderada superior al 0,5 en el coeficiente de correlación, esto indica que en la mayoría de los metales no existe una correlación entre la calidad del agua superficial y la calidad de sedimentos, en los ríos evaluados.
De la verificación realizada de causalidad de estos cuatro metales (As, Na, Ni y Zn), solo se obtuvo en el As un valor de R2 de 0,729 con una causalidad de tendencia alta, lo que indica que el 72,9% de la concentración de arsénico en agua es causada por la concentración de arsénico presente en los sedimentos.
El sodio presentó una causalidad media, el níquel una causalidad muy baja y el zinc no presento causalidad.
La presencia del arsénico en las aguas del área de estudio, se debe principalmente a que esta se encuentra en los sedimentos y por lo tanto es necesario tomar acciones conducentes a controlar los efectos que esta pueda tener en el medio ambiente y el ser humano, en caso sea utilizada en caso sea utilizada para consumo o actividades productivas como la agricultura.