Introducción
La angiogénesis es el proceso que permite la formación de nuevos vasos a partir de capilares preexistentes. La misma envuelve una secuencia compleja de eventos mediados por moléculas señalizadoras para crecimiento, migración, diferenciación y muerte de diversos tipos celulares. El análisis del crecimiento celular en la angiogénesis, es un objetivo terapéutico en enfermedades en animales y en el ser humano, particularmente en condiciones crónicas relacionadas a procesos inflamatorios y neoplasias.1
Para el estudio de la angiogénesis, uno de los modelos más empleados es el desarrollado en la membrana corioalantoica (CAM por sus siglas en inglés de Chorioallantoic Membrane) de embriones de pollos. El huevo posee tres membranas que circundan el embrión y son las encargadas del intercambio entre el mismo y el ambiente: amnio, corion y alantoide. La fusión de estas dos últimas crea la CAM. Esta membrana es responsable del transporte del calcio a partir de la cáscara de huevo, funciona como medio del intercambio de gases, la reabsorción de los electrólitos a partir de la cavidad alantoide y el equilibrio ácido-base, resultando ser crucial para el desarrollo embrionario.2
La regulación de la angiogénesis se lleva a cabo mediante un perfecto equilibrio entre la producción y la liberación de diversos factores estimulantes como el factor de crecimiento endotelial vascular (VEGF por sus siglas en inglés de Vascular Endothelial Growth Factor) y factor básico de crecimiento fibroblástico (bFGF, por sus siglas en inglés de Basic Fibroblast Growth Factor). Así como inhibidores (Trombospondina-1, Angiostatina, Interferón Alfa y Beta), que varían en función de las necesidades y el tipo de tejido.3 La existencia de inhibidores específicos para la angiogénesis fue postulada por primera vez por Judah Folkman en el año 1971.4 Debido a la importancia de la correcta evaluación de los efectos de este tipo de compuestos, continuamente aparecen nuevas investigaciones que permiten validar sus propiedades a partir de realizar la cuantificación de desarrollo de vasos por procesos de angiogénesis y de otros procesos de formación de vasos, por ejemplo, la vasculogénesis embrionaria usando como ambiente experimental la CAM.5
Para el propósito de esta investigación, fueron revisadas un conjunto de propuestas usadas para evaluar la angiogénesis bajo la influencia de determinados agentes inhibidores o angiogénicos a partir del uso del ensayo de la CAM. NOWAK‐SLIWINSKA 6 realizó un estudio para estudiar los efectos inhibidores de la angiogénesis de los compuestos Nexavar® (sorafenib), Tarceva® (erlotinib) y Sutent® (sunitinib). Los resultados fueron comparados con los obtenidos después del tratamiento con Visudyne® más Avastin® (bevacizumab), este último es un anticuerpo monoclonal conocido como compuesto inhibidor. Las valoraciones realizadas están en el orden de determinar el número de puntos de bifurcaciones por mm2 y el tamaño de la malla vascular, obteniéndose para ambos casos reducciones significativas.
Por su parte, ÖZCETIN et al. 7 evaluaron los efectos inhibidores del imatinib, aplicado en varias concentraciones a implantes de tumor en la CAM. La inhibición de la angiogénesis fue observada a partir de la determinación del número o diámetro total de los vasos que se interceptan. También se demostró que el cálculo del índice de los vasos definido como, el diámetro total de los vasos/circunferencia del tumor, corrobora los efectos inhibidores del imatinib.
El marco de trabajo desarrollado por SHI 8, permitió cuantificar los efectos inhibidores de la angiogénesis del Icaritin (ICT) en el modelo de la CAM a partir del análisis de tamaño total de los vasos sanguíneos ( ), área total de los vasos sanguíneos (µm2), total de segmentos de los vasos sanguíneos, por ciento de área de los vasos sanguíneos en la región de la CAM (%), tamaño promedio de los vasos sanguíneos ( ) y ancho promedio de los vasos sanguíneos ( ). Los resultados cuantitativos demostraron que el área total de los vasos sanguíneos y el total de segmentos de los vasos sanguíneos, disminuyeron significativamente lo cual sugiere que el ICT posee características anti-angiogénicas.
Con relación al efecto del Naproxeno Sódico sobre la angiogénesis en la CAM, las imágenes fueron procesadas para obtener el diámetro de los diferentes vasos sanguíneos en mm, así como una clasificación de los mismos dada en primarios, secundarios y terciarios.9 Los resultados obtenidos mostraron efectos angiogénicos del Naproxeno Sódico en altas concentraciones (0,086g/100μl, 0,042g/100μl,) y un efecto anti-angiogénico en bajas concentraciones (0,021g/100μl and 0,011g/100μl).
En el presente trabajo, se propone el estudio del efecto del MJ sobre la angiogénesis evaluada en la CAM a través de un sistema de análisis de imágenes denominado AnGioSoft, desarrollado para esta investigación por los autores de este trabajo. El MJ es un compuesto cuyos efectos anti-angiogénicos se han demostrado en diversos ambientes experimentales tanto para muestras in vivo como in vitro.10-12 Además, imágenes de la CAM tratadas con MJ, han sido valoradas desde el punto de vista computacional.11 Dichas imágenes fueron analizadas con el software Image J , a partir del análisis del área que comprende la red vascular, la cual se determina considerando el número de píxeles que conforman la misma segmentada a través del método de umbralización.
Para el propósito de la presente investigación se seleccionaron un conjunto de características consideradas globales para la caracterización de la CAM, debido a que brindan una panorámica general de la red vascular para cuantificar el proceso. Para validar la propuesta realizada se utilizaron un conjunto de imágenes de la CAM tratadas con diferentes dosis de MJ dadas por 7.5, 15 y 30 µM en suspensiones de agua y liposomas y conteniendo el MJ.
Materiales y métodos
Preparación de las muestras y capturas de las imágenes
La preparación de las muestras y captura de las imágenes fue realizada en el Laboratorio de Análisis Clínicos y Toxicológicos de la Facultad de Ciencias Farmacéuticas de la Universidad de Sao Paulo, Brasil. Los ensayos fueron realizados sobre huevos blancos de Gallus Domesticus (raza Bovans White) con peso medio de 60,1 g. Los huevos fueron incubados en un equipo automático marca Zagas Ltda., Brasil, con un termostato que permitió controlar cuidadosamente la temperatura y humedad general dentro del recinto.
Las muestras de la CAM fueron tratadas con tres dosis de MJ (7,5, 15 y 30 µM , en agua o en suspensiones de liposomas.
Los pasos de los ensayos comprendieron la abertura de los huevos el día 4 de incubación, la aplicación de los compuestos durante los días 7/8 y la colecta en los días 11/12 de vida del embrión.
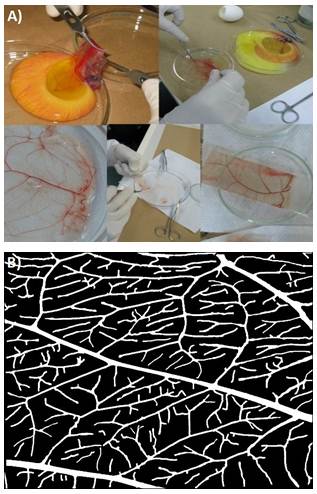
Para obtener las muestras, la CAM fue lavada y disecada con material microquirúrgico sobre placas de Petri. Los vasos de mayor calibre fueron tratados para evitar la pérdida de sangre. Finalmente, una porción de la membrana fue separada y montada sobre una lámina de microscopía para iniciar la captura de las imágenes (Figura 1 a), la cual fue realizada mediante el programa ACT-2U, usando una lupa estereoscópica Nikon SMZ 1800 acoplada a una cámara digital DS-U1 Nikon. Las imágenes fueron almacenadas en formato TIFF en una resolución de .
En total se obtuvieron 30 imágenes. Estas imágenes fueron previamente segmentadas utilizando un software auxiliar desarrollado por los autores de este trabajo, donde la segmentación se realiza de dos formas: una automática y otra opcional que utiliza un software de creación propia de corrección manual de la segmentación. El resultado final de la segmentación fue una imagen binaria con el fondo de color negro y los vasos en color blanco (Figura 1 b).
Características de interés para la cuantificación de la angiogénesis en la CAM
Se empleó el software AnGioSoft desarrollado en lenguaje Matlab®, el cual fue creado específicamente para el trabajo con imágenes de la CAM, y que contempla un conjunto de características de interés para la cuantificación de la angiogénesis que se obtienen a partir de la imagen binaria, el esqueleto de la misma y una representación de la red vascular a través de una estructura de árbol. En el caso del esqueleto de la imagen de la CAM es posible el proceso de extracción de medidas cuantitativas de manera más sencilla. Algunas de las características, desde el punto de vista global, que pueden ser valoradas debido a la valiosa información que brindan con respecto al estado de la angiogénesis son 13:
Estructuras de ramificación: puntos terminales, puntos de bifurcación, dimensión fractal.
Densidades de elementos de interés en los vasos: densidad de puntos terminales, densidad de puntos de bifurcación, densidad de área de los vasos, densidad de longitud de los vasos.
Medidas extraídas a partir de la taxonomía de Strahler: razón de bifurcación , razón de área promedio de vasos y razón de longitud de flujo ( ).
Medidas extraídas a partir de la taxonomía de Tokunaga: matriz de bifurcaciones.
A continuación, se hace una propuesta de las definiciones formales de las estructuras de ramificación, específicamente de los puntos terminales y los puntos de bifurcación, así como de las densidades de elementos de interés en los vasos y se definen las particularidades de las taxonomías de Strahler y Tokunaga.
Punto terminal: un punto denotado por p en un esqueleto E se dice que es un punto terminal o extremo, si en una vecindad N 8 (correspondiente a los 8 pixeles adyacentes al mismo), solo un vecino pertenece a E. Este concepto es descrito de la siguiente forma:
Punto de bifurcación: un punto denotado por p en un esqueleto E se dice que es un punto de bifurcación, si tiene exactamente tres vecinos pertenecientes al esqueleto en una vecindad N 8 de un pixel y no se conecten los tres vecinos tomándolos dos a dos. Formalmente un punto de bifurcación puede ser definido por la siguiente ecuación:
Densidad de puntos extremos: se define como la proporción de puntos terminales p en un esqueleto E, en razón del área de la imagen original en términos de m (ancho) y n (largo). Es formulado por:
Densidad de puntos de bifurcación: es definida como la proporción de pixeles p en un esqueleto E correspondientes a puntos de bifurcación, relativo al área de la imagen original en términos de m (ancho) y n (largo). Es formulado por:
Densidad de área de vasos: es definida por la proporción de los pixeles correspondientes al área de la red vascular A v en la imagen I, relativo al área de la imagen original en términos de m (ancho) y n (largo), esto es:
Densidad de longitud de vasos: la densidad de longitud de los vasos, es representada como la densidad del esqueleto de los vasos y se define como: la proporción de pixeles p correspondientes al esqueleto E, relativo al área de la imagen original en términos de m (ancho) y n (largo):
Dimensión fractal: Para calcular la dimensión de un objeto fractal, se extiende una malla uniformemente espaciada y se cuenta cuántas cajas se requieren para cubrir el conjunto del objeto de interés. La dimensión fractal de este objeto en cuestión se calcula viendo cómo cambia este número al ir haciendo la malla más fina. Suponiendo que N 8 es el número de cajas de longitud requeridas para cubrir el conjunto, entonces su dimensión fractal se define conforme a la fórmula de Minkowski-Bouligand como sigue 14:
Taxonomía de Strahler (también conocida como taxonomía de “Horton-Strahler”): explica que los segmentos que terminan en un punto extremo, excepto el punto de origen de la red, son definidos como segmentos de orden 1 (o segmentos de 1er orden) y sirven como base para la clasificación de los demás segmentos. Los segmentos de orden son caracterizados por la convergencia de dos segmentos de orden . Los primeros resultados empíricos sobre estas regularidades se conocen como la Ley de Horton. Esta plantea que dado la cantidad total de segmentos de orden 1 ≤ i ≤ Ω, el promedio de área de vasos de orden i y siendo el promedio de sus longitudes, la razón de bifurcación ( ), la razón de área promedio de vasos ( ) y la razón de longitud de flujo ( ) de orden i, , son definidas respectivamente por 15:
Taxonomía de Tokunaga: considera las ramificaciones laterales de una red vascular una valiosa fuente de información. Esto hace que redes similares, según la taxonomía de Strahler, puedan ser diferentes cuando se clasifican de acuerdo a la taxonomía de Tokunaga.17-18 En este enfoque, cada segmento de la estructura tiene dos valores de orden 18: un valor para el hijo ( ), correspondiente al valor de orden según la taxonomía de Strahler; un valor de orden principal ( ), dependiente del tipo de ramificación. Esto es si es un segmento lateral entonces se asocia a el valor del orden de Strahler del segmento al cual está conectado (al cual llamaremos ), en caso contrario el valor de será el mismo que el de . Formalmente los valores de y para un segmento s quedan definidos como:
donde nStra(s) es el orden de acuerdo con la taxonomía de Strahler.
Una característica de esta taxonomía es que dado que un segmento tal que , entonces se tiene que para cualquier segmento lateral de s se cumple que el valor de se encuentra en el conjunto . Una ventaja interesante de esta clasificación es que ella puede ser representada por una matriz de bifurcaciones , tal que cada elemento que pertenece a expresa la cuantidad de segmentos tal que y .
Resultados y discusión
Para comprobar la efectividad del tratamiento de las muestras con el MJ se procesó el conjunto de muestras divididas en un grupo control y otro grupo de muestras tratadas con las diferentes dosis del MJ para cada grupo, en agua o en liposomas. Se consideró como valor representativo para cada conjunto de imágenes, en el caso de los dos primeros conjuntos de medidas, el valor promedio de los parámetros determinados.
La figura 2 (a) muestra cómo en el ambiente agua, la cantidad de puntos terminales aumenta en la concentración de 15 µM con respecto a las muestras control, no siendo así para la concentración de 7.5 µM donde se mantiene muy cercano al valor obtenido por el control. En la concentración de 30 µM se encontró una disminución de la cantidad, que al final es el efecto esperado debido al carácter anti-angiogénico del MJ. Es conocido que sustancias que presentan efecto inhibidor de la angiogénesis resultan en producir un estímulo del mismo proceso en concentraciones más bajas que las necesarias para la actividad anti-angiogénica lo que ocurre con el MJ.7 En el caso del ambiente experimental de liposomas, para todas las concentraciones se observó una disminución en la cantidad de puntos terminales con respecto a las muestras control; en especial a la concentración de 15 µM se llega a tener una disminución de más de la mitad y a la de 30 µM de hasta el 33%. En general, para este ambiente se obtuvo un comportamiento anti-angiogénico en todas las concentraciones. Esto es lo esperado realmente, porque la biodisponibilidad del MJ puede ser mayor en liposomas que en agua y los efectos más intensos ocurren en concentraciones menores. El vehículo es completamente biocompatible.
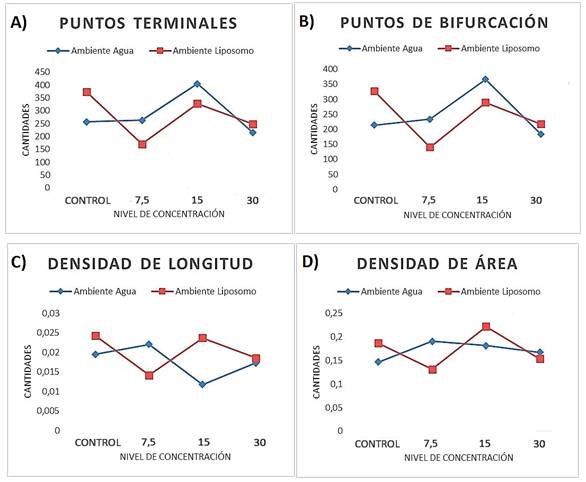
Fig. 2 Gráficos comparativos en ambientes agua y liposomas de (a) puntos terminales, (b) puntos de bifurcación, (c) densidad de longitud de vasos y (d) densidad de área de la región vascular en membranas corioalantoicas tratadas con MJ
Este efecto de concentración se ve aún más claro cuando se observan los resultados correspondientes a puntos de bifurcación (Figura 2 (b)), de manera similar a lo que ocurre con los terminales, en el ambiente con liposomas se destaca la tendencia anti - angiogénica. En agua se obtuvo un comportamiento diferente, debido a que hay un aumento de los puntos terminales cuando se trata con 15 µM de MJ, que aumenta en este caso hasta un 67%. Esto se corresponde con un aumento en la aparición de nuevos vasos. El efecto pro-angiogénico observado en la exposición en agua puede surgir debido a que la biodisponibilidad del compuesto es menor en ese vehículo, que resulta en concentraciones más bajas en la señalización de los objetivos, exactamente como es verificado para los puntos terminales.
Las densidades de longitud de vasos y de área de la región vascular, se muestran en la Figura 2 (c) y (d), respectivamente. Ambos parámetros informan sobre la estructura del árbol vascular, más que sobre el suceso de eventos locales de aparición de vasos, que son mejor reflejados por la medida. Para la densidad de longitud de vasos en el ambiente agua se observó que, en todas las concentraciones, a diferencia de lo que venían mostrando los resultados con respecto a los puntos de interés, hay una disminución con respecto a las muestras control. Ello indica que el comportamiento es anti angiogénico, y refleja mudanzas en la estructura de toda la red, con disminución en el número y el calibre de vasos perfundidos que pueden surgen de una pérdida de calidad funcional, incluso considerando las variaciones observadas de los puntos terminales o de bifurcación. Por otro lado, en el ambiente experimental de liposomas, el proceso angiogénico es observado en presencia de todas las concentraciones estudiadas.
La densidad de área muestra la llegada de la sangre a los tejidos, y es un parámetro global que puede mantenerse aún más estable que la densidad de longitud. La densidad de área revela cuándo la perfusión total fue modificada por variaciones de volemia, por obstrucción vascular de una rama importante o por pérdida de elementos vasculares debido a la toxicidad. El desplazamiento de la distribución de la sangre de la microcirculación para vasos mayores puede producir un aumento en la densidad de área, como se observa con las muestras en agua. Eso ocurre porque la sensibilidad de los instrumentos de captura no considera adecuadamente los vasos más finos en la binarización de la imagen. Los vasos más finos pueden acomodar cantidades no despreciables de volemia. Las imágenes analizadas mostraron poca variación en la densidad de área asociada a exposición independiente del medio de soporte.
Otro parámetro determinado es la dimensión fractal, el cual caracteriza la complejidad estructural de la red y puede ser útil para analizar la ocupación de esta red en la imagen. Se afirma que una dimensión fractal con valor próximo a 2 es la condición necesaria para que una red hidrográfica cubra cualquier punto de la superficie.17 Considerando la similitud entre una red hidrográfica y una red vascular podemos asumir este valor como referencia. En la figura 3, se muestra el comportamiento de esta medida para los conjuntos de imágenes de control y los correspondientes a las concentraciones de 7,5, 15 y 30 µM de MJ.
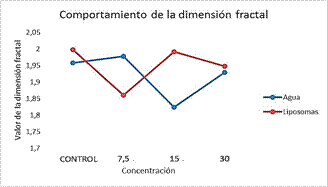
Fig. 3 Gráfico comparativo de la dimensión fractal en ambientes agua y liposomas en imágenes de membranas corioalantoicas tratadas con MJ
El comportamiento de la dimensión fractal resulta muy semejante a lo mostrado en la figura 2 (c). Cuando el ambiente es agua, para las concentraciones de 15 y 30 µM se tiene una disminución en este valor con respecto a las muestras control, donde para estas últimas la media del conjunto de imágenes muestra que la dimensión fractal es muy cercana a 2. Estos resultados obtenidos indican que no hay una distribución homogénea de la red vascular sobre la imagen para estos dos casos. En el caso de 7,5 µM, hay un incremento del parámetro con respecto al control y el valor es mucho más cercano a 2, lo que garantiza un mayor despliegue de la red sobre la imagen. Para el caso de liposomas se mantiene en todas las concentraciones una disminución en el valor de la dimensión fractal con respecto a las muestras control, indicando un menor despliegue de la red vascular sobre la imagen. Este comportamiento corrobora el del resto de los parámetros, lo que permite sustentar que el compuesto en liposomas tiene un carácter anti-angiogénico.
En general, la propiedad anti - angiogénica del MJ se evidencia en los ensayos realizados en las distintas concentraciones cuando el ambiente experimental es liposomas. Especialmente se destaca la concentración de 7,5 µM donde las medidas de cuantificación usadas para caracterizar el proceso de la angiogénesis en las imágenes de la CAM disminuyen de manera relevante hasta un 57 %.
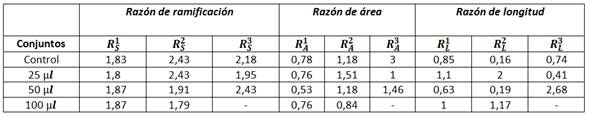
El otro análisis realizado se relaciona con la clasificación de los vasos. Las medidas extraídas usando las taxonomías de Strahler y Tokunaga, brindaron resultados que posibilitaron la comparación de la forma en que se distribuyeron los vasos jerárquicamente. Las medidas derivadas de la ley de Horton brindaron los resultados que se muestran en las tabla 1 y 2, para los diferentes conjuntos de imágenes valoradas.
Tabla 2 Resultados obtenidos de las medidas derivadas de la ley de Horton para el ambiente liposomas
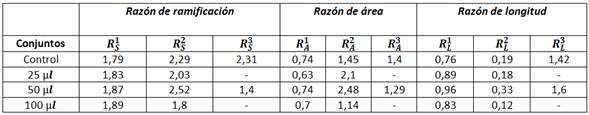
Por otra parte, las matrices de bifurcaciones derivadas de la taxonomía de Tokunaga, mostradas en la tabla 3, muestran información más precisa sobre la estructura de ramificación de una red vascular. Se tomó como valor representativo para cada orden de vasos, el promedio sobre todo el conjunto de muestras. Es evidente en los resultados obtenidos en agua, que las concentraciones de 15 y 30 µM de MJ provocan que aumente la formación de nuevos vasos (señalizados como los vasos de orden 1) para el primer caso y disminuya de manera significativa para el segundo, con respecto a las muestras control. Esto se corresponde con los valores de la cantidad de puntos terminales para estas concentraciones.
Tabla 3 Matrices de bifurcaciones derivadas de la taxonomía de Tokunaga. Resultados para los diferentes conjuntos de imágenes en agua, a) conjunto control, b) conjunto 7,5 µM, c) conjunto 15 µM y d) conjunto 30 µM
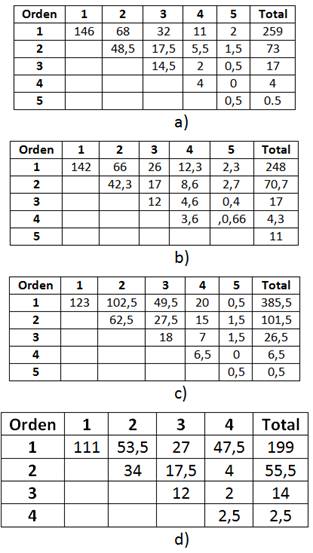
Al contrario de lo mostrado por los resultados en el ambiente experimental correspondiente al agua, la totalidad de las concentraciones de MJ en liposomas presentaron una disminución en cuanto a la formación de nuevos vasos sanguíneos con respecto a las muestras control (tabla 4). Esto también se corresponde con los resultados obtenidos para la cantidad de puntos terminales. Los resultados confirman lo encontrado en la literatura sobre los efectos de MJ, formulado en vehículos lipídicos de dimensiones nanométricas.10,11
Tabla 4 Matrices de bifurcaciones derivadas de la taxonomía de Tokunaga. Resultados para los diferentes conjuntos de imágenes en liposomas, a) conjunto control, b) conjunto 7,5 µM, c) conjunto 15 µM y d) conjunto 30 µM
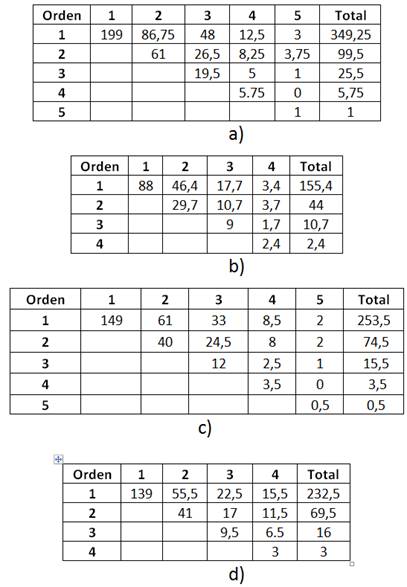
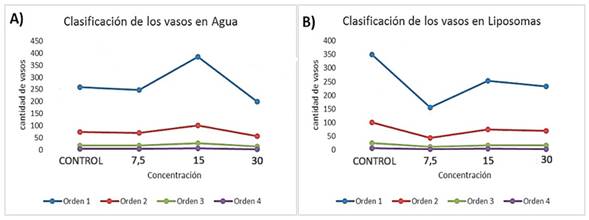
Estos resultados pueden apreciarse gráficamente en las figuras 4 (a) y (b), donde se muestra la distribución de vasos sanguíneos según su orden.
Conclusiones
El análisis realizado de forma automática en imágenes de muestras de membrana corioalantoica (CAM) de embriones de pollos con el sistema AnGioSoft, demostró las propiedades anti-angiogénicas del MJ a las distintas concentraciones evaluadas, particularmente en el vehículo liposomal, asociado a una mejor biodisponibilidad de dicho compuesto