INTRODUCCIÓN
El cacao (Theobroma cacao L.) es afectado por varias enfermedades fúngicas en todas las zonas de cultivo. Una de las enfermedades más devastadoras es la pudrición negra de la mazorca, la cual es causada por varias especies de Phytophthora (Oomycota). La taxonomía de las especies de Phytophthora asociadas al cacao ha sido controversial por largo tiempo. Históricamente, las cepas aisladas de tejidos afectados se identificaron como una sola especie, P. palmivora. Brasier y Griffin (1979) reconocieron la presencia de un complejo de especies y más tarde definieron cuatro especies principales: P. palmivora, P. megakarya, P. capsici y P. citrophthora. De estas especies, P. palmivora es la más devastadora y extendida a nivel mundial (Bailey et al., 2015), mientras que P. megakarya es la más agresiva en África (Ploetz, 2016).
En la región de Latinoamérica la situación de las especies de Phytophthora asociadas al cacao es la más compleja; están implicados varios taxas, cuyas identidades, diversidad genética, distribución geográfica e impacto están aún bajo discusión (Fister et al., 2016). Esto puede estar ligado al hecho de que América del Sur es el área nativa de T. cacao con antiguas poblaciones dispersas a través del cauce del río Amazonas.
Cuba centra la producción de cacao en el municipio de Baracoa, región oriental del país. Esta área posee condiciones climáticas apropiadas para el cultivo; alto nivel de precipitaciones, humedad y temperatura (Hartmann y Larramendi, 2011).
Las plantaciones cubanas de cacao son severamente atacadas por la pudrición negra de la mazorca, en parte debido al pobre manejo de las mismas. Igualmente, la Guyana Francesa es un país pequeño productor de cacao y sus plantaciones (mayormente antiguas, del siglo XIX) están dispersas. No obstante, es posible encontrar poblaciones nativas de T. cacao y especies locales de Phytophthora en la zona centro-sur del país. Durante estudios previos, un set de cepas de Phytophthora, originarias de antiguas plantaciones de cacao fueron tentativamente identificadas como P. capsici (Lachenaud et al., 2015). Sin embargo, en Cuba no se ha realizado un estudio detallado, con el empleo de técnicas modernas de caracterización, para identificar las especies de Phytophthora que afectan al cultivo.
El objetivo de este estudio fue identificar y caracterizar dos sets de cepas de Phytophthora aisladas de mazorcas enfermas con pudrición negra, originarias de Cuba y la Guyana Francesa.
MATERIALES Y MÉTODOS
Colección de cepas
Se aislaron noventa cepas de Phytophthora de mazorcas con síntomas de pudrición negra, durante varias expediciones a diferentes plantaciones en Baracoa (tabla 1). Ocho aislados se obtuvieron en la Guyana Francesa (tabla 2), todos originarios del área de Régina. Los aislados se mantuvieron en agar V8 en un rango de temperatura de 24-29 °C.
Caracterización morfológica
Se observaron varios caracteres morfológicos de las cepas (micelio, esporangio, oosporas, clamidosporas) con un microscopio Olympus BX50. Se tomaron fotografías de las estructuras fúngicas usando el programa Ulead Photo explore SE (V 7.0). El crecimiento del micelio se observó en placa Petri para cada individuo.
Tabla 1 Cepas de Phytophthora colectadas en Baracoa, Cuba
| Zona | Localidad | Cepas | Fecha | |
|---|---|---|---|---|
| Poa, El Chocolate | 20°17'19,39"N 74°27'56,10"W | PHYTO15 PHYTO16 PHYTO17 PHYTO18 PHYTO19 | PHYTO20 Poa1 Poa2 Poa3 Poa5 | Abril, 2009 Abril, 2010 |
| Boris Miraflores, El Porvenir | 20°13'47,20"N 74°26'45,90"W | PHYTO25 PHYTO26 PHYTO27 PHYTO28 PHYTO29 | PHYTO30 PHYTO31 PHYTO32 PHYTO33 PHYTO34 | Abril, 2009 |
| Lomo de Camagüay | 20°30'41,12"N 74°42'34,90"W | CU/09-41 CU/09- PL6812 CU/09- PL6813 | CU/09-42 CU/09-43 CU44 CU0944 CU/0944c CU/09-44d | Noviembre, 2009 |
| Juan Romero | 20°12'25,86"N 74°23'17,08"W | CU/09-50 CU/09-60 CU/09-63 CU/09-71A CU/09-71B CU/09-73 CU/09-74 | CU/09-75 CU/09-76 CU/09-77 CU/09JR06 CU09JR08 CU/09JR10B CU/09JR11A | Noviembre, 2009 |
| Naranjal del Toa | 20°23'49,69"N 74°32'55,62"W | PHYTO36 PHYTO39 | PHYTO40 | Abril, 2009 |
| Arroyo de la vieja finca | 20°12'29,52"N 75°38'27,42"W | CU/09-56 CU/0957 | CU/09-61 CU/09-62 | Noviembre, 2009 |
| Capiro, Nueva vista | 20°13'06,24"N 74°23'29,34"W | CU0958 CU/09-59 | Cuba | Noviembre, 2009 |
| Esteban Silot | 20°13'34,49"N 74°30'21,89"W | CU/09- SILOT3 | CU/09- SILOT5 | Noviembre, 2009 |
| Los hoyos de Sabanilla | 20°16'51,32"N 74°27'52,87"W | Est1 Est2 Est3 Est4 | Est5 Est6 Est7 | Abril, 2010 |
| Cayayal | 20°15'44,02"N 74°27'51,28"W | Cay1 | Cay2 | Abril, 2010 |
| Paso de Cuba | 20°20'03,72"N 74°28'05,66"W | P-C1 P-C2 | P-C3 | Abril, 2010 |
| Santa Rosa | 20°21'20,47"N 74°31'58,65"W | S-R1 | S-R2 | Abril, 2010 |
| Mabujabo, Silina | 20°19'06,92"N 74°26'49,33"W | Mab1 | Mab2 | Abril, 2010 |
| Guayabo | 20°26'24,98"N 74°36'12,74"W | Gua1 | Gua2 | Abril, 2010 |
| Saibá | 20°26'02,89"N 74°36'27,70"W | Sai1 | Abril, 2010 | |
| San Luis, Victor Prieto | 20°18'11,43"N 74°25'56,35"W | S-L2 | Abril, 2010 | |
| Jamal | 20°16'34,65"N 74°25'32,35"W | Jam1 | Abril, 2010 | |
| Jobo Dulce | 20°19'22,55"N 74°26'46,31"W | Job2 | Abril, 2010 | |
| Sabanilla | 20°16'42,11"N 74°27'52,86"W | Hur1 | Abril, 2010 | |
Tabla 2 Cepas de Phytophthora colectadas en Guyana Francesa
| Zona | Localidad | Cepas | Fecha | |
|---|---|---|---|---|
| Régina, Crique Courouaïe, right bank | 4°16'07,24"N 51°57'52,13"W | Reg 2-1 Reg 2-3 Reg 2-4 Reg 2-6 | Reg 2-7 Reg 2-8 Reg 2-10 | Marzo 2009-2014 |
| Régina, Approuague River, left bank | 4°20'43,95"N 52°02'01,35"W | Reg 3-1 | Marzo 2014 | |
Test de cruzamiento
El mating type (MT) de las cepas aisladas de Phytophthora se determinó por cruzamientos con las cepas de referencia de MT, A1 y A2 de P. palmivora (MUCL 52539 y MUCL 52540) en agar V8. Para realizar los cruces con las 88 cepas cubanas se asumió que estas pertenecían a P. palmivora. Cada aislado a estudiar se colocó a un lado de una placa Petri y, en el lado opuesto de la misma se colocó el mating type de referencia. Las placas Petri se incubaron a 25 °C, en oscuridad, alrededor de 14 días. Según la aparición de oosporas, los aislados en estudio se clasificaron como mating type A1 y A2 (Tooley et al., 1989).
Determinación de secuencias de AND y análisis filogenéticos
Se extrajo el ADN, de micelio fresco, de cepas cultivadas en agar malta a 25 °C, en condiciones de oscuridad. Las extracciones se realizaron con el empleo de QIAGEN Dneasy plant Mini Kit (QIAGEN Inc., Hilden, Germany), y posteriormente se purificaron con Geneclean( III kit (Q-Biogene, USA), según las recomendaciones del fabricante. Los pares de primer TUBUR1-TUBUF2 (Kroon et al., 2004) y NS7-ITS4 (White et al., 1990) se emplearon para la amplificación de β-tubulin, respectivamente.
Los ensayos de PCR resultaron en una simple banda observada a 0,8%, m/v, en gel de agarosa, que corresponde aproximadamente a 900 bps (ITS) y 500 bps. Los productos PCR se purificaron con el empleo de QIAquick( PCR purification kit (250) (QIAGEN Inc., Hilden, Germany), según las instrucciones del protocolo del fabricante.
Las reacciones de secuenciación se realizaron con el empleo de CEQ DTCS Quick Start Kit( (Beckman Coulter Inc), con los primers ITS2, ITS3, e ITS4 (White et al., 1990), Bt2a y Bt2b. Las secuencias de nucleótidos se determinaron con el secuenciador capilar automático CEQ 2000 XL (Beckman Coulter Inc). Inicialmente, las secuencias de nucleótidos se alinearon automáticamente con Clustal X para MacIntosh (version 1.5b), y posteriormente ajustadas manualmente con el editor PAUP* (version 4.0b10).
Los análisis filogenéticos de las secuencias alineadas se realizaron por el método de máxima parsimonia de PAUP* versión 4.0b10 (Swofford, 2002) con los gaps tratados como una quinta base. Los árboles más parsimoniosos se identificaron mediante búsquedas heurísticas con un intervalo de adición de secuencia (1000), max tree set a 100, y una seguida evaluación por análisis de bootstrap, reteniendo los clados compatibles con el 50% en el consenso de los árboles en bootstrap. La cepa de Phytophthora multivora (CBS 124094) se usó como grupo externo.
Las secuencias de ITS y β-tubulin se compararon con las encodadas en Genbank, con el empleo de la opción de búsqueda del BLAST en el National Center for Biotechnology Information (NCBI).
RESULTADOS Y DISCUSIÓN
Caracterización morfológica
Las observaciones microscópicas mostraron que 88 cepas cubanas tienen un patrón de crecimiento petaloide en medio V8. Dos cepas cubanas (CU58 y PHYTO40) y las 8 cepas de la Guyana Francesa mostraron un patrón de crecimiento en crisantemo, en medio V8 (fig. 1).
Al microscopio, se observó abundante producción de esporangios, de formas ovoides a elipsoidal, (pedicelio≤ 4 µm de longitud), los cuales tienen un rango entre 38-60 µm en longitud y 27-40 µm de ancho, con un radio L / A (largo / ancho) que varió desde 1.25 a 1.92 (figura 2a). En la figura 2c se observan las clamidosporas formadas, las que presentaron un diámetro de 32.5-43.5 µm. Estas características morfológicas observadas en 88 aislados cubanos, corresponden a las observadas en P. palmivora (Ali et al., 2014; Bush et al., 2006).
 a: forma petaloide (cepa MAB1) b: forma crisantemo (cepa CU58)
a: forma petaloide (cepa MAB1) b: forma crisantemo (cepa CU58)Fig. 1 Características morfológicas delas especies de Phytophthora aisladas de cacao en medio agar V8 después de 4 días de crecimiento a 24-29°C, en la oscuridad
En dos aislados cubanos (CU58 y PHYTO40) y en todos los aislados de la Guyana Francesa, los esporangios midieron 37-50 µm de longitud y 22-32 µm de ancho, con un radio L / A en una relación 1.8-2.4.
En estos esporangios se observó una larga hifa (longitud de 50 µm) (figura 2d). Acorde a estas características estas cepas pertenecen al complejo P. capsici - P. tropicalis cuyos caracteres morfológicos no permiten distinguirlos (Aragaki y Uchida, 2001).
Cruzamientos
Se encontró que las 88 cepas cubanas eran compatibles con la cepa correspondiente al mating type A, y dio como resultado la formación de oosporas. Las oosporas se observaron con un aspecto globoso, y presentaron un diámetro de 25 µm (figura 2b).
Dos cepas cubanas, CU58 (MUCL 55783) y PHYTO40 (MUCL 55782), resultaron estériles en presencia de cada uno de los mating type de referencia de P. palmivora.
Análisis filogenéticos
Las cepas de P. palmivora comparadas mostraron un alto grado de similaridad (fig. 3, 4); con una pequeña variación intraespecífica en las regiones de ADN analizadas. Basados en esto, una selección de cepas se utilizó en la construcción de árboles filogenéticos de la región ITS y el gen TEF1- α. Se observó un máximo de 5 bp entre los 700 pares de bases de longitud de la región ITS, lo que corresponde a una proporción de sitios variables de alrededor de 0,01. La región TEF1-α de 1000 pares de bases de longitud fue más variable con un máximo de 20 bp diferentes, lo que corresponde a una proporción de sitios variables de alrededor de 0,02 bp.
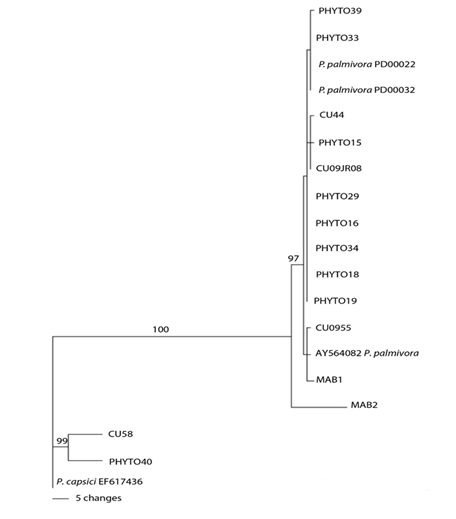
 *Los números en los nodos indican los valores de soporte de bootstrap
*Los números en los nodos indican los valores de soporte de bootstrapFig. 3 Árbol filogenético que muestra las cepas cubanas de Phytophthora basado en las secuencias de la región ITS, inferido por análisis de máxima parsimonia
Complejo P. tropicalis / capsici β-tubulin data set
Los análisis filogenéticos de β-tubulin incluyeron 40 taxa y P. multivora (CBS 124094) como grupo externo. El set de datos contó con un total de 865 bp, de los cuales 67 fueron informativos para la parsimonia. El análisis resultó en 981 árboles más parsimoniosos (MPT) (140 steps in length, CI = 0,771, RI = 0,904), de las 1000 búsquedas heurísticas. De estos árboles se seleccionaron dos topologías concurrentes para las cepas de la Guyana Francesa (fig. 5 y 6). Estas topologías forman un clado bien soportado, pero las afinidades no están bien soportadas.
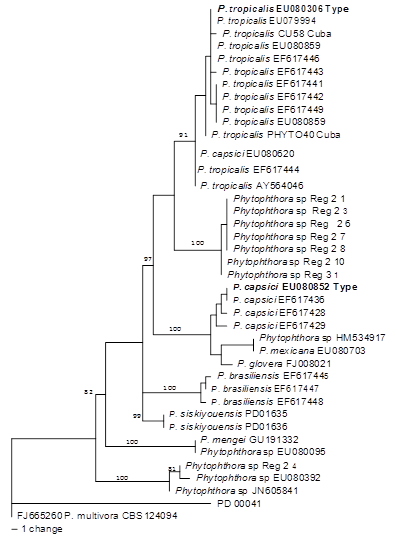 Los números en los nodos indican los valores de soporte de bootstrap. En negrita las cepas tipo de P. tropicalis y P. capsic
Los números en los nodos indican los valores de soporte de bootstrap. En negrita las cepas tipo de P. tropicalis y P. capsicFig. 5 Árbol filogenético que muestra las cepas cubanas de Phytophthora basado en las secuencias del gen β-tubulin, inferido por análisis de máxima parsimonia (topología más frecuente)
 *Los números en los nodos indican los valores de soporte de bootstrap. En negrita las cepas tipo de P. tropicalis y P. capsici
*Los números en los nodos indican los valores de soporte de bootstrap. En negrita las cepas tipo de P. tropicalis y P. capsiciFig. 6 Árbol filogenético que muestra las cepas cubanas de Phytophthora basado en las secuencias del gen β-tubulin, inferido por análisis de máxima parsimonia
En los árboles filogenéticos y en todas las secuencias utilizadas (ITS, β-tubulin), los aislados de Cuba (CU58, PHYTO40) tentativamente identificados como P. tropicalis / capsici complex se agruparon en el clado P. tropicalis s.s.; este clado contiene a la cepa tipo de P. tropicalis (CBS434.91), otras cepas de varios orígenes y varios hospederos y está bien soportado. Las cepas cubanas difieren de P. tropicalis (type) en 4 a 5 bp, 6 a 7bp, 3 a 5bp, en ITS y β-tubulin, respectivamente.
Los aislados de la Guyana Francesa tentativamente identificados como P. capsici (Lachenaud et al., 2015) se ubicaron en todas las filogenias en dos diferentes linages, lo cual está correlacionado con sus diferencias morfológicas.
El primer “clado” comprende 7 cepas mientras el segundo clado contiene una cepa (Reg 2-4). El linage Reg 2-4 fue en todas las filogenias, distantemente relacionado con P. tropicalis y P. capsici linage. Las otras 7 cepas forman un clado bien soportado en los tres análisis filogenéticos, aquí referido como “Guyana linage”.
En las inferencias filogenéticas basadas en los análisis de β-tubulin, el linage de Guyana formó un clado bien soportado (Bootstrap 100) que se ubicó en una posición aislada. Sin embargo, sus afinidades no están resueltas. Se obtuvieron topologías concurrentes del análisis individual de cada gen, en su topología dominante (figura 5), el clado de Guyana fue asociado al clado de P. tropicalis (type). En la topología menos frecuente (figura 6), este clado se asoció a P. capsici. No obstante, ninguna de estas posiciones fue bien soportada.
CONCLUSIONES
Dos especies de Phytophthora son causantes de la pudrición negra de la mazorca del cacao en Cuba, viz. P. palmivora, la cual fue predominante en nuestro muestreo y P. tropicalis, detectada con una baja frecuencia.
En la Guyana Francesa se identificaron dos especies de Phytophthora, de ellas P. tropicalis / capsici complex dominante en nuestro muestreo y una nueva especie representada por un simple aislado