INTRODUCCIÓN
El enfermo en insuficiencia o falla cardíaca cada día resulta más complejo en su abordaje terapéutico, toda vez que el envejecimiento poblacional que acompaña al mundo, así como las altas expectativas de vida y la supervivencia a afecciones antes fatales -gracias a las alternativas terapéuticas que así lo respaldan-, han incrementado considerablemente la prevalencia de la enfermedad. Según la American Heart Association, entre 2012 y 2030 su prevalencia se incrementará en un 50%, lo que significa que más de ocho millones de personas mayores de 18 años padecerán de insuficiencia cardíaca1; pero, además, su incidencia tampoco es despreciable, sobre todo en jóvenes, fundamentalmente con enfermedades como las miocardiopatías, cuya expresión clínica, además de la muerte súbita, es principalmente la insuficiencia cardíaca. Y no es infrecuente entonces encontrarnos con enfermos cuya clase funcional, según la NYHA (New York Heart Association), sea III o IV prácticamente desde el inicio de la enfermedad, en quienes el tratamiento farmacológico resulta insuficiente en su abordaje terapéutico integral.
Tal es así, que las diferentes sociedades científicas de referencia en EEUU y Europa enuncian, en sus respectivas guías de actuación2,3, criterios puntuales en este sentido, basados en la evidencia científica que los grandes estudios multicéntricos ofrecen en sus resultados. Pero, a su vez, expertos de las diferentes sociedades dedicadas a esta subespecialidad abren un poco el diapasón de opciones no farmacológicas y abordan el tema involucrando otros elementos fisiopatológicos de la enfermedad, lo que genera alternativas no consideradas previamente en las guías, pero con basamento científico y con estudios experimentales, unos ya con resultados y otros aún en fase de ejecución, pero con una visión más abarcadora frente a una enfermedad creciente, donde la conducta terapéutica que tomemos con los pacientes debe ir en consonancia con la multifactorialidad y la muy alta comorbilidad asociada, más allá del límite del trasplante cardíaco como última opción4.
FASES DE LA ENFERMEDAD Y PACIENTES
En la bibliografía del tema, el abordaje de esta enfermedad es muy general; sin embargo, existen clínicamente dos momentos o formas de presentación en los cuales la conducta terapéutica tiene particularidades. Es por ello que afirmamos que no solo en la insuficiencia cardíaca crónica se implementan estas alternativas terapéuticas, sino también en su fase aguda; y algunas de estas medidas se aplican y complementan en ambos estados clínicos, según el estadio de la enfermedad.
De manera general, entre las alternativas terapéuticas no farmacológicas de la insuficiencia cardíaca se encuentran:
Terapia de resincronización cardíaca (TRC) / cardiodesfibrilador automático implantable (CDAI)
Cirugía de afectación valvular y disfunción ventricular
Asistencia mecánica circulatoria
Tratamientos experimentales
Trasplante cardíaco
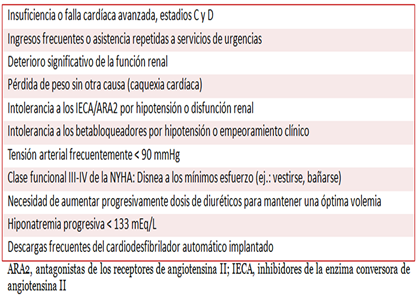
Entre los enfermos con insuficiencia cardíaca, quienes más se beneficiarían con estas opciones terapéuticas serían aquellos que presentan las características que se exponen en el recuadro 5.
INSUFICIENCIA CARDÍACA AGUDA
Optimizar oxigenación (PO2>90%)
Ventilación no invasiva
La ventilación mecánica no invasiva puede ser utilizada para aliviar la disnea y mejorar la saturación de oxígeno en pacientes con edema pulmonar agudo6. La evidencia muestra que no modifica la mortalidad en estos pacientes y los efectos sobre la reducción de la necesidad de ventilación mecánica invasiva son discordantes. (Nivel de evidencia B); pero esta modalidad ventilatoria tiene importantes efectos en el paciente con insuficiencia cardíaca2,6,7.
Efectos sobre el sistema respiratorio6:
Reclutamiento alveolar (evita su colapso), con mejora del intercambio de gases y de la oxigenación
Inducción del desplazamiento de líquidos que vuelven de los alvéolos y el espacio intersticial a la circulación pulmonar
Reducción de la carga de los músculos respiratorios y del trabajo de la respiración
Efectos hemodinámicos7:
Reducción del retorno venoso sistémico y disminución de la carga ventricular derecha al aumentar la presión intratorácica
Cambios en la resistencia vascular pulmonar total, que es el principal factor determinante de la poscarga ventricular derecha.
Circulación: garantizar gasto cardíaco >2,2 L/minuto
Asistencia mecánica circulatoria8,9
La indicación de asistencia circulatoria mecánica se debe considerar en pacientes con insuficiencia cardíaca refractaria, que requieren inotrópicos intravenosos en forma continua, y con parámetros de deterioro hemodinámico grave: a) presión capilar pulmonar > 20 mmHg, b) índice cardíaco < 2 L/min/m2 y c) presión arterial sistólica < 80 mmHg.
La asistencia circulatoria mecánica puede ser de corta duración o prolongada. Entre los dispositivos de corta duración, el balón de contrapulsación intraórtica es el de más amplia difusión. Una asistencia circulatoria mecánica compleja puede utilizarse como puente al trasplante, a la recuperación o, a largo plazo, en pacientes no susceptibles de trasplante8.
Indicaciones del balón de contrapulsación intraaórtico
Clase I
Shock cardiogénico por infarto agudo de miocardio asociado con estrategia de reperfusión (Nivel de evidencia B).
Comunicación interventricular o insuficiencia mitral grave por infarto agudo de miocardio (Nivel de evidencia B).
Shock cardiogénico sin respuesta a la terapia de apoyo con fármacos vasoactivos y factibilidad de trasplante cardíaco (Nivel de evidencia C).
Clase IIa
Insuficiencia cardíaca refractaria con causa potencialmente reversible (puente a la recuperación) en ausencia de dispositivos complejos (Nivel de evidencia C).
Clase IIb
Como puente a alternativa quirúrgica o a otra forma de asistencia mecánica circulatoria compleja y prolongada (Nivel de evidencia C).
Clase III
Pacientes con shock cardiogénico refractario sin el reconocimiento de una causa potencialmente reversible (Nivel de evidencia C).
Pacientes con insuficiencia aórtica, disección aórtica o enfermedad aorto-ilíaca grave (Nivel de evidencia B).
Perfusión tisular
Ultrafiltración
Una terapia nueva en la insuficiencia cardíaca aguda es la ultrafiltración, en particular para aquellos pacientes con retención hidrosalina, refractaria a la terapia médica convencional, y deterioro de la función renal. Sin embargo, en la actualidad no hay un rol claramente establecido para este procedimiento en pacientes que responden en forma adecuada a la terapia diurética. (Nivel de evidencia B)10.
Indicaciones
Tratamiento médico óptimo (TMO)
Insuficiencia cardíaca avanzada refractaria al tratamiento
Alteración de la función renal (filtrado glomerular < 45 ml/min/1,73 m2 de superficie corporal)
Sobrecarga de volumen: disnea, NYHA III-IV, edema, ascitis, refractariedad al TMO.
Más de dos ingresos por insuficiencia cardíaca en menos de seis meses.
Contraindicaciones
Insuficiencia renal en tratamiento con diálisis.
Paciente inestable.
Comorbilidades extracardíacas con esperanza de vida de menos de un año.
Alteración de la integridad de la pared abdominal por cirugías abdominales recientes o prótesis vasculares intraabdominales recientes (menos de cuatro meses).
Contractilidad.
Afectación valvular y disfunción ventricular: Alternativas quirúrgicas
La insuficiencia cardíaca como consecuencia de la enfermedad coronaria se debe a la disfunción ventricular asociada con isquemia aguda o crónica, disfunción ventricular sistólica o diastólica aguda reversible, complicaciones mecánicas del infarto agudo de miocardio, insuficiencia mitral, rotura ventricular, comunicación interventricular, aneurisma ventricular o una combinación de estos procesos13.
Se considera el tratamiento quirúrgico, con indicación Clase IIa y nivel de evidencia C, en pacientes con insuficiencia mitral primaria (orgánica) grave y sintomática en clase funcional II-IV (NYHA), que presenten deterioro grave de la función del ventrículo izquierdo (FEVI < 0,30 o diámetro telesistólico > 55 mm, o ambos) en quienes el éxito de la plastia es altamente probable13.
INSUFICIENCIA CARDÍACA EN FASE CRÓNICA
Las Guías de la Sociedad Europea de Cardiología de 20162 enunciaron las indicaciones terapéuticas con un resumen sintético de las alternativas no farmacológicas; en este caso, la TRC cuando la anchura del complejo QRS es mayor de 130 mseg. Por su parte, las de la American Heart Association3, en su resumen terapéutico, hace consideraciones más abarcadoras en los estadios C y D, donde estas opciones tienen clara indicación. Sin embargo, se deben de hacer otras consideraciones en este sentido, abogar por la necesidad de ofrecer otras opciones a estos enfermos y considerar la etiología de la enfermedad y las comorbilidades asociadas, entre otros aspectos.
Denervación renal
La denervación renal guiada por un catéter es un procedimiento mínimamente invasivo que se basa en la premisa fisiológica de que la interrupción de los nervios renales aferente y eferente resultará en una disminución de la señal simpática renal, que reduce la liberación de renina y la retención del sodio, e incrementa el flujo sanguíneo renal; lo que, consecuentemente, disminuye la tensión arterial (Figura 1)14,15. Los resultados de los estudios realizados hasta la fecha, indican que en la hipertensión refractaria es un tratamiento efectivo y seguro, complementario al tratamiento farmacológico; por lo tanto, es útil en los enfermos en quienes la hipertensión arterial resistente es la causa de la insuficiencia cardíaca14.
La ultrafiltración y la hemodiálisis también son útiles en este estadio clínico.
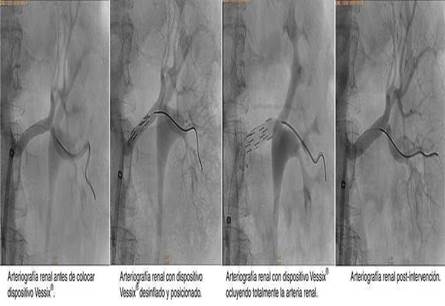
Figura 1 Secuencia de imágenes arteriográficas durante el procedimiento de denervación renal. Tomada de Marín-Orozco et al. Rev Colomb Cardiol. 2015;22:305-1115 (Licencia CC BY-NC-ND 4.0).
Terapia de resincronización cardíaca2,5,16-18
La TRC está contraindicada en pacientes con QRS < 130 ms. Sus indicaciones según las Guías de la Sociedad Europea de Cardiología2 son las siguientes:
Clase de recomendación I y nivel de evidencia A
Se recomienda para pacientes sintomáticos con insuficiencia cardíaca, en ritmo sinusal con QRS ≥ 150 ms y morfología QRS de bloqueo de rama izquierda, con FEVI ≤ 35% a pesar de recibir TMO, a efectos de mejorar los síntomas y reducir la morbimortalidad.
Se recomienda la TRC, en lugar de marcapasos del ventrículo derecho, para pacientes con insuficiencia cardíaca y FEVI reducida, independientemente de la clase funcional de la NYHA, que tienen una indicación para marcapasos ventricular y bloqueo aurículo-ventricular de alto grado, a efectos de reducir la mortalidad. Esto incluye a los pacientes con fibrilación auricular.
Clase de recomendación I y nivel de evidencia B
Se recomienda la TRC para pacientes sintomáticos con insuficiencia cardíaca en ritmo sinusal con QRS de 130-149 ms y morfología QRS de bloqueo de rama izquierda, con FEVI ≤ 35% a pesar de recibir TMO, a efectos de mejorar los síntomas y reducir la morbimortalidad.
Clase de recomendación IIa y nivel de evidencia B
Se debe considerar la TRC para pacientes sintomáticos con insuficiencia cardíaca, en ritmo sinusal con QRS ≥ 150 ms y morfología QRS sin bloqueo de rama izquierda, con FEVI ≤ 35% a pesar de recibir TMO, a efectos de mejorar los síntomas y reducir la morbimortalidad.
Se debe considerar la TRC para pacientes con FEVI ≤ 35% y NYHA III-IV pese al TMO, a efectos de mejorar los síntomas y reducir la morbimortalidad si el paciente está en fibrilación auricular y tiene una duración del QRS ≥ 130 ms, siempre que se disponga de captura biventricular o se espera que el paciente vuelva a ritmo sinusal. Respecto a la clase funcional, se debe usar el juicio médico para los pacientes con insuficiencia cardíaca en fase terminal tratables de manera conservadora, en vez de emplear tratamientos para mejorar los síntomas o el pronóstico.
Clase de recomendación IIb y nivel de evidencia B
Se puede considerar la TRC para pacientes con insuficiencia cardíaca sintomáticos, en ritmo sinusal con QRS de 130-149 ms y morfología del QRS sin bloqueo de rama izquierda, con FEVI ≤ 35% a pesar de recibir TMO, a efectos de mejorar los síntomas y reducir la morbimortalidad.
Se puede considerar la TRC para los pacientes con insuficiencia cardíaca y FEVI reducida que tienen un marcapasos convencional o un CDAI, y después sufren un empeoramiento de la insuficiencia cardíaca pese al TMO y tienen un porcentaje alto de estimulación del ventrículo derecho. Esto no es aplicable a los pacientes con insuficiencia cardíaca estable.
Cardiodesfibrilador automático implantable
Las recomendaciones para el uso de este dispositivo se muestran en la tabla 2,3,19-21.
Tabla Recomendaciones para el uso de cardiodesfibrilador automático implantable en pacientes con insuficiencia cardíaca. Modificada de Ponikowski et al. Eur Heart J. 2016; 37:2129-2002.

Tratamiento quirúrgico de la afectación valvular y la disfunción ventricular
Está indicado en pacientes con: a) infarto de miocardio anterior extenso previo (con gran escara aneurismática), b) disfunción sistólica grave del ventrículo izquierdo, c) insuficiencia cardíaca grave y c) área de acinesia ≥ 35% del perímetro del ventrículo.
La plastia circular endoventricular o cirugía de Dor (Figura 2)22, es una técnica quirúrgica consistente en reducir el volumen ventricular izquierdo y recuperar su forma elipsoide normal, a través de la exclusión del segmento miocárdico necrótico y acinético, aunque hay situaciones no favorables para la realización de una cirugía de restauración ventricular (que incluye cirugía valvular mitral, si insuficiencia mitral concomitante; y revascularización aortocoronaria, si la anatomía es favorable):
Disfunción grave de ventrículo derecho con necrosis inferior asociada.
Hipertensión pulmonar no asociada a insuficiencia cardíaca.
Acinesia marcada sin dilatación ventricular.
Patrón restrictivo de llenado ventricular izquierdo con mala clase funcional e insuficiencia mitral.
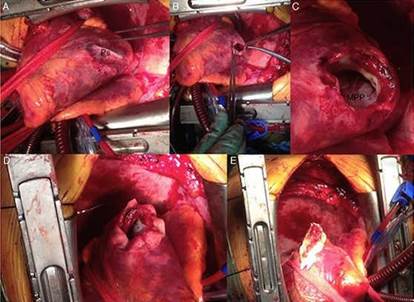
Figura 2 Anatomía quirúrgica y técnica de Dor modificada para reparación del seudoaneurisma ventricular izquierdo. A, B y C: apréciese la correspondencia con las pruebas de imagen*, quedando el defecto de rotura transmural de la pared ventricular con músculo “fresco” (C) tan solo contenido por una capa de epicardio que se invagina con la presión negativa intraventricular ya en circulación extracorpórea (A). D y E: técnica de Dor modificada con una primera ventriculorrafia circular apoyada en parche de pericardio bovino y posterior cierre hemostático con una segunda capa de sutura continua también apoyada en pericardio bovino. Tomada de Martín Gutiérrez et al. Cir Cardiov. 2016;23(4):21222) (Licencia CC BY-NC-ND 4.0). MPP: músculo papilar posterior. Ps: seudoaneurisma de ventrículo izquierdo. * Se mantiene el texto del pie de figura de la publicación original22, razón por la que no se corresponde con las pruebas de imagen.
Asistencia mecánica circulatoria izquierda9
Uno de los principales avances con esta técnica ha sido el reconocimiento de que el soporte con equipos de asistencia ventricular izquierda es suficiente para la gran mayoría de pacientes con insuficiencia cardíaca avanzada, aun con falla biventricular. La indicación más frecuente de este complejo tipo de asistencia, que representa el 80% de los implantes, es el puente al trasplante cardíaco en pacientes con falla cardiocirculatoria grave9,23.
Entre las indicaciones precisas se encuentra la presencia de síntomas graves de más de 2 meses de duración, a pesar de TMO con fármacos y dispositivos, ausencia de disfunción ventricular derecha e insuficiencia tricuspídea graves, y más de uno de los siguientes factores2,9,23:
FEVI < 25% y VO2 pico < 12 ml/kg/min (si se ha medido).
Al menos 3 hospitalizaciones por insuficiencia cardíaca en los últimos 12 meses sin una causa precipitante obvia.
Dependencia de tratamiento inotrópico endovenoso.
Disfunción progresiva de órganos vitales (deterioro de la función renal o hepática) debido a perfusión reducida y no a presiones inadecuadas de llenado ventricular (PEP ≥ 20 mmHg y PAS ≤ 80-90 mmHg o índice cardíaco ≤ 2 L/min/m2).
Las indicaciones como terapia de destino o puente a la recuperación son menos frecuentes23. El alto costo actual de estos dispositivos limita su utilización en nuestro medio, por lo cual las recomendaciones para su indicación sólo se refieren para su aplicación en centros de alta complejidad que dispongan de estos equipos y de personal entrenado para su uso24.
En este sentido son tres los estudios, uno de ellos iniciado alrededor de 2001.
Terapia de células madre o miocardioplastia celular
Técnica que consiste en el implante de células madre (Figura 3)25, con el fin de inducir el crecimiento de nuevas fibras musculares (miogénesis) y el desarrollo de angiogénesis en el miocardio dañado, que podría contribuir a mejorar la función ventricular y revertir el proceso de remodelado postisquémico de las cámaras ventriculares26,27. Por tanto, el objetivo final de esta tecnología es que las células trasplantadas se diferencien en miocardiocitos, regeneren el tejido cardíaco y contribuyan, finalmente, a mejorar la función cardíaca del paciente28.
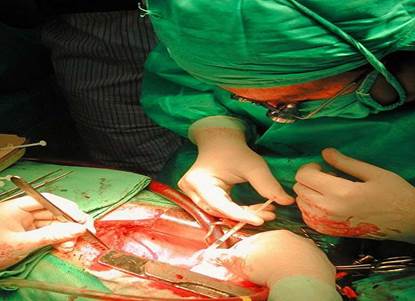
Figura 3 El Dr. José R. Hidalgo Díaz (Instituto de Cardiología y Cirugía Cardiovascular, La Habana, Cuba) implanta células madre de forma directa (por vía quirúrgica) al corazón de un paciente que había sufrido un infarto de miocardio. Tomada, con permiso de CorSalud, de Hidalgo Díaz et al. CorSalud. 2018;10:47-5125.
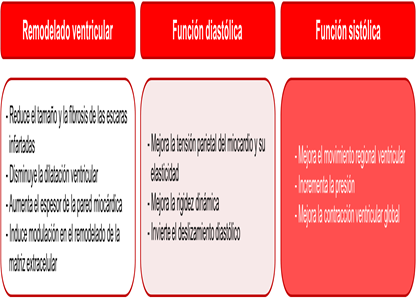
Los mecanismos de acción de la miocardioplastia celular, según Chachques et al29, se muestran en la figura 4; sin embargo, la eficacia de esta alternativa ha sido parcialmente cuestionada por estudios que no encontraron cambios en la FEVI, variable dependiente de cambios de la precarga, la poscarga, la contractilidad miocárdica y la activación neurohumoral, entre otras.
La terapia celular representa un avance promisorio para la Cardiología, aunque aún quedan muchas dudas por resolver, que incluyen: los criterios de selección de pacientes proclives a esta modalidad de tratamiento, las fuentes celulares a utilizar, su vía de implantación, la cantidad de células a implantar y el momento de su aplicación, entre otros.
Marcapasos en el nervio vago
El incremento de la estimulación del sistema simpático en la insuficiencia cardíaca responde al desequilibrio de un complejo sistema de señales inhibitorias y estimuladoras aferentes (especialmente por una depresión de los reflejos simpático-inhibidores) procedentes de barorreceptores arteriales y cardiopulmonares, quimiorreceptores arteriales, receptores metabólicos musculares y pulmonares30,31. El resultado neto es un incremento del tono simpático eferente (con la atenuación del tono parasimpático) cuya consecuencia es el incremento de los niveles de noradrenalina circulante, fruto tanto del aumento de su secreción como de la reducción de su recaptación32. En contra de las hipótesis iniciales que consideraban que el sistema nervioso central era un simple integrador de la información aferente y un transmisor pasivo de las señales eferentes, los modelos actuales establecen que los mecanismos reflejos vegetativos pueden modularse en el SNC por la acción de otras moléculas, como la angiotensina II30.
La nueva terapia, que se comenzó a evaluar hace varios años con el ensayo clínico multicéntrico europeo NECTAR-HF31, consiste en la estimulación del nervio vago (responsable en parte de la inervación cardíaca); pues estudios previos habían demostrado que la estimulación de este nervio es capaz de mejorar la función sistólica y, por tanto, de mejorar la sintomatología. Para el implante del neuroestimulador, el neurocirujano realizará dos incisiones de unos 5 cm: una en el lado derecho del cuello, por encima de la clavícula, donde se sitúa el nervio vago, y otra debajo, para alojar -a nivel subcutáneo- un dispositivo de tamaño similar a un marcapasos, que se conecta a un electrodo helicoidal que se enrolla alrededor del nervio vago, tras haber sido expuesto en unos 4 cm de longitud, entre la arteria carótida y la vena yugular interna. Sin embargo, según Zannad et al31, el mencionado ensayo clínico NECTAR-HF no pudo demostrar que la estimulación vagal tuviera un efecto significativo sobre el remodelado cardíaco y la capacidad funcional de los pacientes con insuficiencia cardíaca sintomática, pero sí lo tuvo sobre la calidad de vida.
Reducción del estrés de la pared del ventrículo izquierdo y la mejoría de la función: uso de Algisyl
La reducción de la tensión de la pared ventricular se considera piedra angular en el tratamiento de la falla cardíaca, en su forma más simple -basada en la ley de Laplace- la tensión de la pared ventricular es directamente proporcional al diámetro y la presión ventriculares, e inversamente proporcional al espesor de su pared. La opinión generalizada es que el aumento de tensión de la pared ventricular es responsable del proceso de remodelado adverso en el que los ventrículos se vuelven progresivamente más dilatados y, finalmente, llevan a la insuficiencia cardíaca. Los estudios clínicos y en animales de experimentación han demostrado que el aumento de tensión de la pared induce cambios en las proteínas, la síntesis de elemento contráctil y la expresión génica que apoyan el proceso de remodelación33. Según Hung et al34, el aumento del estrés de la pared ha demostrado ser un predictor independiente de la posterior remodelación del ventrículo izquierdo.
Recientemente, la inyección Algisyl (hidrogel de alginato, absorbible y biocompatible) en el ventrículo izquierdo, como tratamiento para la miocardiopatía dilatada, ha ganado la atención en la comunidad médica35. Este tratamiento ha demostrado ser eficaz para prevenir o incluso revertir la progresión de la insuficiencia cardíaca en los estudios en animales y, más recientemente, en un ensayo clínico en humanos35,36. Contrariamente a otros dispositivos, este tratamiento busca reducir la tensión de la pared ventricular al aumentar su espesor mediante la inyección del mencionado material en la pared libre del ventrículo izquierdo, que se engruesa y continúa reduciendo el tamaño del ventrículo izquierdo con el tiempo35-37. Lee et al36 demostraron, mediante resonancia magnética cardíaca, el engrosamiento de la pared del VI y la reducción significativa de su tamaño, en un paciente 6 meses después de recibir Algisyl-LVR (LoneStar Heart Inc., Laguna Hills, CA, EEUU).
Se ha demostrado que la inyección de biomateriales en el miocardio enfermo reduce el estrés de la miofibrilla y de la pared, restaura la geometría del ventrículo izquierdo y mejora su función; por lo que este tratamiento representa una promesa en los estudios preclínicos y clínicos35. Anker et al37 y Mann et al38 encontraron, en el estudio AUGMENT-HF, que el uso de Algisyl, unido al tratamiento médico estándar, proporcionó beneficios sostenidos a los 6 meses y al año en la capacidad de ejercicio, los síntomas y el estado clínico, en pacientes con IC avanzada; aunque no aportó resultados significativos en cuanto a mortalidad.
TRASPLANTE CARDÍACO
El trasplante cardíaco es un tratamiento aceptado para la insuficiencia cardíaca en fase terminal39,40. Aunque nunca se han realizado estudios aleatorizados, hay consenso en que el trasplante, siempre que se apliquen criterios de selección adecuados, mejora significativamente: la supervivencia, la capacidad de ejercicio, la calidad de vida y la posibilidad de reincorporación laboral.
Aparte de la escasez de donantes de corazón, los problemas principales del trasplante son consecuencia de la poca eficacia y las complicaciones del tratamiento inmunosupresor a largo plazo: rechazo mediado por anticuerpos, infección, hipertensión, insuficiencia renal, enfermedad maligna y vasculopatía coronaria. Los pacientes a considerar para trasplante cardíaco son aquellos con insuficiencia cardíaca terminal, síntomas graves y pronóstico desfavorable, sin otras alternativas de tratamiento; que estén motivados, bien informados y emocionalmente estables, y con capacidad para cumplir el tratamiento intensivo requerido durante el postoperatorio4,39,40.
Infección activa.
Enfermedad arterial periférica o cerebrovascular grave.
Hipertensión pulmonar irreversible con tratamiento farmacológico (se valorará implantar un dispositivo de asistencia ventricular izquierda y reevaluar al paciente).
Cáncer (en colaboración con los oncólogos se evaluará a cada paciente según el riesgo de recurrencia del tumor).
Insuficiencia renal irreversible (aclaramiento de creatinina < 30 ml/min).
Enfermedad sistémica multiorgánica.
Otras comorbilidades con mal pronóstico.
Índice de masa corporal antes del trasplante > 35 kg/m2 (se puede reevaluar tras la pérdida de peso corporal).
Abuso actual de alcohol o drogas.
Cualquier paciente cuyo apoyo social se considere insuficiente para alcanzar los requisitos del tratamiento en atención ambulatoria.
CONSIDERACIONES FINALES
Finalmente, más allá de todas las alternativas terapéuticas, farmacológicas y no farmacológicas, el tratamiento más efectivo en la insuficiencia cardíaca y en todas las enfermedades crónicas no trasmisibles cumplen un principio general, más sustentable que cualquier otro, basado en la evidencia científica de su efecto positivo sobre la salud, y es el protocolo de intervención para modificar estilos de vida.
Desde la atención primaria de salud, los programas de intervención para modificar los estilos de vida, a partir de los factores de riesgo modificables, así como la estabilidad clínica y humoral de las enfermedades que degeneran en insuficiencia o falla cardíaca, no solo prevén las consecuencias nefastas para la salud, sino que también abaratan los costos sanitarios insostenibles de no existir un sistema de salud con los niveles de atención que escalonen la asistencia médica.