Introducción
La catarata constituye una de las enfermedades oculares de mayor prevalencia, se estima que el 60 % de la ceguera en el mundo está originada por esta enfermedad; alrededor de 2 000 a 5 000 por millón de habitantes. Esta tiene diversos orígenes; sin embargo, en la mayoría de los casos está relacionada con el proceso normal de envejecimiento.1
No se puede predecir el ritmo de progresión de las cataratas, pues varía según el paciente y sus necesidades visuales. La solución es quirúrgica1) y es el procedimiento oftalmológico más comúnmente realizado;2 se trata de una intervención segura, rápida y eficaz, que consigue un buen resultado en 90-95 % de los casos. Se considera de bajo riesgo, de ahí que sea bien aceptada por los pacientes.1
El objetivo de la cirugía es eliminar el cristalino opacificado y sustituirlo con lentes intraoculares de diversos materiales para lograr una rehabilitación de la función visual.3)
La cirugía de catarata es, sin duda, uno de los procederes en la oftalmología con más avances tanto en tecnología como en la modernización de las técnicas quirúrgicas, lo que ha llevado a tener cada día mejores resultados en la visión de los pacientes. Al mismo tiempo, este avance ha provocado que los pacientes sean más exigentes y ya no sólo quieran ver, sino ver mejor, por lo que se han perfeccionado los métodos de medición de la lente intraocular (LIO) y la posición efectiva de la lente (ELP).4
La posición efectiva de la lente es uno de los grandes retos para el cirujano de catarata, ya que puede influir ampliamente en el resultado visual del paciente y está dada por el tamaño de la bolsa capsular, el modelo de la lente intraocular, así como la fibrosis de la bolsa capsular produciendo un desplazamiento de la LIO a los pocos meses después de la cirugía.5
Se sabe que la determinación de la ELP puede influir en el resultado visual final de los pacientes, por lo que, en la actualidad, la determinación final de la lente ha despertado gran interés.6
Tradicionalmente se evaluaba la morfología del cristalino por diferentes métodos clínicos subjetivos, en la actualidad se han desarrollado múltiples sistemas de diagnóstico no invasivo que permiten el análisis del segmento anterior ocular.7,8
El IOL Master 700, usa la tomografía de coherencia óptica de fuente de barrido (OCT SS, por su nombre en inglés: swept-source optical coherence tomography) de 1,050 nm de láser infrarrojo y 6 escaneos OCT a 0, 30, 60, 90, 120 y 150 grados que le permiten medir la longitud axial, profundidad de cámara anterior, grosor del cristalino y grosor corneal central. La profundidad de cámara anterior se determina desde el epitelio corneal hasta la superficie anterior del cristalino.9
El IOL Master utiliza una técnica de no contacto que tiene múltiples ventajas respecto a los biómetros anteriores, por ejemplo: evitar las distorsiones y errores que puede producir la depresión corneal de la biometría ultrasónica de contacto; no requiere anestesia local, ni dilatación pupilar y no lleva implícito riesgo de infección ni lesiones corneales.8
La posición efectiva de la lente se define como la distancia efectiva desde la superficie anterior de la córnea al plano del cristalino donde se espera se posicione la LIO.10) Es la única variable que no puede medirse en el preoperatorio y que debe predecirse. Al principio, la mayoría de las LIO eran de cámara anterior (CA) o prepupilares, por lo que en las fórmulas teóricas originales este factor se denominó profundidad de la CA (ACD, del inglés Anterior Chamber Depth) y se le asignó un valor constante (normalmente 2,8 o 3,5). Este valor se incorporó como “constante A” de la LIO en las fórmulas de regresión en los años ochenta, como la SRK. Aunque las fórmulas SRK I y II no se utilizan actualmente se sigue empleando la constante A de la LIO en representación de su posición en el ojo (ELP).11
La posición efectiva de la lente depende del posicionamiento final del mismo en el interior del ojo (saco, sulcus).12,13
La parte principal del cálculo del poder de la lente intraocular está dirigido a predecir correctamente la posición efectiva de la lente (ELP) para cualquier paciente y lente intraocular.12
En la actualidad algunos investigadores han dirigido sus estudios a la incorporación de nuevos parámetros biométricos del cristalino para formar parte importante en las fórmulas en el cálculo del lente. Aunque aún existen escasos resultados, los planos anatómicos del cristalino prometen ser variables de gran valor en ellas para lograr una mayor exactitud en el cálculo y en la predicción de la posición de la lente intraocular.
Es por ello que determinar la relación entre el plano ecuatorial y el plano central del cristalino con la posición real de la lente intraocular puede ayudar en el desarrollo de nuevas fórmulas de cálculo de la posición efectiva de la LIO.
Métodos
Se realizó un estudio observacional, descriptivo, prospectivo longitudinal en pacientes que requirieron cirugía de catarata con implante de lente intraocular (LIO) mediante extracción extracapsular del cristalino (EECC), por la técnica de facoemulsificación, operados por el mismo cirujano en el Centro de Microcirugía Ocular del ICO “Ramón Pando Ferrer” en el período comprendido de enero de 2018 a enero de 2021.
Se incluyeron los pacientes mayores de 18 años con diagnóstico de catarata, con criterio de cirugía, que estuvieron de acuerdo a participar en la investigación. Se excluyeron del estudio aquellos pacientes que tenían una o varias de las siguientes condiciones: Enfermedades generales como: diabetes mellitus, enfermedades inmunológicas, enfermedades del colágeno. Enfermedades oftalmológicas como: glaucoma, leucoma corneal, uveítis, traumatismos oculares, operados de cirugía refractiva. La muestra del estudio quedó constituida por 89 ojos de 67 pacientes con diagnóstico de catarata que acudieron al servicio de Catarata del ICO “Ramón Pando Ferrer” y que necesitaron cirugía en el período antes mencionado.
Para la realización de la investigación, la información referente al preoperatorio de los pacientes se tomó de la planilla de recolección de datos, que se utiliza de forma regular en la institución como parte del protocolo de la línea preoperatoria de catarata y se le añadió los resultados del posoperatorio a los tres meses de la cirugía. La fórmula utilizada para el cálculo del poder de la LIO fue la fórmula de tercera generación SRK/T.
Se realizó anamnesis y examen oftalmológico completo e integral que incluyó: toma de la mejor agudeza visual sin corrección (MAVSC) y con corrección (MAVC) por cartilla de Snellen, examen en lámpara de hendidura (Haag Streit BQ 900).
Además, se obtuvo la imagen sagital del ojo previo a la cirugía, obtenida mediante OCT-SS del IOL Master 700 (Carl Zeiss Meditec AG, Jena, Alemania).
Se midieron los planos ecuatorial y central del cristalino a través del programa Matlab mediante el uso del algoritmo canny: Canny.exe, Calcpotencia.exe (creado para tal finalidad) que permite la detección de los bordes de la imagen.
Todas las cirugías se realizaron por el mismo cirujano, mediante la técnica quirúrgica de facoemulsificación (Faco-chop).
En el posoperatorio inmediato se le indicó a cada paciente desocluir el ojo a las dos horas de operados y aplicar colirios de prednisolona 0,5 % (Quimefa, Cuba) y ciprofloxacino 0,3 % (Quimefa, Cuba) cada 2 horas, hasta ser evaluado al día siguiente en consulta.
La evaluación posoperatoria consistió en un examen del segmento anterior del ojo mediante biomicroscopía de igual manera que en el examen preoperatorio. Los pacientes fueron evaluados de la misma manera al sexto día, a los treinta días y a los 3 meses de operados.
A los 3 meses de la cirugía se les realizó a todos los pacientes examen con IOL Master 700 para obtener la imagen sagital del ojo con la posición final de la lente intraocular y posteriormente realizar el procesamiento de la misma a través del programa Matlab mediante el uso del algoritmo canny: lens.exe, lenspos2.exe (creado para tal finalidad).
Con la información que se obtuvo se confeccionó una base de datos en formato Excel de la Microsoft Office versión XP.
El análisis estadístico se realizó por la Prueba T- Student para comparar medias de datos pareados para las comparaciones múltiples de medias, con pruebas a posteriori de Scheffé al encontrar diferencias significativas en las comparaciones. Para el análisis de variables cualitativas se empleó chi cuadrado. En todos los casos se consideró una confiabilidad del 95 %. El análisis estadístico se realizó con el paquete estadístico SPSS v15.0.
Resultados
El estudio se realizó en 89 ojos de 67 pacientes. Existió un predominio del sexo femenino representado por el 53 %. El promedio de edad fue de 68,5 años, con una desviación estándar de ± 9,13 años; el grupo de edad con mayor representación fue el de 60 a 79 años con un 72 %.
Según el análisis de las variables biométricas de la totalidad de los ojos estudiados (tabla 2), las mensuraciones oculares estuvieron en valores promedio considerados estándar según la literatura;14 representado por una AXL promedio de 23,58 mm, Km de 44,29 D. La profundidad de la cámara anterior fue de 3,14 mm y el grosor del cristalino (LT) fue de 4,53 mm como promedio.
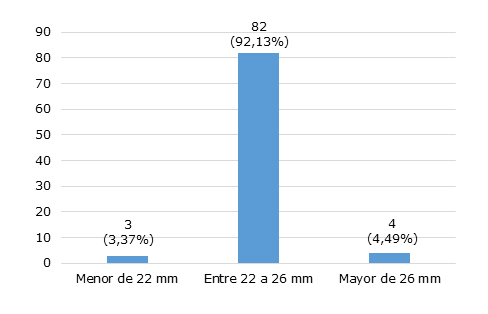
Se obtuvo que los ojos de tamaño entre 22 a 26 mm, constituyeron la gran mayoría de la muestra, representados por el 92,13 % del total. Los ojos cortos y los ojos largos estuvieron representados solo por el 3,37 % y el 4,49 %, respectivamente (fig. 1).
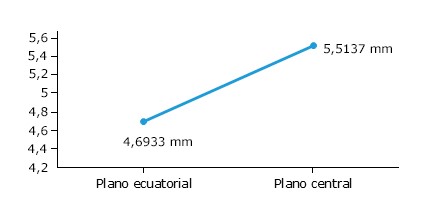
En la figura 2 se relacionan las variables plano ecuatorial y plano central del cristalino. El plano ecuatorial se encontró a una distancia promedio de 4,6933 mm mientras que el plano central se halló aproximadamente a 5,5137 mm como promedio. La diferencia entre ambas medias fue de -0,82045 mm con una p < 0,05 (p = 0,000); lo que resultó en diferencias estadísticamente significativas entre las mismas.
El plano ecuatorial medido a través del software desarrollado para la determinación del mismo, tuvo una media de 4,6933 mm, mientras que la posición real de la lente se encontró a una distancia promedio de 4,4721 mm. La diferencia de ambas medias fue de 0,22112 mm, diferencia que resultó significativa (p = 0,000). La media de la posición del plano central del cristalino fue de 5,5137 mm y la posición real media de la LIO de 4,4721 mm, con una diferencia de medias de 1,04157 mm y una p = 0,000. El análisis estadístico mostró diferencias significativas entre ambas variables (fig. 3).
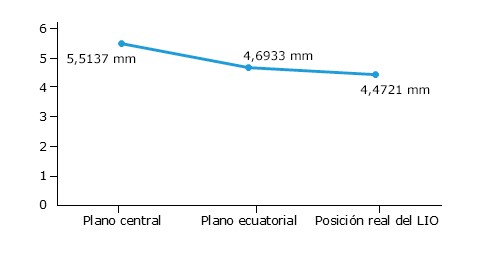
Fig. 3 Comportamiento de la posición real de la lente y su relación con los planos anatómicos del cristalino.
Todos los planos tienen diferencias significativas entre sí; sin embargo, la diferencia entre el plano ecuatorial y la posición real de la lente es menor en comparación a la diferencia entre el plano central y su posición real. No se puede decir que la posición real de la lente se relaciona exactamente o es similar al plano ecuatorial porque tienen diferencias significativas, pero si se puede plantear que tienen una menor diferencia en comparación con el plano central.
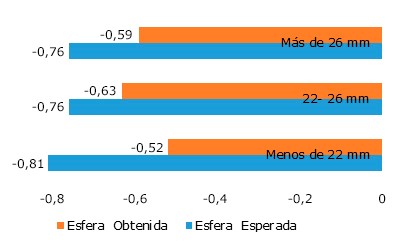
Al evaluar el resultado refractivo en función de la longitud axial, se observó que en los tres grupos de AXL el cálculo de la potencia de la lente se realizó para valores miopes como promedio (-0,50 a -1,00) y se obtuvo un valor refractivo posoperatorio según lo estimado para valores negativos, sin diferencias significativas entre ellos, p > 0,05 para cada uno de los grupos de longitud axial (fig. 4).
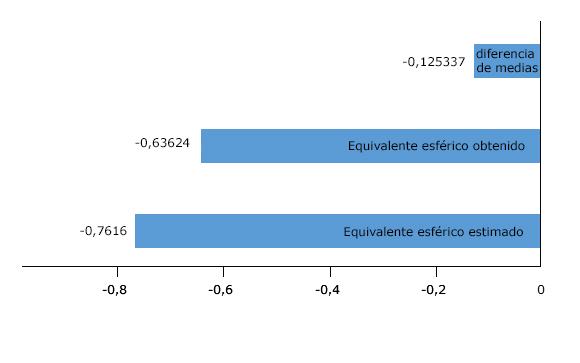
Finalmente, el equivalente esférico estimado de toda la muestra tuvo una media de -0,7616 D y el equivalente esférico obtenido fue de -0,63624 D como promedio. La diferencia de ambas medias (error de predicción) fue de -0,125337 y el valor de la p > 0,05 (p = 0,116); por lo que no existió diferencia significativa entre los valores de equivalente esférico estimado por la fórmula y los valores de equivalente esférico obtenidos; evidencia de un adecuado cálculo de la lente intraocular y del correcto posicionamiento de la misma (fig. 5).
Discusión
El desarrollo actual de las nuevas técnicas quirúrgicas y la alta tecnología, asociadas a biometría por interferometría, permite analizar múltiples variables en diferentes grupos de pacientes en los cuales se facilita la obtención de resultados más predictibles y evitar la aparición de sorpresas refractivas.15 El IOL Master 700 es un ejemplo de esta tecnología de punta que facilita la obtención de imágenes por tomografía de coherencia óptica por fuente de barrido sin contacto con el globo ocular en un corto período de tiempo y cuya exactitud en las mediciones ha sido comprobada.
En un estudio realizado en el Instituto Cubano de Oftalmología,15 así como estudios publicados por el Instituto Universitario de Valladolid y la Universidad de Zaragoza, revelan que el sexo femenino es el más frecuente, así como el grupo etario mayor de 60 años,16,17 resultados similares a los obtenidos en esta investigación y que se relacionan con las características demográficas de la población cubana, en la cual el sexo femenino predomina sobre el masculino, así como la población mayor de 60 años debido al envejecimiento poblacional, y además, por tratarse la catarata, de una enfermedad relacionada en gran medida con el envejecimiento.15,18
El hecho de que la mayoría de la muestra coincida con ojos de longitudes axiales medias, hace que los resultados para este rango sean muy similares a los del rango total de longitud axial. La escasa presencia de ojos cortos y largos constituye de por sí una limitante del estudio y es común en investigaciones donde la casuística pertenece a un solo cirujano, puesto que el volumen de pacientes necesario para lograr resultados con significación estadística en ojos incluidos en estas longitudes axiales solo es posible en estudios con muestras amplias que incluyen múltiples cirujanos, preferiblemente multicéntricos.
En la presente investigación, los resultados coinciden con los obtenidos por el Dr. Hernández López en estudio realizado en el ICO Ramón Pando Ferrer en más de 20000 casos estudiados en los cuales la AXL promedio fue de 23,52 mm.14,19
Por otra parte, en estudios realizados a nivel mundial se reporta una AXL promedio menor al utilizar ultrasonido e interferometría de coherencia parcial, respectivamente.20,21
En investigación previa realizada en Cuba en el año 2014 se reporta un valor promedio de AXL superior,22 en comparación a los obtenidos en la presente investigación.
La ACD promedio en la presente investigación fue de 3,14 mm, la misma resultó menos profunda que el promedio de ACD reportada en poblaciones latinas y asiáticas, aunque en menor medida en poblaciones asiáticas en la cual al establecer comparación fue prácticamente similar.19,23,24
Los resultados obtenidos en relación con el promedio del grosor del cristalino (LT) fueron similares a los encontrados por el Hernández López en su estudio sobre biometría reportado en el presente año19 y de igual manera son superiores a los reportados al estudiar poblaciones latinas y asiáticas.23,24
En los últimos años, se ha comenzado a estudiar el uso de parámetros anatómicos preoperatorios del cristalino como el plano ecuatorial, el área de superficie, el volumen y el diámetro, que no estaban considerados dentro de las fórmulas tradicionales previamente mencionadas.
El plano ecuatorial del cristalino se define como la intersección de las curvaturas anterior y posterior de las superficies del lente.25,26 Algunos estudios han sugerido que su estimación podría tener un gran valor para calcular el poder de la lente y mejorar el resultado refractivo de cada paciente.27
Yoo y otros, usan el plano ecuatorial del cristalino como nuevo parámetro para mejorar los resultados refractivos en la cirugía de catarata en un programa de trazado de rayos.26 En su estudio reportan el plano ecuatorial del cristalino medido como promedio a 4,81 ± 0,29 mm; 4,84 ± 0,27 mm y 4,97 ± 0,23 mm para los tres grupos de estudio establecidos según las lentes intraoculares implantadas,26 en la presente investigación el plano ecuatorial y el plano central del cristalino se encontraron a 4,6933 mm y 5,5137 mm, respectivamente como promedio.
Tsunehiro y otros usan imágenes del cristalino tomadas por OCT de segmento anterior que permiten calcular el plano ecuatorial, para predecir la posición efectiva de la LIO. Este se encuentra a 4,84 mm del epitelio corneal central como promedio.25) Resultado similar al obtenido en el presente estudio en el cual el ecuador del cristalino se localizó a 4,69 mm como promedio.
Se sabe que la posición real de la LIO depende del saco capsular. En su investigación, Tsunehiro propone que los hápticos de la LIO coinciden con la posición postoperatoria del ecuador del saco capsular. Esto podría sugerir una asociación entre los planos del cristalino y la posición final de la LIO.25 Es por ello que establecer la relación entre el plano ecuatorial y el plano central del cristalino con la posición real de la lente intraocular, puede ayudar en el desarrollo de nuevas fórmulas de cálculo de la posición efectiva de la LIO.
En el presente estudio se encontró que el plano ecuatorial presentó diferencias significativas con la posición real de la lente intraocular. Del mismo modo, el plano central del cristalino presentó diferencias significativas con la posición real de la lente intraocular. Finalmente, se obtuvo que ambos planos anatómicos del cristalino fueron diferentes entre sí. Sin embargo, se podría decir que la diferencia entre el plano ecuatorial y la posición real de la lente intraocular fue menor a la observada entre el plano central y la posición real de la LIO. Por lo tanto, el plano ecuatorial podría usarse en el preoperatorio como una variable a tener en cuenta para predecir la posición real de la LIO. La escasa casuística de la muestra en el estudio puede influir en que aceptemos la hipótesis nula cuando probablemente sea cierta, teniendo en cuenta lo observado por varios investigadores.25,26,28
Yoo reporta en su estudio que el plano ecuatorial del cristalino puede ser usado como medida de la posición real de la lente intraocular después de su implante por lo que este parámetro podría considerarse en nuevas fórmulas de cálculo de LIO; sin embargo, explica que el plano ecuatorial no está exactamente en la posición de la lente por lo que se podría determinar una constante entre ambas variables.26
La mayoría de los pacientes antes de la cirugía presentaban un defecto refractivo miópico como era de esperarse debido a que se ha demostrado que las cataratas inducen un cambio miópico en la refracción.29)
Hasta hace muy poco, los rangos dióptricos tradicionalmente analizados en la literatura eran ± 0,50 D; ± 1,00 D y ± 2,00 D de error de predicción refractivo.30) La emetropía aún se considera dentro de las ± 0,50 D y al realizar este análisis en el presente estudio donde los pacientes fueron calculados para valores miópicos entre -0,50 y -1.00 D se obtuvo un valor refractivo posoperatorio promedio en el rango calculado con independencia de la longitud axial. Jinho y otros observan que la refracción posoperatoria con el uso de fórmulas de tercera generación (dentro de las que se incluye la SRK/T) tienen tendencia hacia la hipermetropía, en comparación a las fórmulas más actualizadas,31 aun cuando el cálculo de la lente se planifique para valores discretamente miópicos. Los resultados de la presente investigación, no coincidieron con los obtenidos por Jinho y otros, pues la lente se calculó para valores negativos y el resultado posoperatorio se mantuvo en valores negativos en el rango para los que fueron calculados.
En investigación realizada en el Instituto de Óptica “Daza de Valdés” en España en el 2018 por Martinez-Enriquez se estudia una nueva fórmula para calcular la ELP usando parámetros preoperatorios como el plano ecuatorial, el área de superficie, el volumen y el diámetro del cristalino, y se obtiene un menor error de estimación en comparación con las fórmulas convencionales. El promedio de error refractivo que se obtiene en dicha investigación es de 0,20 ± 0,53;28 mientras que el promedio de error de predicción obtenido en el presente estudio fue de -0,12. Por su parte, el error de predicción que muestran Tsunehiro y otros en su estudio es de 0,41 ± 0,53 para la fórmula SRK/T.25
Los errores de predicción que constata Yoo en su estudio, utilizando los planos del cristalino son menores en comparación con los errores de predicción de la fórmula de Haigis, (0,13 D, 0,10 D y 0,15 D en los tres grupos de estudio establecidos según las lentes intraoculares implantadas).26) En el presente estudio, el promedio de error de predicción fue de -0,12 D.
En estudio realizado por el Hernández López relacionado con la comparación de varias fórmulas biométricas para el cálculo del lente intraocular encuentra que con la fórmula SRK/T el menor error de predicción refractivo medio es de 0,48 ± 0,40; un valor más positivo de lo esperado según su reporte, no obstante dentro de la emetropía que aún se considera dentro de las ± 0,50 D.32 Los resultados obtenidos en la presente investigación son inferiores a los obtenidos por otros autores según la literatura consultada,25,26,28,32 pero todos se encuentran en rangos de emetropía.
En la presente investigación predominaron los pacientes mayores de 60 años y el sexo femenino. Los valores de las medidas biométricas oculares y el tamaño de los ojos estuvieron en valores promedios considerados estándar. El plano ecuatorial ocupó una posición más cercana a la posición real de la LIO que el plano central del cristalino. No existieron diferencias significativas entre el valor promedio del equivalente esférico estimado y el obtenido independientemente de la longitud axial del ojo y el error de predicción de la fórmula SRK/T es cercano a cero para el rango total de longitudes axiales.
En la actualidad, a nivel mundial y en Cuba, aún no existen suficientes estudios desarrollados sobre el tema y que describan resultados de investigaciones con un gran volumen de pacientes estudiados, pero el correcto cálculo y la adecuada estimación de la posición de la lente intraocular, en la bolsa capsular, empleando mediciones de la geometría del cristalino independiente a la longitud axial; permitirá mejorar los resultados refractivos y que estén en correspondencia a lo esperado previo a la cirugía.