Introducción
El síndrome de May-Thurner (SMT) es una afección que compromete la vena ilíaca común izquierda (VICI), la cual es comprimida por la arteria ilíaca común derecha (AICD) contra la columna vertebral.1) Se considera una variante anatómica normal, presente hasta en el 22-32 % de las personas.2) La compresión a nivel ilíaco generalmente no es significativa para desencadenar manifestaciones clínicas y complicaciones, es necesario la suma de fenómenos protrombóticos predisponentes como cirugías recientes, la inmovilización prolongada y más recientemente el SARS-CoV-2 causante de COVID-19; el cual causa un desequilibrio entre factores anti y procoagulantes, favoreciendo la activación de la coagulación,3,4) generando las complicaciones, que suelen ser trombosis venosa profunda (TVP) y tromboembolismo pulmonar (TEP).1,3
El diagnóstico se realiza a través de imágenes. El norma de oro es la ecografía intravascular (IVUS), la cual permite la visualización directa de la compresión de la vena ilíaca. Sin embargo, la angiotomografía o resonancia magnética (RMN) también permite la visualización de la variante anatómica.5,6
El tratamiento del SMT y sus complicaciones se fundamentan en el uso de trombolíticos, anticoagulantes y la revascularización con implantación de stents. Asimismo, la terapia antiplaquetaria prolongada es importante para disminuir el riesgo de oclusión del stent y síndrome postrombótico.1,7
Al ser una enfermedad de baja incidencia a nivel mundial y en nuestro medio, presentamos el caso en la ciudad de Bucaramanga, Colombia, con el objetivo de comparar la clínica y la posible relación de la enfermedad tromboembólica venosa en el curso de la COVID-19 en pacientes con SMT.
Caso clínico
Mujer de 24 años, secretaria de profesión y residente en Bucaramanga. Presentó un cuadro clínico de 20 días de evolución que inició con rinorrea hialina, tos ocasional y mialgias; cinco días después manifestó fiebre no cuantificada y tos con expectoración hemoptoica. En los últimos tres días se asoció a edema progresivo asimétrico, parestesias y dolor moderado en miembro inferior (MMII) izquierdo, que limitaba la deambulación.
Al examen físico se observó una paciente sin signos de dificultad respiratoria, peso de 65 kilogramos, talla de 158 centímetros, presión arterial de 109/58 mmHg, frecuencia respiratoria de 18 respiraciones por minuto y pulsioximetría 97 %. Como hallazgos anormales se encontraron frecuencia cardíaca de 110 latidos por minuto, temperatura 38,1 °C, leve dolor a la palpación profunda en hemiabdomen izquierdo y en MMII izquierdo, además de edema asimétrico grado III, signo de fóvea pretibial, frialdad distal, palidez, signos de Pratt y Homans positivos, llenado capilar de cuatro segundos y pulso pedio no palpable en MMII izquierdo. Dada la historia clínica y los hallazgos al examen físico se inició terapia con heparinas de bajo peso molecular (HBPM).
Las pruebas para SARS-Cov-2, rtPCR y antígeno en hisopado nasofaríngeo fueron negativos, con anticuerpos IgM negativo/IgG positivo.
Se realizó ecografía Doppler venosa de miembros inferiores (MMIIs) que reportó imagen ecogénica desde la vena femoral común, la cual se extendía hacia la confluencia safenofemoral y fémoro-femoral, por lo que se sugirió posible SMT. Por sospecha clínica de TEP se solicitó tomografía (TAC) de tórax con protocolo para TEP, que evidenció ocupación por material con densidad de tejido blando de la luz de las arterias lobares inferiores, segmentarias y subsegmentarias además de vidrio esmerilado en la periferia del segmento posterior del lóbulo inferior derecho (figura 1). Por lo tanto, se definió TEP bilateral agudo. Dado su estado hemodinámico y las características imagenológicas no se consideró trombólisis sistémica ni manejo endovascular. Se ampliaron los hallazgos con TAC contrastada de abdomen y pelvis, en la que se observó compresión de VICI por AICD contra el cuerpo vertebral de L4.
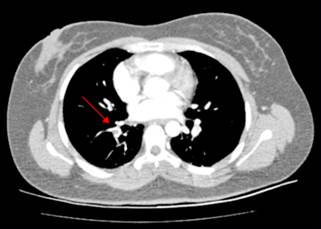
Fig. 1 TAC de tórax. La flecha blanca señala la ocupación isodensa (émbolo) de la arteria lobar inferior derecha.
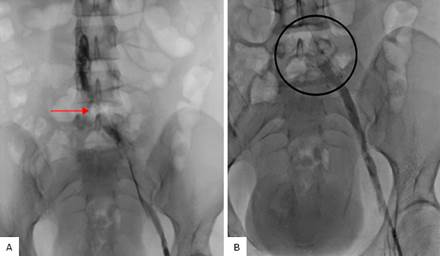
Posteriormente, se indicó flebografía de MMII izquierdo, que reportó oclusión marcada en todo el trayecto venoso a nivel de la unión iliocava (figura 2), la cual definió el diagnóstico de SMT con TVP extensa, por consiguiente, se realizó angioplastia con implantación de dos stents y trombectomía venosa con manejo posterior en unidad de cuidados intensivos. Finalmente, la paciente mostró evolución clínica satisfactoria, por lo cual se dio egreso al octavo día de hospitalización bajo manejo con ácido acetilsalicílico (ASA) y anticoagulantes orales directos (DOACs) prolongado.
Discusión
El SMT, también conocido como síndrome de compresión de la vena ilíaca, es una enfermedad vascular poco diagnosticada, que implica el estrechamiento de VICI por compresión contra la columna vertebral lumbar, ejercida por AICD, la cual predispone a una trombosis iliofemoral izquierda.1,5
Se desconoce la prevalencia real del SMT dado que es una afección subdiagnosticada, debido a que la mayoría de los pacientes son asintomáticos. Aun así, se estima que está presente entre el 2 y el 5 % de los pacientes con enfermedad venosa de MMIIs y su prevalencia asciende entre el 18 al 49 % cuando hay presencia de TVP proximal del MMII izquierdo. Por otra parte, otros estudios describen el SMT como una variante normal frecuente presentada entre el 22-32 % de las autopsias realizadas.2,6
El diagnóstico de SMT, y por ende las complicaciones, suelen ocurrir en personas de entre 18 y 50 años, con el doble de frecuencia en mujeres según Kaltenmeier y otros.3 No obstante, según otros autores las mujeres tienen hasta cinco veces más probabilidad de ser afectadas.1 No hay diferencia entre género en la proporción de pacientes que desarrollan TVP. Sin embargo, es más probable que las mujeres presenten TEP en el momento del inicio de las manifestaciones clínicas.3 Como es nuestro caso, donde era una paciente femenina en el grupo etario mencionado que debutó con TVP y TEP.
Fisiopatológicamente, la compresión pulsátil crónica sobre VICI altera el retorno venoso del MMII a nivel iliofemoral; además, produce una lesión endotelial, la cual estimula la formación de bandas de colágeno denominados espolones venosos que, finalmente desencadenan TVP. La obstrucción generalmente no es crítica y es necesaria la presencia de factores predisponentes para el desarrollo de TVP.5,8 La cirugía reciente, el cáncer, la inmovilización prolongada, la hipercoagulabilidad, la terapia de reemplazo hormonal, el trauma, el embarazo, el uso de anticonceptivos orales y las infecciones son los principales factores predisponentes en las personas con SMT para desarrollar TVP y TEP.1,5
Ahora bien, en la actualidad se conoce que la COVID-19 más allá de ser una enfermedad respiratoria, su fisiopatología corresponde a un fenotipo protrombótico, el cual se asocia con trombosis arterial y venosa.4,9 La coagulopatía en la COVID-19 no se ha esclarecido completamente; sin embargo, se conoce que la respuesta inflamatoria sistémica y la tormenta de citocinas que desencadena produce un desequilibrio entre los factores anti y procoagulantes, como lo son la elevación del factor de von Willebrand y la trombina, asimismo favorece la disminución de la fibrinolisis. Cabe destacar que estos fenómenos se desarrollan más frecuentemente en pacientes con alguna comorbilidad que predisponga a la formación de coágulos.4,9 Si bien aún no se ha dilucidado la etapa de la enfermedad en que existe una mayor probabilidad de presentar eventos trombóticos, dada la cronología de los eventos, consideramos que, en nuestro caso, el factor desencadenante para el desarrollo de TVP/TEP fue la infección reciente por SARS-Cov-2.
La mayoría de las personas con SMT no presentan síntomas; sin embargo, cuando ocurre una oclusión significativa de la VICI, estos aparecen. Este estrechamiento puede provocar edema y dolor del MMII izquierdo, claudicación venosa, hiperpigmentación y endurecimiento o adelgazamiento de la piel e incluso desarrollo de úlceras o venas varicosas por estasis venosa. Existen síntomas infrecuentes que incluyen flegmasia cerúlea dolens y ruptura espontánea de la vena ilíaca. Los síntomas generalmente afectan al MMII izquierdo o la pelvis, pero también se han reportado en el lado derecho y bilateral, asimismo, estos pueden ser intermitentes durante el día.1,3 En este caso, la paciente presentó edema progresivo asociado a dolor moderado, palidez y pulsos no palpables en MMII izquierdo dos semanas posteriores de la sintomatología respiratoria.
Se reconocen tres estadios clínicos del SMT:
Los principales diagnósticos diferenciales del SMT son la obstrucción venosa por linfadenopatía, hematomas o celulitis asociados a neoplasias malignas subyacentes,7 los cuales fueron descartados en nuestro caso mediante las imágenes.
La sospecha del SMT es clínica, pero el diagnóstico es imagenológico. La ecografía Doppler de MMIIs suele ser la herramienta inicial de elección para la valoración en el contexto de TVP. En este caso fue importante para el abordaje diagnóstico, ya que permitió definir la probabilidad de la variante anatómica, así como visualizar los signos indirectos de la trombosis venosa. Por otro lado, tanto las imágenes de TAC como de RMN tienen alta sensibilidad y especificidad en la valoración de la sospecha de SMT, principalmente para descartar otras causas de compresión de VICI. El Gold standard para el diagnóstico de SMT es la IVUS, que tiene una sensibilidad y especificidad mayor al 98 %, la cual permite la valoración directa de la compresión de VICI en tiempo real y, a su vez, puede evaluar el tamaño exacto del diámetro luminal y el grado del espolón. Las pruebas invasivas suelen reservarse para los casos en los que se planifica tratamiento con angioplastia o endoprótesis.5,6,7,8,10,11 La flebografía, al igual que la IVUS, es útil en identificar la compresión de la VICI y para determinar su gravedad con una sensibilidad y especificidad cercana al 95 %; por lo tanto, es una herramienta alternativa estándar para definir el diagnóstico ante la poca disponibilidad de la IVUS.1,8 En este caso se usó flebografía, dado que en la institución no se contaba con IVUS para el diagnóstico definitivo de SMT.
Las estrategias de tratamiento han evolucionado. Las técnicas más recientes se basan en el uso de trombolíticos y revascularización con implantación de stents. Aunado a ello, la terapia anticoagulante prolongada también se considera un pilar en el tratamiento de la TVP. Además, se recomienda la terapia antiplaquetaria (sin consenso de su duración) y medias de compresión mecánica después de la colocación de un stent, para prevenir su oclusión y la formación recurrente de coágulos.1,2,7 Según la literatura, la duración de la terapia anticoagulante posangioplastia con stens debe ser por lo menos de seis a doce meses en caso de único episodio de complicaciones tromboembólicas, o de forma indefinida en pacientes con múltiples episodios de TVP o trombofilia.6 Se desconoce el régimen anticoagulante óptimo ajustado en pacientes con SMT y COVID-19. No obstante, aunque las guías no son unánimes en las recomendaciones, dada la mayoría de evidencia disponible, la recomendación actual en pacientes con infección por SARS-Cov-2 que cursan con TVP y/o TEP, es mantener terapia anticoagulante por tres meses tras el alta médica, prefiriendo los DOACs antes que otros anticoagulantes, como la warfarina, por su eficacia y seguridad.12 Sin embargo, hacen falta estudios que evalúen el riesgo-beneficio de DOACs frente a otros anticoagulantes posterior a la intervención quirúrgica en pacientes con SMT.
Otras opciones de tratamiento suelen reservarse para el fallo de las terapias de primera línea como es el caso de trombectomía con reposicionamiento de AICD lejos de VICI.1,11 En nuestro caso, el tratamiento definido fue el uso de terapia anticoagulante aunado a angioplastia venosa y trombectomía de MMII izquierdo, además terapia antiplaquetaria al egreso.
La supervivencia de los pacientes con SMT depende de la gravedad y del riesgo estimado de recurrencia de sus complicaciones; este último, a su vez, precisa el tiempo de terapia anticoagulante posterior al egreso hospitalario, pero aún hacen falta estudios fundamentando el uso de estos tratamientos después del manejo con stens venosos. Se debe llevar un control multidisciplinario dirigido por hematología o medicina vascular, para optimizar el manejo.1,2 Por otra parte, no existen estudios que comparen gravedad y mortalidad de TEP en pacientes con SMT vs sin SMT.
En el caso, la paciente posterior al manejo endovascular tuvo una evolución clínica favorable, por lo cual a los ocho días de estancia hospitalaria se le dio alta médica, con indicación de continuar tratamiento ambulatorio con ASA y DOACs por tres y seis meses, respectivamente.
Conclusiones
Se ha demostrado que dentro de la fisiopatología de la infección por SARS-CoV-2 se desarrollan mecanismos procoagulantes, lo cual incrementa el riesgo de eventos trombóticos en pacientes con o sin factores de riesgo. Por su parte, el SMT es una enfermedad que, aunque generalmente cursa asintomática, acompañada de otros factores protrombóticos puede generar manifestaciones clínicas y complicaciones que incluyen la TVP y el TEP, como fue en nuestro caso, el cual presentó un desenlace satisfactorio dado el diagnóstico e intervención oportuna.
Aporte científico
El caso presentado permite reconocer en la asociación SMT/COVID-19 una mayor probabilidad de eventos trombóticos. Sin embargo, en la mayoría de los casos la identificación de la variante vascular se hace durante el evento agudo, no siendo posible establecer estrategias de seguimiento estrecho o prevención en pacientes con infección por SARS-CoV-2.