INTRODUCCIÓN
La conservación de la biodiversidad en Cuba es una preocupación constante dada la riqueza florística y vulnerabilidad de las comunidades vegetales. Por ello, en la Lista Roja de la Flora de Cuba (González y Torres et al., 2016) se reconoce la necesidad de realizar monitoreo continuo a la flora que habita los matorrales xeromorfos costeros, por constituir ecosistemas muy afectados por eventos climáticos y la acción del hombre.
Los estudios florísticos costeros de la provincia Cienfuegos se fomentaron en el Siglo XX a partir de expediciones botánicas dirigidas por el Atkins Institution of Arnold Arboretum, actual Jardín Botánico de Cienfuegos (JBC). En estos trabajos se describieron nuevas especies, entre ellas: Thespesia cubensis (Britton & P. Wilson) J.B. Hutch, Acalypha hutchinsonii Britton, Caesalpinia cubensis Greenm; Hebestigma cubense (Kunth) Urb.; Pectis ritlandii R.A. Howard y se localizaron otras de interés como Dendrocereus nudiflorus (Engelm.) Britton & Rose y Annona havanensis R.E. Fr. El calentón de Don Bruno es un accidente geográfico de índole marina ubicado en el extremo sur-oeste de la Bahía de Cienfuegos. El sector costero correspondiente es un sitio de interés científico por su riqueza de especies referida por Combs (1897) y Howard y Briggs (1953a); además, por ser la localidad tipo de Agave grisea Trel. (Trelease, 1913) y Paspalum jaguenseLeón (1946). Sin embargo, hasta la fecha no se cuenta con un estudio actualizado de la flora y la vegetación en esta zona, la cual se considera vulnerable por el crecimiento poblacional e industrial. Por tanto, el objetivo de este trabajo es caracterizar la flora y vegetación de Caletón de Don Bruno para trazar futuras líneas de trabajo en función de preservar su patrimonio florístico.
MATERIALES Y MÉTODOS
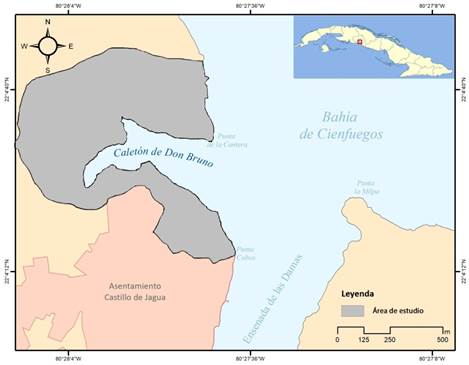
La zona de estudio se localiza en los 22°04'34''N, -80°27'48''O, según puntos de coordenadas tomados con el Sistema de Posicionamiento Global (GPS). Limita al norte con Calicito, al oeste y sur con las comunidades Castillo de Jagua-El Perché y la Ciudad Nuclear respectivamente y al este con la bahía de Cienfuegos. Desde el punto de vista fitogeográfico corresponde al distrito “Casildense” según Borhidi (1991). La zona terrestre correspondiente al Caletón de Don Bruno ocupa un área de 3 km2 (Figura 1).
Se realizaron inventarios de flora en el área de estudio, mediante 20 transectos a lo largo de las terrazas marinas y cuatro transectos descendentes desde la máxima altitud hasta el nivel del mar. El listado de especies de la flora se elaboró a partir de observaciones y colectas a cada lado de los transectos, hasta dos metros. Los materiales recolectados fueron depositados en el Herbario Atkins del Jardín Botánico de Cienfuegos (AJBC). Las especies se identificaron utilizando claves dicotómicas, materiales de herbario y descripciones botánicas. El endemismo y los nombres de los taxones fueron revisados de acuerdo a Greuter y Rankin (2017) y las formaciones vegetales se clasificaron siguiendo los criterios de Capote y Berazaín (1984). Se listaron las especies, con sus respectivas familias y categoría de amenaza según Gonzáles-Torres et al. (2016). Se determinaron aquellas con potencial invasor de acuerdo a Oviedo et al. (2015). Adicionalmente se describió el hábitat y se identificaron las amenazas en el mismo. Se describió la vegetación a partir de la caracterización de las formaciones vegetales, sus estratos predominantes y especies más abundantes.
RESULTADOS Y DISCUSIÓN
Con el estudio de la flora de Caletón de Don Bruno se registraron 164 taxones, de 131 géneros, pertenecientes a 55 familias botánicas (Tabla 1). De ellas 124 son autóctonas y 26 exóticas, entre las cuales 14 son potencialmente invasoras. Las familias representadas por el mayor número de géneros son Fabaceae (12), Malvaceae (8), Poaceae (7), Rubiaceae (7) y Euphorbiaceae (6).
Tabla 1 Listado florístico del Caletón de Don Bruno, Cienfuegos
| Familia | Nombre Científico | End | Aut | Exot | Cat. Amenaza |
|---|---|---|---|---|---|
| Avicennaceae |
|
X | LC | ||
| Acanthaceae |
|
X | NE | ||
| Amaranthaceae |
|
X | NE | ||
|
|
X | NE | |||
| Amaryllidaceae |
|
X | |||
| Anacardiaceae |
|
X | LC | ||
|
|
X | LC | |||
|
|
X | ||||
| Apocynaceae |
|
X | NE | ||
|
|
X | NE | |||
|
|
X | ||||
|
|
X | NE | |||
|
|
X | NE | |||
| Aquifoliaceae |
|
X | |||
| Arecaceae |
|
X | CR | ||
|
|
X | LC | |||
| Asparagaceae |
|
X | LC | ||
|
|
X | CR | |||
| Asteraceae |
|
X | LC | ||
|
|
X | ||||
|
|
X | LC | |||
|
|
X | DD | |||
| Bignoniaceae |
|
X | A | ||
|
|
X | ||||
| Boraginaceae |
|
X | LC | ||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | NT | |||
|
|
X | LC | |||
| Bromeliaceae |
|
X | LC | ||
|
|
X | NE | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
| Burseraceae |
|
X | NE | ||
|
|
X | NE | |||
| Buxaceae |
|
X | NT | ||
| Cactaceae |
|
X | |||
| Capparaceae |
|
X | LC | ||
|
|
X | LC | |||
| Cleomaceae |
|
X | |||
| Combretaceae |
|
X | NE | ||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | NE | |||
| Convolvulaceae |
|
X | |||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | ||||
| Cyperaceae |
|
X | LC | ||
|
|
X | LC | |||
| Ebenaceae |
|
X | LC | ||
|
|
X | A | |||
| Erythroxylaceae |
|
X | LC | ||
|
|
X | LC | |||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | NE | |||
| Euphorbiaceae |
|
X | LC | ||
|
|
X | DD | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | ||||
|
|
X | ||||
|
|
X | DD | |||
|
|
X | LC | |||
|
|
LC | ||||
| Phyllantaceae |
|
X | LC | ||
|
|
X | LC | |||
| Fabaceae |
|
X | |||
|
|
X | NE | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | ||||
|
|
X | CR | |||
|
|
X | ||||
|
|
X | ||||
|
|
X | LC | |||
|
|
X | A | |||
|
|
X | LC | |||
| Hypericaceae |
|
X | LC | ||
| Lamiaceae |
|
X | NE | ||
| Malpighiaceae |
|
X | A | ||
|
|
X | LC | |||
| Malvaceae |
|
X | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | ||||
|
|
X | LC | |||
| Meliaceae |
|
X | LC | ||
| Myrsinaceae |
|
X | LC | ||
| Myrtaceae |
|
X | NE | ||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | NE | |||
| Nyctaginaceae |
|
X | NE | ||
| Ochnaceae |
|
X | NE | ||
| Orchidaceae |
|
X | NE | ||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | ||||
|
|
X | DD | |||
|
|
X | NE | |||
| Phyllanthaceae |
|
X | |||
|
|
X | LC | |||
| Picrodendraceae |
|
X | NE | ||
| Poaceae |
|
X | NE | ||
|
|
X | ||||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | ||||
|
|
X | NE | |||
|
|
X | ||||
| Polygonaceae |
|
X | LC | ||
| Primulaceae |
|
X | |||
|
|
X | NE | |||
| Rhamnaceae |
|
X | NE | ||
|
|
X | NE | |||
| Rhizophoraceae |
|
X | NE | ||
| Rubiaceae |
|
X | LC | ||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | DD | |||
|
|
X | ||||
|
|
LC | ||||
|
|
X | LC | |||
|
|
X | LC | |||
| Salicaceae |
|
X | NE | ||
|
|
X | LC | |||
| Sapindaceae |
|
X | NE | ||
|
|
X | NE | |||
|
|
X | NE | |||
|
|
X | ||||
|
|
X | DD | |||
| Sapotaceae |
|
X | LC | ||
|
|
X | EN | |||
|
|
X | EN | |||
|
|
X | LC | |||
|
|
X | LC | |||
|
|
X | LC | |||
| Scrophulariaceae |
|
X | NE | ||
| Simaroubaceae |
|
X | NE | ||
| Smilacaceae |
|
X | LC | ||
| Solanaceae |
|
X | LC | ||
|
|
X | ||||
| Turneraceae |
|
X | NE | ||
| Urticaceae |
|
X | LC | ||
| Verbenaceae |
|
X | NE | ||
|
|
X | NE | |||
|
|
X | NE | |||
| Zygophyllaceae |
|
X | LC |
Leyenda: End=Endémica, Aut=Autóctona, Exót=Exótica, CR=En Peligro Crítico, EN: En Peligro, A= Amenazada, NT= Casi amenazado, LC= con preocupación Menor, NE= No Evaluadas, DD=Datos Insuficientes
La flora identificada coincide en cuanto a familias más representadas con los estudios florísticos realizados en la zona por Howard y Briggs (1953 a), debido a que en estas abundan especies con características morfológicas para adaptarse a las condiciones edafoclimáticas en estos ecosistemas. En este sentido la flora de Caletón de Don Bruno se caracterizó por el predominio de especies esclerófilas y micrófilas en respuesta adaptativa a factores tensionantes en este hábitat. De las 74 especies identificadas por estos autores para la costa oeste de la Bahía de Cienfuegos, solo 15 coinciden para este sector en el estudio actual. Además, en los inventarios de Howard y Briggs (1953 a) se reportaron 16 especies representadas por un único individuo con alto riesgo de perderse, de las cuales solo persisten Caesalpinia glaucophylla y Clomocladia dentata.
Es interesante la presencia en el área de Pectris ritlandii, especie que desde su descubrimiento sobre la roca caliza costera entre Pasacaballos y Punta Lobas y en las cercanías del Castillo de Jagua (Howard y Briggs, 1953 b) no se había colectado. Este registro ubica a Caletón de Don Bruno como una nueva localidad de la especie. También se reporta Rondeletia combsii en la zona colindante con Calicito que constituye el locus clásico para la especie de acuerdo a Combs (1897), lo que sugiere una ampliación de su extensión de presencia.
La mayor diversidad de especies por género se presentó en Tillandsia (5), Erytroxylum (5) y Eugenia (4). Resultados similares han sido registrados en los estudios previos de Howard y Briggs (1953 a) quienes identificaron a Eugenia axillaris, Erytroxylum aerolatum, Tillandsia fasciculata y T. flexuosa como especies abundantes de la costa oeste de la bahía. Se reportan las especies Echites umbellatus, Bursera angustata y Lantana camara presentes en Calicito y Cordia sebestena, Tournefortia gnaphalodes y Jacquemontia havanensis reportadas desde esta zona hasta el Castillo de Jagua, semejante a lo descrito por Combs (1897). La flora presenta un 14,63 % de endemismo. Dentro de estos valores se destacan dos endémicos estrictos: Agave grisea Trel. según Álvarez (1996) y Erythroxylum minutifolium var. cubense O. E. Schulz de acuerdo a Oviedo (2003).
Caletón de Don Bruno atesora once especies con categoría de amenaza según González y Torres et al. (2016), de ellas tres En Peligro Crítico (CR), dos En Peligro (EN), cuatro con categoría preliminar de Amenazadas (A) y dos Casi amenazadas (NT). Del resto de las especies, 66 se consideran con Preocupación Menor (LC), 45 no han sido evaluadas (NE) y seis presentan datos insuficientes (DD), lo que indica la necesidad de reforzar los estudios en la zona para contribuir a la actualización del estado de conservación de estas.
Las observaciones realizadas a las especies locales reafirman la categoría En Peligro Crítico otorgada para A. grisea siguiendo los criterios de UICN (2012), teniendo en cuenta que la distribución de la especie se restringe a esta única localidad donde presenta escaso registro de individuos maduros y área de ocupación reducida, al igual que Erythroxylum minutifolium var. cubense. En el caso de Pectis ritlandii se propone la categoría En Peligro Crítico atendiendo a los criterios de evaluación anteriores que indican un riesgo extremadamente alto de extinción en estado silvestre (UICN, 2012). La distribución de esta especie fue mayor de acuerdo a Borhidi (1991) al punto de considerarla característica de la vegetación costera perteneciente a la clase Sesuvio-Rachicallietea, pero los escasos individuos reportados indican reducción de su área de ocupación. Las amenazas que se ciernen sobre la conservación de la vegetación nativa en esta localidad, fundamentalmente sobre la flora endémica con distribución geográfica restringida sugieren una necesidad inminente de manejo, ya que el área de estudio se encuentra fuera del Sistema Nacional de Áreas Protegidas.
Este sector posee una orilla ondulada con fragmentos fangosos y con bancos de piedras calizas paralelos a la costa formando terrazas, aspectos descritos por Howard y Briggs (1953 a). La caliza costera de este sector, según Borhidi (1991) se relaciona con suelos húmicos carbonatados de poca profundidad que permiten el establecimiento de una vegetación xerofítica con especies suculentas y micrófilas. Se observaron tres terrazas entre las cuales no se observó una continuidad paisajística, sino una fragmentación como resultado de actividades antrópicas. La vegetación de este sector (Figura 2) se corresponde con el matorral xeromorfo costero y subcostero y el bosque siempre verde micrófilo de acuerdo al criterio de Capote y Berazaín (1984).
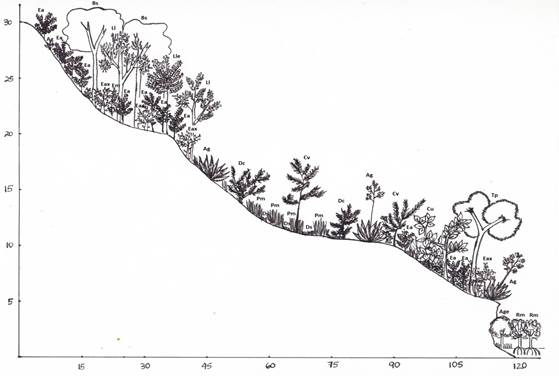 Ag=Agave grisea, Age=Avicennia germinans, Bs=Bursera simaruba, Cu=Coccoloba uvifera, Cv=Caesalpinia vesicaria, Dc=Dichrostachys cinerea, Ds=Distichlis spicata, Ea=Erythroxylum aerolatum, Eax=Eugenia axillaris, Em=Eugenia monticola, Ll=Lysiloma latisiliquum, Lle=Leucaena leucocephala, Rm= Rhizophora mangle, Tp=Thespesia populnea
Ag=Agave grisea, Age=Avicennia germinans, Bs=Bursera simaruba, Cu=Coccoloba uvifera, Cv=Caesalpinia vesicaria, Dc=Dichrostachys cinerea, Ds=Distichlis spicata, Ea=Erythroxylum aerolatum, Eax=Eugenia axillaris, Em=Eugenia monticola, Ll=Lysiloma latisiliquum, Lle=Leucaena leucocephala, Rm= Rhizophora mangle, Tp=Thespesia populneaFigura 2 Perfil esquemático de la vegetación en terrazas en Caletón de Don Bruno
En la parte más alta del área (tercer nivel de terraza) se observa una vegetación más densa correspondiendo con el bosque siempreverde micrófilo distribuido en las zonas de pendientes pronunciadas donde existen árboles medianos de 7-8 m y bajo el dosel se aprecia un estrato arbustivo en su mayoría espinescente y esclerófilo con una altura de 2-4 m (Figura. 2). En esta zona los taxones más frecuentes son: Bursera simaruba, Lysiloma latisiliquum, Bucida buceras, Metopium toxiferum, Cordia sebestena, Cordia sulcata, Leucaena leucocephala, Trichilia hirta y especies de los géneros Eugenia y Erythroxylum predominando en el estrato arbustivo, como en Borhidi (1991). El estado de conservación que presenta el hábitat a este nivel sugiere que el acceso humano es menor, así como los efectos que trae consigo la antropización.
Aun cuando el bosque siempreverde micrófilo continúa al descender al segundo nivel de terraza se observaron diferencias en cuanto a la composición y distribución de especies. Esto se debe a que el estrato arbóreo está reducido a individuos aislados y se observan extensas zonas de vegetación herbácea y arbustiva, probablemente como consecuencia de las áreas de aclareo creadas por los pobladores para hornos de carbón. En esta terraza las especies más representadas son: Dichrostachys cinerea, Lysiloma latisiliquum, Corchorus hirsutus, Sida ulmifolia, Melochia nodiflora, Urena lobata y Comocladia dentata, Lantana camara y Caesalpinia vesicaria. En este nivel se realizan talas ilegales y frecuentes quemas que provocan reducción de la cobertura vegetal y pérdida de suelo.
Las zonas de desmonte pueden generar condiciones favorables que justificarían el establecimiento de especies oportunistas con potencial invasor, coincidiendo con Oviedo et al. (2015), con el consecuente desplazamiento de la flora nativa semejante a las observaciones de Castell et al. (2013). La pérdida y modificación de hábitat y la presencia de especies invasoras se consideran las principales amenazas que afectan la conservación de la flora cubana, de acuerdo a Gonzáles-Torres et al. (2016). Es probable que estas amenazas se relacionen con la pérdida de especies tales como Citharexylum spinosum, Amyris elemifera, Bumelia glomerata y Guaiacum sanctum, consideradas abundantes en este sector del litoral cienfueguero por (Combs, 1897) y que no fueron encontradas en este inventario. Sin embargo, el desarrollo de mecanismos adaptativos para sobrevivir con mayor exposición al sol justificaría la prevalencia de adultos de A. grisea en este nivel, semejante a lo observado por Gonzáles et al. (2017) en Agave offoyana en la Reserva Ecológica Caletones.
El primer nivel de terraza se corresponde con el matorral xeromorfo costero y subcostero caracterizado por una vegetación baja, esclerófila y xeromorfa (Figura 3), donde las especies más representadas son Hypericum fasciculatum, Hippomane mancinella, Caesalpinia vesicaria, Thespesia populnea, Calyptranthes decandra, Coccoloba uvifera, Coccothrinax cupularis y Erytroxylum aerolatum. Las epífitas fundamentalmente Tillandsia sp. son comunes sobre las ramas de los arbustos coincidiendo con resultados de Combs (1897) y García-Lahera y Orozco (2018).
Se observa predominio de un estrato arbustivo con presencia de lianas, mientras que el estrato herbáceo es escaso, coincidiendo con las observaciones de Richard y Howard (1953 a), a excepción de individuos de Phyllanthus epiphyllantus que ocupan las zonas bajas hasta Calicito, semejante a las observaciones de Combs (1897). Estas características se corresponden con la vegetación orófila halofítica de zonas costeras del Caribe descrita por Borhidi (1991) donde predominan arbustos de hojas suculentas, mientras que las hierbas están restringidas, probablemente por la influencia del spray salino y al suelo extremadamente pobre.
Se distingue la presencia de elementos de manglar intercalados que ocupan la primera línea de costa en algunas zonas permanentemente inundadas, donde se destacan Rhizophora mangle, Laguncularia racemosa y Avicennia germinans que se extienden hasta Calicito, coincidiendo con Combs (1897). No obstante, estas especies son menos abundantes respecto al lado noreste y noroeste de la bahía según Menéndez et al. (2011), que reciben el aporte de importantes cuencas hidrográficas y poseen suelo fangoso. En el caso de los individuos de Conocarpus erectus L. var. erectus se encontraron más distante de la línea de costa, como es usual para este taxón coincidiendo con la distribución reportada dentro del matorral xeromorfo costero y subcostero en la Península Ancón por García-Lahera y Orozco (2018).
CONCLUSIONES
A partir del inventario de la flora en el Caletón de Don Bruno, se registró la presencia de 164 especies de plantas fanerógamas en esta localidad del sector costero sur-oeste de la Bahía de Cienfuegos, donde el 14,63 % son endemismos y tres tienen carácter restringido. Además, existen 11 especies con categorías de amenaza que requieren necesidad de conservación dada la vulnerabilidad de este ecosistema. La vegetación caracterizada por el matorral xeromorfo costero y subcostero y el bosque siempreverde micrófilo, se encuentra amenazada por tala ilegal y los incendios forestales, que han ocasionado variaciones en la composición y distribución de las especies respecto a los estudios anteriores