Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd v.21 n.1 Ciudad de la Habana ene.-mar. 2002
Instituto de Ciencias Básicas y Preclínicas Victoria de Girón
Desarrollo de un modelo de aterosclerosis inducida por inmunocomplejos de forma pasiva en ratones BALB/CBJ transgénicos al antígeno de superficie de la hepatitis B
Lic. Liudmila López Matilla, Lic. Lien López Matilla, Dr. Antonio González Griego, Dr. Víctor Manuel Sosa, Dr. José A. Castillo Herrera, Dr. Leonel Falcón Vilaú, Dr. Adonis Montenegro Perdomo y Dra. Leysis McCoock Noa
Resumen
Se obtuvieron anticuerpos-HBs a partir del desarrollo de ascitis en ratones BALB/CBJ. Se emplearon 2 grupos de animales BALB/CBJ transgénicos al AgsHb, de 8 meses de edad y un régimen de agua y comida ad libitum. A un grupo se le inoculó Ac anti-HBs con una dosis doble a la de su concentración de AgsHb y al otro grupo se le inoculó solución salina. Se realizaron 7 inoculaciones con un intervalo de 5 d entre ellas por la vena caudal. Una semana después de la última inoculación se realizó extracción de sangre y se les determinó inmunocomplejos circulantes en plasma. Se les practicó eutanasia y se les extrajo las aortas donde se comprobó la formación de placas de ateromas de forma macroscópica por observación al estereoscopio y microscópicamente por tinción con hematosilina-eosina. A partir de estos resultados se concluyó que se logró un modelo de aterosclerosis en ratones BALB/CBJ Tg al AgsHb por formación de inmunocomplejos de forma pasiva.
DeCS: ATEROSCLEROSIS; TECNICAS INMUNOLOGICAS; ANTIGENOS DE SUPERFICIE DE LA HEPATITIS B/análisis; RATONES TRANSGENICOS.
La aterosclerosis, es el proceso más común subordinado a la morbilidad y mortalidad cardiovascular.1 La cardiopatía isquémica como consecuencia del proceso aterosclerótico, ocupa en Cuba un lugar importante, con tasas que la hacen alcanzar el primer lugar entre las causas de defunciones no violentas. Los grupos más afectados en orden decreciente son los de 65 años y más, de 64 a 45 y de 44 a 15 años. Su presentación en menores de 15 años es excepcional.2,3
La aterosclerosis es una enfermedad multifactorial que comienza en la infancia aunque no suele ser clínicamente evidente hasta que se alcanza una edad mediana. Afecta principalmente las arterias elásticas y musculares de tamaño grande y medio, y son la aorta y los sistemas coronario y cerebral los principales objetivos. Las anomalías morfológicas claves en la arterosclerosis consisten en engrosamientos focales de la íntima y acumulaciones lipídicas; que producen las características placas ateromatosas.4
La relación de las reacciones inmune celular y humoral con los estados del desarrollo aterosclerótico, se ha olvidado por muchos años en la investigación de la aterosclerosis. Verdaderamente, el fenómeno inmunológico ha sido considerado de naturaleza secundaria en esta enfermedad.5
La tendencia actual es considerar que la aterosclerosis es una respuesta inflamatoria crónica de la pared vascular a diversos acontecimientos iniciadores que pueden presentarse en etapas tempranas de la vida. Múltiples mecanismos patogénicos contribuyen a la formación y progresión de la placa incluidas la disfunción endotelial, la adhesión e infiltración de los monocitos, la proliferación de células musculares lisas, el depósito de matriz extracelular, la acumulación de lípidos y la trombosis.4
El compromiso del sistema inmune en la aterosclerosis ha sido muy estudiado en los últimos años.5,6 Una hipótesis reciente sostiene que la huella de la autoinmunidad puede ser detectada dentro de la lesión aterosclerótica. Varios antígenos y sus respectivos anticuerpos (Acs) han sido sugeridos como factores en la aterogénesis.7
La posible relación de los inmunocomplejos (ICs) con la patogénesis de la aterosclerosis fue sugerida por primera vez hace 20 años atrás, basada en la detección de ICs solubles por técnicas de pesquisaje en pacientes con aterosclerosis.8 En humanos se ha comprobado que las lipoproteínas de baja densidad circulantes que contienen ICs, están presentes en la circulación de pacientes con enfermedades vasculares y en algunos sujetos saludables, y tienen un papel patogénico en el desarrollo de la aterosclerosis.9,10
Sobre la base de lo planteado anteriormente y a solicitud del Centro de Investigaciones y Referencia de Aterosclerosis de La Habana este colectivo se enfrascó en el estudio de la aterosclerosis desde el punto de vista inmunológico. Para lograr esto, es de gran importancia contar con modelos animales que faciliten la comprensión de algunos de estos fenómenos que ocurren en el proceso aterogénico. En la bibliografía consultada, no se encontraron reportes de modelos experimentales de aterosclerosis obtenidos que indujeran un fenómeno inflamatorio a través de ICs; por lo que el propósito con este trabajo ha sido obtener un modelo experimental pasivo de aterosclerosis inducido por IC en ratones BALB/CBJ transgénicos (Tg) para el antígno de superficie de la hepatitis B (AgsHb).
Métodos
Procedencia y cuidado de los animales
Todos los animales que se emplearon en esta investigación procedían del bioterio del Departamento de Inmunología del ICBP Victoria de Girón. Todo el tiempo se mantuvieron atendidos por personal especializado y según las normas establecidas para este tipo de animales convencionales. El suministro de agua y comida fue ad libitum y se distribuyeron para los distintos tratamientos de forma aleatoria según el grupo de estudio. Se marcaron con ácido pícrico en diferentes sitios anatómicos para su identificación.
Obtención de IgG anti-HBs de ratón
Se utilizaron 20 ratones isogénicos de la línea BALB/CBJ, hembras de 10 semanas y un peso promedio de 25 g. A 10 de ellos se les práctico un esquema de inmunización 0-1-2 semanas por vía intraperitoneal empleando una dosis de 4 mg de la vacuna cubana antihepatitis B Heberbiovac HB.11 Los 10 animales restantes se inmunizaron de la misma forma con tampón fosfato salino (NaCl 0,137 mol/L, KCl 0,0027 mol/L, Na2HPO4, 0,0081 mol/L, KH2PO4 0,0011 mol/L).
A la semana de la última inmunización, se realizó extracción de sangre por el plexo retrorbitario con capilares heparinizados, estos se centrifugaron durante 2 min en centrífuga de capilares marca Teknika HC-240c a 9 000 rpm (1 750 g) y el plasma obtenido se usó en un ensayo inmunoenzimático ligado a enzima (ELISA), heterogéneo, tipo sandwich de doble Ag para la detección y cuantificación de Ac contra el AgsHb (anti-HBs), desarrollado y validado en el Laboratorio de Inmunología del Instituto de Ciencias Básicas y Preclínicas Victoría de Girón.12
Se sensibilizó la cavidad peritoneal de los animales con 0,5 mL de adyuvante incompleto de Freund y 4 d después se les inoculó por vía intraperitoneal 2 x 106 células de mieloma de la línea SP2OAG14 suministradas por el Centro de Inmunología Molecular. Se esperó una semana y se extrajo la ascitis formada. Esta se incubó 1 h a 37 °C y toda la noche a 4 °C, se centrifugó a 3 000 g durante 10 min según lo recomendado por Pico y otros en 1997.13 El sobrenadante obtenido se sometió a un proceso de purificación por cromatografía.
La cromatografía que se utilizó para la purificación de los Acs fue de afinidad, se usó una matriz de proteína G Sepharose FF y se realizó en una columna XK 1.5X5 (Pharmacia LKB, Suecia). La corrida se realizó en un equipo de purificación de cromatografía estándar con colector SuperFrac, bomba peristáltica P-1, unidad óptica UV1 y un registrador REC 102 (Pharmacia LKB, Suecia). El flujo empleado en la corrida fue de 30 mL/h y el volumen de matriz hidratada empaquetada en la columna fue 10 mL. La corrida se realizó de acuerdo con las instrucciones del fabricante. Se utilizó tampón fosfato salino 0,1 M pH= 7 para equilibrio y para efectuar la elución se utilizó glicina-HCl 0,1 M pH= 2,5. Al eluato se le ajustó el pH con tampón Tris-HCl 1M, pH 7.
La fracción producto de la cromatografía que contenía la IgG en el caso del grupo tratado fue ultrafiltrado en un equipo AMICON 8010 (USA) con tampón fosfato salino y se realizaron 3 lavados. Se utilizó una membrana de tamaño de poro nominal de 10 kD y una presión de nitrógeno de 3,5 atmósferas. El proceso se realizó a 4 °C. Posteriormente el ultrafiltrado fue colectado y pasado por un filtro de membrana de 0,22 mm minisart (Sartorius, Italia) para esterilizarlo. Se determinó la concentración de IgG anti-HBs en el concentrado total de IgG mediante el ELISA para la detección y cuantificación de anti-HBs ya descrito; a la fracción del grupo control que no se desechó también se le detectó por esta técnica la presencia de anti-HBs.
Modelo pasivo
Se emplearon 10 hembras de la línea BALB/CBJ Tg para el AgsHb de 8 meses de edad y un peso promedio de 20 g. Se formaron 2 grupos de 5 animales cada uno. Se les realizó extracción de sangre como fue descrito anteriormente y con el plasma se efectuó un ensayo inmunoenzimático ELISA, heterogéneo, tipo sandwich de doble Ac, con peroxidasa de rábano picante para la cuantificación de AgsHb.14
Posterior a esto se realizaron siete inoculaciones con un intervalo de 5 d entre ellas por vía endovenosa, específicamente por la vena caudal. Se inoculó al grupo tratado una dosis de anti-HBs de ratón que duplicó la concentración de AgsHB de cada animal, diluida en solución salina de ser necesario, para un volumen de inóculo de 0,05 mL. Al grupo control se le suministró ascitis libre de IgG de la misma forma que al grupo tratado.
Detección de ICs circulantes
Una semana después de concluidas las inmunizaciones se realizó extracción de sangre de la forma descrita con anterioridad. Se utilizó la técnica para detectar inmunocomplejos circulantes inespecíficos por el micrométodo de precipitado con polietilenglicol (PEG) 6 000. Para ello se diluyen 3 veces las muestras en tampón borato 0,1M pH= 8,4. En una placa de 96 pocillos de cloruro de polivinilo (Titertek Flow Laboratories) se añaden 200 mL de tampón borato en un pocillo y 200 mL de tampón PEG (10 g de PEG en 240 mL de tampón borato 0,1 M), se añaden las muestras en los pocillos de forma que la dilución final sea 1/180. Se incubó 1 h a temperatura de laboratorio y se realizó la lectura a 492 nm en lector Organon Teknika.
Como control positivo se utilizó suero de un paciente con artritis reumatoidea y como control negativo suero humano normal. A la DO del pocillo con PEG se le resta la DO del que contiene tampón borato y si el resultado excedió el valor de 0,05 (valor límite de la técnica) la muestra se consideró positiva.
Procesamiento de las muestras
Se practicó eutanasia por inhalación del éter etílico y se les extrajo la aorta desde el cayado aórtico hasta la ilíaca común con ayuda de un estereoscopio marca XTD-01 con un aumento de 10x. Las aortas fueron abiertas en sentido longitudinal, fijadas en cartulina y se conservaron en formol 10 %, hasta el momento en que se pasó a determinar la presencia o ausencia de lesiones macroscópicas con ayuda del esteroscopio.
Posteriormente, las aortas se incluyeron en parafina y se colorearon por la técnica de hematosilina-eosina. Para la observación de los cortes se utilizó un microscopio óptico Carl Zeiss con un aumento de 40 x.
Resultados
Obtención de IgG anti-HBs en ratón
En el caso del grupo control la ascitis obtenida contenía una fracción de IgG que fue desechada. De este grupo se utilizó en la inoculación la primera fracción que eluyó correspondiente a los contaminantes de la técnica en la que se comprobó la ausencia de anti-HBs. En el grupo de animales inmunizados para producir los anti-HBs se obtuvo una fracción de IgG que después de ultrafiltrada alcanzó una concentración de 7 700 UI/L.
Modelo pasivo
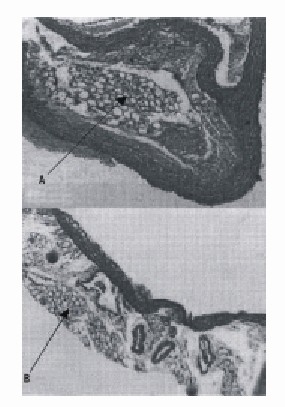
En la observación macroscópica en todos los animales del grupo tratado se observaron las elevaciones típicas de las placas ateromatosas, no así en los animales del grupo control. En cuanto a la microscopia en el grupo tratado, se vio en la pared de la arteria presencia de células espumosas e infiltrado de linfocitos en la íntima y en algunos casos se observaron vasos de neoformación. En el grupo control se vió la presencia de células espumosas aisladas (fig.).
Fig. Tinción con hematosilina-eosina. A. Grupo tratado. B. Grupo control. La flecha indica las células espumosas.
Detección de ICs circulantes
En todos los animales de ambos grupos se detectó la presencia de ICs circulantes en el plasma.
Discusión
La obtención de grandes cantidades de Acs a partir de su suero no es factible debido al pequeño volumen de sangre de un ratón. Como uno de los objetivos de este estudio fue explorar el comportamiento de la aterosclerosis en ratones Tg para el AgsHb mediante la formación de ICs; suministrándoles Acs anti-HBs, estos debían ser obtenidos en la misma especie animal donde se iban a transferir pasivamente, para evitar la formación de Acs antiespecie y que produjeran efectos indeseados que interfirieran con la investigación. Es por ello que se obtuvieron los Acs a partir de la formación de ascitis en ratones, vía mediante la cual se pueden obtener a partir de un solo animal, volúmenes considerables de ascitis en comparación con el tamaño del ejemplar.13
En el proceso de purificación, el grupo control en la obtención de Acs a partir de la ascitis, mostró una fracción de IgG que se desechó para evitar inespecificidades cuando se inocularan los animales controles del modelo pasivo; estos fueron inoculados con la otra fracción que eluyó y no contenía Acs de tipo IgG.
Esta fracción de IgG en los controles fue bastante alta, por lo que se descartó la posibilidad de que toda la IgG obtenida en el grupo tratado sea anti-HBs; dado que la cromatografía utilizada como se señaló, empleó una matriz de proteína G por lo que se unió toda la fracción de IgG contenida en la ascitis. Como se mencionó, estos animales están en condiciones convencionales por lo que pueden estar expuestos a retos antigénicos.
Otro factor que puede haber influido en el caso del grupo vacunado, es el desarrollo de respuesta contra Pichia pastoris, levadura que se transforma genéticamente para la obtención del AgsHb empleado en la vacuna. En experiencias previas realizadas en el departamento, en el ELISA que se utiliza para la detección y cuantificación del anti-HBs en ratón se le añade al conjugado dicha levadura para adsorber los Acs y se disminuye notablemente la inespecificidad del ensayo. Se requirió un paso de concentración de los Acs porque a pesar de que el reto se produjo por vía intraperitoneal; es mayor el número de células plasmáticas que se encuentran en órganos linfoides que drenan Ac a la sangre periférica que las que lo hacen a la cavidad peritoneal.
En cuanto a la vía de inoculación de los animales para la formación de ICs se escogió la endovenosa, para crear la mayor cantidad posible de estos en los vasos sanguíneos. En el caso de estos animales se conocía por experiencias previas de este grupo de investigación que expresan el AgsHb en los vasos sanguíneos.
La dosis de inoculación que se usó fue el doble de la concentración de Ag que tenían los animales, para garantizar estar en la zona de exceso de Ac de una curva de titulación, donde todo el Ag existente precipita en forma de ICs y quedan Acs en el suero.
El caudal de conocimientos que se tienen hasta el momento sobre la aterosclerosis, hablan de un fenómeno que está influenciado por diversos factores más que por uno solo. Es por ello que se trabajó con más de un factor de riesgo; para esto se provocó una reacción de hipersensibilidad tipo III para que se produjera la cascada de eventos como consecuencia de ella y se trabajó con animales viejos (8 meses de edad al comienzo del experimento), porque se plantea que la edad tiene una influencia primaria y clínicamente importante en el desarrollo de la aterosclerosis.15
En el grupo tratado se observó en las aortas placas fibrosas, no así en el grupo control. En los animales tratados, los ICs formados cuando se depositan en la lámina elástica interna de los vasos sanguíneos fijan complemento. El principal factor inflamatorio derivado de la cascada del complemento es C5a que es quimiotáctico para neutrófilos de la circulación y tejidos circundantes. Los neutrófilos liberan enzimas lisosómicas y generan oxidantes tóxicos en el proceso de fagocitosis del IC, que causan la lesión del endotelio arterial. Como respuesta a este daño tisular las células endoteliales aumentan su volumen y proliferan, se incrementa la permeabilidad para los constituyentes plasmáticos, tiene lugar la adhesión de monocitos y plaquetas, así como la liberación de factores de crecimiento incluido el factor de crecimiento derivado de plaquetas, los cuales conducen a la migración y proliferación de las células musculares lisas.16 Estas células producen grandes cantidades de colágeno y proteoglucanos, que contribuyen a la evolución de la placa ateromatosa.4
Los resultados obtenidos en este modelo están en concordancia con lo obtenido por otros autores en el estudio de la relación de fenómenos autoinmunes con la aterosclerosis, fundamentalmente en lo que se refiere a Ac contra HSP 60/65.1,5,17 En este modelo pasivo se simula una reacción autoinmune, desde el punto de vista que se suministran Acs contra una proteína propia de este tipo de animales.
Según el tipo de lesión que se observó macroscópicamente, se puede disminuir la cantidad de inoculaciones en los animales, por lo que es importante realizar este tipo de cinética con varios grupos de animales que se somentan a distintos números de inoculaciones y comprobar cuándo se forma el primer tipo de lesión o estría grasa y cuándo se empieza a observar la placa ateromatosa.
Por el hecho de que no se observaran lesiones macroscópicamente ocasionadas por la acción de los ICs en los grupos controles, no se puede afirmar que no existan eventos ateroscleróticos en esta arteria; por ello fue que se realizaron cortes microscópicos del tejido porque la estría grasa se observa a través de estas técnicas.
Los resultados obtenidos a partir de los cortes histológicos muestran el desarrollo de estrías grasas en los 2 grupos de animales. Esto se corresponde a lo planteado por otros autores, al afirmar que el proceso aterosclerótico está presente desde edades tempranas en todos los individuos, pero se hace clínicamente evidente en aquellos que entran en los grupos de riesgo.4
A pesar de observar las células espumosas, en el grupo control no se observó infiltrado linfocitario que se vio en el grupo tratado, donde además se observaron vasos de neoformación característicos de la fibrosis de la placa y que contribuyen a perpetuarla.
El hecho de que todos los animales fueran positivos a la presencia de ICs circulantes puede deberse, a que poseen niveles en el orden de los mg AgsHb en el suero. Esta proteína tiene un PM de 24 000 D y se encuentra en el suero en forma de partículas de 100 moléculas cada una por lo que se alcanza un PM de 2 400 000 D y puede que el PEG las haga precipitar. Esta experiencia sería muy interesante llevarla a pacientes portadores del virus de la hepatitis B, para comprobar si esto sucede de igual forma en ellos y así tener un pronóstico evolutivo de la enfermedad.
A partir de estos resultados se puede concluir que se logró un modelo de aterosclerosis en ratones BALB/CBJ Tg al AgsHb por formación de ICs de forma pasiva. Se recomienda continuar realizando estudios en cuanto a la cinética de aparición de las lesiones macroscópicas para su exitoso uso por el personal que investiga esta patología.
Summary
Anti-HBs antibody was obtained starting from the development of ascites in BALB/CBJ mice. Two groups of 8-month-old BALB/CBJ animals transgenic to HBsAg on an ad libitum water and food regimen were used. A group was inoculated anti-HBs antibody with a dose that doubled its concentration of HBsAg, whereas the other group was inoculated saline solution. 7 innoculations were made by the caudal vein with an interval of 5 days between them. A week after the last inoculation, blood was extracted and the immunocomplexes circulating in plasma were determined. Euthanasia was practiced and the aortas were extracted. The formation of plaques of atheromas was proved in a macroscopic way by observation on the stereoscopico and, microscopically, by staining with haematoxylin-eosin. Based on these results, it was concluded that an atherosclerosis model was attained in BALB/CBJ mice transgenic to HBsAg by the formation of immunocomplexes in a passive way.
Subject headings: ATHEROSCLEROSIS; IMMUNOLOGIC TECHNIQUES; HEPATITIS B SURFACE ANTIGENS/analysis; MICE, TRANSGENIC.
Referencias bibliográficas
- Shoenfeld Y, Sherer Y, George Y, Harats D. b2 glicoprotein in human and murine atherosclerosis. b2GP1. Atherosclerosis 2001;3:85-7.
- Ministerio de Salud Pública. Anuario Estadístico 1999;24-44.
- Falcón L, Fernández-Britto JE, Castillo JA. La lesión aterosclerótica coronaria en la muerte súbita: aplicación del sistema aterométrico. Rev Cubana Invest Biomed 2000;19(2):144.
- Robbins SL, Cotran RS, Kuran V. Patología estructural y funcional. Primera Parte. Quinta Edición. Edición Revolucionaria, 1998:519-6.
- Wick G, Schett G, Amberger A, Kleindienst R, Xu Q. Is atherosclerosis an immunologically mediated disease?. Immunology Today 1995;16:27-33.
- Libby P, Hasson GK. Involvement of the immune system in human atherogenesis: current knowledge and unanswered questions. Lab Invest 1991;64:5-11.
- Shoenfeld Y, Sherer Y, George J, Harats D. Autoantibodies associated with atherosclerosis. Ann Med 2000;32(1):37-40.
- Fust G, Szondy E, Szekely J, Nanai I, Gero S. Studies on the ocurrence of circulating immune complexes in vascular disease. Arteriosclerosis 1978;29:181-190.
- Tertov VV, Orekhov AN, Kacharava AG, Sobenin IA, Perova NV, Smirnov VN. Low density lipoprotein containig circulating immune complexes and coronary atherosclerosis. Exp Mol Pathol 1990;52:300-8.
- Tertov VV, Orekhov AN, Sayadyan KS, Serebrennikov SG, Kacharava AG, Lyakishev AA, Smirnov VN. Correlation between cholesterol content and circulating immune complexes and atherogenic properties of CHD patients serum manifested in cell culture. Atherosclerosis 1990;81:183-9.
- Certificado de análisis para el producto final. Vacuna antihepatitis B recombinante Heberbiovac HB. Centro de Ingeniería Genética y Biotecnología de la Habana 2000; Lote Nro. 805610. Ciudad de La Habana, Fecha de vencimiento: agosto de 2001.
- García M, Alerm A. Desarrollo de un método inmunoenzimático para la detección y cuantificación de anticuerpos específicos para el HbsAg. [Tesis para optar por el título de Especialista de I Grado en Inmunología. Ciudad de La Habana: ICBP Victoria de Girón. 1994:50 pp.]
- Pico MC, Giraldino IG, Otero A. Inmunología experimental. Ciudad Habana: Editorial Félix Varela, 1997:70.
- González A, Alerm A, Ramírez V. Cuantificación del antígeno de superficie del VHB (HBsAg) en muestras biológicas con fines asistenciales y preparativos. Biotecnol Aplicada 1993;10(2):102.
- Robbins SL, Cotran RS. Patología estructural y funcional. Primera Parte. Tercera edición. Edición Revolucionaria, 1987:507.
- Stites DP, Abba IT. Inmunología Básica y Clínica. Séptima Edición. México, D.F. El Manual Moderno, 1993:177-79.
- Xu Q, Willeit J, Marosi M, Kleindients R, Oberhollenzer F, Kiechl S. Association of serum antibodies to heat shock protein 65 with carotid atherosclerosis. Lancet 1993;341:255-9.
Recibido: 20 de julio de 2001. Aprobado: 6 de septiembre de 2001.
Lic. Liudmila López Matilla. Instituto de Ciencias Básicas y Preclínicas Victoria de Girón. Avenida 146 No. 3102. Reparto Cubanacán, Playa, Ciudad de La Habana, Cuba. CP 11600.