Introducción
Las enfermedades no transmisibles constituyen un problema de salud pública en todo el mundo y entre ellas, la diabetes mellitus (DM) tiene una elevada prevalencia.1 En las personas con esta enfermedad, la prioridad del tratamiento es lograr un buen control metabólico y así evitar el riesgo de valores extremos de la glucemia, con lo cual se evitarían futuras complicaciones de esta enfermedad.2,3,4,5,6 Evitar la hiperglucemia tiene un valor particular, pues se conoce que ella constituye un marcador de gravedad en pacientes críticos que se asocia con peores resultados y es un factor independiente de mortalidad.7
Las razones del aumento de la glucemia en estos pacientes se relacionan con el no cumplimiento del tratamiento indicado y en general con conductas inadecuadas de autocuidado de la DM. Las limitaciones financieras para acceder a los medicamentos utilizados para el correcto tratamiento de esta enfermedad, también pueden contribuir al descontrol metabólico. Mientras, la hipoglucemia en los pacientes con DM, generalmente ocurre como resultado de un consumo inadecuado o errático de carbohidratos, después de la administración de sulfonilureas o insulina.2
Para el adecuado tratamiento de la DM, existen varios grupos de medicamentos. Entre estos, se dispone de los llamados agentes normoglucemiantes orales y de los hipoglucemiantes; estos últimos pueden ser usados por vía oral o parenteral. Uno y otro grupo de fármacos reducen la glucemia, pero los segundos, pueden -además- aumentar el riesgo de hipoglucemia de no usarse de manera adecuada.8 De ahí, la importancia de incorporar al mercado nuevos agentes hipoglucemiantes que no comprometan los mecanismos de contra regulación endógenos, lo que facilitaría disminuir la frecuencia de este negativo evento.8 Los medicamentos inhibidores del cotransportador sodio-glucosa (iSGLT, por sus siglas en inglés), cumplen con esa condición y actualmente los iSGLT tipo 2 (iSGLT2, por sus siglas en inglés) constituyen una opción para el tratamiento de la DM tipo 2 (DM2).8,9,10,11,12
Los iSGLT2, también son conocidos con el seudónimo de “glifozinas”, aunque pueden ser usados en monoterapia, son considerados como un grupo farmacológico coadyuvante en el control de los pacientes con DM2, que reciben tratamiento con otros medicamentos de tipo normo o hipoglucemiantes, que no han alcanzado las metas de control. Como todo medicamento, se debe señalar que a pesar de sus bondades, no está libre de algunos efectos adversos y reacciones secundarias.8,9
Del mismo modo -desde 2015- se viene trabajando en el desarrollo y comercialización de un nuevo inhibidor, en este caso dual, de los SGLT tipo 1 (SGLT1, por sus siglas en inglés) y SGLT2. Este nuevo producto se encuentra en fase de investigación, es administrado por vía oral e igualmente promete ser una opción relevante en el tratamiento de las personas con DM.13,14
En Cuba, aún no están disponibles los SGLT2 y en nuestro medio existen pocas publicaciones sobre estos medicamentos. No obstante, por su importancia -como una nueva opción- para la obtención de un buen control glucémico en los pacientes con DM, es necesario que nuestros profesionales conozcan a cerca su empleo. De ahí, que el objetivo del presente artículo fue describir el papel de los iSGLT2 en el tratamiento de la DM.
Métodos
La información necesaria para redactar el presente artículo se realizó en el segundo semestre de 2020. Esta se obtuvo de la evaluación de diferentes trabajos de revisión, de investigación y páginas Web, que en general tenían menos de 10 años de publicados, en idioma español, portugués o inglés. Se utilizó como buscadores de información científica a Google Académico, Google, Pubmed y SciELO. Fueron usadas como palabras clave: glifozinas, inhibidores del cotransportador sodio-glucosa, diabetes mellitus, tratamiento y pérdida de peso. Fueron excluidos los artículos que no reunían las condiciones señaladas. Esto permitió el estudio de 98 artículos, de los cuales 75 fueron referenciados.
Resultados
La DM2 constituye una causa importante de morbilidad y mortalidad en el mundo.15 En la actualidad, las opciones terapéuticas para obtener un mejor control y evolución de la DM2 se incrementan de manera considerable y los medicamentos que se utilizan permiten abarcar diferentes perfiles de efectividad y distintos mecanismos de acción, la mayoría de ellos dependientes de la acción de la insulina.16,17 Uno de los grupos farmacológicos que su efecto no depende de este mecanismo son los iSGLT2,18 de ahí el interés que han despertado en el campo de la investigación y la asistencia médica.
Mecanismo de acción de los inhibidores del cotransportador sodio-glucosa
La reabsorción renal de glucosa es el mecanismo primario mediante el cual los riñones influyen en la homeostasia de la glucosa. Esta función es fundamental e involucra la gluconeogénesis renal, la que es capaz de producir de 15 a 55 g de glucosa al día, mientras que el riñón puede metabolizar de 25 a 35 g de esta en el mismo periodo de tiempo. La captación de glucosa procedente de la circulación y del filtrado glomerular constituyen otro de los mecanismos que intervienen en la glucemia.19
De forma hipotética, si se considera que existe una concentración de glucosa de 100 mg/dl, con una tasa de filtrado glomerular normal de aproximadamente 180 L diarios, las personas sanas deben filtrar aproximadamente 180 g al día de glucosa.19 Esta es reabsorbida -casi toda- en el túbulo contorneado proximal y regresa a la circulación, de manera tal que en la orina de sujetos sanos no se debe excretar nada de glucosa. La eficiencia de este sistema es excelente y permite la conservación de la glucosa en el organismo, la que constituye una fuente valiosa de energía.19
Aunque se conoce de la existencia varios tipos de cotransportadores sodio-glucosa (SGLT, por sus siglas en inglés), la presente revisión se centra en la actividad de dos de sus tipos, el SGLT-1, distribuido en casi todo el organismo -intestino, tráquea, riñón, corazón, cerebro, testículo y próstata-, y el SGLT2, localizado predominantemente a nivel renal, permitiendo teóricamente su acción local.15,20 Estos últimos se expresan en los túbulos contorneados proximales del riñón -en el segmento S1- y son responsables de la mayor parte de la reabsorción de la glucosa filtrada desde la luz de los túbulos (aproximadamente 90 %).21
Se ha demostrado que los pacientes con DM2 presentan una mayor reabsorción renal de glucosa, lo que puede contribuir a la elevación persistente de las concentraciones de glucemia.21 Los iSGLT2 actúan de forma competitiva, reversible y selectiva a nivel de los receptores SGLT2 ubicados en los túbulos contorneados proximales y su acción es independiente de la secreción o acción de la insulina y de la etapa evolutiva de la DM2. La inhibición reduce el umbral de saturación para la glucosuria de manera tal, que ésta se inicie con niveles de glucemia entre 60-80 mg/dL (<100 mg/dL). Así mismo, aumenta la excreción urinaria de glucosa en 60-80g/día22 y disminuye entre 30 y 50 % la reabsorción renal de glucosa.8,9,10,11,12
Algunas características a cerca de los inhibidores del cotransportador sodio-glucosa como parte del tratamiento de la diabetes mellitus
La absorción por vía oral de los iSGLT2 es rápida (Cmáx 1-2 hs) y no se modifica con la ingesta de alimentos. Al mismo tiempo presentan un metabolismo hepático por glucuronidación, con escasa oxidación y participación de los citocromos y se confirma que 60 % de dichos fármacos se elimina a través de las heces, mientras que 33 % lo hace por vía urinaria.20 En base al perfil de eficacia y seguridad observado, los iSGLT2 se pueden considerar una opción de tratamiento en pacientes con un filtrado glomerular renal > 60 ml/min, con especial precaución en pacientes de edad avanzada, que no presenten enfermedades agudas o crónicas que puedan causar hipoxia tisular.21
Existen varios medicamentos que tienen la capacidad de actuar a través de los receptores de SGLT2 y producir una diuresis osmótica; entre ellos se describen: la dapaglifozina, la canagliflozina y la empagliflozina- aunque más recientemente se incorporó la ertuglifozina a este grupo-. Estos medicamentos, actúan de forma independiente de la concentración de insulina o de la resistencia periférica a esta hormona y de manera dependiente de las concentraciones de glucosa plasmática, así como de la tasa de filtrado glomerular del sujeto.19,23,24,25,26
Inicialmente, los iSGLT2 han sido autorizados para el tratamiento exclusivo de la DM2.10 Sin embargo, por las dificultades existentes en el adecuado manejo terapéutico de algunos pacientes con DM tipo 1 (DM1) y la necesidad de buscar medicamentos que puedan ser utilizados en combinación con la insulina para obtener un óptimo control glucémico, se considera la exploración del empleo de los iSGLT2, en estos pacientes.11 Por este motivo, la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés) ha aceptado revisar la presentación del expediente de registro de la sotagliflozina, la cual es un inhibidor dual, de los SGLT tipo 1 y 2. El tratamiento por vía oral -de ser autorizado- se utilizaría como un complemento del tratamiento con insulina para mejorar el control glucémico en adultos con DM1.14 No obstante en marzo de 2019, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés) rechazó la aprobación de sotagliflozina, solicitada en enero 2019.27
Importancia de los inhibidores del cotransportador sodio-glucosa y cuales se usan en la actualidad en el tratamiento de la Diabetes mellitus
Los iSGLT2 constituyen el grupo de agentes orales de más reciente incorporación aprobados para el tratamiento de la DM2 en Estados Unidos y en Europa. En general, son medicamentos de segunda o tercera línea, por lo que establecen una adición útil a las opciones terapéuticas disponibles para el tratamiento de la DM2.23,24,25,28,29,30
Los iSGLT2 se indican en adultos de 18 años de edad o mayores con DM2 y se pueden usar en monoterapia, biterapia (junto con metformina, sulfonilureas, pioglitazona o insulina y otros) o en triple terapia,21 aunque todavía ninguno de ellos está aprobado, para el tratamiento de pacientes con DM1, aunque se conoce que los iSGLT2 pueden tener un efecto benéfico en el control glucémico de los pacientes con DM1 y DM2 que estén con terapia insulínica.31,32 Así mismo, existen otros iSGLT-2 que han sido aprobados para su uso, en Japón desde 2014. Estos son la ipragliflozina, luseogliflozina y la tofogliflozina.33
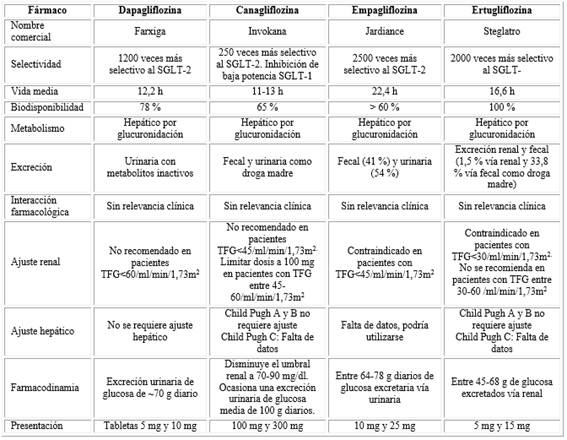
Los agentes iSGLT2 aprobados por la FDA y por la EMA para pacientes con DM2, se encuentran en fase comercial y aún están en pruebas clínicas de seguridad a largo plazo. Las propiedades fármaco cinéticas y farmacodinámicas de ellos se presentan en el cuadro 1.31
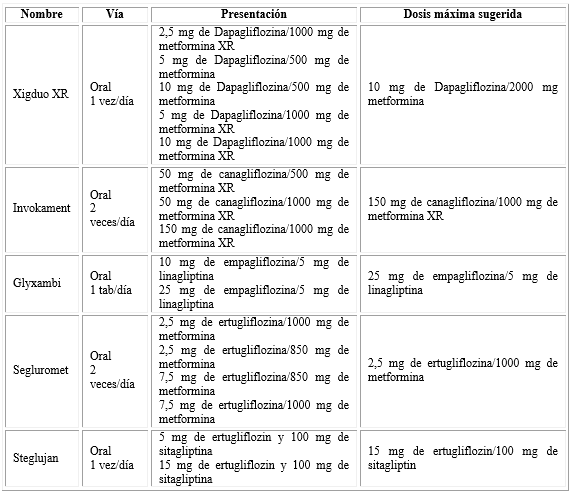
Estos medicamentos están disponibles tanto como productos de un solo ingrediente, como en formulaciones combinadas con otros fármacos para el tratamiento de la DM, para hacer más factible su uso31,31,34,35,36,37,38) (Cuadro 2).
Cuadro 2 Formulaciones combinadas de fármacos inhibidores del SGLT2 con otros medicamentos para el tratamiento de la diabetes mellitus
Los iSGLT2 pueden llegar a jugar un importante papel como “antidiabético” oral (ADO), esto se debe a que tienen una efectividad similar a las sulfonilureas y logran una disminución de HbA1c equivalente a la metformina (0,8 % a 1,0 %), si partimos de un valor de 8% durante dos años de tratamiento.8,9,39,40,41,42,43 La glucosuria que provoca la administración de los iSGLT2 induce un descenso de la glucemia basal, la glucemia posprandial y la HbA1c, y se muestra a la misma altura de otros ADO en la disminución de la HbA1c, siendo superiores -en algunos casos- en descenso de peso o presión arterial, con una incidencia de hipoglucemias similar a la observada con placebo.44,45,46 Todo lo cual aporta un elemento de tranquilidad para el paciente y el facultativo.
Los iSGLT2 inducen una disminución de la albuminuria en el paciente con DM2 y -como ya se mencionó- pérdida de peso secundaria a la excreción de glucosa (calorías) por la orina, que se acompaña de una reducción del perímetro de la cintura y de la masa grasa, especialmente de tejido adiposo visceral.44,45,46 Sin embargo, la respuesta farmacodinámica a los iSGLT2 disminuye en la Enfermedad renal crónica, lo cual se relaciona con la severidad de la insuficiencia renal. De ahí, la recomendación de consultar la información de prescripción relacionada con los ajustes de la dosis o las restricciones en la disfunción renal moderada a grave, donde no se recomienda su uso.43,47
Algunos resultados de interés relacionados con el uso de los inhibidores del cotransportador sodio-glucosa en personas con diabetes mellitus
Dandona y otros se dieron a la tarea de estudiar el uso de la dapagliflozina -primero de estos medicamentos en ser aprobado y comercializado en 2012- en pacientes con DM. Sus resultados sugieren que es promisorio adjuntar este medicamento al tratamiento insulínico para así mejorar el control glucémico en estos pacientes.48
Wiviott y otros49 en un estudio en pacientes con DM2 y tratamiento con dapagliflozina encontraron que el uso de este medicamento no resultó en una tasa más alta o más baja de muerte cardiovascular, infarto de miocardio o accidente cerebrovascular isquémico que el placebo. No obstante, encontraron una tasa más baja de muerte cardiovascular o de hospitalización para la insuficiencia cardíaca. Diferentes resultados encontraron Persson y otros50 los que observaron que la dapagliflozina se asoció con menores riesgos de eventos cardiovasculares y mortalidad por todas las causas, al compararlos con los inhibidores de la dipeptidil peptidasa-4, en un entorno clínico del mundo real y una población amplia de DM2.
En una revisión sistemática que incluyó doce ensayos clínicos aleatorizados, con un total de 3986 pacientes, se comparó grupos de pacientes tratados con dapaglifozina más metformina contra placebo más metformina, o dapagliflozina más insulina versus placebo más insulina, con un seguimiento entre 12 a 104 semanas. Se observó que la adición de la dapagliflozina al tratamiento convencional de la DM optimizó el control en los niveles de la HbA1c y de los niveles glicémicos en comparación con el grupo control; además se encontró que el grupo de pacientes con DM tratados con dapagliflozina redujeron peso corporal, condición favorable para el control metabólico de estos pacientes.51
En un estudio observacional retrospectivo, Ramírez y otros52 describen los resultados del tratamiento con diferentes iSGLT2 en 2113 pacientes con DM2 (0,74 % de todos los tratados con ADO); de los que 53,10 % eran hombres. La edad media fue de 64,54 años y el tratamiento por un periodo superior a seis meses, entre 2014-2015. Sus resultados plantean que una adecuada prescripción de los iSGLT2 en pacientes con DM2 ofrece un beneficio a corto plazo en la disminución de las cifras de Índice de masa corporal (IMC), HbA1c y colesterol, sin repercusión en la tensión arterial y la función renal.
El programa CANVAS integró datos de dos ensayos con un total de 10,142 participantes con DM2 y alto riesgo cardiovascular. Los participantes en cada ensayo fueron asignados al azar para recibir canagliflozina o placebo y se les dio seguimiento durante una media de 188.2 semanas. Se evidenció que los pacientes tratados con canagliflozina tuvieron un riesgo menor de eventos cardiovasculares que los que recibieron placebo, lo que apoya su efecto cardioprotector, pero desafortunadamente se constató un mayor riesgo de amputación, principalmente a nivel de los dedos del pie o del metatarso.46 Es de señalar que los resultados del programa CANVAS son similares al obtenido en el ensayo EMPA-REG OUTCOME,53) donde la empagliflozina, redujo el riesgo de eventos cardiovasculares mayores en pacientes con DM2 con esta condición.
Asimismo, se conoce que los iSGLT2 tienen -además- un efecto nefro protector,54,55 criterio apoyado por otros autores. En una investigación de Heerspink y otros55 sobre la acción de la canagliflozina sobre el riñón en 1450 pacientes con DM2 en tratamiento con metformina que fueron aleatorizados a recibir diariamente canagliflozina 100 mg (483), canagliflozina 300 mg (485) o glimepirida (482) en dosis creciente entre 6-8 mg/día, se observó como la canagliflozina, en comparación con la glimepirida disminuyó la progresión de la enfermedad renal de pacientes con DM2 en tratamiento con metformina en los dos años que duró el estudio, e independientemente del descenso glucémico, lo que sugeriría un efecto reno protector. Según Gómez y otros56) estos efectos, probablemente se fundamentan en los efectos favorables de los iSGLT2 sobre la hemodinámica glomerular disminuyendo la hiperfiltración, en la reducción de la toxicidad tubular de la glucosa, así como sus efectos beneficiosos sobre la glucemia, la presión arterial, el peso y la uricemia.
Como se puede observar, uno de los méritos que en la actualidad se le atribuyen al uso de los iSGLT2 es la protección cardiovascular y renal.46,54,55 Algunos investigadores22,55 han propuesto hipótesis que tratan de explicar dicho comportamiento, basados en los efectos metabólicos y hemodinámicos que provocan estos medicamentos y que se describen a continuación:
Efectos metabólicos: incluye la reducción de la glucotoxicidad inducida por la glucosuria, la reducción de masa grasa (especialmente peri visceral), el efecto hipouricemiante por la uricosúrica y la utilización preferente de las grasas en lugar de los hidratos de carbono, lo que conduce al aumento de producción de cetoácidos, que son un combustible más eficiente para el corazón y el riñón isquémico.
Efectos hemodinámicos: la diuresis osmótica inducida por la glucosuria y la natriuresis reduce la precarga (volemia) y la poscarga (presión arterial) y mejora el feed-back tubuloglomerular y la presión intraglomerular, todo ello sin incrementar el tono simpático. Además, la hemoconcentración aumenta el hematocrito (aunque parece existir también un incremento de eritropoyetina), lo que puede facilitar la liberación de oxígeno a tejidos isquémicos.
Garg y otros57 realizaron un ensayo fase III, doble ciego, en 133 centros de todo el mundo, se asignaron al azar a 1402 pacientes con DM1 que recibían tratamiento con cualquier terapia con insulina (bomba o inyecciones) para recibir sotagliflozina (400 mg al día) o placebo durante 24 semanas. Se observó que 28 % de los pacientes que recibieron el fármaco logró el objetivo primario de mantener la HbA1c a un nivel inferior a 7 %, sin sufrir hipoglucemias graves ni cetoacidosis en comparación con el 15% de los pacientes del grupo de placebo. En el grupo tratado con sotagliflozina, la cifra de HbA1c se redujo un 0,46%, la pérdida de peso fue de 2,98 kg, la presión arterial disminuyó entre los que padecían hipertensión arterial en 3,5 mm Hg y la dosis de insulina diaria se rebajó significativamente. La incidencia de episodios de hipoglucemias severas fue significativamente menor en comparación con el grupo placebo; en cambio, los casos de cetoacidosis diabética fueron superiores. Situación señalada con anterioridad por la FDA y la EMA, con el uso de otros iSGLT2.30,58,59
Esta situación concuerda con lo reportado por Pereyra y otros60 en una paciente de 17 años sin cetosis durante 9 años con DM1, la cual inició tratamiento con dapagliflozina 10 mg/día y la que de manera inesperada hizo un evento de esta naturaleza. Como es lógico, los autores opinan que este resultado aporta una preocupación especial, por el uso de iSGLT2 en personas con DM1 y apoyan el criterio de Taylor y otros61) los que sugieren que los profesionales de la salud deben buscar y evaluar cuidadosamente la presencia de cetoacidosis en estos pacientes. Ante dicha situación, se debe descontinuar los iSGLT2 y tomar las medidas apropiadas para corregir este problema de salud, lo antes posible.
Uno de los elementos de gran interés que señalan varias publicaciones, es el efecto benéfico que ejercen los iSGLT2 en la pérdida de peso, lo cual se había esbozado con anterioridad. Se plantea que su uso está asociado con una pérdida de peso dosis/respuesta, reducción promedio de 2.1 kg en comparación con el placebo después de 12 semanas de uso y reducción promedio de 2.9 kg después de dos años, en comparación con otros medicamentos.62,63,64
La evaluación de la eficacia de ertugliflozina y el ensayo de resultados cardiovasculares de seguridad (ensayo VERTIS-CV; NCT01986881) que abordan la salud cardiovascular en personas que usan este producto no fue posible compararla con los resultados de las investigaciones comentadas con anterioridad, pues dicha investigación estaba en curso en el momento de la redacción de este artículo.
Lo antes referido hace que los iSGLT2, al menos en teoría, se puedan considerar como candidatos de interés, al menos como coadyuvante, asociados a la metformina, para el tratamiento del Síndrome de insulino resistencia al contribuir a la mejoría de sus componentes, a pesar de no actuar directamente sobre la insulinorresistencia.
Los efectos secundarios y reacciones adversas más comunes observadas durante el uso el uso de los inhibidores del cotransportador sodio-glucosa
Los inhibidores de los iSGLT2 representan un abordaje novedoso en el tratamiento de la DM2. Pueden ser usados en terapia de combinación con otros medicamentos normo o hipoglucemiantes orales o incluso con insulina21 y tienen aplicación potencial en pacientes que son intolerantes a la metformina por efectos adversos de tipo gastrointestinal.65
La inhibición del SGLT1 se asocia con reacciones adversas potencialmente graves. Si bien, a nivel renal los SGLT1 juegan un papel poco apreciable, este transportador localizado fundamentalmente en el intestino delgado, facilita la absorción de la glucosa procedente de la alimentación y su inhibición puede conducir al incremento de la glucosa en la luz intestinal, con riesgo de aparición de diarrea osmótica.66,67
Los medicamentos iSGLT2 recientemente introducidos en la terapéutica de la DM, son suficientemente selectivos sobre los SGLT2 como para que no se produzcan efectos sobre los SGLT1 intestinales. La capacidad para inhibir los SGLT2 renal sin modificar el SGLT1 intestinal, es importante para el empleo práctico de estos fármacos. Asimismo, un incremento de glucosa en el intestino distal podría incrementar la secreción de péptido similar al glucagón tipo 1 (GLP1, por sus siglas en inglés),68 lo cual es útil en los sujetos con DM2.
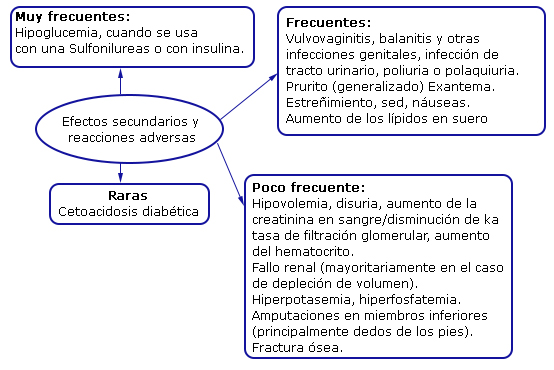
Los efectos secundarios y reacciones adversas más comunes observadas en personas que usan iSGLT, se relacionan con el mecanismo de acción de ellas23,24,25,29 (fig.).
De hecho, Jiménez y otros69 indican que los efectos secundarios y reacciones adversas más comunes observadas en población española que usa los iSGLT-2 desde su comercialización, han sido las infecciones del tracto urogenital, cetoacidosis y daño renal. Las sepsis urinarias en su mayoría no fueron graves, aunque la cetoacidosis y el daño renal sí lo fueron, generando ingresos y en ocasiones han hecho peligrar la vida de los pacientes.
Ramírez y otros52 en una investigación desarrollada por ello, describen efectos adversos y reacciones secundarias al tratamiento con iSGLT2, aunque estos fueron escasos en frecuencia (infecciones del tracto urinario (ITU): 5,31 %; micosis vaginal: 2,65 %; hipoglucemias: 0,88 %; cetoacidosis diabética: 0,00 %; intolerancia a dapagliflozina: 4,42 %). Lo cual, en parte coincide con la mayoría de las efectos adversos y reacciones secundarias notificadas por otros autores.60,61,69
A pesar de sus bondades de los iSGLT, la realidad obliga a hacer una prescripción cuidadosa, a consultar las advertencias publicadas por las autoridades sanitarias y notificar cualquier reacción adversa cuando esta se sospeche. De esta manera, se contribuye a su mejor y más completo conocimiento.58,59,69
Algunas reflexiones sobre el uso de los inhibidores del cotransportador sodio-glucosa
La utilización de los iSGLT-2 no solo reduce la reinyección de la glucosa ya filtrada desde la orina hacia la sangre, mejorando el control metabólico de la DM, sino que además restaura el “feed-back” tubuloglomerular al aumentar la glucosuria y el flujo urinario distal. Pero el efecto más notable se debe a la inhibición de la entrada de glucosa en la célula tubular proximal, pues la glucosuria es tóxica para el riñón, en particular para las células capaces de transportar glucosa, es decir, las células proximales dotadas de SGLT2. Estos efectos de los iSGLT2 en la clínica humana, han mostrado su capacidad para reducir el daño renal y el riesgo cardiovascular de los pacientes con DM2,70 cuando estos son indicados, teniendo en cuenta las recomendaciones para su uso.
La inhibición del cotransportador SGLT2 conlleva un déficit calórico y un conjunto de adaptaciones metabólicas y endocrinas como: uso de los lípidos como sustrato energético, aumento de la cetogénesis, aumento de la gluconeogénesis y aumento de la sensibilidad a la insulina. Los iSGLT2 han demostrado revertir la disfunción endotelial, la inflamación, el estrés oxidativo y la fibrosis intersticial, lo que retrasa la progresión de las complicaciones crónicas de la DM y mejora el perfil cardio-metabólico.71 Así mismo, se ha visto la reducción del volumen circulante efectivo y aumento en la actividad de bloqueadores del sistema renina-angiotensina-aldosterona circulantes, por lo que se crea un efecto nefro protector.54
Algo especialmente útil del uso de los iSGLT-2 y que ha sido indicado por varios investigadores,72,73,74 es que la pérdida de peso que se logra con su uso es predominantemente de tejido adiposo y en particular del tejido adiposo visceral, lo que representa un importante aspecto en la mejoría del perfil cardio-metabólico de estos pacientes. La reducción de peso se debe, principalmente, a la glucosuria, con un déficit calórico estimado de 50 kcal/día, a pesar de la posible contribución de otros mecanismos, como la activación del tejido adiposo marrón y la reducción de insulina.
En pacientes con DM1 y DM2 tratados con insulina y iSGLT2 se observa que disminuyen las necesidades diarias de las dosis de insulina y la hipoglicemia es menos frecuente. No obstante, estos medicamentos deben ser prescritos de manera cautelosa, sobre todo en pacientes jóvenes con DM1, por la mayor posibilidad de cetoacidosis y con un índice de masa corporal bajo, por la pérdida de peso que puede inducir.75
A manera de conclusión señalar que la administración de los iSGLT2 induce cambios favorables en la HbA1c, el peso corporal y la presión arterial; exhibiendo un bajo riesgo de hipoglucemia. Aunque constituyen un grupo farmacológico que se puede utilizar como monoterapia, por lo general los iSGLT2 se usan como coadyuvantes en el tratamiento de los pacientes con DM2 que reciben tratamiento farmacológico con otros medicamentos normo o hipoglucemiantes, en caso de que con ellos no se haya alcanzado las metas de control. Se debe estar alerta por la aparición de posibles efectos secundarios y reacciones adversas, para en este caso, descontinuar el tratamiento y tomar las medidas necesarias para resolver dicha situación.