Introducción
La cirugía de nervios periféricos constituye una subespecialidad practicada por neurocirujanos, cirujanos plásticos, ortopédicos y traumatólogos, a la cual se le relacionan preceptos erróneos e imprecisos, tales como que el déficit neurológico en las lesiones nerviosas periféricas es permanente e irreversible, la imposibilidad de regeneración neural y la desfavorable recuperación funcional a largo plazo.1 No se considera una cirugía de supervivencia sino transformadora, pues tiene un impacto sustancial en la calidad de vida del paciente, al optimizar su desempeño en las actividades rutinarias y profesionales, así como su bienestar físico y psicológico.2
Las lesiones del plexo braquial (LPB), devastadoras e incapacitantes, conllevan a la pérdida parcial o completa de las funciones sensitivas y motoras del miembro superior, dolor neuropático crónico, morbilidad psíquica e implicaciones socioeconómicas considerables, con un costo indirecto estimado en $1 113 962 anuales por paciente, solo en los Estados Unidos.3
La etiopatogenia clásica de las LPB en adultos, descrita por Narakas hace más de tres décadas,4 se fundamentó en una población de 1068 pacientes registrados en un período de 18 años (de los cuales se intervinieron solo 338), y formulaba la “regla de 7x70”:
más del 70 % de las LPB fueron causadas por accidentes de tránsito
el 70 % ocurrieron en motocicletas o bicicletas
el 70 % del último grupo sufrieron politraumatismos
el 70 % tuvo una lesión supraclavicular
un 70 % presentó al menos una lesión radicular
el 70 % de las avulsiones fueron en el plexo braquial inferior (C8-T1)
el 70 % de los pacientes con avulsión radicular desarrolló dolor neuropático crónico.
Kaiser y otros5 realizaron una revisión sistemática y metaanálisis de artículos publicados entre 1985 y 2017, donde se registraron LPB graves que requirieron cirugía reconstructiva (n: 3032). Como datos epidemiológicos y etiopatogénicos relevantes se constata una prevalencia de LPB cerradas del 93 %, de las cuales el 67 % se debieron a accidentes de motocicletas, el 14 % a automóviles; y el 93 % de los afectados fueron del sexo masculino, con un rango de edad promedio entre 23-34 años.
Las LPB originadas durante el trabajo de parto, comúnmente denominadas como parálisis braquial obstétrica,6 lesión del plexo braquial del nacimiento,7 o la definición más recomendable, parálisis del plexo braquial neonatal8,9 tienen una incidencia estimada entre 1.6-2.6 cada 1000 nacimientos.10 Entre sus principales factores de riesgo se encuentran la distocia de hombro, macrosomía fetal, diabetes materna, parto instrumentado y la presentación podálica.8
Las LPB se pueden clasificar como altas (C5, C6, con o sin lesión de C7), bajas (C8, T1) o totales (C5, C6, C7, C8, T1). Entre las técnicas quirúrgicas principales se incluyen la reparación con o sin injerto neural, neurólisis, transferencia neural (neurotización), transferencia tendinosa, transferencia muscular, y la transferencia muscular de libre funcionamiento;11 intervenciones que favorecen el progreso en la rehabilitación funcional,12,13 principalmente, si se realizan dentro de un marco temporal inferior a los 6 meses de evolución.14
La estimulación eléctrica de nervios periféricos o neuroestimulación, procedimiento desarrollado durante la década de 1970 para la localización neural durante la realización de bloqueos terapéuticos,15 ha sido relegada a un rol secundario en la anestesia regional en favor de la ultrasonografía como método complementario para la monitorización del contacto del nervio con la aguja, o la detección de nervios difíciles de visualizar con el ecógrafo.16 Sin embargo, la neuroestimulación intraoperatoria constituye una técnica esencial durante la cirugía del plexo braquial (CPB), pues permite la identificación específica de las estructuras neurales, y en determinadas circunstancias (transferencias nerviosas distales, neurólisis de neuromas en continuidad), la intensidad precisa de la estimulación nerviosa y la respuesta motora evocada son fundamentales para la toma de decisiones críticas durante el acto quirúrgico.17,18,19
El objetivo de la investigación fue describir la utilización de un neuroestimulador de anestesia regional para la localización neural intraoperatoria durante la cirugía del plexo braquial en dos pacientes.
Presentación de casos
Caso 1
Paciente masculino de 27 años de edad, con antecedentes de salud, que sufrió una herida por arma blanca a nivel de la cara anterior del hombro derecho. Comenzó a presentar dificultad para la movilización del miembro superior ipsilateral. Acude a consulta con 11 meses de evolución refiriendo dificultad para la flexión del codo y la extensión de la muñeca y los dedos, lo que le dificultaba la realización de sus actividades diarias.
Datos positivos al examen físico
Inspección: cicatriz de herida a nivel infraclavicular, en el borde superior del hueco axilar. Marcada atrofia de los compartimentos anterior y posterior del brazo, así como de la región posterior y lateral del antebrazo. Codo en extensión, antebrazo en pronación, mano péndula con los dedos medianamente flexionados y el pulgar en flexión y aducción.
Palpación: signo de Tinel positivo a nivel de la cicatriz. Disminución del diámetro circunferencial del miembro superior derecho. Imposibilidad a la supinación y extensión activa del codo, pero no pasiva. Imposibilidad para la extensión activa de muñeca y de las articulaciones metacarpo-falángicas.
Tono y trofismo muscular: hipotonía marcada de la musculatura del brazo, tanto del compartimiento anterior como posterior, así como de la región dorso lateral del antebrazo.
Fuerza muscular: grado 0/5 (método de Daniels) de los músculos flexores (braquial anterior, bíceps braquial y coracobraquial) y extensores (tríceps) del codo, así como los músculos dorsolaterales del antebrazo (extensor radial largo y corto del carpo, braquiorradial).
Reflejos: ausencia de los reflejos bicipital, tricipital, estilorradial y estilocubital.
Sensibilidad: parestesias en el borde dorsal lateral del antebrazo, desde el codo hasta la muñeca.
Impresión diagnóstica: lesión del fascículo lateral del plexo braquial derecho, lesión alta del nervio radial homolateral.
Intervención quirúrgica: técnica de Oberlin.
Se realiza una incisión a nivel del tercio medio del brazo derecho, en su región interna, localizada a 10 cm del hueco axilar. Se profundiza por planos entre los músculos bíceps y tríceps, se localizan y diferencian los nervios medianos, cubital, musculocutáneo y cutáneo braquial lateral, mediante neuroestimulación, utilizando estímulos graduales y progresivos (Fig. 1). Se localiza el fascículo motor del nervio cubital que inerva el músculo cubital anterior, y el fascículo motor del nervio musculocutáneo que inerva el bíceps; posteriormente, se realiza la neurotización del fascículo del nervio cubital hacia el fascículo del nervio musculocutáneo.
Al momento de la redacción del manuscrito, el paciente tenía tres meses de evolución posquirúrgica, aún insuficientes para realizar una valoración de la recuperación funcional objetiva.
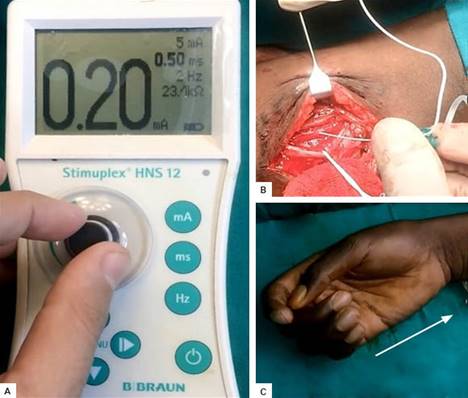
Fig. 1 A. Manipulación del neuroestimulador por el anestesiólogo, fuera del campo quirúrgico (Intensidad: 0.20 mA; Frecuencia: 2 Hz; Duración: 0.50 ms). B. Estimulación del nervio mediano a nivel del tercio medio del brazo derecho, utilizando una aguja B.Braun Stimuplex® D 22 Ga. C. Flexión radial de la muñeca secundaria a la estimulación del nervio mediano.
Caso 2
Paciente masculino de 22 años de edad, con antecedentes de politraumatismo consecuencia de un accidente de tránsito en un ciclomotor, que acude a consulta con una lesión del plexo braquial izquierdo de 12 meses de evolución, refiriendo dolor neuropático crónico de gran intensidad (VAS de 8-9 puntos) en las regiones dorsal de la mano y dorso lateral del antebrazo.
Datos positivos al examen físico
Inspección: miembro superior izquierdo péndulo. Movimiento ascendente del hombro por la acción del músculo trapecio. No se constata signo de Horner. Signos simpático-vegetativos: piel fina y brillante, con ausencia de pliegues, anhidrosis, uñas con estrías y curvas anormales en los planos longitudinales y transversales.
Palpación: disminución del diámetro circunferencial del miembro superior izquierdo. Se confirma la contracción de los músculos paravertebrales dorsales, romboides mayor y menor izquierdos.
Tono y trofismo muscular: hipotonía y atrofia marcada de todos los grupos musculares del miembro superior izquierdo.
Fuerza muscular: grado 0/5 (método de Daniels) de todos los músculos del miembro superior izquierdo.
Reflejos: ausencia de los reflejos bicipital, tricipital, estilorradial y estilocubital.
Sensibilidad: dolor neuropáticoen las regiones dorsal de la mano y dorso lateral del antebrazo izquierdo.
Impresión diagnóstica: lesión total del plexo braquial izquierdo, post ganglionar.
Intervención quirúrgica: exploración y neurólisis.
Se realiza un abordaje supraclavicular izquierdo, mediante incisión en Z, siguiendo el borde posterior del músculo esternocleidomastoideo, y el borde inferior de la clavícula; se eleva la aponeurosis superficial con el músculo platisma, se identifica el músculo omohioideo como punto de guía y se secciona en su porción tendinosa. Se diseca la aponeurosis del músculo escaleno anterior y se localiza el nervio frénico mediante neuroestimulación (intensidad: 0.05 mA; frecuencia: 3 Hz; duración: 0.10 ms), constatando descensos transitorios agudos en la meseta espiratoria de la capnografía (modo ventilación controlada por presión, VCP).
Se observa una zona de abundante fibrosis que dificulta la localización y disección de las estructuras anatómicas. Luego de la neurólisis, se identifica el tronco superior, se efectúa la estimulación eléctrica gradual, requiriendo una elevada intensidad (2.60 mA), tras la cual se registra, únicamente, como respuesta motora evocada la contracción débil del músculo pectoral mayor ipsilateral (Fig 2). Se identifica el tronco medio, sin evidencia de respuesta motora tras la estimulación a alta intensidad, y no fue posible localizar el tronco inferior, debido a la fibrosis circundante y el elevado riesgo de lesión de estructuras vasculares adyacentes.
A los treinta días de evolución posquirúrgica, se constata la disminución de la intensidad del dolor neuropático (VAS de 2-3 puntos), localizado en la región posterior del codo.
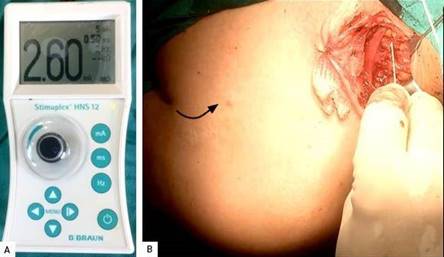
Fig. 2 A. Neuroestimulador (Intensidad: 2.60 mA; Frecuencia: 2 Hz; Duración: 0.50 ms). B. Estimulación del tronco superior, a nivel supraclavicular izquierdo, utilizando una aguja B. Braun Stimuplex® D 22 Ga, tras lo cual solo se registra como respuesta motora evocada la contracción del músculo pectoral mayor ipsilateral.
Conducción anestésica
En ambos pacientes se utilizó la técnica de anestesia total intravenosa y analgesia multimodal, basadas en la administración de propofol [Infusión controlada por objetivo (TCI), modelo farmacocinético Marsh, Cp 2.5-4 µg/mL], ketamina (TCI manual, modelo farmacocinético Domino, Cp 0.2 µg/mL), sulfato de magnesio (bolo de 10 mg/Kg; seguido de infusión 10-15 mg/Kg/h), lidocaína (bolo de 1 mg/Kg; seguido de infusión 1-1.5 mg/Kg/h), fentanilo (bolo de 3µg/Kg en la inducción), así como antieméticos (ondansetrón, dexametasona), analgésicos complementarios (diclofenaco, metamizol, tramadol) y la infiltración de la herida quirúrgica con bupivacaína al 0,25 %.
La utilización del neuroestimulador requiere evitar los bloqueantes neuromusculares durante el período intraoperatorio, pues imposibilitan la obtención de una respuesta motora evocada. Solo se administró una dosis única de un agente de acción intermedia (atracurio 0,5 mg/Kg) para facilitar la intubación orotraqueal.
Se realizó monitorización estándar con electrocardiograma continuo DII, tensión arterial no invasiva, SpO2 y etCO2.
Discusión
La elección del tipo de neuroestimulador a utilizar durante la CPB difiere según la disponibilidad de los múltiples modelos comerciales existentes en el mercado, aunque de forma general, se pueden definir tres modalidades principales: la utilización de pinzas quirúrgicas unipolares20 o bipolares21,22,23 convencionales, con la desventaja de que están diseñadas para la electrocauterización tisular, no para la localización neural, por lo que pueden ocasionar lesiones térmicas aún sin estar en contacto directo con las fibras nerviosas;24 los neuroestimuladores desechables7,12,17,25 y los neuroestimuladores para anestesia regional.17
Además de la neuroestimulación, existen otros métodos experimentales para la localización neural intraoperatoria durante la cirugía de nervios periféricos, como la electroneurografía26 y espectroscopia óptica de reflectancia difusa;27 entre otras técnicas más complejas y exclusivas desarrolladas para la diferenciación de fascículos como el análisis histoquímico (acetilcolinesterasa, anhidrasa carbónica, colina acetiltransferasa), inmunohistoquímico (annexina V, agrina), métodos físicos (espectroscopia cercana al infrarrojo, radioisótopos, potenciales evocados) y la observación de puntos cuánticos.28
Neuroestimuladores totalmente desechables versus neuroestimuladores para anestesia regional
Los neuroestimuladores totalmente desechables se han utilizado en la CPB debido a que todo el dispositivo es estéril y portátil, lo que facilita su inserción dentro del campo quirúrgico. El modelo de referencia es el VARI-STIM® III (Medtronic Inc., Minneapolis, Minnesota, Estados Unidos); permite administrar estímulos con una intensidad fija de 0.5, 1 y 2 mA, sin regular la duración ni la frecuencia, el ánodo se introduce mediante punción en el tejido celular subcutáneo, y tiene un precio de $ 100 por set de 10 unidades.
Otro modelo más reciente y sofisticado es el Checkpoint® (Checkpoint Surgical Inc., Cleveland, Ohio, Estados Unidos), que administra estímulos de onda bifásica, con una intensidad fija de 0.5, 2 y 20 mA, frecuencia de 16 Hz que origina contracciones tetánicas, duración hasta 0.20 ms, y un precio de $159 por unidad.
Thallaj y otros17 realizaron un estudio retrospectivo donde compararon la efectividad de dos dispositivos para la neuroestimulación intraoperatoria durante la CPB (n: 60). En el primer grupo (n1: 30) utilizaron el VARI-STIM® III, y en el segundo grupo (n2: 30), el B. Braun Stimuplex® HNS 11 (B. Braun Medical Inc., Bethlehem, Pennsylvania, Estados Unidos), lo que constituye el primer reporte sobre el empleo de un neuroestimulador para anestesia regional en la CPB. Los dispositivos desechables presentaron mal funcionamiento al menos una vez por cirugía, requiriendo 70 unidades para las 30 intervenciones realizadas en ese grupo, y no se constataron fallas en el dispositivo para anestesia regional.
Alternativa para la neuroestimulación intraoperatoria durante la CPB
Los autores del presente artículo utilizan rutinariamente el neuroestimulador B. Braun Stimuplex® HNS 12 (B. Braun Mensulgen AG, Melsungen, Alemania) durante las cirugías del plexo braquial realizadas en su centro asistencial, pues presenta ventajas prácticas relevantes en relación a los dispositivos desechables, así como una relación costo-beneficio apropiada para su implementación en entornos y naciones de recursos limitados.
El dispositivo, no estéril, alimentado por una batería reemplazable de 9V, aunque tiene un precio de $1000 por unidad en el mercado internacional, el fabricante certifica una vida útil de 999 meses, lo cual le otorga una rentabilidad superior a largo plazo. Para su utilización se recomiendan las agujas de la serie Stimuplex® y Contiplex® (B. Braun Mensulgen AG, Melsungen, Alemania), con un precio promedio entre $ 9-15 según modelo. Si bien el cable de conexión, de tipo RBW-5U o RBW-5L, posibilita su compatibilidad con agujas de otros fabricantes como Pajunk® (Pajunk GmbH Medizintechnologie, Geinsingen, Alemania) y Avanos® (Avanos Medical Inc., Georgia, Estados Unidos), y le brinda mayor versatilidad al producto.
Previa desinfección con povidona iodada y solución hidroalcohólica, se recubren los cables de conexión (cable doble de 1,25 m de longitud) con fundas estériles independientes, así el ánodo se conecta a un electrodo de electrocardiograma estándar, situado en la extremidad a intervenir, a más de 20 cm del foco de estimulación, cubierto por el campo quirúrgico, y el cátodo se enlaza a la aguja de estimulación, estéril y solo manipulada por los cirujanos. Las agujas se esterilizan posteriormente con óxido de etileno, lo que aumenta su vida útil y capacidad de reutilización.
Al contrario que los dispositivos desechables, que tienen intensidades de estimulación predeterminadas por el fabricante, (0.5, 1, 2 y 20 mA), el neuroestimulador B. Braun Stimuplex® HNS 12 suministra estímulos desde 0.1 hasta 5 mA, con incrementos progresivos de 0.01 mA (para intensidades inferiores a 1 mA) y 0.1 mA (para intensidades superiores a 1 mA), además de una frecuencia (1, 2 y 3 Hz) y duración (0.05, 0.1, 0.3, 0.5 y 1 ms) variables, que permiten individualizar la estimulación a las características específicas de las fibras nerviosas.
Ejemplos:17
La intensidad mínima de los dispositivos desechables (0.5 mA) puede causar sobreestimulación de los fascículos adyacentes, particularmente, antes de la disección interfascicular, lo que requiere aumentos graduales de la intensidad comenzando desde 0.1 mA.
La decisión intraoperatoria sobre escindir los neuromas en continuidad o realizar neurólisis se basa, principalmente, en la respuesta motora evocada, que precisa de estímulos graduales y progresivos.
Un nervio lesionado puede necesitar duraciones del estímulo más largas para lograr una respuesta motora efectiva.
Determinados nervios pueden requerir frecuencias superiores a 1 Hz para su adecuada localización, como el espinal accesorio.
Entre las múltiples técnicas quirúrgicas empleadas en la CPB, la reinervación del nervio supraescapular, mediante la transferencia del nervio frénico, uno de los métodos para restaurar la función del hombro, tiene características de particular interés para el anestesiólogo, debido al compromiso de la función respiratoria. Luego de la extracción del nervio frénico, se produce parálisis hemidiafragmáticaipsilateral, que origina una disminución de los parámetros espirométricos durante los 12 a 24 meses posteriores a la cirugía.11 En consideración, los pacientes con comorbilidades respiratorias asociadas, como la enfermedad pulmonar obstructiva crónica, obesidad, antecedentes de traumatismo de tórax o trastornos restrictivos pulmonares, no son candidatos para la transferencia del nervio frénico, por lo que deben valorarse técnicas alternativas como la transferencia del nervio espinal accesorio.
La respuesta evocada a la estimulación eléctrica del nervio frénico puede monitorizarse, indirectamente, a través de la capnografía, las curvas de presión-tiempo y flujo-tiempo del ventilador. La capnografía muestra descensos transitorios agudos en la meseta espiratoria (modo ventilación controlada por presión, VCP) o reducción gradual de su amplitud (modo ventilación controlada por volumen, VCV). Las curvas de presión-tiempo exhiben elevaciones sucesivas en “forma de sierra”; y las curvas flujo-tiempo evidencian cambios variables en la línea basal, como ciclos respiratorios “en miniatura” luego del flujo espiratorio (VCP), u ondulaciones súbitas en el flujo inspiratorio (VCV).29
La utilización de un neuroestimulador de anestesia regional para la localización neural durante la cirugía del plexo braquial, presenta ventajas prácticas relevantes en relación a los neuroestimuladores desechables, así como una relación costo-beneficio apropiada para su implementación en entornos y naciones de recursos limitados.














