Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Habanera de Ciencias Médicas
versión On-line ISSN 1729-519X
Rev haban cienc méd vol.12 no.4 Ciudad de La Habana oct,.dic. 2013
CIENCIAS QUIRÚRGICAS
Universidad de Ciencias Médicas de La Habana
Instituto Nacional de Oncología y Radiobiología
Exenteración pélvica en el cáncer avanzado de la vulva. Presentación de caso
Pelvic exenteration in advanced cancer of the vulva. Case presentation
Roberto P. Esperón NoaI, Jesús M. Valdés JiménezII, Jorge Felipe Montero LeónIII, Omar de Jesús Bosque DiegoIV, Juan Mario Silveira PablosV, Alejandro Linchenat LambertVI
I Especialista Primer Grado en Cirugía General. Diplomado en Ginecología Oncológica. Asistente. e.mail: resperon@infomed.sld.cu
II Especialista Primer Grado en Cirugía General. Diplomado en Cuidados Intensivos del Adulto y Ginecología Oncológica.
III Especialista Primer Grado en Cirugía General. Profesor Auxiliar. Investigador Agregado.
IV Especialista Primer Grado en Oncología. Asistente. Investigador Agregado.
V Especialista Primer Grado en Oncología. Profesor Auxiliar. Investigador Auxiliar.
VI Especialista Segundo Grado en Oncología. Asistente. Investigador Agregado.
RESUMEN
Introducción: el carcinoma de la vulva es un tipo de cáncer raro que constituye entre 4 y 5 % de todos los cánceres ginecológicos. La Exenteración Pélvica les ofrece una última oportunidad de "curación" a algunas pacientes con enfermedad neoplásica ginecológica maligna, avanzada o recurrente. Sin embargo, la morbilidad de esta cirugía radical compleja es alta.
Objetivo: presentar una paciente con cáncer avanzado de vulva y operada con la técnica de Exenteración Pélvica.
Presentación del caso: se describen las características clínicas de la paciente; el resultado de los complementarios; estadio inicial, proceder terapéutico, resultado del estudio histopatológico, estadio postquirúrgico, la evolución postoperatoria, así como los datos del seguimiento.
Conclusiones: postoperatorios satisfactorios a los 3 años de seguimiento; se presentó una sola complicación: edemas en ambos miembros inferiores en el primer año de operada que evolucionó adecuadamente. En la actualidad, mantiene relaciones sexuales satisfactorias por vagina.
Palabras clave: carcinoma, exenteración pélvica, vulva.
ABSTRACT
Introduction: carcinoma of the vulva is a rare cancer that is between 4 and 5 percent of all gynecologic cancers. The Pelvic exenteration offers one last chance to "cure" some patients with gynecological malignant neoplastic disease, advanced or recurrent. However, the morbidity of radical surgery is high complex.
Objetive: describe the clinical case of a patient studied and treated with a primary squamous cell carcinoma of the vulva.
Case presentation: we describe the clinical characteristics of the patient, the result of the complementary; initial staging, the therapeutic procedure, results of the histopathological study, the postoperative staging, postoperative course, and follow-up data.
Conclusions: postoperative results are satisfactory at 3 years follow-up, there was a single complication: edema of both lower in the first year after the surgery that evolved properly. Currently holds satisfactory for vaginal sex.
Key words: carcinoma, pelvic exenteration, vulva.
INTRODUCCIÓN
La Exenteración Pélvica es una intervención quirúrgica desarrollada en los años 40 del siglo pasado en varios centros norteamericanos. Brunschwig publicó su primer artículo en 1948, describiendo la operación como la escisión completa de las vísceras y el peritoneo pélvicos en los cánceres avanzados y recurrentes del cérvix, la vagina, la vulva, el útero y el rectosigmoides; relató su experiencia en 22 pacientes sometidos a esa cirugía ultraradical que llevó a cabo con mayor frecuencia en cánceres localizados en el cérvix, la vagina y la vulva.1-4 Bricker demoró la publicación de su artículo hasta 1951, pero en 1950 reportó un avance técnico substancial, el aislamiento de un asa ileal para derivar la orina, separada de las heces fecales. La Exenteración Pélvica (EP) ha evolucionado mucho con los años. Puede ser total (EPT), o parcial. La primera implica la exéresis de la vejiga, la uretra, el útero y los anejos -en caso de no haber sido extirpados antes- de los parametrios hasta la pared pélvica lateral, el peritoneo pélvico, la vagina, la vulva, el rectosigmoides y el ano. La segunda puede ser anterior (EPA), cuando se limita a los genitales internos, la vejiga y la uretra; o posterior (EPP): si con los genitales se resecan el rectosigmoides y el ano; y en ambos casos (EPA, EPP), la vagina y/o la vulva. Si lo requiere el caso, se realiza también linfadenectomía pélvica y/o disección ganglionar inguinocrural bilateral; y además, una diversión urinaria y/o colostomía, con o sin reservorios. Cuando sea necesario, la intervención quirúrgica se complementará con radioterapia intraoperatoria o radioquimioterapia adyuvante. En otra variante, la fase ablativa se realiza hasta el plano de los músculos elevadores (EPS) para conservar la función del esfínter anal y el diafragma urogenital. Una intervención ultraradical es la Exenteración Pélvica extendida (EPE), ya sea hacia delante, lateralmente o hacia atrás. La EP es una IQ en extremo mutilante y deja secuelas que afectan la calidad de vida de las pacientes, pero en estos momentos las nuevas variantes técnicas permiten realizarla sin dejar estomas o construir una neovagina. Al mismo tiempo era y es "la única opción terapéutica que permitirá el control de la enfermedad" en algunas de las pacientes, cuando no se cuenta, se han descartado o se han realizado ya otros tratamientos oncoespecíficos. 4-8
De 30 a 40 % de las pacientes con cáncer en la vulva acuden en estadio III_IV y pueden ser tratadas con Exenteración Pélvica, aunque Gadducci et al, 9 consideran esta "como una cirugía con graves complicaciones postoperatorias, que ofrece una pobre calidad de vida, asociada a una tasa de supervivencia poco satisfactoria".
OBJETIVO: Presentar una paciente con cáncer avanzado de vulva y operada con la técnica de exenteración pélvica.
PRESENTACIÓN DEL CASO
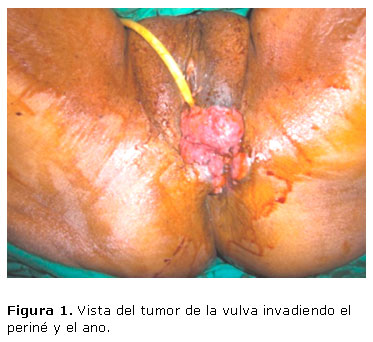
Paciente de 49 años de piel negra, con antecedentes de salud e historia obstétrica de dos partos eutócicos, eumenorreica, quien acudió al Servicio de Ginecología del INOR en el 2010 refiriendo tener una "lesión" en la vulva desde hacía alrededor de 3 años, que creció mucho con el paso del tiempo, asociándosele prurito intenso, exudación mal oliente, dolor, y sangrado en ocasiones. (Figura 1).
Examen Físico (datos positivos)
Inspección genital: Se observa un tumor vegetante que se extiende desde el tercio posterior del labio mayor izquierdo y la horquilla vulvar, al centro tendinoso del periné, la parte interna de la raíz del muslo izquierdo y al ano, que mide aproximadamente 8 cm de diámetro y sangra con facilidad al contacto.
Examen con espéculo: Existe infiltración tumoral de los tercios inferior y medio de la vagina.
Tacto vaginal: La masa tumoral tiene consistencia firme y sangra al tacto.
Tacto rectal: El tumor infiltra más de dos tercios del esfínter del ano y los tercios medio e inferior del tabique rectovaginal.
Regiones inguinocrurales: No existen adenopatías.
Exámenes complementarios:
Hematimetría, Hemoquímica, Ultrasonografía, RX de Tórax y Pelvis: Todos dentro de los límites normales, excepto la eritrosedimentación de 80 mm/h. La tomografía axial computarizada excluyó las metástasis linfáticas y hepáticas. La biopsia por ponche arrojó: carcinoma epidermoide infiltrante, bien diferenciado, de la vulva.
Diagnóstico preoperatorio
Carcinoma epidermoide de la vulva en Estadio II (T2N0M0).
Informe operatorio
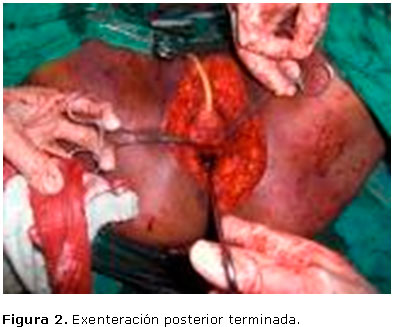
Se realizó linfadenectomía inguinocrural superficial bilateral a través de incisiones separadas. Se practicó una celiotomía media supra e infra umbilical y después de excluir la presencia de carcinosis peritoneal y metástasis hepática, y evaluar el retroperitoneo de arriba abajo, exponiendo la aorta y la vena cava desde las fosas lumbares e inspeccionando los ganglios linfáticos periaórticos, se determinó la resecabilidad lateral y se procedió a realizar la histerectomía total abdominal con doble anexectomía (tipo Rutledge II), disecando ambos uréteres para resecar los parametrios. Se seccionó la fascia de Todd por fuera del asa sigmoidea y se disecó el mesorecto hasta la unión sacrococcígea. Se ligaron la tercera rama de la arteria y la vena sigmoidea, y las arterias y venas hemorroidales superiores. Se seccionaron y ligaron los alerones del recto y los vasos hemorroidales medios. Se seccionaron los bordes laterales de la vagina hasta su tercio inferior, ligando selectivamente los vasos que la irrigan; la pared posterior de la vagina permaneció unida a la cara anterior del recto. Se procedió entonces a realizar la vulvectomía total, extendiendo la incisión hacia atrás abarcando el centro del periné y el ano, para completar la proctosigmoidectomía por vía perineal. (Figura 2). Se peritonizó el suelo pélvico y se realizó el taponamiento y drenaje de la cavidad. Se realizó plastia vaginal utilizando la mucosa de la cara anterior de la misma. Se completó la sigmoidostomía y se terminó la operación al suturar la herida abdominal. No hubo accidentes peroperatorios.
Informe histopatológico
Carcinoma epidermoide bien diferenciado, infiltrante, de la vulva que se extiende a la pared posterior de la vagina, el esfínter del ano y el tabique rectovaginal. No hay evidencia de tumor maligno en el rectosigmoides ni metástasis en las cadenas ganglionares resecadas ni en los bordes de sección quirúrgica. Concluyendo, se trataba de un carcinoma escamoso infiltrante, bien diferenciado de la vulva. Estadio II (pT2N0M0).
Evolución
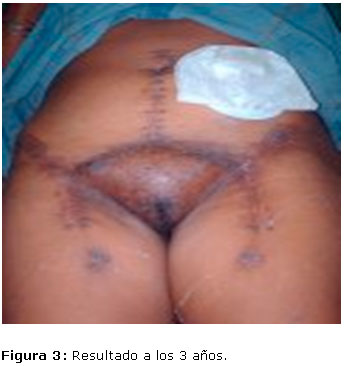
La paciente tuvo una magnífica evolución postoperatoria. Únicamente presentó, al 15º día del período postoperatorio, linfedema en los miembros inferiores que mejoró notablemente con reposo, elevación de los MI y flebotónicos. Tres años después la paciente solo ha presentado linfedemas discretos de los miembros inferiores y una actividad sexual satisfactoria vía vaginal según refiere.
Seguimiento
Actualmente la enfermedad neoplásica está controlada y se continúa el seguimiento por consulta externa cada 6 meses. (Figura 3).
DISCUSIÓN
Cuando han pasado casi 65 años desde la publicación de Brunschwig, la EP sigue siendo blanco de controversias; expusimos los criterios de Gadducci et al, y se añade que Wahlen et al, 9 la utilizan solo para el rescate de los casos, en los que ha fallado la radioquimioterapia. Eso a pesar de las series de casos publicadas que reportan que la tasa de mortalidad perioperatoria es hoy, generalmente, < 10% y tan baja como 2%, cuando la original ascendía a 23%; que la tasa de supervivencia a los 5 años aumentó de 23 a 61 % en las pacientes con cánceres primarios, con calidad de vida excelente, aunque sigue siendo < 23% en las pacientes con recurrencia; y por demás, que la tasa de complicaciones quirúrgicas y postquirúrgicas, aunque se mantiene alta, disminuyó notablemente: (la morbilidad reportada fluctúa entre 30 y 75 %). 3, 4, 6-8, 10- 24
Actualmente se realizan más EP en pacientes con recidivas que ya habían sido tratadas con RQT adyuvante o no, que en pacientes con cánceres primarios, o recidivas en pacientes previamente tratadas solo con cirugía. Esta aseveración no está avalada por los criterios de otros autores. 7, 8, 20-27 Höckel & Dornhöfer, 28 dividen a sus pacientes en cuatro categorías diferentes: las que tienen una pelvis previamente irradiada y las que no; las que tienen una enfermedad avanzada no tratada; y aquellas con síntomas pélvicos graves sin oportunidad de curación. Para ellos, en la primera categoría, la supervivencia a 5 años era nula si el tumor medía más de 5 cm, y muy baja (4%) si hubiera un resto tumoral microscópico, descendía hasta 10% si había infiltración del íleon o el sigmoides; la presencia de metástasis ganglionares pelvianas y periaórticas reducen, pero no necesariamente abolirían la oportunidad de curación. Las contraindicaciones de la EP son: la enfermedad metastásica extrapélvica; la extensión a la pared pélvica manifestada por la triada _ edema unilateral de un MI, con ciatalgia y obstrucción ureteral ipsilateral. La edad avanzada no es una contraindicación, si acaso, es relativa. No obstante, un mal performance status y las enfermedades crónicas no trasmisibles asociadas graves excluyen una opción terapéutica de tanta envergadura. Las complicaciones más frecuentes están relacionadas con los estomas (necrosis, retracción, estenosis, hernia, prolapso), las suturas (dehiscencias, fugas, fístulas), las heridas (infección, absceso, hematoma, seroma y disrupción) y los colgajos (seroma, necrosis, infección, dehiscencia). Las menguas de la imagen corporal y la sexualidad, que poco preocupaban antes de la cirugía, constituyen las secuelas más sobresalientes después del tratamiento. Los problemas son más pronunciados entre las mujeres jóvenes con dos estomas permanentes y una vagina no funcional. Sin embargo, muchas pacientes se adaptan a la nueva situación y pueden exhibir una calidad de vida similar, desde el punto de vista cognoscitivo y emocional, a la de los individuos saludables. 7-9, 12, 18, 27-30
En el INOR, la mayoría de las EP en los últimos años se realizan en pacientes con tumores primarios de la vulva y son exenteraciones posteriores. En general aceptamos los criterios que hemos expuesto en este acápite y nos hemos limitado a presentar este caso para interesar al lector a ampliar la revisión bibliográfica. Hemos omitido exprofeso libros de texto clásicos y trabajos de autores reconocidos.
CONCLUSIONES
1. La exenteración pélvica posterior es una modalidad terapéutica adecuada con equipo entrenado.
2. La morbilidad quirúrgica postoperatoria no es tan alta ni tan significativa y proporciona a las pacientes una buena calidad de vida.
REFERENCIAS BIBLIOGRÁFICAS
1. Brunschwig A. Complete excision of pelvic viscera for advanced carcinoma. Cancer 1948; 1:177-83.
2. Bricker EM, Modlin EJ. The role of pelvic evisceration in surgery. Surgery. 1951; 30:76-94.
3. Carter J, Chi DS, Abu_Rustum N, Brown CL, McCreath W, Barakat RR. Brief Report: Total Pelvic Exenteration _ A Retrospective Clinical Needs Assessment. Psycho_Oncology. 2004; 13:125-31.
4. Durgatosh P, Shuaib Z, Vikas M, Ravi K. Pelvic exenteration: A perspective from a regional cancer center in India. Indian J Cancer. 2004; 41(3):109-14.
5. Lambrou NC, Pearson JM, Averette HE. Pelvic Exenteration of Gynecologic Malignancy: Indications,and Technical and Reconstructive Considerations. Surg Oncol Clin North Am. 2005; 14:289-300.
6. Benn T, Brooks RA, Zhang Q, Powell MA, Thaker PH, Mutch DG, Zighelboim I. Pelvic exenteration in gynecologic oncology: A single institution study over 20 years. Gynecol Oncol. 2011; 122:14-8.
7. Mitulescu G, Ungureanu C, Gluck G, Stîngu C, Mitulescu D, Stãnculeanu D, Sgarburã O, et al. Exenteratia pelvinã totalã în tratamentul cancerului pelvin avansat. Chirurgia. 2007; 102 (2):143-154.
8. Schneider A, Köhler C, Erdemoglu E. Current developments for pelvic exenteration in gynecologic oncology. Curr Opin Obstet Gynecol. 2009; 21(1):4-9.
9. Gadducci A, Cionini L, Romanini A, Fanucchi A, Genazzani AR. Old and new perspectives in the management of high_risk, locally advanced or recurrent, and metastatic vulvar cancer. Crit Rev Oncol Hematol. 2006; 60:227-41.
10. Berek J, Howe C, Lagasse L, et al. Pelvic exenteration for recurrent gynaecologic malignancy: survival and morbidity analysis of the 45-year experience at UCLA. Gynecol Oncol. 2005;99:153-59.
11. Marnitz S, Dowdy S, Lanowska M, Schneider A, Podratz K, Köhler C. Exenterations 60 years after first description: results of a survey among US and German Gynecologic Oncology Centers. Int J Gynecol Cancer. 2009; 19(5):974-7.
12. Goldberg J, Piver S, Hempling R, et al. Improvement in pelvic exenteration: factors responsible for reducing morbidity and mortality. Ann Surg Oncol. 1998; 5:399-406.
13. Magrina J, Stanhope C, Waever A. Pelvic exenterations: supralevator, infralevator, and with vulvectomy. Gynecol Oncol. 1997; 64:130-35.
14. Vieira SC, Costa DR, Meneses AD, Silva JB, Oliveira AKS, Sousa RB. Exenteração pélvica para câncer do colo uterino recidivado pós-radioterapia: experiência de um centro terciário do Nordeste brasileiro. Rev Bras Ginecol Obstet. 2009; 31(1):22-7.
15. Morley G, Hopkins M, Lindenauer S, et al. Pelvic exenteration, University of Michigan: 100 patients at 5 years. Obstet Gynecol. 1989; 74:934-43.
16. Rutledge F, Smith J, Wharton J, et al. Pelvic exenteration: analysis of 296 patients. Am. J Obstet Gynecol. 1977; 129:881-92.
17. Sharma S, Odunsi K, Driscoll D, et al. Pelvic exenteration for gynecological malignancies: twenty-year experience at Rosewell Park Cancer Institute. Int J Gynecol Cancer. 2005; 15:475-82.
18. Shingelton H, Soong S, Gelder M, et al. Clinical and histopathologic factors predicting recurrence and survival after pelvic exenteration for cancer of the cervix. Obstet Gynecol. 1989; 73:1027-34.
19. Redondo A, Castelo B, Gómez C. Cáncer de vulva y vagina. En: Cortés-Funes H, Colomer R (Eds.) Tratado de Oncología. 2ª Ed. Barcelona: P. Permanyer; 2009. [Edición en CD-ROM].
20. Roos E, de Graeff A, van Eijkeren M, et al. Quality of live after pelvic exenteration. Gynecol Oncol. 2004; 93:610-14.
21. Ferenschild FTJ, Vermaas M, Verhoef C, Ansink AC, Kirkels WJ, Eggermont AMM, de Wilt JHW. Total Pelvic Exenteration for Primary and Recurrent Malignancies. World J Surg. 2009; 33:1502-08.
22. Fotopoulou C, Neumann U, Kraetschell R, Schefold JC, Weidemann H, Werner L., Sehouli J. Long?Term Clinical Outcome of Pelvic Exenteration in Patients with Advanced Gynecological Malignancies. Journal Surg Oncol. 2010; 101:507-12.
23. Forner DM, Lampe B. Intestinal Complication after Pelvic Exenterations in Gynecologic Oncology. Int J Gynecol Cancer. 2009; 19:958-62.
24. Moore K, Gold M, McMeekin D, et al. Vesicovaginal fistula formation in patients with stage IVA cervical cancer. Gynecol Oncol.2007; 106:498-501.
25. Morris M, Eifel P, Lu J, et al. Pelvic radiation with concurrent chemotherapy compared with pelvic and para-aortic radiation for high-risk cervical cancer. N Engl J Med. 1999; 340:1137-43.
26. López H, Morales F, Ochoa E, Ochoa P, Ruiz J. Major complications following exenteration in cases of pelvic malignancy: an 18-year experience. BMC Cancer. 2007; 7(Suppl 1):A37.
27. Park JY, Choi HJ, Jeong SY, Chung J, Park JK, Park SY. The Role of Pelvic Exenteration and Reconstruction for Treatment of Advanced or Recurrent Gynecologic Malignancies: Analysis of Risk Factors Predicting Recurrence and Survival. Journal of Surgical Oncology. 2007; 96:560-68.
28. Höckel M, Dornhöfer K. Pelvic exenterations for gynecological tumours: achievements and unanswered questions. Lancet Oncol. 2006;7:837-47.
29. Höckel M. Laterally extended endopelvic resection—novel surgical treatment of locally recurrent cervical carcinoma involving the pelvic side wall. Gynecol Oncol. 2003; 91:369-77.
30. Robertson G, Lopes A, Beynon G, Monaghan J. Pelvic exenteration: a review of the Gateshead experience 1974_1992. Br J Obstet Gynecol. 1994; 101:529-31.
Recibido: 3 de junio de 2013
Aprobado: 20 de septiembre de 2013