INTRODUCCIÓN
La biotecnología ha tenido en los últimos años un gran impacto en el área de producción de edulcorantes, no solo desde el punto de vista tecnológico sino también en lo económico y social. En la actualidad existen diferentes tipos, algunos de estos se encuentran de forma natural en los alimentos, tal es el caso de la sacarosa. Este disacárido se agrega a diferentes tipos de alimentos, bebidas y jarabes.
La sacarosa es el azúcar de mesa que se obtiene de la caña y de la remolacha y es el compuesto orgánico de mayor producción en forma pura (Cortés y col., 2020 a).
La glucosa es una aldohexosa, fuente de energía en el metabolismo del ser humano y precursor metabólico de prácticamente todos los azúcares, incluyendo los amino azúcares. Puede ser convertida en fructosa potenciando su capacidad edulcorante.
La fructuosa es el azúcar más dulce de los edulcorantes naturales que unido a su gran estabilidad en alimentos ácidos y bebidas, constituye una alternativa atractiva al empleo de la sacarosa. De acuerdo a estas propiedades alcanza una gran aplicabilidad en la elaboración de dulces y bebidas refrescantes. Mientras que la glucosa, con un poder edulcorante menor que la sacarosa, tiene un amplio mercado en la industria química, farmacéutica y alimentaria, constituyendo una fuente de materia prima fundamental para otras producciones.
A nivel global una de las principales fuentes de obtención de glucosa es a partir del azúcar refino, al igual que el almidón de maíz como sustratos más utilizados; donde la inversión se logra a partir de la acción de un ácido a temperatura elevada, por intercambio iónico o por la presencia de la enzima invertasa (Díaz y col., 2020).
En la UEB Derivados Chiquitico Fabregat existe una planta productora de glucosa y fructosa a partir de la inversión ácida de la sacarosa. La glucosa obtenida en dicha planta es empleada como materia prima en la obtención de sorbitol. El empleo de este método de inversión unido con deficiencias operacionales y tecnológicas, ha ocasionado que los niveles productivos de glucosa anuales son insuficientes para satisfacer la demanda actual de este producto (Cortés y col., 2020 b), (Acosta, 2021).
Resultados obtenidos con el empleo de la hidrólisis enzimática de la sacarosa demuestran un aumento del rendimiento del proceso en comparación al reportado con la utilización de un ácido (Cortés y col., 2020 a), además de ofrecer otras ventajas como: mayor estabilidad química y microbiológica de la glucosa; y la eliminación de los procesos corrosivos, los productos coloreados y la generación de cenizas.
El CIGB de Sancti Spíritus en Cuba, desarrolló un biocatalizador de enzima invertasa recombinante termoestable, a partir de la expresión consecutiva a altos niveles en Pichia Pastoris de un gen con uso de codones optimizados que codifica la invertasa de Thermotoga marítima (BfrA) (Menéndez y col., 2014).
Para el empleo de esta enzima recombinante termoestable en la producción de glucosa, Cortés (2021) determinó las condiciones operacionales óptimas para la inversión en operación sumergida a escala de laboratorio con resultados satisfactorios para la operación de hidrólisis. De acuerdo a estos resultados, la implementación de una tecnología enzimática capaz de operar a elevadas temperaturas con una termoestabilidad que permita la hidrólisis de soluciones concentradas de sacarosa, constituye una alternativa novedosa desde el punto de vista técnico-económico.
Teniendo en cuenta estos antecedentes, el objetivo del presente trabajo es realizar un análisis comparativo de los métodos de producción de glucosa por hidrólisis ácida y enzimática de la sacarosa, considerando la tecnología instalada en la UEB Derivados Chiquitico Fabregat y la concepción tecnológica para la operación que emplea el biocatalizador.
MATERIALES Y MÉTODOS
Balances de masa y energía en el proceso por hidrólisis ácida de la sacarosa
Para la cuantificación de las corrientes que intervienen en cada una de las etapas del proceso, se tuvo en cuenta la tecnología instalada (Gómez, 2015) y la secuencia operacional que garantiza el flujo productivo. Se estructuró el proceso en seis etapas en correspondencia a lo establecido por Acosta (2021): disolución e inversión, primera cristalización, filtración, disolución de la torta, segunda cristalización y centrifugación.
Se estableció como base de cálculo el procesamiento de 22 500 kg de azúcar refino correspondientes a un ciclo de operación. Los datos de las corrientes fueron obtenidos en la práctica productiva y a través de las especificaciones de los manuales operacionales.
Estudio cinético del biocatalizador en un reactor tipo tanque agitado
Se emplearon los resultados de los estudios realizados con el biocatalizador de enzima invertasa termoestable ofertado por el CIGB de Sancti Spíritus. Se obtuvieron datos de la concentración de azúcares reductores totales presentes en el medio en el trascurso del tiempo para evaluar el avance de la reacción, según los experimentos desarrollados por (Cortés, 2021). El estudio se realizó en un volumen de trabajo de 500 mL, un pH ajustado a 5,5, velocidad de agitación de 200 rpm, una temperatura de 86 °C y en las condiciones óptimas de concentración de sustrato (Azúcar refino A) y concentración de enzima, para un valor de 75ºBrix y 28 U/g refino respectivamente.
Se evaluó el ajuste a una ecuación que describa su comportamiento cinético según los modelos descritos por Michaelis - Menten y para el caso de una reacción monomelecular irreversible de primer orden.
De la aproximación de estado causi-estacionario de Michaelis - Menten (Ismail y col., 2017) se obtuvo que la velocidad de reacción a la que se forma el producto, integrando en las condiciones límites CS= CS0 para t=0 y arreglando, representa un relación lineal de pendiente negativa como se muestra en la ecuación (1).
Donde: Vmáx es la velocidad máxima de reacción (mol/Lh); CS es la concentración de sustrato (mol/L); CS0 es la concentración de sustrato inicial (mol/L); km es la constante de Michaelis-Menten (mol/L) y t es el tiempo de reacción (h).
Se ensayó la ecuación cinética para reacciones monomoleculares irreversibles de primer orden (Viera, 2007), donde para un sistema de densidad constante se obtiene la relación lineal que se representa en la ecuación (2).
Donde: XA es la conversión del sustrato en fracción, t es el tiempo de reacción (h) y k es la k constante cinética de la reacción (h-1).
Balance de masa y energía para el desarrollo de la hidrólisis enzimática de la sacarosa
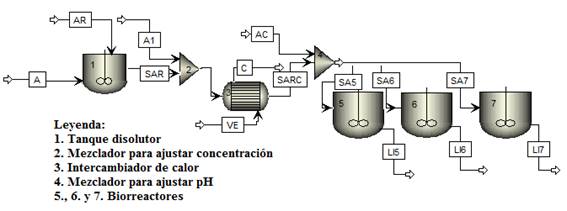
Las evaluaciones de la hidrólisis enzimática a escala industrial se realizaron para las capacidades instaladas y la disponibilidad de tres biorreactores de 10 m3 con un volumen de trabajo de 7,51 m3, para los cuales se determinaron los consumos asociados mediante balances de materiales y energía. En la concepción tecnológica de esta etapa se tuvo en cuenta, al igual que para el empleo de esta enzima inmovilizada (PpABfrA) (Acosta y col., 2022), la inserción de un tanque disolutor y un intercambiador de calor, que garanticen los parámetros operacionales en el reactor. El diagrama de flujo concebido se muestra en la figura 1, donde A y A1, indican corrientes de agua; AR, azúcar refino; SAR, solución de azúcar refino; VE, vapor de escape; C, condensado; SAR, solución de azúcar refino caliente; AC, ácido clorhídrico; SA5, SA6 y SA7, soluciones alimentadas a los biorreactores y LI5, LI6 y LI7, licor invertido que se obtiene en la salida de los biorreactores.
Se asumió como base de cálculo un ciclo de inversión como criterio comparativo con el método de hidrólisis ácida. Se tuvo en cuenta además igual concentración y temperatura en el medio de reacción, dadas las características termoactivas y termosestables de la enzima.
En el balance energético para elevar la temperatura del sustrato desde 30 °C hasta 86 °C (Espinosa y col., 2019; Núñez y col., 2020), se determinó la demanda de vapor de escape (Mv) como medio de calentamiento a 113 ºC y 156 040,5 Pa.
Con la concentración de enzima óptima con que se trabajó en el estudio cinético (28 U/grefino) y una actividad reportada de 400 U/ mLenzima, se determinó el volumen de biocatalizador requerido para cada biorreactor.
A partir de la concentración molar de la sacarosa en el medio, se determinó la concentración de glucosa generada para la conversión reportada en el estudio cinético (XA) y por tanto la masa de acuerdo a su peso molecular.
Escalado de la reacción de hidrólisis enzimática de la sacarosa y diseño del sistema de disolución
En base a los estudios experimentales desarrollados, se realizó la propuesta de escalado a un volumen piloto de 0,0536 m3 y para la inversión de un volumen de solución de sacarosa de 7,51 m3 en cada biorreactor industrial. Se consideraron las relaciones de escalado aplicadas por Martínez y col., (2017) y Acosta y col., (2022) para el desarrollo de la reacción biocatalítica de esta enzima inmovilizada (PpABfrA), garantizando la similitud geométrica, química e igual velocidad en la punta del impulsor.
En el diseño de la chaqueta para la circulación del medio de intercambio con régimen de flujo en mezcla perfecta, que permite mantener las condiciones isotérmicas en el reactor, se calculó el calor de reacción mediante el modelo de Kirchoff (Matos y Hing, 2014) a una temperatura constante de 86 ºC según el procedimiento aplicado por Pérez y col., (2022) adecuado a las sustancias participantes. Además, se tuvo en cuenta la constante cinética determinada para las condiciones ensayadas. La determinación de los coeficientes de transferencia de calor y el área requerida se realizó por la metodología reportada para sistemas con estas características (Viera, 2007), (Espinosa y col., 2019).
El sistema de disolución que garantiza la alimentación al sistema de reacción de la solución de sacarosa a una concentración de 75ºBrix, se diseñó en función de las características del fluido y los criterios establecidos por Kasatkin, (1985).
Indicadores de consumo y generación anuales para ambos métodos de hidrólisis
Para la valoración anual de los indicadores de consumo de la etapa de hidrólisis y la generación de productos del proceso por ambos métodos, se tuvo en cuenta un periodo anual laborable de 330 días, donde se realizan por hidrólisis ácida un total de 165 ciclos con una inversión cada uno. Para la tecnología propuesta se concibió el mismo número de ciclos con la sustitución del método de inversión y preparación de la materia prima.
Se consideró en este análisis el consumo de potencia eléctrica para la tecnología instalada, y se determinó dichos requerimientos para la agitación y bombeo en la preparación del sustrato para la hidrólisis enzimática.
RESULTADOS Y DISCUSIÓN
Cuantificación de las corrientes del proceso por hidrólisis ácida de la sacarosa
En la Tabla 1 se muestran los resultados del balance de masa y energía en cada una de las etapas del proceso de producción de glucosa por hidrólisis ácida de la sacarosa para un ciclo de inversión.
Tabla 1 Resultados de los balances de masa y energía del proceso de producción de glucosa por hidrólisis ácida
| Etapas | Corriente | Valor | |
|---|---|---|---|
| Identificación | Comentario | ||
| Disolución e inversión | SlnAR (kg) | Solución de azúcar refino | 29 191 |
| VH2O (m3) | Volumen de agua consumido en la disolución | 6,80 | |
| Q (J) | Calor intercambiado | 3,94*109 | |
| Mv (kg) | Vapor consumido | 1 962,27 | |
| VH3PO4(m3) | Volumen de ácido consumido | 0,014 | |
| SI (kg) | Sirope invertido | 29 215,14 | |
| Primera Cristalización | MC1 (kg) | Masa cristalizada | 32 786,24 |
| SG (kg) | Sirope de glucosa recirculado | 2 554,73 | |
| SE1 (kg) | Pie de semilla | 1 016,37 | |
| Filtración | SF (kg) | Sirope rico en fructosa generado | 26 550 |
| TG (kg) | Torta de glucosa | 6 236,24 | |
| Disolución de la torta | TG(D) (kg) | Torta de glucosa disuelta | 6 564,46 |
| VH2O (m3) | Volumen de agua consumido en la disolución | 0,32 | |
| Q (J) | Calor intercambiado | 7,48*108 | |
| Mv (kg) | Vapor consumido | 372,46 | |
| Segunda cristalización | MC2 (kg) | Masa cristalizada | 6 520 |
| SE2 (kg) | Pie de semilla | 69,77 | |
| Centrifugación | G (kg) | Glucosa producida | 5 253,40 |
| VH2O (m3) | Volumen de agua consumido en la centrifugación | 1,29 | |
En los valores calculados se reportan bajos rendimientos de glucosa para un elevado consumo de azúcar refino, de acuerdo a lo plantado por (Cortés y col., 2020a) para este método de operación. Este indicador a su vez está influenciado por la existencia de zonas muertas en el reactor, que ocasiona dificultades para lograr la homogenización del medio. Por otra parte, la operación con soluciones ácidas acelera los procesos corrosivos en el equipamiento instalado y la generación de productos ácidos que afectan la calidad de la glucosa obtenida. En base a estos planteamientos, se recurre al estudio del empleo de la hidrólisis enzimática de la sacarosa teniendo en cuenta los resultados reportados al efecto (Cortés, 2021); (Acosta y col., 2022).
Parámetros cinéticos de la reacción de hidrólisis enzimática de la sacarosa
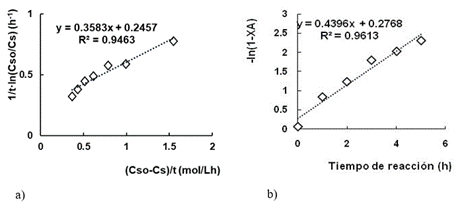
En la figura 2 se representan las relaciones de las ecuaciones (1) y (2) a partir de los datos experimentales reportados (Cortés, 2021).
a) Relación lineal para la determinación de los parámetros del modelo de Michaelis-Menten;
b) Ensayo de la reacción de primer orden
En la representación a) se muestra una recta de pendiente positiva, por lo que a partir de la misma no es posible obtener el modelo que describe el comportamiento de los datos en el tiempo de estudio.
Para un ajuste adecuado en la predicción del tiempo de hidrólisis a concentraciones iniciales de sacarosa de 75ºBrix, en la representación b) se obtiene una recta que pasa por el origen cuya pendiente se corresponde con el valor de k. Del gráfico se obtiene que la constante cinética k= 0,44 h-1, con un coeficiente de regresión (R2) igual a 96,13 %. Para este valor, se verifica a las 4 horas de reacción una concentración de sacarosa remanente de 168,21 g/L para un 84 % de hidrólisis, lo que no representa una diferencia significativa respecto a 86,79 % que se reporta experimentalmente para el mismo tiempo (Cortés, 2021). Cabe desatacar, que al igual que el comportamiento anterior, se registró el ajuste a una cinética de reacción de primer orden con el empleo del biocatalizador PpABfrA en soluciones concentradas de sacarosa (Martínez y col., 2015). Este parámetro cinético determinado fue empleado en la determinación del régimen de transferencia que calor que permite mantener la temperatura constante en el medio de reacción (Pérez, 2018).
Cuantificación de las corrientes de la etapa de hidrólisis enzimática de la sacarosa
En la tabla 2 se muestran los resultados del balance de masa y energía en las etapas de preparación del sustrato e hidrólisis enzimática para un ciclo de inversión.
Tabla 2 Resultados de los balances de masa y energía en las etapas de preparación del sustrato e hidrólisis enzimática
| Corriente | Valor | ||
|---|---|---|---|
| Identificación | Comentario | 1 biorreactor | 3 biorreactores |
| AR (kg) | Azúcar refino | 7 241,64 | 21 724,92 |
| SlnAR (kg) | Solución de azúcar refino | 9 408 | 28 224 |
| VH2O (m3) | Volumen de agua consumido en la disolución | 2,16 | 6,48 |
| Venzima (m3) | Volumen de enzima | 0,51 | 1,53 |
| G (kg) | Glucosa generada | 3 199,39 | 9 598,17 |
| SF (kg) | Sirope rico en fructosa generado | 7 418,88 | 22 25/6,64 |
| Q (J) | Calor intercambiado en el calentador | 1,47*109 | 4,41*109 |
| Mv (kg) | Vapor consumido | 731,34 | 2 194,03 |
Los valores de las corrientes de la tabla 2 indican que esta tecnología es más exigente en cuanto a requerimiento auxiliar de vapor, lo que unido al volumen de enzima demandado, significa un incremento del costo operacional del proceso. Sin embargo, la especificidad de este biocatalizador por el sustrato (Mendoza y col., 2021), genera un elevado rendimiento de glucosa en la operación de hidrólisis.
Parámetros de diseño de los biorreactores y el sistema de disolución
En la tabla 3 se muestran las características de diseño y los parámetros operacionales de los biorreactores en las distintas escalas. La determinación de las consecuencias se realizó a través del cálculo teórico de cada uno de los parámetros para una densidad (ρ) de 1344 kg/m3 y una viscosidad (μ) igual a 0,046 Pa.s.
Tabla 3 Características de diseño y parámetros operacionales de los biorreactores experimental, piloto e industrial
| Características | Experimental | Piloto | Industrial |
|---|---|---|---|
| Diámetro del impelente (m) | 0,04 | 0,19 | 1 |
| Diámetro del biorreactor (m) | 0,10 | 0,63 | 3,33 |
| Altura del impelente (m) | 0,02 | 0,09 | 0,50 |
| Volumen total (m3) | 0,00065 | 0,07 | 10,00 |
| Volumen de trabajo (m3) | 0,0005 | 0,0536 | 7,51 |
| Tipo de impelente | hélice | hélice | hélice |
| Velocidad de agitación (rpm) | 200 | 42,1 | 8,11 |
| Número de Reynold | 156 | 741,16 | 3848,49 |
| Potencia (W) | 0,003 | 0,06 | 1,23 |
| Potencia por unidad de volumen (W/m3) | 6 | 1,26 | 0,25 |
La entalpía de hidrólisis a una temperatura de trabajo de 86 ºC arrojó un valor de 106,98 kJ/mol. Este resultado muestra que la reacción se desarrolla sin efectos energéticos apreciables, pero con un comportamiento ligeramente endotérmico.
En la tabla 4 se muestran los resultados de la determinación de la demanda de transferencia de calor. Para el intercambio energético necesario, se calculó un área de transferencia de 18 m2 inferior a 21 m2 de superficie lateral que presentan los biorreactores.
Tabla 4 Resultados de la determinación de los requerimientos de transferencia de calor en la hidrólisis enzimática de la sacarosa
| Parámetros calculados | Resultados |
|---|---|
| Coeficiente pelicular de transferencia de calor (J/s m2 ºC) | 77,97 |
| Coeficiente pelicular de transferencia de calor referido al diámetro exterior (J/s m2 ºC) | 76,41 |
| Coeficiente total de transferencia de calor limpio (J/s m2 ºC) | 38,60 |
| Coeficiente total de transferencia de calor sucio (J/s m2 ºC) | 38,10 |
| Área de transferencia de calor (m2) | 18 |
| Calor intercambiado (J/s) | 950 |
| Temperatura de entrada del medio (ºC) | 90 |
| Temperatura de salida del medio (ºC) | 87 |
Un tanque agitado con un volumen de trabajo de 3,5 m3, un diámetro de 1,6 m y agitador de hélice de 0,4 m de diámetro, garantiza la obtención de una solución concentrada de sacarosa (75 ºBx) que se alimenta al sistema de reacción. Establecido un régimen turbulento de mezclado (Re) de 4 000, la velocidad de agitación requerida según la ecuación es de 692 rpm, con un consumo de potencia de 7,08 kW para un Kn correspondiente de 0,3.
Indicadores de consumo y generación comparativos de las etapas de hidrólisis ácida y enzimática de la sacarosa
En la tabla 5 se muestran principales consumos anuales de la etapa de hidrólisis y los productos que se generan por ambos métodos.
Tabla 5 Resumen de los principales consumos anuales de las etapas de hidrólisis ácida y enzimática y los productos generados en el proceso
| Indicadores de consumo y generación | Hidrólisis ácida | Hidrólisis enzimática | |
|---|---|---|---|
| Materias primas | Azúcar refino (t) | 3712,00 | 3583,80 |
| Materiales | Ácido fosfórico (t) | 3,89 | - |
| Biocatalizador (m3) | - | 252,45 | |
| Requerimientos | Agua* (m3) | 1 122,30 | 1 069,20 |
| Vapor (t) | 323,40 | 361,35 | |
| Electricidad (kWh) | 32 914,20 | 28 632,00 | |
| Productos generados | Sirope rico en fructosa (t) | 4 380,75 | 3 672,90 |
| Glucosa (t) | 866,75 | 1 583,69 | |
* Incluye agua para la disolución del azúcar refino
En un análisis comparativo de los resultados de la tabla 5, se puede apreciar que la producción anual de glucosa enzimática supera en 1,83 veces a la producción de la glucosa ácida. Aunque con una disminución de la masa de sirope rico en fructosa generado, la producción total de ambos productos por la vía enzimática supera al del empleo de un ácido, lo que se traduce en igual diferencia del valor de la producción.
La demanda de biocatalizador sin posibilidad de reúso influye considerablemente en los costos totales de esta variante, sin embargo, los elevados rendimientos en glucosa, garantizan un costo unitario inferior al de la tecnología instalada, según los resultados obtenidos por Gómez y col., (2017) con el empleo del biocatalizador invertasa-quitosana: quitina-carboximetilcelulosa.
CONCLUSIONES
El desarrollo de los balances de masa y energía para la tecnología instalada en la UEB Derivados Chiquitico Fabregat y la propuesta de implementación de la hidrólisis enzimática de la sacarosa, permite establecer criterios comparativos y decisivos sobre los procesos productivos e inversionistas.
En el empleo de la hidrólisis enzimática de la sacarosa se alcanza un elevado porciento de inversión con la enzima invertasa termoestable, donde los datos experimentales se ajustan a la cinética de una reacción irreversible de primer orden.
El análisis comparativo a través del estudio cinético y los parámetros operacionales a escala industrial para la operación de hidrólisis enzimática y las tecnologías asociadas a la preparación del sustrato, arroja resultados alentadores para el empleo de este método, donde el incremento de la producción de glucosa para igual número de ciclos y la sustitución de sustancias agresivas, garantizan la factibilidad técnica, económica y ambiental del proceso.