INTRODUCCIÓN
La significación clínica de los marcadores de riesgo electrocardiográficos puede ser probada o desaprobada en base a su reproducibilidad y su verdadero vínculo a importantes situaciones o variables clínicas. Los intentos por reforzar su significación clínica son explicados por mecanismos electrofisiológicos, por ejemplo, en artículos científicos que estudian el electrocardiograma (ECG). 1 La dispersión de ondas e intervalos del ECG (Onda P, onda QRS, intervalos QT y JT), han sido ampliamente estudiadas en la literatura como herramienta útil en la predicción de fibrilación atrial (dispersión de la onda P) y arritmias ventriculares asociadas a muerte súbita (intervalo QT y su dispersión). Pero estas variables han sido aceptadas o no en dependencia de los defensores o detractores. Los defensores de estos temas plantean la asociación de ellas a eventos clínicos relacionados; los detractores plantean que estos fenómenos de dispersión ocurren porque el ECG de 12 derivaciones siempre encontrará dispersiones en sus ondas o segmentos, pues es el resultado de vectores en diferentes puntos de la superficie del cuerpo. 2
Una simple búsqueda en la Web of Science, muestra artículos relacionados con el intervalo QT medido y su dispersión en diferentes escenarios clínicos, relacionándolo siempre, en todos ellos, con eventos adversos. El intervalo QT es la suma matemática del complejo QRS y el intervalo JT. Durrer et al., en 1970, después que revisaron varios estudios consideraron que el conocimiento de la distribución instantánea de la despolarización (QRS del ECG) es de gran valor para entender lo que sucede con el QRS. 3 Existe una disincronía electromecánica normal, se ha descrito que el registro del QRS aparecía de 0 ms a 15 ms luego del inicio de la activación del VI y que el ápex se despolariza “relativamente tarde” respecto a otras regiones del miocardio. La activación del endocardio del VI se completó de 29 ms a 52 ms (promedio 43 ms), lo que representa sólo el 41 % de la duración del complejo QRS en el ECG de superficie. 4-6
Estos hallazgos determinaron las bases para explicar por qué en unas derivaciones electrocardiográficas el complejo QRS tiene mayor duración que en otras. 5,7
Los estudios del intervalo QT comenzaron mucho antes, desde 1920, cuando Bazett describe la fórmula para calcularlo de forma corregida. 8 Quizás la relación en el tiempo para Bazett en 1920 y Durrer en 1970, permitió que el intervalo QT fuera más ampliamente estudiado y que en la actualidad cuente con muchos más seguidores que justifican su continuo estudio como variable de riesgo de muerte súbita en diferentes escenarios clínicos 9,10 y existan entonces muchas más referencias sobre el intervalo QT, que sobre el complejo QRS. Fue 14 años después que Cassidy et al. 11) realizaron un mapa de despolarización endocárdica de VI.
Actualmente ha comenzado a estudiarse la variable dQRS, incluso separando en el intervalo QT la despolarización (QRS) de la repolarización (intervalo JT); Ferrer Orozco L et al, demostraron que los incrementos del intervalo QT en los hipertensos estudiados dependían de los incrementos del QRS y no del JT; 12 lo cual, en ese estudio, da mayor implicación a la despolarización que a la repolarización. Chávez González et al. demostraron una mayor asociación de arritmias ventriculares malignas en la cardiopatía isquémica aguda a los incrementos de la dQRS que del intervalo y dispersión del QT. 13 La morfología de BRIHH ha sido asociada a disincronía y puede ser tomada como variable predictora de respuesta satisfactoria a la terapia de resincronización cardiaca. 14-17
La estimulación desde punta de ventrículo derecho (VD) genera un BRIHH que dicho bloqueo ocasiona un estrés parietal importante trastornando la contractilidad miocárdica y ocasiona disincronía mecánica. En la década de los ochenta comenzaron a describirse algunos efectos nocivos de la estimulación en el ápex de VD. 18-21 El estudio DAVID, demostró que en pacientes con indicación de desfibrilador implantable y fracción de eyección del VI de 40 % (en ausencia de indicación de estimulación antibradicardia), los asignados aleatoriamente a estimulación DDDR (doble cámara, aurícula y ventrículo derecho) con frecuencia mínima de 70 lpm tuvieron peor evolución clínica (objetivo combinado de muerte u hospitalización por insuficiencia cardíaca) que los asignados a estimulación VVIR (unicameral, solo en punta de VD) con frecuencia mínima de 40 lpm. 22 Un subestudio del estudio MOST (trabajo que comparó la estimulación DDDR con la VVIR en pacientes con disfunción sinusal) se analizó la relación entre proporción de latidos con estimulación ventricular y hospitalización por insuficiencia cardíaca o aparición de fibrilación auricular. 23 Se encontró una relación significativa en ambos casos, de forma que, independientemente del modo de estimulación (ya fuera DDDR o VVIR), una proporción elevada de latidos estimulados era un fuerte predictor de deterioro de la función ventricular izquierda. 23,24
La presencia de BRIHH, con depresión de la FEVI, ha convertido al BRIHH en blanco de estudio para la resincronización cardiaca, dentro de estos estudios, ha sido ampliamente investigada la duración y morfología del QRS. 14-17
Los estudios para determinar, en diferentes condiciones clínicas y terapéuticas, el uso de la variable dispersión del QRS (dQRS) relacionada a esa disincronía electromecánica, no son amplios en el mundo, no encontramos en la literatura revisada referencias al respecto. La dQRS ha sido evaluada en el BRIHH, insuficiencia cardiaca congestiva, resincronización cardíaca, displasia arritmogénica de ventrículo derecho. Sin embargo, en algunas de esas situaciones existen discrepancias en los resultados. 25 Cabe señalar también que no se encontró en la literatura revisada estudios sobre dQRS en el BRIHH inducido por la estimulación cardiaca permanente desde la punta de VD, ni desde la región septal interventricular alta; como tampoco estudios relacionando la variable dQRS con la disincronía o sincronía inter e intraventricular en pacientes que reciben terapia de resincronización cardiaca.
Basado en la idea anterior de la falta de estos estudios, nos hemos propuesto demostrar la relación entre la dispersión del QRS calculada desde el electrocardiograma con la sincronía o disincronía mecánica del corazón evaluada por ecocardiograma, en pacientes que recibieron estimulación eléctrica permanente desde diferentes sitios cardiacos. Dentro de la investigación se seleccionan 3 grupos de estudio independientes:
Grupo 1: Selección y estudio de los pacientes estimulados en punta de ventrículo derecho.
Grupo 2: Selección y estudio de los pacientes con estimulación en punta de ventrículo derecho que evolucionaron a disfunción contráctil de ventrículo izquierdo y fueron llevados a estimulación en región septal alta o parahisiana.
Grupo 3: Selección y estudio de los pacientes sometidos a estimulación biventricular (terapia de resincronización cardiaca).
MÉTODOS
Se brinda una descripción y fundamentación de la población de estudio y de la muestra, así como la tecnología utilizada. En los 3 grupos se realizó un estudio descriptivo longitudinal y prospectivo.
Población de estudio
Se seleccionaron los pacientes según los 3 grupos estudiados.
Primer grupo: pacientes estimulados en punta de ventrículo derecho
Se estudiaron 82 pacientes que requirieron implantación de un marcapasos permanente atendidos en el servicio de electrofisiología del cardiocentro Ernesto Guevara de Santa Clara durante el año 2014. Todos recibieron implante del electrodo ventricular en punta de ventrículo derecho.
Criterios de inclusión: Pacientes con indicación de primo implante de marcapasos en cualquier modalidad de estimulación, que antes del implante del dispositivo presentaron una FEVI ≥ 50 %. Al considerar, que el estudio fue realizado en un solo centro y la muestra puede ser considerada pequeña, pues decidimos incluir 12 pacientes con fibrilación atrial crónica, que no tenían asociada otra cardiopatía (valvular, miocárdica o isquémica) y que en el momento de la decisión del implante la geometría ventricular y la FEVI eran normales.
Criterios de exclusión:
pacientes con antecedentes de cardiopatía isquémica conocida;
pacientes que una vez implantado el dispositivo se diagnostique cardiopatía isquémica;
pacientes con enfermedad renal crónica, diabetes mellitus y valvulopatía preexistente u otra cardiopatía estructural;
pacientes con antecedentes de etilismo crónico;
pacientes con tratamiento quimioterpéutico y radioterapéutico previo;
pacientes con exposición a sustancias cardiotóxicas como metales pesados;
pacientes con tratamiento con fármacos antirretrovirales;
pacientes con antecedentes de enfermedades infiltrativas;
pacientes con implante de un cardiorresincronizador;
pacientes con cirugías cardiacas correctivas de cardiopatías congénitas o valvulares.
Seguimiento programación de marcapasos: Un mes después del implante (momento del seguimiento en el que no se toman variables de estudio), 3, 6, 12 y 24 meses posteriores al implante. En cada uno de esos seguimientos se tomaron variables para ser estudiadas.
Segundo grupo: pacientes para estimulación en región septal alta.
Segundo grupo: pacientes para estimulación en región septal alta
Muestra de estudio. Criterios de inclusión y salida
De una población de 27 pacientes, la muestra quedó conformada por 24 pacientes tras criterios de inclusión y de salida, 22 varones y 2 mujeres, con rango de edad entre 40 años y 65 años, promedio de 53 años ± 5,1 años, de raza blanca y sin comorbilidades descritas en sus antecedentes personales, con FEVI previa al primoimplante (estimulación en punta de VD, la cual lleva a la disfunción sistólica) del marcapasos de 59,2 % ± 5,8 % y un volumen latido de 115,78 mL ± 37,4 mL. En estos pacientes se decidió la estimulación paraseptal alta, que cumplieran los siguientes criterios de inclusión y salida.
Criterios de inclusión:
pacientes con disfunción sistólica secundaria a la estimulación en punta de VD.
que presenten previo a la estimulación en punta de VD un electrocardiograma con QRS estrecho;
que presenten previo a la estimulación en punta de VD una fracción de eyección del ventrículo izquierdo conservada;
que el porciento de estimulación tanto en punta de VD como en región paraseptal alta sea ≥ 90 %.
Criterios de salida:
personas que abandonan el estudio;
personas que fallecen;
desplazamiento del electrodo o aumentos muy exagerados de los umbrales a nivel del septum interventricular alto que obliguen a tomar otra conducta terapéutica en cuanto a los sitios de estimulación.
Al culminar el implante, se programó un voltaje de estimulación en 7 V y frecuencia de 80 latidos por minuto, con el fin de asegurar la estimulación el mayor tiempo posible y garantizar un por ciento de estimulación ≥ 90 %.
Seguimiento: Semanal durante 2 meses y mensual hasta los primeros 6 meses del implante. Se les realizó ecocardiograma a los 3 meses y 6 meses.
Tercer grupo: pacientes sometidos a estimulación biventricular (terapia de resincronización cardiaca).
Tercer grupo: pacientes sometidos a estimulación biventricular (terapia de resincronización cardiaca)
Muestra de estudio. Criterios de inclusión y exclusión
Se realizó el estudio con 19 pacientes, de un total de 23, que recibieron dispositivo para TRC en el Cardiocentro Ernesto Guevara de Santa Clara, Cuba, entre enero de 2010 y junio de 2014. El período mínimo de seguimiento fue de 11 meses.
Criterios de inclusión:
pacientes con bloqueo de rama izquierda y QRS > 120 ms (milisegundos) y ritmo sinusal;
FEVI ≤ 35 %;
no evidencias de hipertensión pulmonar, descartada por ecocardiografía;
arterias coronarias epicárdicas angiográficamente sin lesiones ateroscleróticas;
no evidencias clínicas al interrogatorio de cardiopatía isquémica;
electrodo de seno coronario colocado en la vena lateral izquierda;
clase funcional II-IV según la Asociación del Corazón de Nueva York (NYHA, por sus siglas en inglés), con tratamiento ambulatorio;
ausencia de respuesta al tratamiento farmacológico óptimo.
Exclusión:
TRC con fibrilación atrial crónica y cardiopatía isquémica demostrada: 1
Muerte por descompensación cardíaca: 1
Electrodo del VI no ubicado en la vena lateral: 2
Seguimiento: A la semana, 1 mes, 3 meses y 6 meses después de implantado el dispositivo.
Recogida de los datos
Para la recogida de datos se tuvo en consideración la aprobación con el consentimiento informado de cada paciente implicado a participar en la investigación, así como la aprobación por parte de los comités de ética de las instituciones implicadas en el estudio. Se cumplió con los requisitos de estudios en humanos aprobados en el acuerdo de Helsinski. 26
Variables del estudio
Variables utilizadas en los 3 grupos de estudios
Variables electrocardiográficas: A todos los pacientes se les realizó ECG de superficie de 12 derivaciones, con un equipo Nyhom Kodem, estandarizando para una velocidad del papel milimetrado de 25 mm/sec y 10 mm de altura se consideró 1 milivolt (mv).
Variable anchura máxima del QRS: El QRS fue medido manualmente por 2 observadores, con velocidad de registro del ECG: 25 mm por segundo; amplitud: 10 mm por mV. Se consideró QRS desde el inicio de la onda q o R hasta el punto J en el inicio del segmento ST.
Anchura máxima del QRS: duración máxima del complejo QRS, en las 12 derivaciones del ECG.
Anchura mínima del QRS: duración mínima del complejo QRS, en las 12 derivaciones del ECG.
Dispersión del QRS (dQRS): diferencia entre el mayor y el menor valor del QRS medido en el ECG de 12 derivaciones
Variables ecocardiográficas: Para obtener las imágenes ecocardiográficas, se utilizó un equipo Aloka 5000, con un transductor de 3,5 MHrz, que fue colocado en el tórax, comenzando por el área paraesternal.
Conceptualización: Según parámetro de la función sistólica obtenido mediante el método de Simpson modificado. 26
Diámetro telediastólico del VI.
Diámetro telesistólico del VI.
Disincronía intraventricular: Retraso del septo de pared posterior: en modo M y eje largo paraesternal, perpendicular a los segmentos basales, se mide desde el pico de la contracción sistólica del septum hasta el de la pared posterior. Se consideró asincronía un valor ≥ 60 ms 27) por ecocardiograma en la vista de 4 cámaras apical.
Disincronía interventricular: Retraso mecánico interventricular: diferencias entre los periodos eyectivos de ambos ventrículos; se mide desde el inicio del QRS hasta el inicio del espectro de flujo de tracto de salida del VI y del ventrículo derecho (VD). Se consideró asincronía interventricular un retraso aortopulmonar ≥ 40 ms 27) por ecocardiograma
Otras variables de estudio según grupo correspondiente
Otras variables utilizadas en el primer grupo
Variable Indicación de estimulación cardíaca:
Conceptualización: según indicación de estimulación cardiaca.
Clasificación: cualitativa nominal politómica.
Escala de medición:
Indicadores: Número absoluto y porcentaje.
Variable Modo de estimulación cardíaca:
Conceptualización: Según forma de estimulación cardíaca.
Clasificación: Cualitativa nominal dicotómica.
Escala de medición:
Indicadores: Número absoluto y porcentaje.
Variable Frecuencia de estimulación:
Otras variables del tercer grupo de estudio
Selección de pacientes respondedores y no respondedores: Se consideraron respondedores aquellos pacientes con decremento mayor de 15 % del volumen telesistólico del VI, un incremento de 5 % de la FEVI y mejoría de la clase funcional comprobado con la caminata de los 6 minutos. Los pacientes que no alcanzaron los valores mencionados se consideraron no respondedores.
Técnicas para el análisis de la información
El análisis estadístico, se realizó en paquete estadístico statistical package for social sciences (SPSS) versión 17.0 para Windows. Se comprobó la distribución normal de la muestra de cada grupo de estudio, se obtuvo p > 0,05 para la prueba Shapiro-Wilk, lo que nos permitió realizar otras pruebas paramétricas.
Se crearon tablas de distribución de frecuencias con valores absolutos y relativos. Se determinó la media en las variables que lo requerían, así como la desviación estándar como medida de variabilidad; para la comparación de las medias se empleó el estadígrafo t-de Student con nivel de significación estadística si p ≤ 0,05. Desde el punto de vista inferencial se aplicó la prueba no paramétrica chi cuadrado (X2) para asociación entre variables con igual nivel de significación. Se realizaron correlaciones lineales (test de Spearman).
Ética
El protocolo de estudio fue aceptado por el comité de ética de la Universidad de Ciencias Médicas de Villa Clara y el Cardiocentro Ernesto Guevara de la misma provincia, y cumplió los requisitos de estudios en humanos aprobados en el acuerdo de Helsinki. 27
RESULTADOS
Primer grupo de estudio: pacientes estimulados en punta de ventrículo derecho
En la figura se muestran los resultados de las tendencias grupales de las medias de las variables ecocardiográficas en los diferentes momentos del estudio. Se observa un incremento de los diámetros telediastólicos y telesistólicos del VI durante el paso del tiempo en el seguimiento.
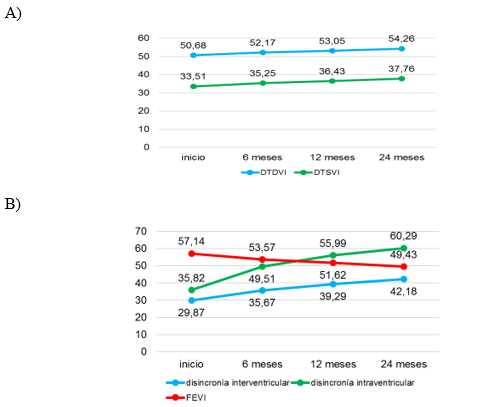
Fig. 1 Tendencias grupales de las medias de las variables ecocardiográficas en los diferentes momentos del estudio. Obsérvese como se incrementan los diámetros telediastólicos y telesistólicos del VI durante el paso del tiempo en el seguimiento. En la figura 1B) obsérvese la caída de la FEVI.
En la tabla 1 la dQRS (variable dependiente) mostró coeficientes de correlación significativos, p ≤ 0,05 al compararlo con la disincronía intraventricular e interventricular y la frecuencia de estimulación y como variable independiente al compararlo con el DTDVI. La FEVI decrece a medida que se incrementa el porcentaje de estimulación y la dQRS.
Tabla 1 Correlaciones entre variables relacionadas con la estimulación cardíaca y ecocardiográficas en los momentos inicial y final del estudio. A) correlaciones directamente proporcionales
| y (dependiente) | x (independiente) | t | p | coeficiente |
|---|---|---|---|---|
| Dispersión del QRS | Disincronía interventricular | 2,496 | 0,015 | 0,454 |
| Dispersión del QRS | Disincronía intraventricular | 3,301 | 0,001 | 0,446 |
| Dispersión del QRS | Frecuencia de estimulación | 3,013 | 0,003 | 0,467 |
| DTDVI | Dispersión qrs | 2,064 | 0,042 | 0,380 |
| FEVI | Frecuencia de estimulación | 12,605 | 0,000 | -0,589 |
| FEVI | Dispersión del qrs | -2,451 | 0,016 | -0,606 |
Leyenda: DTDVI: diámetro tele diastólico del ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo.
Segundo grupo de estudio. Pacientes para estimulación en región septal alta
Existe diferencias significativas al comparar la duración 178,12 ± 14,31 vs. 103,17 ± 3,43 (p < 0,001) y dispersión del QRS 45,07 ± 4,83 vs 33,15 ± 2,14(p < 0,001), mientras los pacientes recibían la estimulación en punta de VD comparado con el momento que recibieron la estimulación septal como nuevo sitio de estimulación ventricular. Tabla 2.
Tabla 2 Distribución de media y desviación estándar de la duración máxima y dispersión del QRS
| Variables | Estimulación en | p | |
| Punta de VD | Paraseptal alta | ||
| Duración máxima QRS | 178,12 ± 14,31 | 103,17 ± 3,43 | < 0,001 |
| dQRS | 45,07 ± 4,83 | 33,15 ± 2,14 | < 0,001 |
Las variables ecocardiográficas (tabla 3) mostraron diferencias significativas. Tras 2 años de estimulación en punta de VD, se constató una FEVI media de 31 % ± 3,1 % vs. 45 % ± 12 %, a los 6 meses postestimulación septal, p = 0,041. El volumen latido hallado fue de 70,18 mL ± 34,11 mL durante estimulación en punta de VD con disfunción sistólica comprobada, luego ascendió a 99,65 mL ± 35,26 mL a los 6 meses de seguimiento, tras estimulación septal, p = 0,004. Los volúmenes telediastólicos en disfunción sistólica fueron 203 mm3 ± 74 mm3 y decrecieron a los 6 meses de estimulación septal hasta 171 mm3 ± 68 mm3, p = 0,032. Los volúmenes telesistólicos disminuyeron desde 151 ± 67 mm3 (estimulación en ápex) hasta 120 ± 53 mm3 (tras 6 meses de estimulación septal), p = 0,006. El retraso septum pared posterior del VI, 138 ms ± 12,5 ms vs. 62 ms ± 9.05 ms, p = 0,000, y el retraso mecánico interventricular 49 ms ± 2,59 ms vs. 29 ms ± 2,15 ms, p = 0,000.
Tabla 3 Distribución de las variables ecocardiográficas de los pacientes al momento del implante y 6 meses de seguimiento de la estimulación paraseptal alta*
| Variables | Momentos de la estimulación paraseptal alta | p | |
|---|---|---|---|
| Al momento del Implante | A los 6 meses de seguimiento | ||
| VTDVI | 203 mm3 ± 74 mm3 | 171 mm3 ± 68 mm3 | 0,032 |
| VTSVI | 151 mm3 ± 67 mm3 | 120 mm3 ± 53 mm3 | 0,006 |
| FEVI (Media ± DE) | 31 % ± 3,1 % | 45 % ± 12 % | 0,041 |
| Retraso septum pared posterior del VI | 138 ms ± 12,5 ms | 62 ms ± 9,05 ms | 0,000 |
| Retraso mecánico interventricular | 49 ms ± 2,59 ms | 29 ms ± 2,15 ms | 0,000 |
* El estudio ecocardiográfico antes del implante del electrodo en región paraseptal alta, se realiza con estimulación en punta de VD, con BRIHH en el ECG.
Leyenda: DE: desviación estándar, FEVI: fracción de eyección de ventrículo izquierdo, VTDVI: volumen telediastólico del ventrículo izquierdo, VTSVI: volumen telesistólico del ventrículo izquierdo
Tercer grupo de estudio: Pacientes sometidos a estimulación biventricular (terapia de resincronización cardiaca)
Pacientes sometidos a estimulación biventricular (terapia de resincronización cardiaca).
La dQRS, (tabla 4) con BRIHH, mostró un valor superior en los respondedores de sexo femenino comparado con los masculinos (40,0 ms ± 28,0 ms vs. 48,0 ms ±24,0 ms); sin embargo, no mostró diferencias significativas (p > 0,05).
Tabla 4 Distribución de la media para la dispersión del QRS previo e inmediatamente después de la implantación, según la respuesta a la TRC
| Respuesta | Sexo | Dispersión del QRS | |||
|---|---|---|---|---|---|
| Con BRIHH | Post-TRC | ||||
| Nº | % | χ ± DE | χ ± DE | ||
| Respondedores | Femenino | 7 | 36,8 | 48,0 ± 24,0 | 24,0 ± 8,9 |
| Masculino | 8 | 42,1 | 40,0 ± 28,0 | 28,0 ± 10,9 | |
| No respondedores | Femenino | 0 | 0 | - | - |
| Masculino | 4 | 21,0 | 30,0 ± 14,1 | 30,0 ± 14,1 | |
| Ambos (Total) | Femenino | 7 | 36,8 | 48,0 ± 24,0 | 24,0 ± 8,9 |
| Masculino | 12 | 63,1 | 37,14 ± 13,8 | 28,57 ± 10,6 | |
χ, media; DE, desviación estándar; p > 0,05 para todas las comparaciones de media entre respondedores y no respondedores; p = 0,000 para comparaciones de media de dQRS antes y después de la TRC en los respondedores;P = 0,04 para comparaciones de dQRS antes de la TRC (con BRIHH) por sexo en los respondedores.
DISCUSIÓN
La evidencia de este estudio muestra el efecto deletéreo de la estimulación del ápex de VD, aun así, es la localización más utilizada en nuestros centros donde se implantan marcapasos, 28,29 de ahí la necesidad de estudiar las características y modificaciones en el seguimiento de estos pacientes y la necesidad del entrenamiento al personal para utilizar sitios alternativos de estimulación como la región septal alta o parahisiana.
El estudio PACE (Pace to Avoid Cardiac Enlargement), 30 multicéntrico, doble-ciego y aleatorizado fue diseñado para determinar si la estimulación biventricular (BiV) era superior a la estimulación en el ápex del VD para prevenir cambios adversos en la función y remodelado del VI, ellos incluyeron pacientes con FE ≥ 45 % con indicación de marcapasos por bloqueo AV de alto grado o disfunción nodo sinusal. A todos los pacientes les implantaron un marcapasos auricular y biventricular, con capacidad de ser programada la estimulación ventricular bien en ápex de ventrículo derecho o biventricular. Tras el implante del dispositivo, luego de 2 días, se estratificaron a los pacientes según presentasen o no disfunción diastólica. En cada grupo fueron aleatorizados a recibir estimulación en ápex de VD o BiV (1:1). En los pacientes evaluables a los 12 meses, el grupo con estimulación en ápex de VD (n = 88) vs. estimulación BiV (n = 89) tuvo una FEVI media significativamente menor (54,8 % ± 9,1 % vs 62,2 % ± 7 % p < 0,001); a los 12 meses, 8 pacientes del grupo con estimulación en ápex de ventrículo derecho (9 %) vs. 1 paciente del grupo otro grupo (1 %) tuvieron una FEVI < 45 % (p = 0,02). El efecto deletéreo de la estimulación en ápex de VD ocurrió en ambos grupos preespecificados, incluyendo pacientes con y sin disfunción diastólica previa, estos datos concuerdan en gran medida con el presente estudio. CM Yu, y otros 31 obtuvieron en su estudio también, una caída de la FEVI en los pacientes con estimulación en ápex de VD. P Vijayaraman et al32 en su revisión mencionan los efectos deletéreos de la estimulación en ápex de VD y el curso actual de las investigaciones en la búsqueda de una conducción eléctrica cardíaca fisiológica, durante la estimulación, que no deteriore la función del ventrículo izquierdo, mencionando a utilidad que demuestra la estimulación en His o para Hisiana.
El Protect-Pace study 33 mencionó las dificultades técnicas al implantar el electrodo en la región septal; sin embargo, The SEPTAL Study 34 hizo mención a la factibilidad a la hora del implante del electrodo de fijación activa en la región septal al usar las vistas radiológicas y la comprobación de un ECG más angosto, según criterios del electrofisiólogo durante el implante. Ortega et al. 35 refirieron que, a pesar de que el QRS de la estimulación septal parahisiana es más ancho, ello no implicaba cambios significativos en el tiempo de la despolarización de la pared libre posterobasal del VI, lo cual mejoraba la sincronía por una despolarización y contracción similares a la fisiológica.
Se propone denominar a la dQRS: índice de disincronía eléctrica del VI en presencia de bloqueo de rama izquierda. Los resultados preliminares que se exponen demuestran la existencia de mayor dQRS en pacientes con los QRS más anchos en presencia de BRIHH y se ha comprobado la existencia de mayor disincronía eléctrica en pacientes con QRS > 150 ms 36-38 aspecto este muy bien señalado por Varma 39 en 2009, al demostrar retrasos en la activación del ventrículo izquierdo. Además, la regresión de la dQRS, es mayor en los que responden favorablemente a la TRC, lo que puede estar asociado al restablecimiento de la sincronía eléctrica y tendría que demostrarse desde el punto de vista electrofisiológico. Se observó además que las derivaciones más anchas fueron DI y a VL, resultados no mostrados en este artículo, que serán objeto de posterior publicación.
Conclusiones
La estimulación en punta de ventrículo derecho constituye un sitio que se relaciona con el deterioro contráctil del corazón; el incremento en la dispersión del QRS constituye una variable electrocardiográfica que puede predecir la disminución de la fracción de eyección. Los pacientes que recibieron estimulación septal mejoraron la sincronía electromecánica, esa mejoría pudiera ser determinada por decrementos de la dispersión del QRS y está relacionada con la secuencia más fisiológica de la conducción post estimulación. Por último, en los pacientes resincronizados, el decremento significativo de la dispersión del QRS puede predecir buena respuesta a la resincronización. Las mujeres, quizás relacionado a diferencias hormonales o electrofisiológicas no descritas, presentan mayores dispersiones del QRS que al de forma biventricular, tienen mayor respuesta a la terapia de resincronización cardiaca.
En los 3 grupos estudiados, le dispersión del QRS demostró estar relacionada con la sincronía o disincronía electromecánica, de forma tal, que el electrocardiograma puede ser una herramienta útil para predecir la aparición de disincronía electromecánica en la estimulación eléctrica cardiaca permanente cuando la dQRS se incrementa o la mejoría de la sincronía cuando se logran QRS más estrechos y disminuye además la dQRS.














